
花火の科学、炎色反応について
今年もすでに、7月です。夏休みも近いですね。夏といえば、花火!
今回は、色鮮やかに夜空を彩る花火について、科学の視点で見ていきたいと思います🎆
花火には、赤青黄色とさまざまな色のものがあって、カラフルで綺麗ですよね?
あの色は、どうやって色をつけているのか、考えたことありますか?すでに、ご存知の方も多いかと思いますが、結論からいうと、、
炎色反応
という現象を利用して、さまざまな物質、薬品が使われているんです。
炎色反応とは、主にある種の金属元素がガスバナーなどで加熱され、そのエネルギーの吸収と放出でおこる発光現象です。
高校化学の範囲で、リアカーなきK村…とかで暗記しませんでしたか?w
各元素と炎の色なんて何の役に立つんだ?だから何?!と冷たい反応で授業を受けたかもしれませんが、、、実際役に立ってて、あなたの心を癒したりしてるんですよ。
花火を見ると綺麗なんですが、私は儚さを感じてしまい、なんとなく寂しくなります。と同時に、フジファブリックの『若者のすべて』が脳内再生されます🎵
オススメの名曲です☝️
さて、炎色反応を示す元素は限られていて、Li,Na,K,Ca,Sr,Ba,Cuなどです。周期表の場所で言うと、主にアルカリ金属、アルカリ土類金属が多いんです。1価や2価のイオンになりやすいものが多く、最外殻に1個か2個の電子をもっていて、これがカギになってきます。
光というのは、エネルギーであって炎からエネルギーを吸収して、吸収したエネルギーを放出することで、色の光がでます。炎色反応を起こる元素はたまたま可視光領域の光エネルギーを放出しているわけで、それが、アルカリ金属系に多く、例外的に、CuやBでも起こります。
光の波長とエネルギーの関係式
E=hν=hc/λ
h:プランク定数
ν:光の振動数
c:光の速度
※短い波長の紫はエネルギーが高く、長い波長の赤はエネルギーが小さい
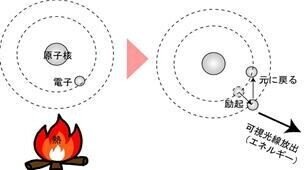
傾向として、最外殻に電子が1〜2個ある元素で、原子核と電子のバランスで励起される軌道間のエネルギーが可視光領域になると考えられます。
炎色反応の様に、色で見えないだけで、その他の元素も加熱されると、紫外線領域など目に見えない光を放出している場合は多くあります。
励起源は異なりますが、発光現象を利用して、スパーク発光分析や誘導プラズマ結合ICPなどで元素分析が可能なんです。総じて発光分光分析と言います。いずれも、可視光やそれ以外の光を、検出して分析に使われています。
さて、家庭でも簡単に実験できるので…安全に配慮して炎色反応をすることができます。
ホームセンターなどで準備できるものとして、
・アルミカップ
・ジェル燃料
・食塩(塩化ナトリウム)
・融雪剤(塩化カルシウム)
・ミョウバン(硫酸アルミニウムカリウム)
・農薬用の塩化銅
手順↓
アルミカップに、ジェル燃料を豆粒大に乗せて、各粉体をジェル燃料に割り箸などで、混ぜ込みチャッカマンなどで安全に点火する。
混合粉体にして、配合を工夫すればカラフルな炎が観察できます🔥
ただし、実験は水道の近くでやる、濡れた布巾を用意するなど安全に配慮しておこなってください。
自由研究などでは、必ず大人の方といっしょに実験してください。
安全第一です!
※この記事では、万が一の火災等の責任は負いません。
@shingakumon36 花火の原理!炎色反応です!#花火#理科 #勉強 #化学 #炎色反応#勉強垢
♬ Fire - Official Sound Studio
Cuの緑の炎

Srの赤い炎

黄 ナトリウム
紫 カリウム
橙 カルシウム
よろしければ、サポート(入塾)お願いします!サポート代での月謝支払いなんでどうでしょう?
