
レプリコン(自己増殖型)ワクチン ベトナムでの臨床試験は成功したと言えるのか?
11月28日に承認されたレプリコン(自己増殖型)ワクチン「ARCT-154」は、Meiji Seika ファルマが日本での供給・販売権を取得していますが、開発したアークトゥルス(Arcturus)はベトナムの企業と製造技術移転契約を締結して、第1相から第3相の臨床試験をベトナムで行いました。アークトゥルスの第4四半期報告(2022年2月)では、すでにベトナムでの緊急使用許可を申請したとありますが、ベトナムではまだ緊急使用許可は出ていないようです。
厚生労働大臣記者会見(12月1日)
レプリコンワクチンが承認されたことについては、前回の記事で書きました。
参考:Meiji Seika ファルマのリリース
新型コロナウイルス感染症に対する次世代 mRNA ワクチン(レプリコン)「コスタイベ筋注用」の国内製造販売承認取得に関するお知らせ
~次世代 mRNA ワクチン(レプリコン)として世界で初めての承認~
12月1日の厚生労働大臣記者会見で、記者からレプリコンワクチンに関する質問がありました。
記者:
11月28日に承認された「レプリコンワクチン」について伺います。分子生物学者・免疫学者の荒川央氏は次のように述べています。
「これまでのmRNAワクチンはスパイクタンパク生産にブレーキのないワクチンでしたが、自己増殖するmRNAワクチン、つまりレプリコンは更に遺伝子の増殖にすらブレーキがありません。それどころかむしろ加速するアクセルが付いているようなものです。ワクチン接種者から他者にワクチンを感染させる事態が発生すると、社会の中でワクチン感染が蔓延し、ワクチン変異株が周囲に拡散されるバイオハザードのような状況すら理論的には起こり得るのです」
PMDA、および薬事・食品衛生審議会が、このたびのレプリコンワクチンの承認を認めたということは、荒川氏が言うようなリスクを超えるベネフィットがあるからだと推測します。レプリコンワクチン接種のベネフィットについて、また荒川氏が懸念するバイオハザードが実現した場合の対処法と責任の所在についてご教示願います。
大臣:
今般承認したレプリコンワクチンは、国内外の臨床試験において、一定の発症予防効果や中和抗体価の上昇が確認されたこと、また有害事象の種類や発現割合等にファイザー社ワクチンと比べて明確な差は認められず、安全性は許容可能と判断できたことから、薬事承認を行いました。
レプリコンワクチンは、接種後に抗原タンパクをコードするmRNAが細胞内で複製され、持続的に抗原タンパクが作られるワクチンであることから、ご指摘のようなワクチンの被接種者から当該ワクチンに含まれる物質等が他の者に伝播するような事象は今のところ確認されておりません。
ベトナムでの臨床試験
下記は、査読前論文です。
Posted Date: September 20th, 2023
This report covers data obtained from enrolment of the first phase 1 participant on 15 August 2021 until to 12 January 2023, the cut-off for data extraction for interim safety and per protocol efficacy analyses from phase 3b.
各フェーズの参加人数

データは2021年8月15日から取っているようですが、臨床試験に参加した人の周囲の人たちについては、データを取ったのでしょうか。厚労大臣は、「伝播するような事象は今のところ確認されていない」と言っていましたが、データを取っていないなら確認のしようがありません。
下記は有害事象のデータです。
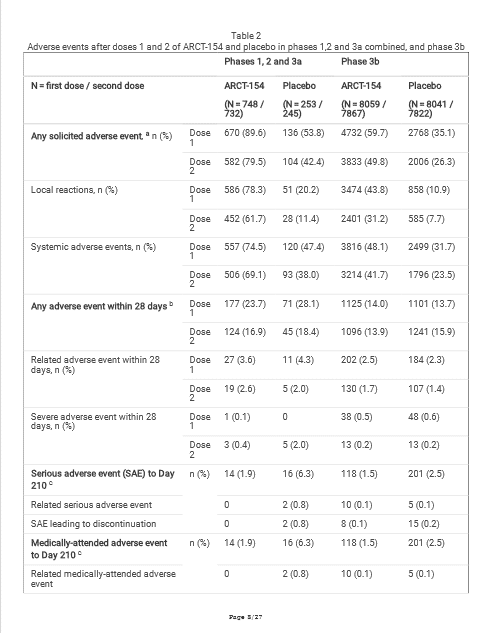
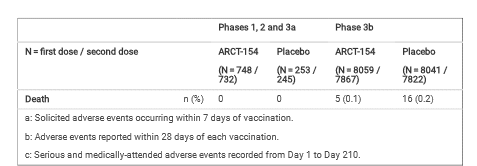
There were no deaths in phases 1, 2, and 3a, but 21 deaths occurred in phase 3b, of 5 vaccinees and 16 placebo recipients. Of these, none were related to vaccination but 10 were considered to be associated with COVID-19 infection, one in a vaccinee and nine in placebo recipients.
フェーズ3bでは21人が死亡したとあり、ワクチン群5人、プラセボ群16人。ワクチン接種に関連したものはなかったが、10 件が新型コロナウイルス感染症に関連していると考えられ、そのうち 1 件はワクチン群、9 件はプラセボ群だったとのこと。
プラセボで16人死亡というのが気になりますし、接種群とプラセボ群、それぞれどのような経緯で死亡したのか明らかにしてほしいです。
論文では、新型コロナウイルス感染症に関連した10件は、プラセボ群では9件死亡しているのに、接種者は1件しか死亡していないことからもワクチンの「効果がある」としています。
Placebo was sterile saline.とあるので、プラセボは生理食塩水だったようですが、この時期にコロナ感染で10人も死亡したというのは、どのような状態だったのでしょうか。
臨床試験の参加条件(他社のコロナワクチン既接種なのかなど)が知りたかったので調べてみたところ、第1/2/3相の募集では、除外条件に「他のコロナワクチン既接種」がありました(下記参照)。つまり、コロナワクチン未接種が参加条件だったようです。
10.Has previously received investigational or approved MERS-CoV, SARS-CoV, SARS-CoV-2 vaccines or who have plans to receive off-study COVID-19 vaccines.
妊娠中や授乳中、癌や自己免疫疾患の治療中の人も除外になっています。
下記では、各フェーズについて詳しく書かれています。
For Phase 1, Phase 3b and participants in Phase 2 and 3a that received placebo in the first vaccination series, the participants will be switched over to the opposite vaccine in the second series.
この意味がよくわからないのですが、プラセボ群だった参加者は第2シリーズでは反対のワクチンにスイッチするということは、結局全員「ARCT-154」接種されてしまうということなのでしょうか?
だとしたら、フェーズ3bのプラセボ群はすでに「ARCT-154」を接種した人ということになるのでしょうか。
追記:審査報告書に詳細がありました(下記参照)。
臨床試験は成功したといえるのか?
参加者の条件などを調べていたら、気になる情報がありました。
この記事(2021年8月2日付)には、「臨床試験が中間評価で成功したと評価されれば、年末までにベトナム保健省により緊急使用許可(EUA)が出る予定」と書かれています。けれども、2021年のうちにEUAが出たという記事は見当たりません。
そして、2022年4月20日の記事には、第3相試験のデータを出した後、アークトゥルスの株価が下落したと書かれています。
アークトゥルス(Arcturus)が発表したARCT-154に関する第3相試験のデータによると、新型コロナウイルス感染症(COVID-19)に対して55%の有効性を達成、重症化および死亡に対する有効性は95%。それを受けてArcturusの株価は、20%下落したとのこと。
マーケット情報を提供しているイギリスの「Evaluate」も、2022年4月時点では、アークトゥルスのワクチンは投資家たちの関心を集めていないと言っています。世界初のレプリコンなのに、関心がないとは・・・。
2022年4月27日付の記事
ベトナムでは、初の国産コロナウイルスワクチンの臨床試験にゴーサインを出してから、ほぼ1年半経過しても、まだ緊急使用が承認された国産ワクチンはないと書かれています。 候補として3社のワクチン(Nano Covax、Covivac、ARCT-154 )があり、アークトゥルス(Arcturus)は同国のVinbiocare Biotechnologyと製造技術移転契約を結んでいるので、ARCT-154も「国産」と考えているようです。
保健省のDo Xuan Tuyen副大臣は2022年4月初旬の政府記者会見で、同省は依然として「成功したワクチンに対して認可を与えたい」と考えていると述べています。さらに、「国立生物医学研究倫理評議会が要求する書類を完成させ、その評価に基づいてすべての条件を満たしていれば保健省はライセンスを与えるだろう。これらのワクチンは高レベルの安全性を確保し、起こり得る事故を防ぐために十分かつ包括的な研究と評価が必要だ」と語っています。
まだEUAが出せないということは、成功とはいえない、あるいは高レベルの安全性が確保できていないということなのではないでしょうか。
1年以上前の記事なので、現在の状況はわかりませんが、ベトナムでEUAが出たという情報は見当たりませんでした。
2022年8月の情報ですが、パンアメリカン保健機構のサイトにWHOの緊急使用リスト(EUL)がありました。
VIGICARIB NEWS 18th AUGUST, 2022
この時点でもARCT-154は「under review」です。WHOのサイトも確認しましたが、緊急使用リスト(EUL)は2022年8月以降は更新されていないのだと思います。それは、もう緊急使用する必要がないことを意味するのではないでしょうか。


この記事を書くために調べたときにはベトナムで緊急使用許可が出たという情報は見つけられませんでしたが、日本で承認されたことが影響して、動きがあるかもしれません。何か情報があれば、追記します。
追記:関連記事
自己増殖型ワクチン(ARCT-154)に対するアメリカでの反応です。
追記:関連記事
インドでは2023年6月に、自己増殖型ワクチンの緊急使用許可が出ていました。
レプリコンワクチンに前のめりなのは日本だけ!?
記事を掘り起こしていくと、レプリコンワクチンの開発に前のめりなのは日本だけのように見えます。
2023年8月14日付
「アークトゥルスのプログラムは 2022 年 4 月に大きな挫折に見舞われた」とあり、それはベトナムでの第 3 相臨床試験において、ARCT-154 が新型コロナ感染症に対する初回免疫として 55% の有効性しか示さなかったことだと書かれています。
しかし、同社は先月(2023年7月)、「日本の第3相試験からのブースターデータを携えて復活した」とあり、そのデータが下記に書かれています。
これも査読前論文ですが、すでに他社のワクチンを接種している人を対象とした臨床試験です。
2022 年 12 月 13 日から 2023 年 2 月 25 日までに、ARCT-154 (n = 420) または ファイザー社コミナティ (n = 408) の追加接種を受けるために 828 人の参加者を 1:1 で無作為に登録したとのこと。すでに約400人、日本でも接種した方たちがいるということです。
ファイザー社やモデルナ社は他のコロナワクチンとの互換性に関するデータはないと添付文書に書いていますが(下記参照)、このような臨床試験で健康被害が起きた場合、どのように評価するのでしょうか。また、責任の所在はどうなるのでしょうか。
いずれはインフルエンザもレプリコンに!?
下記は、2023 年 9 月 27 日付のリリースです。
VLPT ジャパン、BIKEN 財団、デンカ、
季節性インフルエンザに対するレプリコン(次世代 mRNA)ワクチンの共同研究契約を締結
VLPT ジャパン、BIKEN 財団、およびデンカは、レプリコン(次世代 mRNA)技術を用いた季節性インフルエンザワクチン開発に関する共同研究契約を締結しました。この共同研究では、2024 年度中にワクチン試作品のマウスでの有効性・安全性評価と、予備安定性試験まで実施することを目指しているとのこと。
mRNAワクチンの安全性さえ、きちんと検証されていないのに、次々と新しいワクチンが開発されます。
コロナ前までは新しいワクチンの実用化まで、早くても7年ぐらいはかかるといわれていました。だから、SARSのときは間に合わなかったのです。

このようなスピード重視の開発は、いったい誰のために行われているのでしょうか。
<関連記事>
