
ロボット支援下 腹腔鏡下子宮悪性腫瘍手術 -work.07-
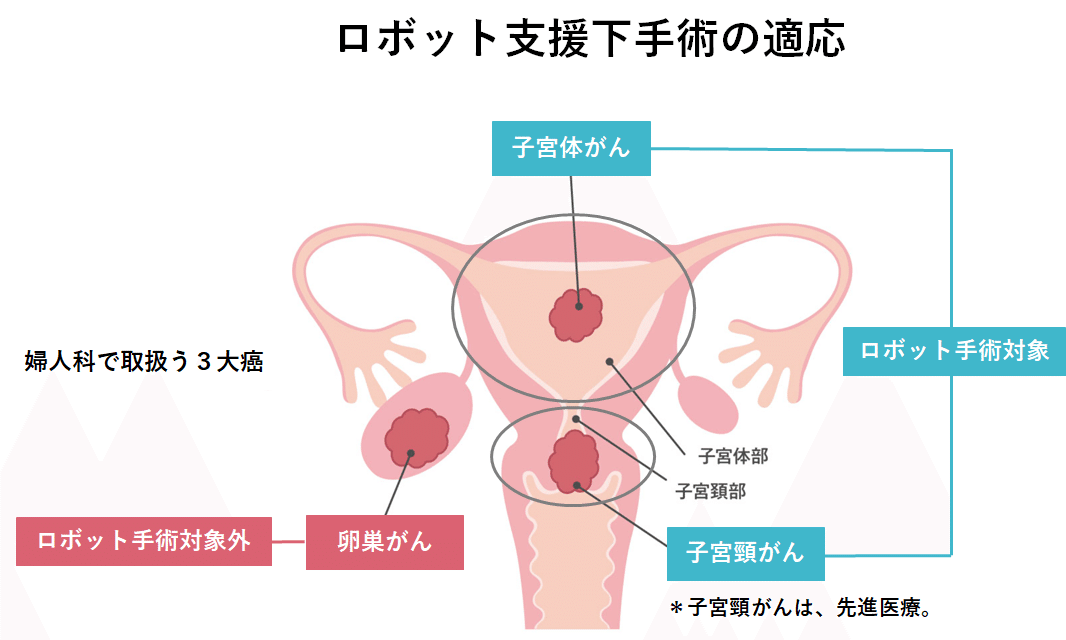
これより、保険適用となっているロボット支援下手術についてまとめていく。まずは婦人科領域から。現在保険適用となっている婦人科ロボット支援下手術は3件(腹腔鏡下子宮悪性腫瘍手術/腹腔鏡下膣式子宮全摘術/腹腔鏡下仙骨膣固定術)。
今回は、そのうちのロボット支援下 腹腔鏡下子宮悪性腫瘍手術(子宮体がんに限る)を中心に整理していく。
1.婦人科におけるロボット手術の保険適用疾患は?
上述したように、婦人科ロボット支援手術においては、現在3つの術式で保険適用となっている。各術式における保険適用疾患について以下に記載する。
2018年4月から、①子宮体癌の中で危険度の低い低リスク体癌(腹腔鏡下子宮悪性腫瘍手術)、②がんではない良性子宮腫瘍(腹腔鏡下膣式子宮全摘術)、そして2020年4月からは、③骨盤臓器脱(腹腔鏡下仙骨膣固定術)においても保険適用となっている。3術式ともにロボット加算は無く、通常の腹腔鏡下手術と同点数。
以下に、診療報酬点数および注釈について記載する。
K879-2 腹腔鏡下子宮悪性腫瘍手術 70,200点
(1) 子宮体がんに対するものについては、日本産科婦人科学会、日本病理学会、日本医学放射線学会及び日本放射線腫瘍学会が定める「子宮体癌取扱い規約」におけるⅠA期の子宮体がんに対して実施した場合に算定する。
(2) 子宮体がんに対するものについては、IA期の術前診断により当該手術を行おうとしたが、術中所見でIB期以降であったため、開腹手術を実施した場合は、区分番号「K879」子宮悪性腫瘍手術を算定する。
(3) 子宮頸がんに対するものについては、関係学会の定める診療に関する指針を遵守し、実施すること。
診療報酬の算定方法の一部改正に伴う実施上の留意事項について(通知)
令和2年3月5日 保医発0305第1号 医科点数表 P529
https://www.mhlw.go.jp/content/12400000/000666093.pdf
2014年4月から保険適用(ロボット支援下は2018年4月から)。算定条件は、『ⅠA期の子宮体がん』に対して実施した場合、つまり骨盤リンパ節郭清までの低リスク体がん手術において保険適用となっている。標準的な手術内容は以下になる。
『単純子宮全摘術』+『両側付属器摘出術』+『骨盤リンパ節郭清』
--------------------------------------------------------------------------------------
K877-2 腹腔鏡下腟式子宮全摘術 42,050点
腹腔鏡下腟式子宮全摘術の対象疾患は、良性子宮疾患とする。
良性疾患には、子宮筋腫(Uterine fibroid)や子宮内膜症(Endometriosis)、子宮腺筋症(Adenomyosis)、卵巣嚢腫(Ovarian cyst)などがある。腹腔鏡下手術においてはこれまでも保険診療ではあったが、ロボット支援下においても保険適用となった。これら個々の良性疾患については、次回のテーマ(Vol.8 ロボット支援下 腹腔鏡下膣式子宮全摘術)でまとめることにする。
--------------------------------------------------------------------------------------
K865-2 腹腔鏡下仙骨腟固定術 48,240点
注:メッシュを使用した場合に算定する。
適応は、通常の腹腔鏡下仙骨腟固定術と同様であり、ほぼ全てのタイプの骨盤臓器脱(子宮脱、膀胱瘤、直腸瘤、腟断端脱など)に対して施行可能。今回は、この術式に関しては触れない。
--------------------------------------------------------------------------------------
次の項目では、「子宮体がんとは何か?」について整理していく。
2.子宮体がん(Endmetorial Cancer)とは?
子宮は女性特有の臓器であり、体部と頸部の2つに分けられる(下図)。子宮体部にできたがんを『子宮体がん』、子宮頸部にできたがんを『子宮頸がん』と呼ぶ。子宮体がんの大半は、子宮内膜(*)という組織から発生し、子宮内膜がんとも呼ばれる。
子宮内膜(*):子宮体部の内側にあり、卵巣から分泌されるエストロゲン(卵胞ホルモン)の作用をうけて月経をおこす組織。

また、子宮体がんと子宮頚がんは、”がん”の性質が異なるため、その違い(発生部位・発生原因・がん細胞の形・症状の進行具合・発生しやすい年代など)を認識しておく。
子宮体がんは、大きく2つに分類
子宮体がんは、①子宮内膜癌(子宮内膜に発生する悪性腫瘍)と②子宮肉腫(子宮筋層に発生する悪性腫瘍)の2つに分類される。どちらも主に子宮体部に発生する悪性腫瘍のことで、95%程度は子宮内膜癌であることから、一般的に「子宮体がんと言えば子宮内膜癌」のことを指す。

子宮壁は粘膜・筋層・漿膜(腹膜)の3層からなり、それぞれ子宮内膜(endometrium)・子宮筋層(myometrium)・子宮外膜(perimetrium)という。子宮体部の平滑筋層は厚く、12~15 mmもある(非月経時の内膜の約5倍の厚さ)。平滑筋線維は子宮の長軸を輪状に取り巻くように走行している。
子宮体がんの患者数
がん登録・統計(国立がん研究センターがん情報サービス)によると、2015年の国内における子宮体がん罹患者は14,909人、10万人当たり約22.8人となっている(女性の総人口:65,253,007人)。

また、年齢別でみると、閉経後の女性(特に50歳代から60歳代の人)に多く見つかり、反対に30歳未満の世代に見つかることは少ない。

https://ganjoho.jp/reg_stat/statistics/stat/summary.html
子宮内膜癌について詳しく見ていく前に、そもそも「”がん”とは何か?」について記載する。
3.そもそも、がんとは?
腫瘍は身体のあらゆる細胞から発生するため、その腫瘍のもととなった組織(母組織)に基づき分類される。身体の組織や細胞は”上皮性”と”非上皮性”に分けられ、”上皮性腫瘍”、”非上皮性腫瘍”とされるが、これをさらに良性と悪性に分ける。
①良性上皮性腫瘍
②良性非上皮性腫瘍
③悪性上皮性腫瘍(癌腫という)
④悪性非上皮性腫瘍(肉腫という)
*通常は、③と④を”がん”と呼ぶ。
がん分類
がんは大きく以下の3つに分類される。

①上皮細胞にできる『癌腫』
肺がん、乳がん、胃がん、大腸がん、子宮がん、卵巣がん、頭頸部がん(喉頭がん、咽頭がん、舌がん)など
②非上皮性細胞からなる『肉腫』
骨肉腫、軟骨肉腫、横紋筋肉腫、平滑筋肉腫、線維肉腫、脂肪肉腫、血管肉腫など
③造血器でできるもの
白血病、悪性リンパ腫、骨髄腫など
「癌腫」と「肉腫」の違い
上皮性細胞に由来する悪性腫瘍(上皮性悪性腫瘍:胃がん、肺がんなど)は癌種と呼ばれ、非上皮性細胞(間葉系細胞:筋肉、骨、結合組織など)に由来する悪性腫瘍は肉腫や間葉性(非上皮性)腫瘍とも呼ばれる。
がん(悪性腫瘍)の種類
発生組織との類似性によって分類される。
Ⅰ.癌腫(悪性上皮性腫瘍)の場合
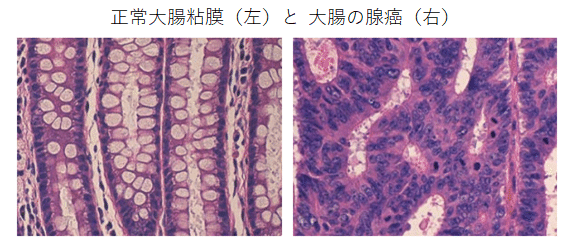
1)腺癌(子宮体がんなど)
--------------------------------------------------------------------------------------
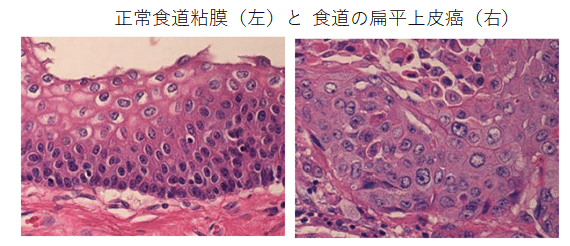
2)扁平上皮癌(子宮頸がんなど)
--------------------------------------------------------------------------------------
他には・・・
3)移行上皮癌(膀胱癌など)
4)その他(肝細胞癌、腎細胞癌など)
--------------------------------------------------------------------------------------
もう少し、深堀る。
人間の体は受精卵からできる。1個の受精卵は母親の子宮の中で分裂を繰り返しながら子供の体を造ってゆく。その過程で、体の表面を覆う、将来は皮膚の表皮(汗腺や皮脂腺および毛を造る細胞も含む)になる外胚葉、呼吸器や消化器という管状の臓器の内面を覆う細胞層となる内胚葉およびその間隙を埋める中胚葉の三つの胚葉に属する細胞群に分かれる。
外胚葉と内胚葉由来の細胞群は表面や管の内面を覆うので、これはすべて上皮性である。中胚葉からは、体内の間隙を埋める組織即ち泌尿器と生殖器となる組織も造られる。泌尿器・生殖器も中が空になっている管状の臓器であるので、中胚葉由来であっても管の内面を覆う上皮と壁を構成する非上皮性の部分からなっている。体の表面を覆う表皮と中空性の管状の臓器の内面を覆う上皮との間隙を埋める組織は中胚葉性であるが、そのうち泌尿器・生殖器の上皮を除いた組織を間葉系あるいは非上皮性と呼ぶ。
腫瘍はこの上皮と非上皮(間葉)を基として、腫瘍細胞が何れの部分から発生したかで分類される。即ち、まず上皮性か、非上皮性(間葉性〕かで大別し、その腫瘍が発生した基になる細胞の名前(発生母地細胞という)あるいは正常の細胞のどの細胞に似ているかで名前をつけ、分類している。
さらに上皮性で悪性のものを癌(あるいは癌腫)という。癌のなかで扁平上皮に似ているものを扁平上皮癌と呼び、腺上皮(液状のものをつくって分泌する)に似ているものを腺癌という。良性の上皮腫瘍には乳頭腫、腺腫などがある。
非上皮性(間葉性)で悪性のものを肉腫と呼び、発生母地細胞の名前を前に付して、線維肉腫、筋肉腫、血管肉腫、脂肪肉腫、骨肉腫、軟骨肉腫などと呼ぶ。良性の非上皮性(間葉性)腫瘍には、線維腫、筋腫、血管腫、脂肪腫、骨腫、軟骨腫などがある。血管は管状の組織であるが、体の中で完全な閉鎖腔を形成していて、外界に接触することはないので、血管内面を覆う細胞を内皮細胞と呼んで、上皮とは呼ばない。血管は完全に間葉性のものである。
何故分類をするのか? それは、それぞれの腫瘍には発生場所、発生し易い年齢層、予後などでそれぞれの特徴があるからである。
知ってもらいたい医学用語の基本より
http://www.c-mei.jp/BackNum/032n.htm
次は、子宮内膜癌(子宮体がん)の発生原因についてまとめていく。
4.子宮内膜癌の発生原因と組織型の判定
子宮内膜癌とは、その殆どが子宮体部における上皮系悪性腫瘍(*)であり、子宮内膜腺細胞由来の腺癌である。
ちなみに、子宮頸癌は扁平上皮癌が主で腺癌も稀にある、といった感じだが、子宮体癌はほとんど腺癌だと思っていい。一応、腺癌以外にも扁平上皮癌・移行上皮癌・小細胞癌・未分化癌があるが、いずれも稀である。
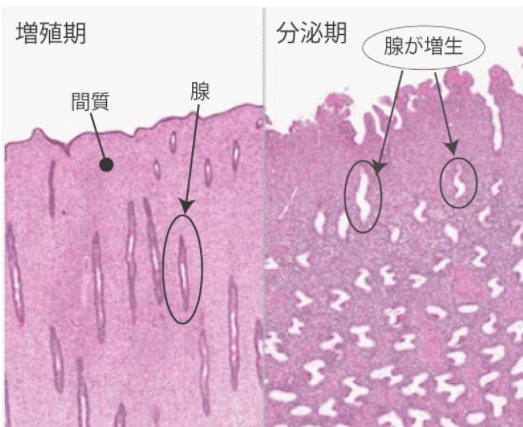
子宮内膜の腺組織(腺細胞)は、上図のように増殖期から分泌期に移行する過程で増殖していく。腺以外の部分を間質とよぶ(間質が悪性化したものが子宮内膜間質肉腫)。腺管の増殖が通常より亢進し、間質より腺管の占める面積の方が大きくなったものを子宮内膜増殖症(*)という。この状態になると、剥離する内膜が増えるので過多月経になる。また、破綻出血を起こすこともあるので、不正性器出血として自覚される。この子宮内膜症に細胞異型が加わったものが子宮内膜異型増殖症(*)であり、子宮体癌に発展する可能性がある。
--------------------------------------------------------------------------------------
◆発生原因(Ⅰ型、Ⅱ型に分類)
子宮内膜がんは、発生原因によって大きく2つに分類される。分類されたものを組織型といい、その傾向も異なる。①エストロゲン(卵胞ホルモン)という女性ホルモンの刺激が長期間続くことが原因で発生するⅠ型と、②エストロゲンとは関係のない原因で発生するⅡ型に分けられる。
--------------------------------------------------------------------------------------
Ⅰ型(類内膜がん)
エストロゲン(卵胞ホルモン)には子宮内膜の発育を促す作用があるため、卵胞ホルモンの値が高い人は、ホルモン曝露の影響を受ける。この影響により子宮内膜増殖症(*)という前段階を経て、子宮内膜がん(類内膜がん、粘液性がん etc)を発症する傾向にあることが既に知られている。Ⅰ型は、子宮内膜増殖症を経てから発症するため、比較的早期に見つかりやすい”がん”と考えられる。
エストロゲンが関係していると考えられる原因(Ⅰ型)
・出産経験がない
・閉経が遅い
・月経不順(無排卵性月経周期)
・肥満
・エストロゲンを産生する腫瘍
・乳がんの治療薬タモキシフェン(*)の内服
・エストロゲン補充薬(*)の単独使用(更年期障害の治療薬、ホルモン療法)
タモキシフェン(*)
抗エストロゲン薬。エストロゲンがエストロゲン受容体へ結合することを妨げることで、乳がんの増殖を抑える薬。
エストロゲン補充薬(*)
ただし、エストロゲンについては黄体ホルモンの併用により、子宮体がんの発生リスクが高くならないことがわかっている。
以下は、タモキシフェンに関する追加情報。
BQ15.タモキシフェンは子宮内膜癌発症リスクを増加させるか?
<ステートメント>
『乳癌術後のタモキシフェン内服により、閉経後女性で子宮内膜癌(子宮体癌)の発症リスクを増加させるが、閉経前女性では子宮内膜癌(子宮体癌)の発症リスクは増加させない』
日本乳癌学会 乳癌診療ガイドラインより
https://jbcs.xsrv.jp/guidline/2018/index/yakubutu/y1-bq-15/
また、海外からの報告では・・・
『タモキシフェンの長期服用(2年以上)により子宮体がん、子宮内膜症の発生が増す可能性があることが指摘されている。50歳以上で2年以上の長期のタモキシフェン服用により子宮体がんになる可能性が2~4倍に増え (10年間で、もともと1,000人に2人程度だった発症リスクが6人へと増える)、長期内服ががそのリスクを高めるといわれている』
--------------------------------------------------------------------------------------
Ⅱ型(非類内膜がん:漿液性がん、明細胞がん)
一方、Ⅱ型はエストロゲンが関連しないものが原因となり、主に閉経後の高齢の方の萎縮内膜を背景に起こるとされている(委縮した内膜に、がん関連遺伝子の異常に伴って発生)。予後の悪い漿液性がんや明細胞がんなどがこのⅡ型に含まれる。
エストロゲンとは関係のない原因(Ⅱ型)
・高齢者に多く
・高血圧
・糖尿病
・血縁者に、乳がん、大腸がんを患った人がいる
・遺伝性腫瘍の1つであるリンチ症候群(*)
国立がん研究センター がん情報サービス
https://ganjoho.jp/public/cancer/corpus_uteri/index.html#a14
遺伝子性腫瘍であるリンチ症候群について、以下にまとめる。
--------------------------------------------------------------------------------------
◆リンチ症候群(遺伝性非ポリポーシス大腸がん)
リンチ症候群(Hereditary Non-Polyposis Colorectal Cancer:HNPCC)は、大腸がんの若年発症、異時性あるいは同時性の大腸多発がんおよび多臓器がんの発症が特徴(元の名前は”大腸がん”だが、大腸以外にも”がん”ができやすいことに注意)。リンチ症候群の平均発症年齢は43-45歳と考えられ、20歳未満での発症は比較的少数。
リンチ症候群の遺伝子変異を持つ人では、生涯の間に約80%が大腸がんを発症、また女性では、生涯に20-60%が子宮内膜がん(子宮体がん)を発症すると報告されている。リンチ症候群は必ずしも他の血縁者と同様の症状を示すわけではなく、遺伝子変異を持っていても生涯発症しない場合もある。

原因遺伝子
リンチ症候群の原因は、生殖細胞系列でのミスマッチ修復遺伝子(MSH2・MLH1・MSH6・PMS2)の変異。リンチ症候群は常染色体優性遺伝形式を示し、性別に関係なく子供に50%の確率で遺伝する。

ミスマッチ修復遺伝子の生殖細胞系列変異がリンチ症候群診断の決め手となるが、家族歴から強くリンチ症候群が疑われる場合でも必ず変異が見つかるわけではない。
リンチ症候群の遺伝子診断では、MSH2・MLH1遺伝子の変異を最初に調べる(これまでに変異報告されている症例の90%以上がMSH2・MLH1遺伝子の変異)。その次に多く変異報告されているのがMSH6遺伝子だが、全報告例の5%以下であり比較的少ないものと考えられる。
リンチ症候群への治療薬
以下の研究結果は、大腸がん臨床試験において、免疫チェックポイント阻害薬であるペンブロリツマブ(PF-1抗体)が、『ミスマッチ修復に不具合のある患者さんに非常に効果を発揮した(腫瘍サイズにポジティブな変化がみられた)』ことを示すものである。
下図:腫瘍サイズの変化を見たもの
赤線:ミスマッチ修復遺伝子が機能している(不具合のない)人
青線:ミスマッチ修復遺伝子が機能していない(不具合のある)人

また以下は、ASCO(米国臨床腫瘍学会)からの報告。再発子宮体癌患者の成績をみたもの。24名中3名(12.5%)に奏功。奏功した人には、長く効果が持続する(60ヵ月以上)。
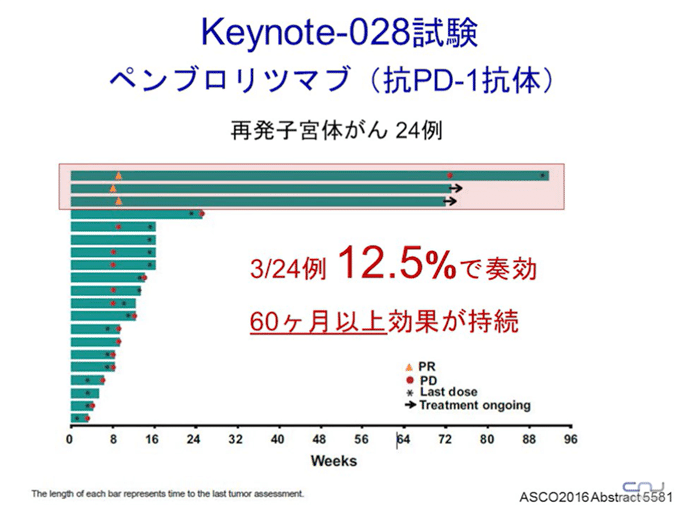
奏効率は12.5%と、一見少なく見えるが、今後、ミスマッチ修復遺伝子に不具合のある人に限定し、ペンブロリツマブを使用していくことで、効率的な患者選択に繋がることが期待されている。
ちなみに、ミスマッチ修復遺伝子の不具合検査は、大腸がんでは保険適用となっているが、子宮体癌においては保険適用外(2016年時点)
【リンチ症候群 まとめ】
・遺伝性大腸癌のひとつ。全大腸がんの2%~5%を占めるといわれる。
・大腸がん、子宮体がん、卵巣がん、胃がん、小腸がん、肝胆道系がん、腎
盂、尿管がんなどのリスクが高まる(元の名前は”大腸がん”だが、大腸
以外にも”がん”ができやすいことに注意)
・発症年齢が若い(50歳未満)
・大腸がんが同時、異時に多発する場合がある。
・原因は生殖細胞系列のミスマッチ修復遺伝子の変異。常染色体優性遺伝。
・リンチ症候群と診断された患者やその血縁者は、関連腫瘍の発生リスクが
高いことを考慮し、適切な定期検査が勧められる。
では、子宮体癌の診断は、どのようにして行われるのか?についても記載する。
--------------------------------------------------------------------------------------
◆組織型を判定するタイミング
摘出範囲などを決定するため、術前に子宮内膜細胞診や子宮内膜組織診(生検)を行い、組織型を推定する。しかし、この検査で分かる組織は全体の一部であるため、手術で摘出された検体で行われる最終組織診断と術前の組織診断が異なることがある。そのため、術後に追加治療が必要かどうかなどは、摘出された検体での最終組織診断をもとに決定される。

1)子宮内膜細胞診
主に子宮体がん検診で行われている検査。子宮内腔に細長い器具を挿入し子宮内膜の細胞を採取。顕微鏡でがん細胞や前がん病変の有無を検査する。検査結果がでるまでに1週間程度を要する。検査には痛みが伴う。

2)子宮内膜組織診(生検)
子宮内腔に細長い器具を挿入して子宮内膜の一部を採取し、顕微鏡で検査。組織診はより精密な検査。細胞診だけでは、がんの確定診断ができないため、正常な子宮内膜か?良性腫瘍(子宮内膜増殖症)か?前癌病変である子宮内膜異型増殖か?子宮体癌か?体がんの悪性度(グレード)の診断は?など鑑別するために最も重要な検査です。結果がでるまで1週間~10日程かかる。
外来での検査では診断が難しい場合、入院して麻酔下により広範囲の組織検査(子宮内膜全面掻爬術)を子宮鏡検査(内視鏡検査)と共に行うこともある。

3)子宮内膜全面掻爬術(ぜんめんそうは)
子宮内膜を一部検査する子宮内膜組織検査で診断確定できない場合(癌か内膜増殖症など)に、子宮内膜の全面を掻き出して組織を採取し顕微鏡で検査を行う。また、癌と鑑別を要するポリープなどに対しては、子宮鏡で子宮内をみて病巣を確認することもある。共に患者さんにかかる負担が大きい検査で、検査に要する時間も長くなるため、一泊入院で麻酔下に行う場合もある。結果がでるまで1週間~10日程かかる。

(上図説明)
子宮頸管拡張と子宮内掻爬術(この手法をD&Cとも呼ぶ)。子宮頸部を観察するために、膣口に膣鏡を挿入して拡張します(左図)。拡張器を用いて子宮頸部を拡張します(中央図)。子宮頸部から子宮方向へキューレット(スプーン状の器具)を挿入して異常な組織をかき出します(右図)。
4)画像診断
組織診で子宮体がんと診断されたら、病巣の大きさと拡がりを調べます。内診と各種の検査(経腟的超音波検査、CT検査、MRI検査など)を行い、がんが子宮の筋層や頸部まで浸潤していないか、遠くに転移していないかについて調べます。

(上図):経腟的超音波検査
膣、子宮、卵管、膀胱を調べるのに用いられる検査法。まず、超音波振動子(プローブ)を膣内に挿入し、高エネルギーの音波(超音波)を発生させ内部の組織や臓器に反射させることにより、エコーを生じさせます。このエコーを基にソノグラムと呼ばれる身体組織の画像が描出されます。医師はこのソノグラムを見ることによって腫瘍を発見することができます。
次の項目では、子宮内膜癌の前癌病変である子宮内膜(異型)増殖症について記載する。
5.子宮内膜増殖症について
子宮内膜増殖症(Endometrial hyperplasia)は、子宮内膜癌の一歩手前の状態、つまり前癌病変である。症状としては、子宮内膜が必要以上に増え、異常に厚くなってしまう状態。このうちの一部が子宮内膜癌へ進行するため検査が必要。40歳代に多い。
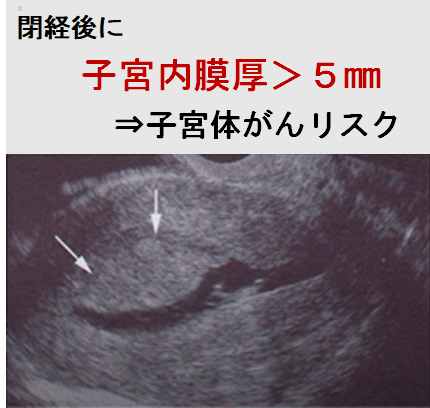
原因
女性ホルモンであるエストロゲンの作用過剰が原因として考えられる。肥満や月経不順の方は、エストロゲンの過剰分泌や刺激を引き起こすため、発症リスクが高いと考えられている。

分類
子宮内膜症は以下組み合わせにより4つに分類。
①異型の有無(細胞異型)
②単純型と複雑型(構造異型)
異型なし
⇒ 子宮内膜増殖症癌化の可能性は低い
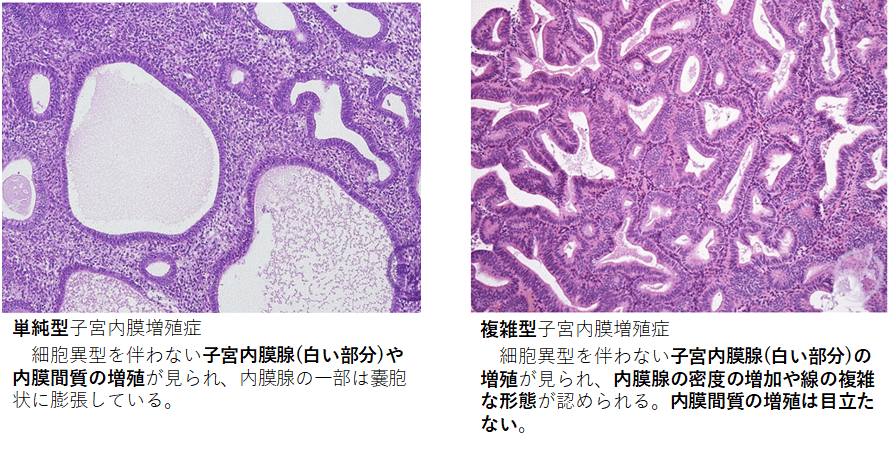
・単純型子宮内膜増殖症(構造異常なし/細胞異型なし)
・複雑型子宮内膜増殖症(構造異型あり/細胞異型なし)
異型あり
⇒ 前癌状態であると考えられている
・単純型子宮内膜異型増殖症(構造異常なし/細胞異型あり)
・複雑型子宮内膜異型増殖症(構造異型あり/細胞異型あり)
①異型か?異型でないのか?(細胞異型)
⇒細胞1つ1つの形が崩れているかどうかで2つに分類される。

②単純型か?複雑型か?(構造異型)
⇒子宮内膜組織の腺細胞(図の中にある白く丸い細胞)が正常か?複雑か?つまり、細胞がどのように連なっているか、全体の形が崩れているかで2つに分けられる。

◆類内膜癌

子宮内膜増殖症の種類と癌化率

疾患について
・症状に不正性器出血や過多月経などがあり、不妊症の原因になることも。
・診断は、経腟超音波検査や子宮内膜細胞を調べる検査(細胞診、組織診)を行う。
・異型のない単純型子宮内膜増殖症は、60%以上が自然に治る。
・異型のない子宮内膜増殖症は、自然に良くなることが多いため経過観察されるが、不正性器出血や過多月経が見られる場合は、ホルモン剤治療が行われる。
・増殖した細胞に、”がん”になりそうな細胞(異型細胞)がある場合は子宮内膜異型増殖症と呼ばれ注意する必要がある。
・子宮内膜異型増殖症の場合、20-30%程度でがんに進行すると言われており、子宮内膜増殖症が見つかった時に既にがんと合併している場合も多い。
・異型のある子宮内膜増殖症では、子宮内膜がん(子宮体がん)に進展するリスクが異型のない場合と比較し高いため、基本的には子宮全摘術を行う。
・手術を希望されない場合、高用量黄体ホルモン療法(MPA療法)が行われることもある。
次の項目では、子宮内膜癌の発生原因になっているエストロゲンについて、月経メカニズムと関連付けてまとめていく。
6.月経(生理)のメカニズム
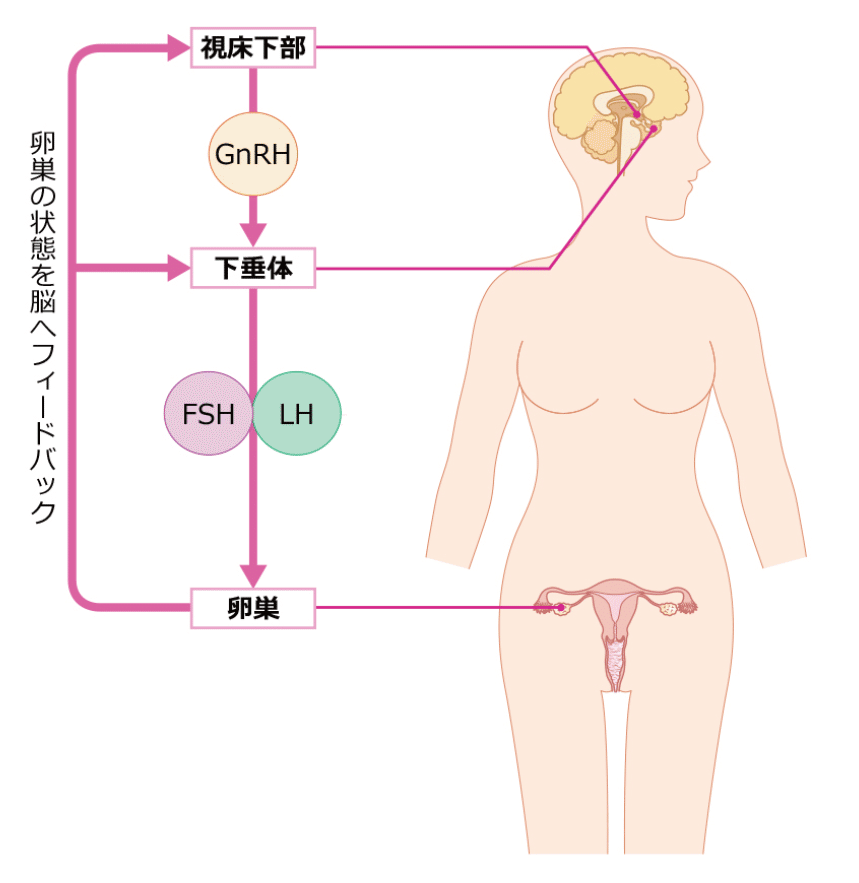
月経周期は、複数のホルモンによって調節されている。女性のからだは、脳の視床下部から分泌される「ゴナドトロピン放出ホルモン(性腺刺激ホルモン=GnRH)」によって支配され、卵胞の発育や成熟、排卵などの月経周期が正常に営まれている。
それでは、月経周期におけるメカニズムについて以下に記載していく。
--------------------------------------------------------------------------------------
◆卵胞期(月経開始日から14日目ぐらいまでの期間)
1)GnRHが脳の視床下部から分泌されると、脳の下垂体がそれを受けて卵胞刺激ホルモン(FSH)や黄体形成ホルモン(LH)が分泌される。つまり、ゴナドトロピン(性腺刺激ホルモン:脳下垂体から分泌されるホルモンの一種)に該当するFSHやLHが脳下垂体から分泌され、血流にのって卵巣まで移動する。

2)その後、卵巣に作用することで卵胞が発育し始め、卵巣(④)の中で卵子が排卵に向けて育つ。
3)さらに、卵子(③)が発育するにつれ(主席卵胞が20mmくらいに発育)、卵胞から大量に分泌されるエストロゲン(卵胞ホルモン)が子宮内膜(②)に働きかけることで子宮内膜を厚くしていく。つまり、子宮(①)の中で育つ赤ちゃんのためのお布団(子宮内膜)と栄養を準備していく。
--------------------------------------------------------------------------------------
◆排卵期(次の月経開始日のおよそ14日前)
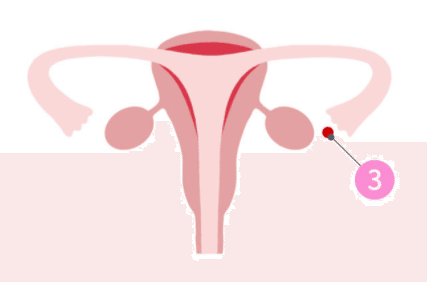
4)エストロゲン(卵胞ホルモン)の分泌がピークに達すると、”卵胞が十分に発育した”と身体が判断をし、黄体形成ホルモン(LH)の濃度が急激に高まる(=LHサージ)。そして卵子は成熟し、卵胞から卵子(③)が飛び出す。これが排卵です。
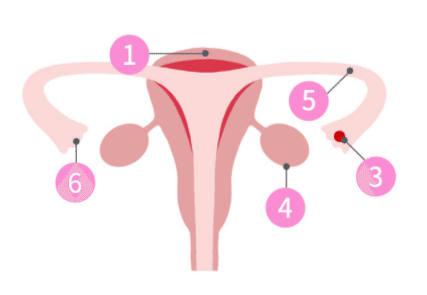
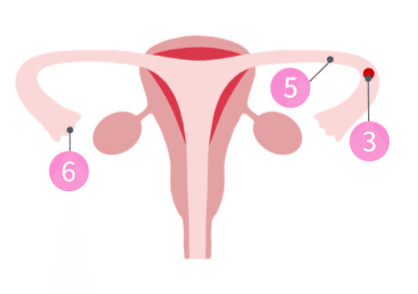
5)子宮(①)の上から卵巣(④)に向かって伸びているのが卵管(⑤)で、卵子(③)と精子および受精卵の通り道となる。卵巣と卵管はつながっていないので、排卵により卵巣から飛び出した卵子を卵管采(⑥)がキャッチ。卵管采(⑥)によってキャッチされた卵子(③)は、卵管(⑤)の中で精子を待つ。
--------------------------------------------------------------------------------------
◆黄体期(排卵後から月経が始まるまでの約14日間)
6)排卵後の卵胞は黄体に変化し、「プロゲストロン(黄体ホルモン)」と「エストロゲン(卵胞ホルモン)」を分泌する。プロゲステロン(黄体ホルモン)は厚くなった子宮内膜を、さらに受精卵が着床しやすい状態にする。
7)排卵した卵子と精子が結合して受精卵となり、子宮内膜に着床すれば妊娠成立となる。
--------------------------------------------------------------------------------------
◆月経
8)受精卵が着床しなかった(妊娠しなかった)場合、黄体は14日程度で寿命を迎え白体となり、プロゲストロン(黄体ホルモン)とエストロゲン(卵胞ホルモン)の分泌が減少。すると、不要になった子宮内膜は剥がれ落ちて血液とともに排出される。これが月経です。
--------------------------------------------------------------------------------------
エストロゲンとプロゲステロンの役割
卵巣から分泌される2種類の女性ホルモン。エストロゲンにより子宮内膜が増殖をし、排卵後の黄体から分泌されるプロゲステロン(黄体ホルモン)が子宮内膜の増殖をSTOPさせる役割をもつ。排卵が無い、月経不順といった人の場合、プロゲステロンが分泌されずエストロゲンの作用を受け続けることで、子宮内膜増殖症を引き起こし、ひいては子宮内膜癌に発展する危険性がある。
また、不妊治療においてエストロゲンおよびプロゲストロンが足りないと判断された場合、子宮内膜の増殖や肥厚を促すための薬として投与することもある。
エストロンゲン(卵胞ホルモン)
卵胞の発育と共に産生されるため、『卵胞ホルモン』ともいう。また、エストロゲンには3種類ある。
①エストロン(E1)
②エストラジオール(E2)
③エストリオール(E3)
性成熟期に働く主なエストロゲンは、エストラジオール(E2)である。エストラジオールは、エストロゲンの中で最も活性が強く、通常、検査で測定される血中エストロゲンの主成分となる。
プロゲストロン(黄体ホルモン)
主に黄体で作られるため、『黄体ホルモン』ともいう。受精卵が子宮内膜に着床しやすい状態に整え、着床(妊娠)後は妊娠を継続させる働きがある。また、体温をつかさどる脳の体温中枢に作用を及ぼし、基礎体温を上げる働きもあるため、排卵後、プロゲストロンが分泌されている間は、体温が高い状態が続き(=高温期)、0.3~0.6℃程度上昇する。

GnRH agonist(偽閉経療法)投与について
GnRH アゴニストとは、脳下垂体に働いて卵巣を刺激するホルモンの分泌を下げて卵巣の働きを抑える薬。胃酸で分解されてしまうため飲み薬としては使⽤できず、注射剤や点⿐薬として投与する。卵巣の働きが抑えられると卵巣から分泌される⼥性ホルモン(エストロゲン)が低下し、閉経したのと同じ状態になる(偽閉経療法とも呼ばれる)。GnRH アゴニストは⼦宮内膜症や⼦宮筋腫、子宮腺筋症の治療薬として使⽤されている。
http://www.nagano-med.jrc.or.jp/department/section/regimen/gnrh.pdf
次の項目では、子宮内膜癌の組織型におけるグレード分類などについて、更に深堀していく。
7.子宮内膜癌の組織型グレード分類
近年、子宮体癌は臨床病理学的、分子病理学的観点からⅠ型とⅡ型に区別されるようになった。前述したが、Ⅰ型はエストロゲン依存症の腫瘍で、類内膜癌と粘液性癌を含むのに対し、漿液性癌や明細胞癌に代表されるⅡ型はエストロゲン非依存症の特殊組織型腫瘍で、主に閉経後の高齢者の委縮粘膜を背景に de novo に発生する(直接、癌が発生)。
日本婦人科腫瘍学会ガイドライン検証委員会が2017年に報告した国内症例解析によると、特殊組織型(Ⅱ型)の頻度は子宮体癌の10%以上を占め、漿液性癌が4.0%、明細胞癌が2.3%と、いずれも増加傾向を示している。
また、Ⅰ型G3(低分化型)の類内膜癌およびⅡ型の漿液性癌、明細胞癌はともに悪性度が高く予後不良であるため、同様に扱われる傾向にある。日本産科婦人科学会による報告では、全体の5年生存率がG1およびG2の類内膜癌では95%、90%と良好であるのに対して、G3では77%、漿液性癌および明細胞癌で60~65%と不良である。
子宮体癌治療ガイドライン 2018年版より
https://jsgo.or.jp/guideline/taigan/2018/taigan2018_04.pdf
ここからは、この組織型分類された各疾患について、グレード分類も含め、まとめていく。
--------------------------------------------------------------------------------------
◆類内膜がん(Ⅰ型:もっとも多い組織型)
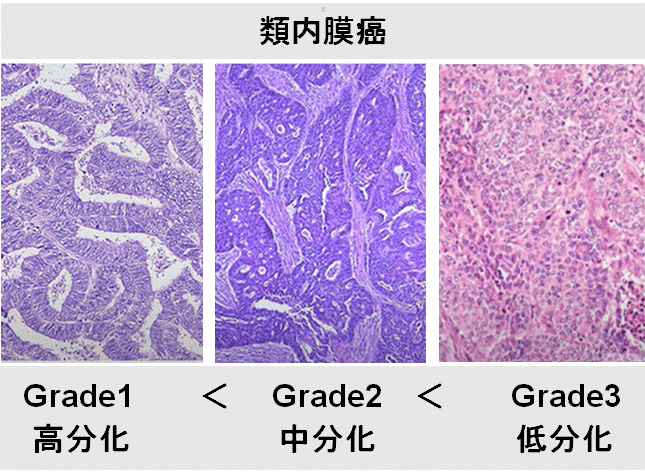
子宮内膜癌でもっとも多い組織型である類内膜がん。構造によりグレード(*)G1、G2、G3の3種類に分けられる(数字が大きくなるほど悪性度は高まる)。グレード分類の定義は、顕微鏡で見たときの組織像の中での充実部(*)の割合で決まる。
グレード(異型度*)分類
G1(高分化型):充実性増殖をする(増殖スピードが速い)部分が5%以下
G2(中分化型):充実性増殖をする部分が5~50%
G3(低分化型):充実性増殖をする部分が50%を超える
*充実部:がんが密集して個々の区別がつかなくなった状態
*異型度:定められたGradeの訳語(取扱い規約 病理編に限り改訂)
分化度に関する補足
一個の受精卵から発生した細胞は、分裂増殖を繰り返し皮膚や粘膜、神経などへと組織固有の形態・機能を持った成熟した細胞へと変化していく。これを細胞分化という。
しかし、がん細胞では細胞増殖が活発に速く行われるため、細胞が十分に成熟することができず(細胞の幼若化という)、未熟な細胞(低分化細胞や未分化細胞)が見られるようになる。
一般的に、高分化ほど細胞の成熟度が高く、比較的悪性度が低いといえる。反対に、低分化ほど悪性度が高く、転移・再発が多く見られる傾向がある。
--------------------------------------------------------------------------------------
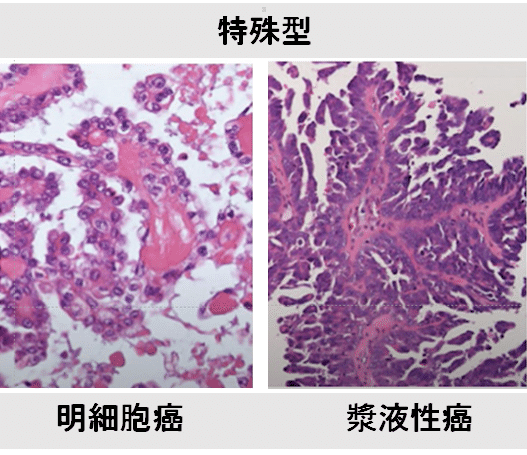
◆非類内膜がん(Ⅱ型:特殊組織型内膜がん)
類内膜がん以外の組織型には、主に漿液性がんと明細胞がんがある。稀に扁平上皮がん、移行上皮がん、小細胞がん、混合がん、未分化がんなどもある。繰り返しになるが、これら組織型は類内膜がんに比べ悪性度が高い。
--------------------------------------------------------------------------------------
組織学的分類に基づき、もう少し深堀る(子宮体癌治療ガイドライン 2018年より)。
組織学的分類
子宮体癌の組織学的分類はWHO分類が国際基準となっており、2014年に第4版が出版された。日本産科婦人科学会では、これらの改訂に本邦の実情を合わせ、取扱い規約の病理編(2017年7月出版)に限って改訂が成し遂げられた。その主な改訂点を以下にまとめる。
主な改訂点
(*子宮体がん取扱い規約 病理編 第4版に限り改訂。2014年にWHOから提示された新しい組織学的分類を参考)
①子宮内膜増殖症は、異型のないものと異型のあるものに二分され、細胞異型に重きをおくことが明示された。後者の子宮内膜異型増殖症に対しては、類内膜上皮内腫瘍(EIN:endometrioid intraepithelial neoplasia)が同義語として位置付けられた。
②類内膜腺癌(endometrioid adenocarcinoma)は類内膜癌(endometrioid carcinoma)とよばれるようになり、他の腺癌も『腺:adeno』が無い形となった。
③Gradeの訳語は『異型度』と定められた。これによって子宮内膜間質肉腫に用いられてきた「悪性度」も「異型度」に変更された。
④Ⅰ型(エストロゲン依存症)とⅡ型(エストロゲン非依存症)からなる混合癌では、Ⅱ型に属する腫瘍割合が10%以上から5%以上に変更された。
⑤脱分化癌(dedifferentiated carcinoma)が新たに加わった。
⑥高異型度子宮内膜間質肉腫(high-grade endometrial stromal sarcoma)が再び疾患単位として明記された。
⑦未分化子宮内膜肉腫(undifferentiated endometrial sarcoma)が未分化子宮肉腫(undifferentiated uterine sarcoma)に変更された。
⑧神経内分泌腫瘍が独立し、低異型度神経内分泌腫瘍と高異型度神経内分泌癌に二分された。前者にはカルチノイド腫瘍、後者には小細胞神経内分泌癌と大細胞神経内分泌癌が含まれる。
⑨扁平上皮癌(squamous cell carcinoma)、移行上皮癌(transitional cell carcinoma)、癌線維腫(carcinofibroma)が項目から削除された。
以下(Ⅰ~Ⅵ)は、組織学的分類に基づき整理したもの。
Ⅰ 上皮性腫瘍および前駆病変(Epithelial tumors and precursors)
A.前駆病変(Precursors)
1.子宮内膜増殖症(Endometrial hyperplasia without atypia)
2.子宮内膜異型増殖症(Atypical endometrial hyperplasia)/
類内膜上皮内腫瘍(EIN:Endometrioid intraepithelial neoplasia)
B.子宮内膜癌(Endometrial carcinomas)
1.類内膜癌(Endometrioid carcinoma)
a.扁平上皮への分化を伴う類内膜癌(Endometrioid carcinoma with squamous differentiation)
b.絨毛腺管型類内膜癌(Endometrioid carcinoma with villoglandular variant)
c.分泌型類内膜癌(Endometrioid carcinoma with secretory variant)
2.粘液性癌(Mucinous carcinoma)
3.漿液性子宮内膜上皮内癌(Serous endometrial intraepithelial
carcinoma)
4.漿液性癌(Serous carcinoma)
5.明細胞癌(Clear cell carcinoma)
6.神経内分泌腫瘍(Neuroendocrine tumors)
a.低異型度神経内分泌腫瘍(Low-grade neuroendocrine tumor:
NET)
(1)カルチノイド腫瘍(Carcinoid tumor)
b.高異型度神経内分泌癌(High-grade neuroendocrine carcinoma:
NEC)
(1)小細胞神経内分泌癌(Small cell neuroendocrine carcinoma:
SCNEC)
(2)大細胞神経内分泌癌(Large cell neuroendocrine
carcinoma:LCNEC)
7.混合癌(Mixed cell carcinoma)
8.未分化癌(Undifferentiated carcinoma)/
脱分化癌(Dedifferentiated carcinoma)
C.類腫瘍病変(Tumor-like lesions)
1.子宮内膜ポリープ(Endometrial polyp)
2.化生(Metaplasias)
3.アリアス-ステラ反応(Arias-Stella reaction)
4.リンパ腫様病変(Lymphoma-like lesion)
子宮に発生する間葉系腫瘍(*)は下記にあるように、平滑筋腫瘍と子宮内膜間質腫瘍、その他の稀な腫瘍に大別される。平滑筋腫と平滑筋肉腫は鑑別が難しい場合があり、形態学的にその判断ができないものは悪性度不明の平滑筋腫瘍(STUMP)と診断される。核異型、核分裂数、壊死の評価が診断に重要である。また類粘液型、類上皮型の亜型もあり、診断において配慮を要する。
子宮内膜間質腫瘍は、子宮内膜間質結節、低異型度子宮内膜間質肉腫、高異型度子宮内膜間質肉腫に分類され、未分化子宮肉腫も関連腫瘍として認識されている。高異型度子宮内膜間質肉腫はその概念が否定されていた時期もあったが、核形態の均一性と高度の核異型という観点から再認識され、YWHAE-FAM22 融合遺伝子の存在が証明されるに及んでその概念が改めて認められた。最近、ZC3H7B-BCOR 融合遺伝子を有する子宮内膜間質肉腫、卵巣性索間質腫瘍に類似した子宮腫瘍(UTROSCT)、血管周囲性類上皮細胞腫瘍(PEComa)、炎症性筋線維芽細胞腫瘍(IMT)も注目されている。
Ⅱ 間葉性腫瘍(Mesenchymal tumors)
A.平滑筋腫(Leiomyhoma) *平滑筋腫:良性腫瘍
1.富細胞平滑筋腫(Cellular leiomyoma)
2.奇怪核を伴う平滑筋腫(Leiomyoma with bizarre nuclei)
3.活動性核分裂型平滑筋腫(Mitotically active leiomyoma)
4.水腫状平滑筋腫(Hydropic leiomyoma)
5.卒中性平滑筋腫(Apoplectic leiomyoma)
6.脂肪平滑筋腫(Lipoleiomyoma)
7.類上皮平滑筋腫(Epithelioid leiomyoma)
8.類粘液平滑筋腫症(Myxoid leiomyoma)
9.解離性(胎盤分葉状)平滑筋腫(Dissecting (cotyledonoid)
leiomyoma)
10.びまん性平滑筋腫症(Diffuse leiomyomatosis)
11.静脈内平滑筋腫症(Intravenous leiomyomatosis)
12.転移性平滑筋腫(Metastasizing leiomyoma)
B.悪性度不明な平滑筋腫瘍(Smooth muscle tumor of uncertain
malignant potential:STUMP)
C.平滑筋肉腫(Leiomyosarcoma) *平滑筋肉腫:悪性腫瘍
1.類上皮平滑筋肉腫(Epithelioid leiomyosarcoma)
2.類粘液平滑筋肉腫(Myxoid leiomyosarcoma)
D.子宮内膜間質腫瘍と関連病変(Endometrial stromal and related
tumors)
1.子宮内膜間質結節(Endometrial stromal nodule)
2.低異型度子宮内膜間質肉腫(Low-grade endometrial stromal
sarcoma:LG-ESS)
3.高異型度子宮内膜間質肉腫(High grade endometrial stromal
sarcoma)
4.未分化子宮肉腫(Undifferentiated uterine sarcoma:EUS)
5.卵巣性索腫瘍に類似した子宮腫瘍(Uterine tumor resembling
ovarian sex cord tumor:UTROSCT)
E.その他の間葉性腫瘍(Miscellaneous mesenchymal tumors)
1.横紋筋肉腫(Rhabdomyosarcoma)
2.血管周囲性類上皮細胞腫(Perivascular epithelioid cell tumor:
PEComa)
3.その他(Others)
Ⅲ 上皮性・間葉性腫瘍(Miscellaneous mesenchymal tumors)
A.線筋腫(Adenomyoma)
B.異型ポリープ状線筋腫(Atypical polypoid adenomyoma)
C.腺線維腫(Adenofibroma)
D.腺肉腫(Adenosarcoma)E.癌肉腫(Carcinosarcoma)
Ⅳ その他の主要(Miscellaneous tumors)
A.アデノマトイド腫瘍(Adenomatoid tumor)
B.神経外胚葉性腫瘍(Neuroectodermal tumors)
C.胚細胞腫瘍(Germ cell tumors)
Ⅴ リンパ性および骨髄性腫瘍(Lymphoid and myeloid tumors)
A.リンパ腫(Lymphomas)
B.骨髄性腫瘍(Myeloid neoplasms)
Ⅵ 二次性腫瘍(Secondary tumors)
子宮体癌取扱い規約 病理編 第4版(2017年7月) 金原出版より
次の項目では、子宮内膜癌からは少し離れるが、上記の組織学的分類にあった子宮肉腫(間葉系腫瘍)についての理解を深めていく。
8.子宮肉腫(Uterine sarcoma)とは?
まず肉腫(Sarcoma:サルコーマ)とは、全身の骨(硬組織)や軟部組織(骨格以外の支持組織のこと:筋肉、脂肪、神経、血管など)にできる悪性腫瘍の総称。または、上皮以外の非上皮性細胞(間葉系細胞:骨、軟骨、筋肉、脂肪、血管、末梢神経、線維組織など)から発生するがんのこと。

婦人科臓器では主に、子宮の筋肉や間質などの組織から発生し、そのほとんどが子宮体部にできる。つまり、子宮肉腫とは・・・
『子宮の筋肉や子宮内膜の間質細胞(結合組織である細胞)に発生する悪性腫瘍』のこと。

肉腫の腫瘍としての特徴は、その希少性と多様性(多種多様なこと)にある。悪性腫瘍全体に占める肉腫の割合は約1%に過ぎない。子宮肉腫は希少がん、かつ、再発可能性の高い難治がんであり、診断と治療には確たるものがないのが実情。繰り返しになるが、良性の子宮筋腫との判別が難しく、子宮内膜から発生する子宮内膜がんとは異なる。
「子宮肉腫」と「子宮筋腫」の違い
2つの疾患の違いは何か?と問われると、それは良性か悪性かの違い。良性のものを子宮筋腫、悪性のものを子宮肉腫(がん肉腫や平滑筋肉腫など)に分類している。また、子宮肉腫は非常に稀な疾患である。両疾患に共通するのは、子宮の筋肉層から発生する腫瘍という点と、(膣式)超音波検査でみても非常に判別が難しく問題となっている点である。
子宮肉腫の疫学
2004年統計によると、子宮肉腫は毎年約800人に発生すると推測されている。子宮体がん全体では年間1万人程度が発症すると考えられているため、子宮体部にできる悪性腫瘍の約8%を占めることになる。

がん登録・統計(国立がん研究センターがん情報サービス)より
https://ganjoho.jp/reg_stat/statistics/stat/summary.html
(2004年統計。子宮体部悪性腫瘍罹患者数:11,092人)
内訳を以下に示す。
国立がん研究センター 希少がんセンターより
(https://www.ncc.go.jp/jp/rcc/about/uterine_sarcoma/index.html)
① 癌肉腫(46%、約360人)
② 平滑筋肉腫(36%、280人)
③ 子宮内膜間質肉腫(13%、約100人)
④ 腺肉腫(かなり稀な疾患)
--------------------------------------------------------------------------------------
癌肉腫
癌の成分と肉腫の成分をもつ腫瘍で、子宮肉腫のなかで最も多くみられる。閉経後の高齢者に多く、平均年齢は60歳代。不正性器出血が代表的な症状で、下腹部痛を伴うこともある。子宮体癌と臨床的に似ている点があるものの、子宮体癌より悪性度が高い疾患である。
また、がん肉腫は、腫瘍病態的に子宮体がんと類似した腫瘍であると考えられており、国内外の治療ガイドラインには「子宮体がんの高悪性度と同様に治療するべし」と記載されている。全体の50%生存期間(mOS)は28カ月と未だ予後不良な疾患で、化学療法(抗がん剤)の選択や再発時の治療などについてもこれからさらに研究が必要。
--------------------------------------------------------------------------------------
子宮平滑筋肉腫
子宮の筋肉にできる悪性軟部腫瘍で、子宮肉腫の中では多くみられるものの、子宮すべての悪性腫瘍に占める割合は1~2%程度と稀。手術前に診断確定することが難しく、半数以上は子宮筋腫として手術を受け、組織を検査して初めて分かる。
残念ながら未だ予後不良な疾患。厚生労働省の報告ではⅠ期からⅣ期までまとめた50%生存期間(mOS)が31カ月だった。ノルウェーの報告でもⅠ期で8年、Ⅱ期で4年、Ⅲ期で2年、Ⅳ期で1年と不良。術前診断は難しく、「子宮筋腫」として治療され、子宮摘出または筋腫摘出によりはじめて診断がつくことも少なくない。病理組織をみても悪性とも良性とも断言できない「悪性度不明な平滑筋腫瘍(STUMP)」という診断になることもある。
Ⅰ期の患者でも約半数が再発する。再発予防として術後化学療法を行う試みもあるが、現時点で十分な根拠をもって「術後の再発予防に貢献している」と断言できる抗がん剤はないのが実情。放射線治療も再発抑制に寄与しないことがほぼ明らかになっている。そのため、施設によっては肉眼的に病変が残っていないと考えられる患者に対しては術後治療を行わずに経過観察し、再発が確認できた時点で治療開始するようにしているところもある。
--------------------------------------------------------------------------------------
子宮内膜間質肉腫
子宮内膜の間質細胞(結合組織である細胞)にできる悪性軟部腫瘍。腫瘍の発生や組織の違いから「低異型度子宮内膜間質肉腫」(LGESS)、「高異型度子宮内膜間質肉腫」(HGESS)と「未分化子宮肉腫」(UUS)に分かれる。いずれも、不正性器出血や過多月経、出血に伴う下腹部痛などの症状がみられる。
子宮内膜間質肉腫はかつて低悪性度(LG-ESS)と高悪性度に分類されていた。しかし、高悪性度間質肉腫は子宮内膜間質との類似性が必ずしも認められないとの理由で、現行のWHO分類では、高悪性度子宮内膜間質肉腫を未分化子宮内膜肉腫(UES)と呼んでいる。(子宮体がん取扱い規約 病理編 第4版(2017年7月出版)に限った改訂項目として、未分化子宮肉腫:USSに変更)
LG-ESSは比較的予後良好で、mOSが76カ月と報告されている。UESは非常に予後不良であるため、国内外のガイドラインでは”LG-ESS”と”UES”を別項目にして記載している。
LG-ESSも平滑筋肉腫と同様に術前診断は難しく、筋腫や腺筋症として摘出した標本ではじめて診断されることが多くある。ときには摘出標本でも変性筋腫などと誤られ、再発したときに見直してはじめてLG-ESSであると診断される場合もある。エストロゲンやプロゲステロンの受容体を発現していることが多く、ホルモン療法が有効。この点が他の子宮肉腫と大きく異なる点で、再発してもホルモン治療で長期生存を見込めることも少なくない。
--------------------------------------------------------------------------------------
腺肉腫
子宮内膜の腺(分泌物を排出する器官)に発生する悪性軟部腫瘍で、発生頻度は癌肉腫の10%程度と、非常に稀です。発症年齢は癌肉腫よりも若いとされている。
--------------------------------------------------------------------------------------
そして、これらは以下2つに分類される。
◆上皮性・間葉性混合腫瘍
⇒がん肉腫(carcinosarcoma)、腺肉腫(adenosarcoma)
◆間葉性(非上皮性)腫瘍
⇒平滑筋肉腫(leiomyosarcoma)、子宮内膜間質肉腫(endometrial stromal sarcoma)など
また、子宮内膜間質肉腫の3分類について再掲(用語の整理)。
◆低異型度(低悪性度)子宮内膜間質肉腫
(LG-ESS:Low-Grade Endometrial Stromal Sarcoma)
◆高異型度(高悪性度)子宮内膜間質肉腫
(HG-ESS:High-Grade Endometrial Stromal Sarcoma)
◆未分化子宮肉腫(UUS:undifferentiated uterine sarcoma)
用語の改訂内容について以下に記載。
『子宮体がん取扱い規約 病理編 第4版』(2017年7月出版)に限った、改訂内容項目。
【改訂内容】
①Gradeの訳語は『異型度』と定められた。これによって子宮内膜間質肉腫に用いられてきた「悪性度」も「異型度」に変更。また、高異型度子宮内膜間質肉腫(HG-ESS:high-grade endometrial stromal sarcoma)が再び疾患単位として明記された。
②未分化子宮内膜肉腫(UES:undifferentiated endometrial sarcoma)
⇒ 未分化子宮肉腫(UUS:undifferentiated uterine sarcoma)に変更。
がん登録・統計(国立がん研究センターがん情報サービス)
https://ganjoho.jp/reg_stat/statistics/stat/summary.html
国立がん研究センター 希少がんセンター
https://www.ncc.go.jp/jp/rcc/about/uterine_sarcoma/index.html
子宮肉腫の治療
子宮体癌(子宮内膜癌)の治療の第一選択は手術療法である。子宮全摘術、両側付属器摘出術を基本として骨盤・傍大動脈リンパ節郭清(生検)、大網切除術、腹腔細胞診などが行われる。
また、子宮肉腫の治療も手術療法が第一選択であり、子宮癌肉腫の場合は骨盤・傍大動脈リンパ節郭清が考慮されるが、子宮平滑筋肉腫に対してのリンパ節郭清の有効性は明らかではない。
「子宮全摘術」+「両側付属器切除術」+「骨盤・傍大動脈リンパ節郭清」+「大網切除」+「腹腔細胞診」
(*)子宮平滑筋肉腫でのリンパ節郭清の有効性は明らかでない
★子宮肉腫の進行期分類
ポイントは以下2点。
①癌肉腫は、子宮内膜癌の進行期分類を使用する。
②平滑筋肉腫/子宮内膜間質肉腫と、腺肉腫とでは、TⅠ分類が異なる。
①に関する補足説明。癌肉腫に限り子宮内膜癌と同じ進行期分類を用いることになっているが、その理由は、癌肉腫がその発生や病態において子宮内膜癌により近いためである。
進行期分類に関する補足事項
子宮体部肉腫の進行期分類は、これまで子宮内膜癌の進行期分類(FIGO 1988)が適用され、1996年刊行の『子宮体がん取扱い規約 第2版』に記載されたが、子宮内膜癌とは異なる本腫瘍の「Biological behavior」を反映させた進行期分類の必要性が高まり、子宮体部肉腫の進行期分類が新たに作成され、FIGO(2008年)ならびに日本産科婦人科学会(2014年)で承認され、『子宮体がん取扱い規約 病理編 第4版』(2017年7月)に掲載された。この中で、平滑筋肉腫/子宮内膜間質肉腫と腺肉腫はT1の分類が異なる点に注意が必要である。なお、癌肉腫は子宮肉腫の進行期分類ではなく、子宮内膜癌の進行期分類を使用(*)することが決められている。
子宮体がん治療ガイドライン2018年版より抜粋
https://jsgo.or.jp/guideline/taigan/2018/taigan2018_02.pdf
各疾患(癌肉腫、平滑筋肉腫/子宮内膜間質肉腫、腺肉腫)の進行期分類は以下になる。
--------------------------------------------------------------------------------------
◆癌肉腫 進行期分類
・子宮内膜癌と同じ進行期分類を用いる。

--------------------------------------------------------------------------------------
◆平滑筋肉腫および子宮内膜間質肉腫 進行期分類
・がん肉腫は除く。
・平滑筋肉腫/子宮内膜間質肉腫と腺肉腫は、TⅠ分類が異なる。

--------------------------------------------------------------------------------------
◆腺肉腫 進行期分類

次の項目では、再び子宮内膜癌に戻り、そのリスク分類について整理していく。
9.術後再発リスク分類
子宮体癌の第1選択は手術療法であり、摘出標本による組織学的検索が行われた後に進行期が決定される(手術で採取したがん細胞の状態、組織型、悪性度などから再発リスクを推測したうえで、術後治療を決定)。
その後、症例は術後再発リスクの評価に基づいてリスク分類され、術後補助療法が考慮される。子宮体癌は組織型により予後が異なることが判明しており、3つのグループに分けられる。
<予後の異なる組織型3グループ>
①最も予後が良い類内膜癌G1/G2
②次に予後が良い、類内膜癌G3
③最も予後が悪い漿液性癌/明細胞癌
そして、症例がどの組織型のグループに属し、どのようなリスク因子を有しているかにより、低リスク群、中リスク群、高リスク群に分類されることになる。下図に示すリスク分類は、『子宮体がん治療ガイドライン 2013年版』を踏襲した再発リスク分類を用いて作成されたものである。なお、臨床試験によって異なったリスク分類が採用されており、現時点で完全にコンセンサスを得た分類はない。

【用語補足】
脈管侵襲・・・血管やリンパ管に広がっている。
頸部間質浸潤あり・・・子宮頸部に広がっている。
子宮外病変あり・・・子宮の周りに広がっている。
子宮体がん治療ガイドライン2018年版より
https://jsgo.or.jp/guideline/taigan/2018/taigan2018_02.pdf
【低リスク】
・類内膜腺がんで悪性度が低い(G1,G2)
・がんの広がりが筋層浸潤1/2未満(ステージⅠA期)
・脈管侵襲(血管やリンパ管に入り込むこと)がない
・頸部浸潤なし
・遠隔転移なし
・腹腔細胞診陰性
【中リスク】
・類内膜がんで悪性度が低く(G1,G2)
・脈管侵襲を認め、筋層の1/2以上(ステージⅠB期以上)に広がる。
・悪性度の高い類内膜がん(G3)で、がんの広がりが筋層浸潤1/2未満にとどまっている。
・組織型が漿液性がん、明細胞がん(typeⅡ型)であるが、がんの広がりが筋層内へ認めない。
・頸部浸潤あり
・腹腔細胞診陽性
・遠隔転移なし
【高リスク】
・類内膜がんで悪性度が高く(G3)、筋層の1/2以上に広がっている。
・漿液性がん、明細胞がんで脈管侵襲を認める、又は筋層に広がっている。
・組織型、悪性度にかかわらず、子宮頸部または子宮の周りに広がっている(ステージⅡ期以上)。
・付属器・漿膜・基靭帯進展あり
・腟壁浸潤あり
・骨盤あるいは傍大動脈リンパ節転移あり
・膀胱・直腸浸潤あり
・腹腔内播種あり
・遠隔転移あり
https://medicalnote.jp/contents/200806-006-YS
次では、進行期分類について整理していく。
10.手術進行期分類
子宮体癌に対する本邦の進行期分類は、下記の国際的機関によって提案された規則を基に、国際標準に準拠した規約にするために『子宮体癌取扱い規約』として日本産科婦人科学会によって策定されてきた。
【国際的機関】
FIGO(International Federation of Gynecology Obstetrics)
UICC(Union for International Cancer Control)
WHO(World Health Organization) etc
進行期分類の歴史
まず、1987年に最初の『子宮体がん取扱い規約 第1版』が発刊され、子宮体癌の進行期は術前に決定される、いわゆる臨床進行期分類が用いられてきた(日産婦 1983、FIGO 1982)。
その後、1996年に改訂版の『子宮体癌取扱い規約 第2版』が発刊され、術後に進行期を決定する手術進行期分類が採用された。
さらに、2008年にFIGO進行期の改定案が出され、本邦では2012年に日本産科婦人科学会、日本病理学会、日本医学放射線学会、日本放射線腫瘍学会の協力のもと、FIGO改定案に合わせた『子宮体癌取扱い規約 第3版』が発刊された。しかし、FIGOとWHOの改訂は必ずしも呼応するものではなく、2014年にWHOから新しい組織学的分類が提示された。
その後、日本産科婦人科学会では最新のWHO分類を本邦の実情に合わせた新たな取扱い規約を策定し、『子宮体癌取扱い規約 病理編 第4版』が2017年7月に出版された。
本治療ガイドラインでの本文中の進行期分類に関しては、原則として『子宮体癌取扱い規約 病理編 第4版』に準じて記載している。第4版(2017年発刊)での進行期分類は第3版(2012年発刊)を基本としているが、注意事項の文言が多少変更となっている。

詳細な手術進行期分類については以下に記載するが、簡潔にまとめると・・・「Ⅰ期では癌が子宮体部に限局」、「Ⅱ期では子宮頸部に広がった状態」、「Ⅲ期は付属器に転移」、「ⅢC期でリンパ節への転移」、そして「Ⅳ期が膀胱や直腸などへの遠隔転移」となる。また、Ⅲ期までなら手術が可能となる。
--------------------------------------------------------------------------------------
1.子宮内膜癌
(1)子宮内膜癌 手術進行期分類(日産婦 2011、FIGO 2008)
Ⅰ期:癌が子宮体部に限局するもの
ⅠA期:癌が子宮筋層1/2未満のもの
ⅠB期:癌が子宮筋層1/2以上のもの

--------------------------------------------------------------------------------------
Ⅱ期:癌が頸部間質に浸潤するが、子宮をこえていないもの(*)
(*)頸管腺浸潤のみは、Ⅱ期ではなくⅠ期とする。

--------------------------------------------------------------------------------------
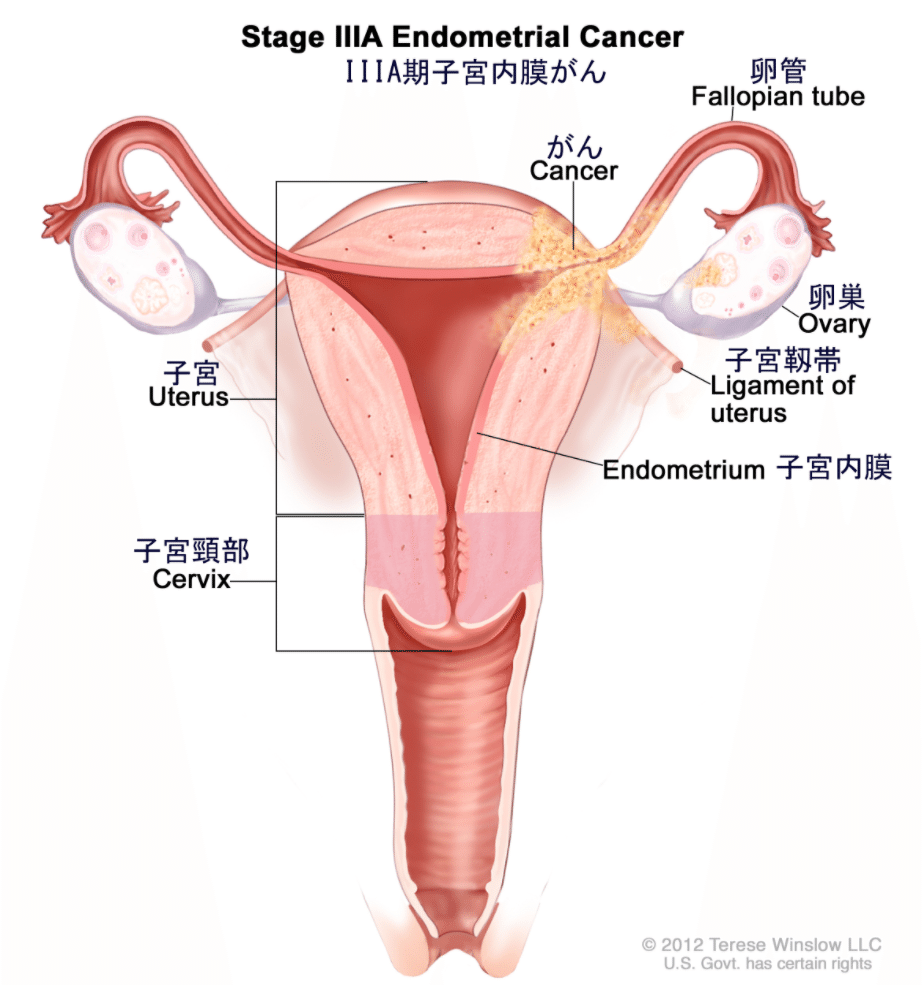
Ⅲ期:癌が子宮外に広がるが、小骨盤腔をこえていないもの。または、所
属リンパ節(*)へ広がるもの。
ⅢA期:子宮漿膜ならびに/あるいは付属器を侵すもの
ⅢB期:膣ならびに/あるいは子宮傍組織へ広がるもの
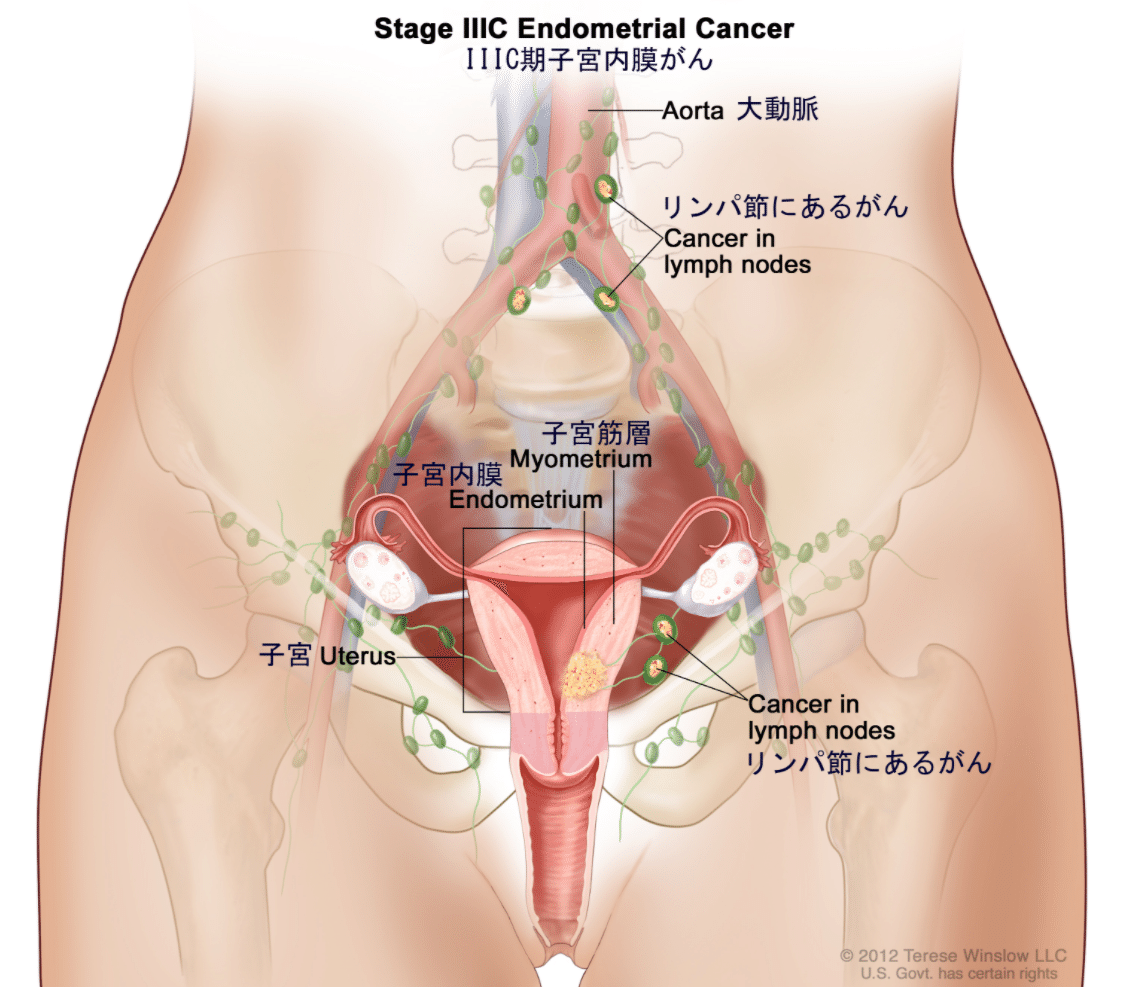
ⅢC期:骨盤リンパ節ならびに/あるいは傍大動脈リンパ節転移のある
もの
ⅢC1期:骨盤リンパ節転移陽性のもの
ⅢC2期:骨盤リンパ節への転移の有無にかかわらず、傍大動脈リンパ
節転移陽性のもの
(*)所属リンパ節
骨盤リンパ節と傍大動脈リンパ節をいう。
(*)骨盤リンパ節
基靭帯リンパ節、仙骨リンパ節、閉鎖リンパ節、外腸骨リンパ節、鼠径上リンパ節、内腸骨リンパ節、総腸骨リンパ節

--------------------------------------------------------------------------------------
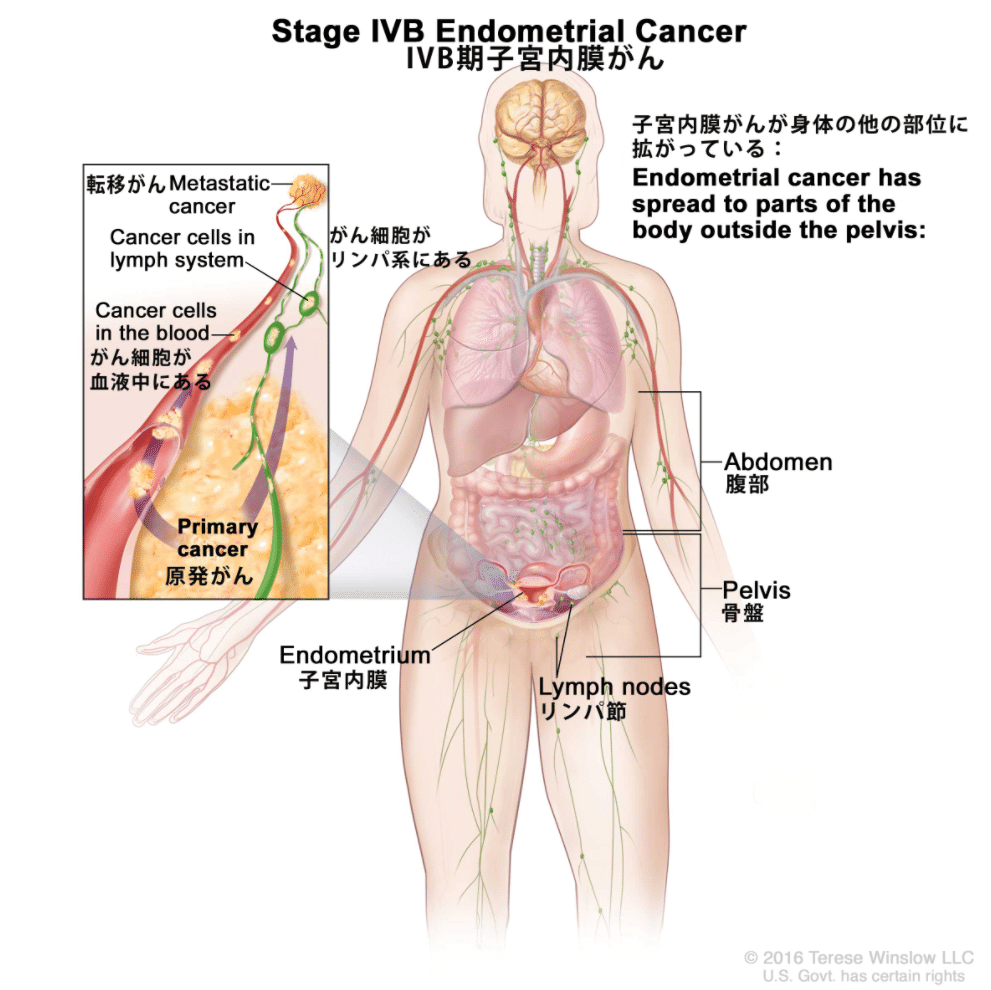
Ⅳ期:癌が小骨盤腔をこえているか、明らかに膀胱ならびに/あるいは腸
粘膜を侵すもの、ならびに/あるいは遠隔転移のあるもの
ⅣA期:膀胱ならびに/あるいは腸粘膜浸潤のあるもの
ⅣB期:腹腔内ならびに/あるいは鼠経リンパ節転移を含む遠隔転移の
あるもの

--------------------------------------------------------------------------------------
[注釈]
注1:すべての類内膜癌は腺癌成分の形態により、Grade1,2,3に分類。
注2:腹腔洗浄細胞診陽性の予後因子としての重要性については一貫した報
告がないので、ⅢA期から細胞診は除外されたが、将来再び進行期決
定に際し、必要な推奨検査として含まれる可能性があり、全ての症例
でその結果は登録の際に記録することとした。
注3:子宮内膜癌の進行期分類は癌肉腫にも適用される。癌肉腫、明細胞
癌、漿液性癌(漿液性子宮内膜上皮内癌を含む)においては、横行結
腸下の大網の十分なサンプリングが推奨される。
[分類にあたっての注意事項]
(1)初回治療として手術がなされなかった症例(放射線や化学療法など)の進行期は、MRI、CTなどの画像診断で日産婦 2011 進行期分類を用いて推定する。
(2)各期とも腺癌の組織学的分化度/異型度を併記する。
(3)従来、子宮内膜異型増殖症は日産婦 1995 分類により0期として登録してきたが、FIGO 2008 分類に従い0期のカテゴリーを削除する。子宮内膜異型増殖症は別に登録を行う。
(4)所属リンパ節とは骨盤リンパ節(基靭帯リンパ節、仙骨リンパ節、閉鎖リンパ節、外腸骨リンパ節、鼠径上リンパ節、内腸骨リンパ節、総腸骨リンパ節)と傍大動脈リンパ節をいう。
(5)本分類は手術後分類であるから、従来Ⅰ期とⅡ期の区別に用いられてきた部位別掻爬(そうは:治療や診断のため、子宮内膜をかきとること)などの所見は考慮しない。
(6)子宮筋層の厚さは腫瘍浸潤の部位において測定することが望ましい。
(7)腹水(洗浄)細胞診陽性は、進行期決定には採用しないが、別に記録する。
(8)従来Ⅱa 期(FIGO 1988)であった頸管腺のみに癌が及ぶものは、FIGO 2008 進行期分類ではⅠ期に分類する。
(9)従来のⅠa 期(FIGO 1988)(癌が子宮内膜に限局するもの)と筋層浸潤が1/2未満のものをFIGO 2008 進行期分類ではⅠA期とし、筋層浸潤が1/2以上のものをⅠB期としている。
(子宮体癌取扱い規約 病理編 第4版(2017年)、金原出版より)
画像は、がん情報サイトより抜粋
(https://cancerinfo.tri-kobe.org/summary/detail_view?pdqID=CDR0000062903&lang=ja#Reference_1.7)
(2)子宮内膜癌 TMN 分類(UICC 第8版に準じる)


子宮体がん治療ガイドライン2018年版
子宮内膜癌 手術進行期分類(日産婦2011、FIGO2008)より抜粋。
(https://jsgo.or.jp/guideline/taigan/2018/taigan2018_02.pdf)
11.リンパ節郭清部位と名称
従来の子宮体癌取扱い規約におけるリンパ節の名称に関しては子宮頸癌取扱い規約ならびに1991年日本癌治療学会リンパ節合同委員会の提唱に基づき命名されてきた。2002年に日本癌治療学会リンパ節規約が改訂されたことを受け、『卵巣腫瘍・卵管癌・腹膜癌取扱い規約 臨床編 第1版』(2015年)よりリンパ節の部位と名称が以下のように定められた。これを勘案して、『子宮体癌取扱い規約 病理編 第4版』(2017年)においても同一の名称が用いられることとなった。
所属リンパ節
子宮内膜癌ならびに子宮体部肉腫の所属リンパ節は、『傍大動脈リンパ節』+『骨盤リンパ節』である。所属リンパ節は、原発巣と直結したリンパ路をもつリンパ節集団であり、領域リンパ節とも呼ばれる。つまり、転移が早期に生じる可能性があるリンパ節の範囲のことをいう。身体の各部位には所属リンパ節が存在し、癌の所属リンパ節転移は病変の進行を示す。したがって、所属リンパ節転移の有無は患者治療における重要な情報であり、多くの場合,患者予後と相関する。
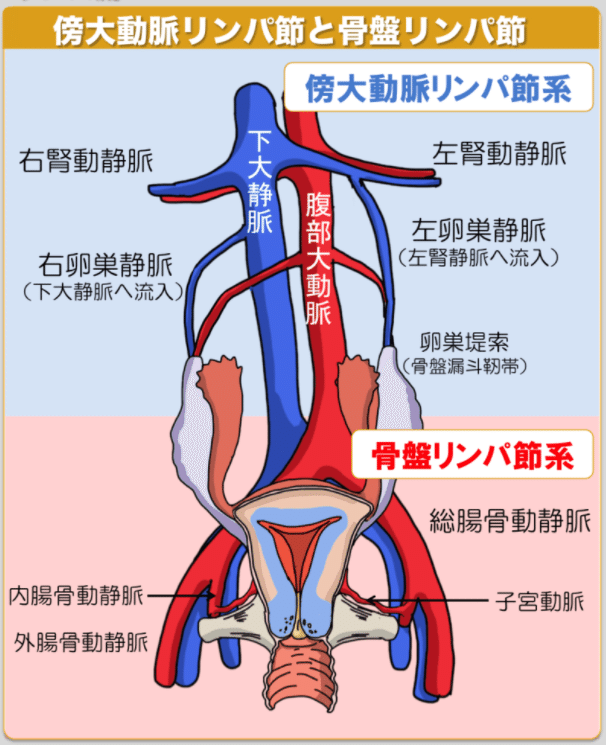
骨盤リンパ節(下図詳細)
②総腸骨リンパ節、③外腸骨リンパ節、④鼠径上リンパ節、⑤内腸骨リンパ節、⑥閉鎖リンパ節、⑦仙骨リンパ節、⑧基靭帯リンパ節を指す。
[参考]
・子宮頸部の所属リンパ節は、②総腸骨、③外腸骨、⑤内腸骨、⑥閉鎖、⑦仙骨リンパ節、⑧基靭帯を指す。
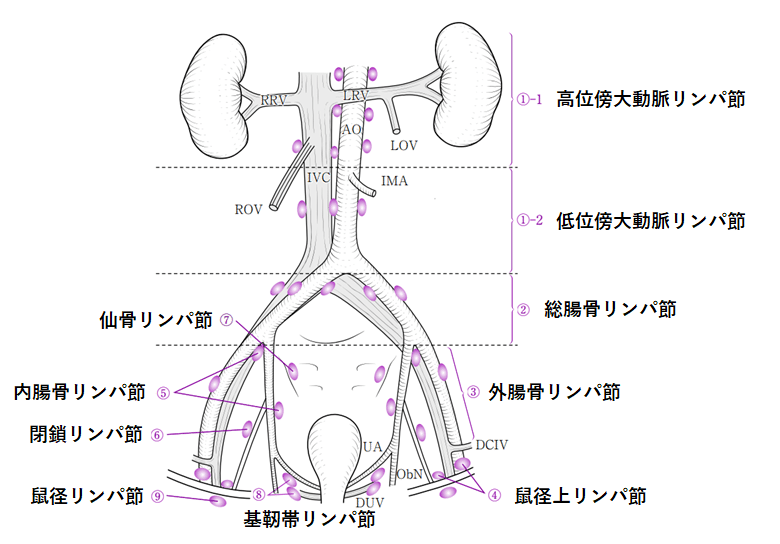

①傍大動脈リンパ節(腹部大動脈周囲リンパ節) Para-aortic nodes
腹部大動脈および下大静脈に沿うもの。
①-1 高位傍大動脈リンパ節:
下腸間膜動脈根部より頭側で、横隔膜脚部までの大動脈周囲にあるリンパ節。この領域の下大静脈周辺のリンパ節も含む。
①-2 低位傍大動脈リンパ節:
下腸間膜動脈根部から大動脈分岐部の高さまでの大動脈および下大静脈周辺のリンパ節を指し、下腸間膜動脈根部の高さに接するリンパ節も含まれる。
大動脈左側から下大静脈右側までのリンパ節を便宜上、傍大動脈リンパ節とよぶが、細区分が必要な場合には、大動脈前面から左側にかけてのリンパ節を傍大動脈リンパ節、大動脈と下大静脈の間に存在するリンパ節を大動静脈間リンパ節、下大静脈前面から右側にかけてのリンパ節を下大静脈周囲リンパ節と記載する。
これまでの子宮体癌取扱い規約では、高位傍大動脈リンパ節を「左腎静脈下縁から下腸間膜動脈根部上縁までの領域」と規定していたが、『卵巣腫瘍・卵管癌・腹膜癌取扱い規約 臨床編 第1版』(2015年)で、左腎静脈より頭側のリンパ節も含まれるようになった。以後、下腸間膜動脈根部より尾側を「低位傍大動脈リンパ節」とし、下腸間膜動脈根部より頭側で、横隔膜脚部までを「高位傍大動脈リンパ節」として分類されることになった。
②総腸骨リンパ節 Common iliac nodes
総腸骨動静脈に沿うリンパ節。浅外側総腸骨リンパ節、深外側総腸骨リンパ節、内側総腸骨リンパ節に細区分される。
③外腸骨リンパ節 External iliac nodes
外腸骨血管分岐部より足方で、外腸骨血管の外側あるいは動静脈間にあるもの。
④鼠径上リンパ節 Suprainguinal nodes
(大腿上リンパ節 Suprafemoral nodes)
外腸骨血管が鼠径靭帯下に入る直前にあるもの。
血管の外側にあって、外腸骨リンパ節に連絡し、深腸骨回旋静脈よりも末梢にあるものを外鼠径上リンパ節といい、血管の内側にあり、閉鎖リンパ節に連絡するものを内鼠径上リンパ節という。
⑤内腸骨リンパ節 internal iliac nodes
内腸骨血管と外腸骨血管とによって作られるいわゆる血管三角部および内腸骨動静脈に沿うもの。
⑥閉鎖リンパ節 obturator nodes
外腸骨血管の背側で閉鎖孔および閉鎖神経、閉鎖動静脈周囲にあるもの。
⑦仙骨リンパ節 sacral nodes
内腸骨血管より内側で仙骨前面とWaldeyer筋膜の間にあるもの。正中仙骨動静脈に沿うものを正中仙骨リンパ節、外側仙骨動静脈に沿うものを外側仙骨リンパ節という。
⑧基靭帯リンパ節 parametrial nodes
基靭帯およびその周辺に存在するもの。子宮傍組織リンパ節、尿管リンパ節などと称せられた表在性のもの(頸部傍組織リンパ節 paracervical nodes)、および基靭帯基部近くに存在する深在性のものすべてを含める。
⑨鼠径リンパ節 inguinal nodes
鼠経靭帯より足方にあるもの。
子宮内膜癌では同リンパ節への転移を認めるものは遠隔転移と規定されており、ⅣB期となる。
病理診断教育支援HPより
https://www.palana.or.jp/ipath/manual/4-female-genital/1-uterus
12.リンパ節郭清の意義と確立へ向けた取り組み
リンパ節郭清の治療的意義に関しては、未だ明確でない。現在のところ、早期癌における骨盤リンパ節郭清は、治療としての意義よりも診断的意義が強調されている。つまり、『骨盤リンパ節郭清の意義は、病理学的な転移有無の証明診断』という点にある。そのため、摘出により転移が証明されるときは非常に有用な手技といえる。骨盤リンパ節郭清は現在標準的な根治手術に含まれており、現在本邦ではどの病院でも行われている。
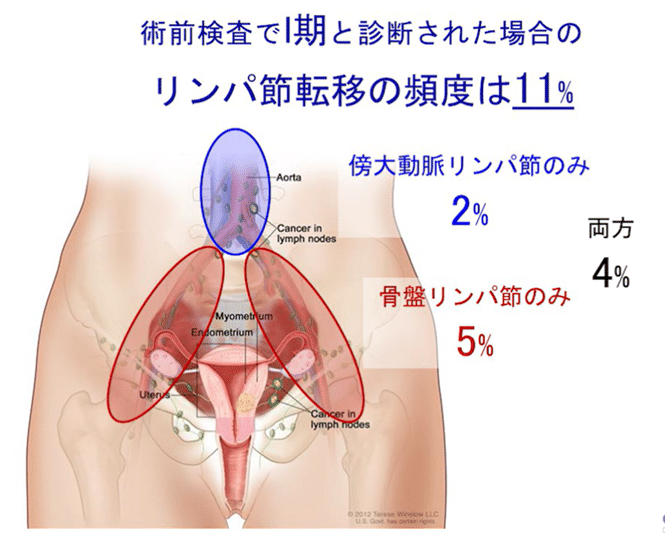
◆リンパ節転移の頻度
術前にⅠ期と診断された場合のリンパ節転移の頻度は、約11%。つまり、10人に1人程度しかリンパ節郭清の必要性はがないことになり、大半の人は必要なくなる。
◆リンパ節郭清(意義、方法、範囲)に関する議論
リンパ節郭清の治療的意義が未だ明確でない中で、米国国立がん研究所(National Cancer Institute:NCI)の多数登録例の解析では・・・
『再発中・高リスク群の子宮体癌の場合、郭清されたリンパ節の個数が予後改善に寄与する』と報告されている(報告1)

--------------------------------------------------------------------------------------
しかし、イタリアと英国のグループによるランダム化比較試験(RCT:Rondomized Controlled Trial)では、『”骨盤リンパ節郭清”は全生存期間や無再発生存期間の延長に寄与しない』との報告がなされた(報告2)。ただし、この試験は再発低リスク症例を多く含んでおり、このような症例ではリンパ節郭清が省略可能であることを示唆したのかもしれない(CQ03)。

--------------------------------------------------------------------------------------
上記2つの報告からもわかるように、中リスクでのリンパ節郭清の必要性に関する報告には矛盾が多い。現在の論調としては、低リスクでは「リンパ節郭清無しでもいいのではないか?」、高リスクでは「リンパ節郭清した方がいいだろう」、中リスクでは「ひょっとしたらリンパ節郭清しなくてもいいかも・・・」といった状況にある。
ちなみに、低リスクでは以下のような報告になっている。

--------------------------------------------------------------------------------------
このように矛盾する中リスクでのリンパ節郭清の実施判断を検討すべく、2016年からヨーロッパにてSTATEC試験(n数=1,000以上となる大規模試験)が開始されている。

--------------------------------------------------------------------------------------
◆リンパ節郭清範囲(骨盤~傍大動脈)の確立へ向けて
子宮体癌の正確な進行期決定のために後腹膜リンパ節郭清(生検)は必要ではあるが、その範囲に関する統一した見解は得られていない。
米国での婦人科腫瘍専門医に対するアンケート調査では、後腹膜リンパ節郭清を施行する割合は69%と推測され、65%の医師がリンパ節郭清は治療的意義があると判断していた。また45%が自分の手技を完全なリンパ節郭清と考えていたが、31%は傍大動脈リンパ節の生検を行っていなかった。
欧州では多くの症例でのリンパ節の検索は視診と触診によってなされ、スコットランドではそのことが患者の予後不良の原因の1つと報告された。
本邦では前述のJGOG調査研究で、骨盤リンパ節郭清はほぼ全施設で施行されていたが、全例に傍大動脈リンパ節(生検)を施行する施設は13%であり、大多数の施設は条件付きで郭清(生検)を行っていた。このように骨盤リンパ節郭清が比較的行われる本邦においても、傍大動脈リンパ節郭清を併用するか否かに関しては施設間差が大きく、骨盤リンパ節(CQ03)や傍大動脈リンパ節(CQ04)の郭清を省略しうる対象を確立していくためには、リンパ節郭清の範囲や程度に関する施設間差を少なくした臨床試験を行っていく必要があると思われる。
また、最近の本邦における比較的大規模な後方視的検討では、『再発中・高リスク症例では傍大動脈リンパ節郭清の追加が予後改善に貢献する』としている(CQ04)。これを検証するために現在、リンパ節郭清法を多施設間で統一した上で骨盤リンパ節郭清に傍大動脈リンパ節郭清を加えることの意義を検証するランダム化第Ⅲ相試験が行われている(CQ04)。このように子宮体癌に対するリンパ節郭清(生検)の意義や方法、範囲については世界的なコンセンサスが得られにくい状況にあり、国内でも議論が尽きない段階にある。
◆傍大動脈リンパ節郭清の実施症例
子宮体がんの所属リンパ節には、骨盤リンパ節と傍大動脈リンパ節が含まれる(下図1)。子宮体がんの標準手術療法としてのリンパ節郭清の範囲は、この2つの領域のリンパ節のうち、より子宮に近い骨盤リンパ節が対象とされているが、より転移リスクが高いと判断される場合は傍大動脈リンパ節も併せて郭清する施設が多く見られる。例えば、慶應義塾大学病院にて傍大動脈リンパ節も併せて郭清するのは以下のような場合になる。
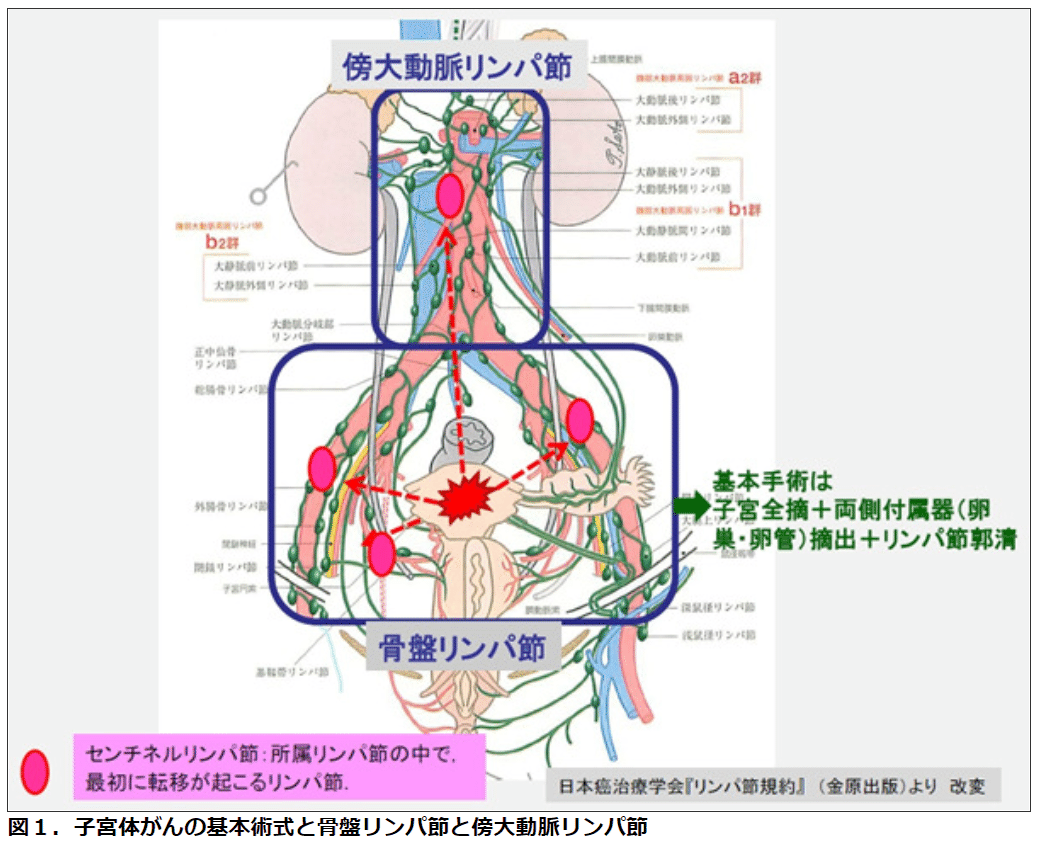
傍大動脈リンパ節郭清 実施症例
1)手術前の子宮内膜組織診または手術中の迅速病理診断にて組織型が漿液性腺がんなど予後が不良のタイプ(Ⅱ型)であるか、または分化度がグレード3(低分化)であると確認される
2)迅速病理診断にて卵巣・卵管への転移が確認される
3)筋層浸潤の深さが半分以上の深い浸潤であることが迅速病理診断にて確認される
4)迅速病理診断にて所属リンパ節転移が確認される
しかしながら、子宮体がんは、比較的早期がん症例が多く、所属リンパ節転移がみられない手術進行期Ⅰ~Ⅱ期(子宮内限局)症例が全体の約70%を占めており、実際にはリンパ節郭清が不要であるケースが相当数含まれている。現在は画像診断(CT、MRI、PET+CT)技術が向上しているが、小さなリンパ節転移を事前に正確に予測する方法は、まだ残念ながら開発されていない。また、骨盤リンパ節郭清後は、下肢や会陰部の浮腫を生じQOL(生活の質)が低下したり、骨盤内リンパ嚢胞や膿瘍などの合併症が生じたりすることがある。また傍大動脈リンパ節郭清も併せて行うと長時間の手術となり、術後腸閉塞などの合併症が生じる頻度も増加する傾向にある。
慶応義塾大学病院 医療・健康情報サイトより http://kompas.hosp.keio.ac.jp/sp/contents/medical_info/presentation/201610.html
◆センチネルリンパ節郭清
主に中リスク患者を対象にした低侵襲手術。最初にがんが転移するリンパ節(センチネルリンパ節)を色素を用いて判別し、その部分を郭清する。摘出したセンチネルリンパ節を調べ、がんの転移がなければそれ以上のリンパ節郭清は行わないというもの。
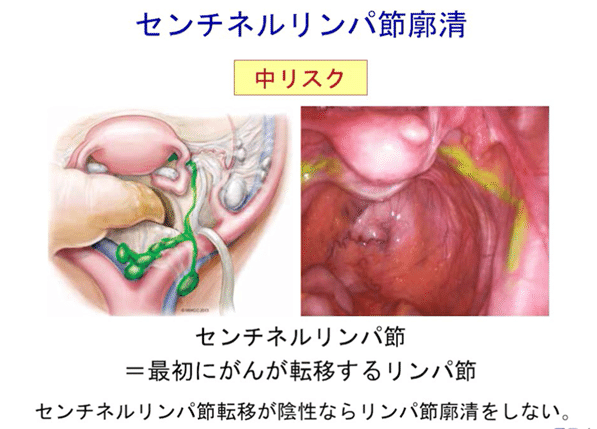
以下は、慶應義塾大学病院 医療・健康情報サイトより引用。
センチネルリンパ節ナビゲーション手術
近年、上述した合併症(下肢や会陰部の浮腫、骨盤内リンパ節嚢胞や腫瘍、術後腸閉塞など)を回避するために、最初に転移が生じると考えられるリンパ節(人によってリンパ節の場所は異なる)を手術中に迅速病理診断で検索し、転移がない場合は、より転移の可能性が低いと考えられるその他の所属リンパ節は摘出せずにおくというセンチネルリンパ節ナビゲーション手術が、乳がんをはじめ様々ながん腫において試みられるようになってきた。
センチネル(sentinel)という語源は『見張り』という意味。乳がんと悪性黒色腫については、平成22年4月から保険診療として承認されており、胃がん、食道がん、頭頸部がん、肺がんなどの診療でも臨床研究として行われている。婦人科領域では、外陰がん、子宮頸がんについて臨床研究が広く行われているが、子宮体がんでは、まだ少数の検討しか報告されていない。
子宮体がんにおいてセンチネルリンパ節ナビゲーション手術が確立されれば、多くの患者さんで縮小手術が可能となる。センチネルリンパ節に転移を認めなければリンパ節郭清が省略できることになり、将来的に患者さんにとっては合併症リスクの低下、医療者側にとっては手術時の負担が軽減し、さらには入院期間の短縮など医療費削減にも寄与すると期待されます。また通常のリンパ節の病理検索では確認しにくい2mm以下のサイズの微小な転移を効率的に確認できることが期待されます。
このような利点が期待されるにもかかわらず、子宮体がんにおいてセンチネルリンパ節ナビゲーション手術の臨床研究が進みにくい理由には、センチネルリンパ節を特定する方法が未確立であること、またセンチネルリンパ節が存在すると考えられる範囲が広く(上図1)、短時間で確実に検索することが容易ではないことが挙げられる。
また、乳がん治療ガイドラインにも『手技に習熟したチーム(外科医、病理医、放射線科医)が行ったセンチネルリンパ節生検で転移陰性であると確認された場合は......』と明記されており、習熟した病理医、放射線科医の協力が欠かせません。当院では、外科領域において世界的に最先端のレベルのセンチネルリンパ節ナビゲーション手術研究が行われている。
そこで婦人科では、当院の倫理委員会に臨床研究として申請し承認を受け、放射線科、病理診断部、消化器外科のご協力のもと、子宮体がんのセンチネルリンパ節ナビゲーション手術を目指した臨床試験を2009年3月より開始。対象となる患者さんは、手術前検査にて子宮体がんと診断された方のうち、画像検査などにて手術進行期Ⅰ~Ⅱ期が推定され、明らかなリンパ節転移がなく、リンパ節郭清を含む手術が予定される20才以上の方。もちろん臨床試験へのご参加は、患者さんの自由意志によります。2015年12月までに約100名の患者さんにご協力いただき、研究を進めて参りました。
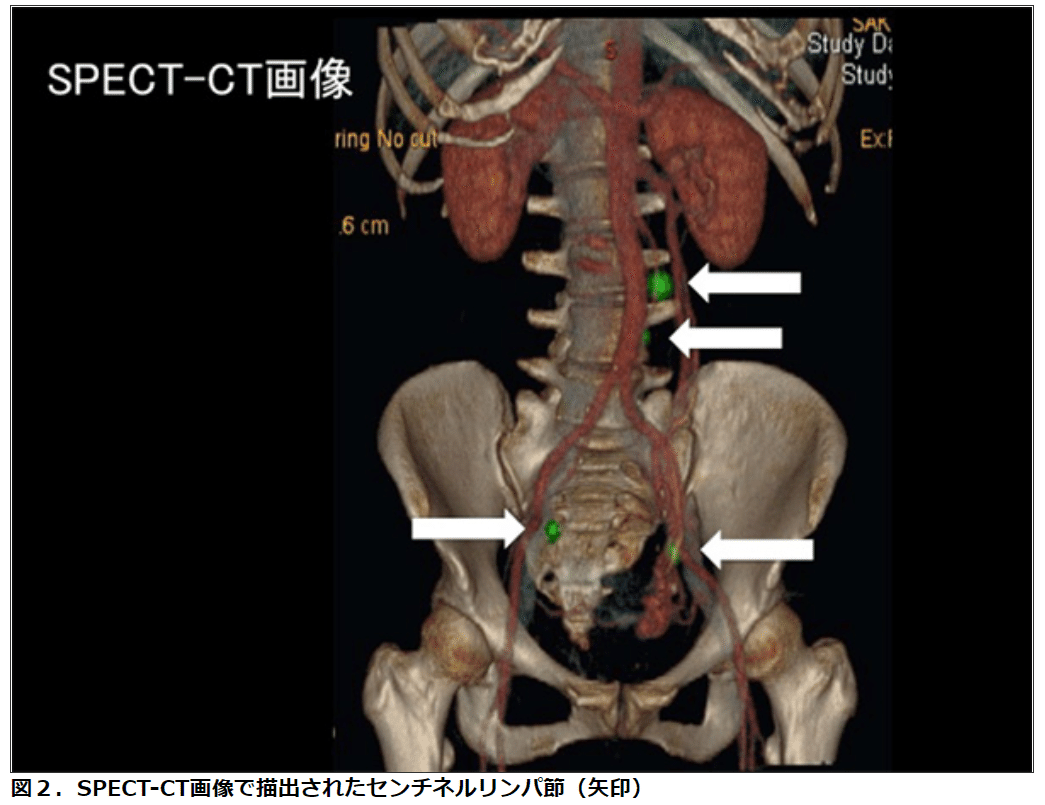
センチネルリンパ節の同定法
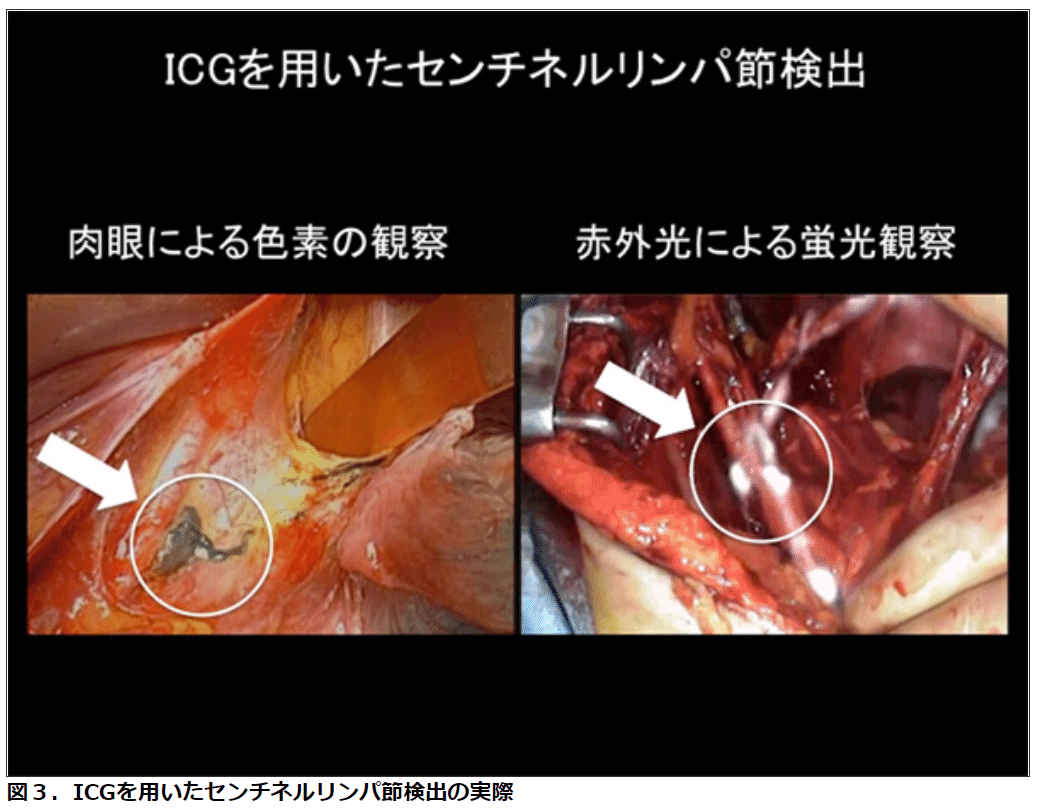
他のがん腫と同様にラジオアイソトープ(RI)法と色素法を原則として併用して行う。RI法に関しては、手術前日に子宮鏡を用いて、子宮体がんの周囲にラジオアイソトープ(99mTc-フィチン酸)を局所注射し、手術当日の朝にSPECT-CTの撮像を行う(上図2)。手術中には、γプローブによる検索も行い、センチネルリンパ節を同定。色素法にはインドシアニングリーン(ICG)という検査用の色素を手術中に子宮漿膜下に局所注射し、その後どのリンパ節に色素が流れ込んでいくかを複数の医師の眼で確認。
また、このICGという色素には、赤外線カメラを通して観察すると蛍光を発する性質があり、蛍光観察でのセンチネルリンパ節の同定についても検討を進めている(下図3)。なお、ラジオアイソトープの量は、骨シンチ検査で使用される放射線量の約50-100分の1であり、人体に悪影響をおよぼす被爆量ではなく、色素についても人体に悪影響をおよぼすようなことは極めて稀。両者の方法にて確認されたセンチネルリンパ節の主な3個を術中迅速病理診断に提出し、また術後の詳細な免疫組織化学的検索も含めて、微小な転移も可及的に見逃さないようにしている。
現段階(臨床研究段階)では標準的なリンパ節郭清を全ての患者さんに実施している。この臨床研究では、子宮体がんにおけるセンチネルリンパ節の個数や部位、最適なセンチネルリンパ節の検出方法、センチネルリンパ節の検出率、リンパ節転移陽性例におけるセンチネルリンパ節転移率(感度)、センチネルリンパ節が転移陰性である場合で他の所属リンパ節が転移陰性である確率(陰性的中率)を検討し、子宮体がんにおいてもセンチネルリンパ節の概念が成立し、センチネルリンパ節ナビゲーション手術が可能か否かを明らかにしたいと考えている。
臨床研究の成果(2009~2015年)
まず、センチネルリンパ節の概念が成立するためには、
1)センチネルリンパ節が確認できる患者さんの割合(検出率)
2)センチネルリンパ節に転移がない場合に他のリンパ節には転移していない確率(陰性的中率)
この2つが、いずれも90%以上であることが必要であると考えられている。2015年末までの研究結果としては、センチネルリンパ節を98.9%の患者さんで検出することが可能であった。また、陰性的中率は100%という良好な結果が得られているため、子宮体がんにおいてもセンチネルリンパ節の概念が成り立つことが明らかになった。
センチネルリンパ節の個数に関しては、患者さん1人あたり平均5.3個が検出されました。標準的なリンパ節郭清を行った場合、摘出されるリンパ節の個数は平均約60個(当院データ)ですので、将来的にセンチネルリンパ節ナビゲーション手術が導入された場合には、摘出するリンパ節の個数を10分の1以下にまで抑えることが可能であると考えている。
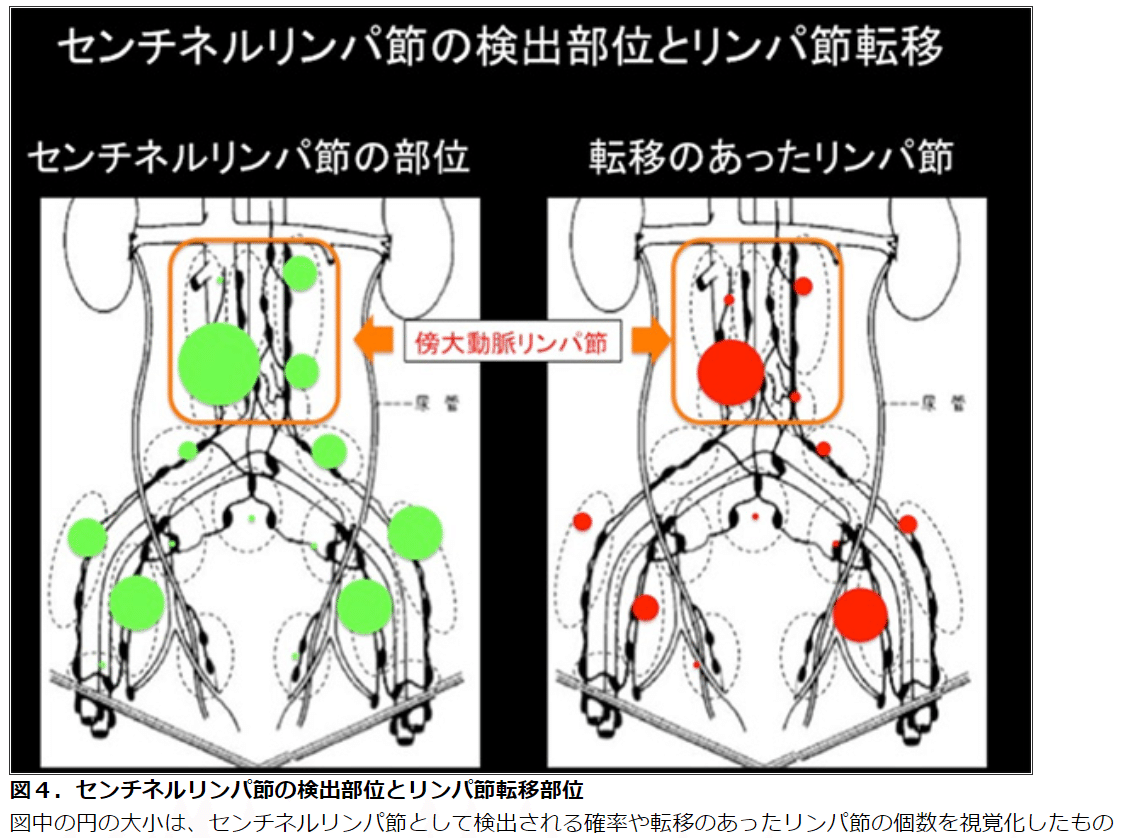
また、これまで早期がんでは傍大動脈リンパ節への転移が起こることは稀であると考えられてきたが、これを覆すデータが得られてきた。センチネルリンパ節の研究を通して、センチネルリンパ節は骨盤リンパ節だけでなく傍大動脈リンパ節にも広く存在していることがわかってきました(下図4)。そしてセンチネルリンパ節の臨床試験に参加いただいた患者さんの中でリンパ節に転移があった方の転移部位を解析してみると、傍大動脈リンパ節への転移を認めた方は67%にも及んでいました。このことから、傍大動脈リンパ節への転移を見逃さないことも重要であると考えています。
センチネルリンパ節には、転移の可能性が高いリンパ節をピックアップして、集中的に詳細な病理学的検索を行うために、通常の病理検査では診断が困難な微小な転移を確認することが可能であるという側面もある。このセンチネルリンパ節の臨床試験に参加していただいた患者さん(94名)の中でリンパ節に転移があった方が21名いたが、そのうち12名(57%)は、転移リンパ節の中の転移病巣が直径2mm未満という微小な転移でした。このような微小な転移は、従来の病理検査では検出できないケースが存在した可能性があります。つまり、微小な転移を効率的に確認することが期待できるセンチネルリンパ節の手法を用いて、手術後の再発リスクに関するより正確な情報を患者さんに提供できると考えています。
現在、当科ではセンチネルリンパ節ナビゲーション手術(センチネルリンパ節に転移がない場合は、その他のリンパ節の摘出を実施しない手術)の導入を検討中です。センチネルリンパ節ナビゲーション手術は、子宮体がんの患者さんの治療後の予後改善やリンパ浮腫などの合併症軽減につながることが期待されている。
13.手術の目的と術式
子宮体がん手術は、病変の治療的摘出と同時に腫瘍の広がり(進行期:ステージ)を診断する目的で行う。
子宮体がん手術の基本戦略
手術をし、病理組織検査(顕微鏡で観察)で、進行期(広がり)、病理組織型(顔つき)、組織分化度(悪さの度合い)を確定していく。

標準的手術
『単純子宮全摘術』+『子宮附属器(卵巣・卵管)切除』+『骨盤(もしくは傍大動脈)リンパ節郭清』+『腹腔洗浄細胞診』となる。
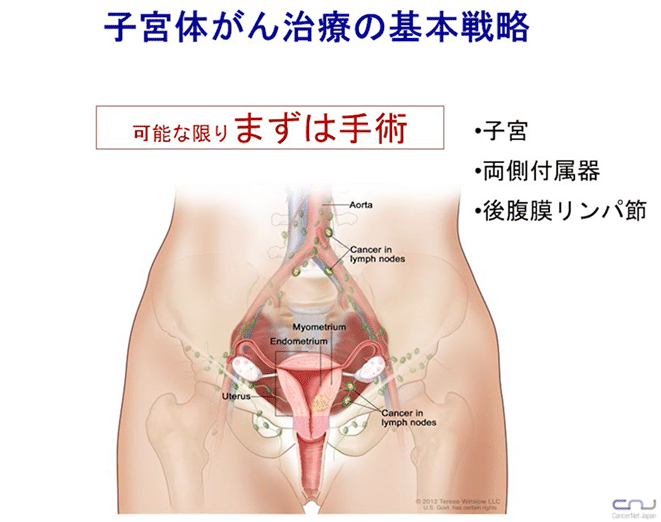
骨盤内のリンパ節は子宮周辺のリンパ節で、癌の広がりを確認するために摘出。腹腔内の癌細胞の有無を検査する細胞診も癌の広がりを確認するために行われる。また肉眼的に見て癌の転移と思われる部分も出来る限り摘出する。これら摘出したものを十分に検査し、最終的な腫瘍の広がりを診断し、手術後の追加治療を検討する。
癌が明らかに広がっていて全部摘出できない場合や、子宮筋層に広がっていない初期の癌の場合には、手術を縮小して子宮と卵巣・卵管のみ摘出する場合もある。遠隔転移を認める等、明らかに進行していると手術できない場合もある。
手術アプローチ例としては、子宮体癌の術前StageⅠA推定の類内膜癌分化度(グレード)1-2に対して腹腔鏡下手術を実施。大きな子宮筋腫を伴う子宮体癌や、類内膜癌グレード3や類内膜癌以外の組織型(漿液性がん、明細胞がんなど)、術前StageⅠB以上の方には従来の開腹手術を行う。
https://www.pref.aichi.jp/cancer-center/hosp/12knowledge/iroirona_gan/09shikyutai.html
◆術式名とその内容
子宮体がん治療ガイドライン2018年版より抜粋。
https://jsgo.or.jp/guideline/taigan/2018/taigan2018_02.pdf

1.単純子宮全摘出術(Simple(total)hysterectomy)
腹式、膣式あるいは鏡視下に行われる。一般の単純子宮全摘出術に準ずるが、腫瘍性病変が存在する場合には子宮頸部組織を残さない術式が必要であり、筋膜内術式(Aldridge術式)は不適当である。病巣最外端と切創縁との間の距離をおくため、膣壁を多少なりとも切除する必要がある。膣壁の一部(cuff)を切除する場合に拡大単純子宮全摘出術という用語が用いられることもある。
--------------------------------------------------------------------------------------

2.準広汎子宮全摘出術(Modified radical hysterectomy)
広汎子宮全摘出術と単純子宮全摘出術の中間的な術式である。膀胱子宮靭帯の前層を切断し、尿管を側方に寄せた後に子宮傍(結合)組織(parametrium)と膣壁を子宮頸部からやや離れた部位で切断する。リンパ節郭清の有無を問わない。
(*)子宮傍(結合)組織
前方にある膀胱子宮靭帯(前層および後層)、側方の基靭帯、後方の仙骨子宮靭帯と直腸膣靭帯の4つを指す。子宮が膣内へ落ちないように支える組織として頚部の周囲に存在しており子宮傍結合織と呼ばれる。
--------------------------------------------------------------------------------------
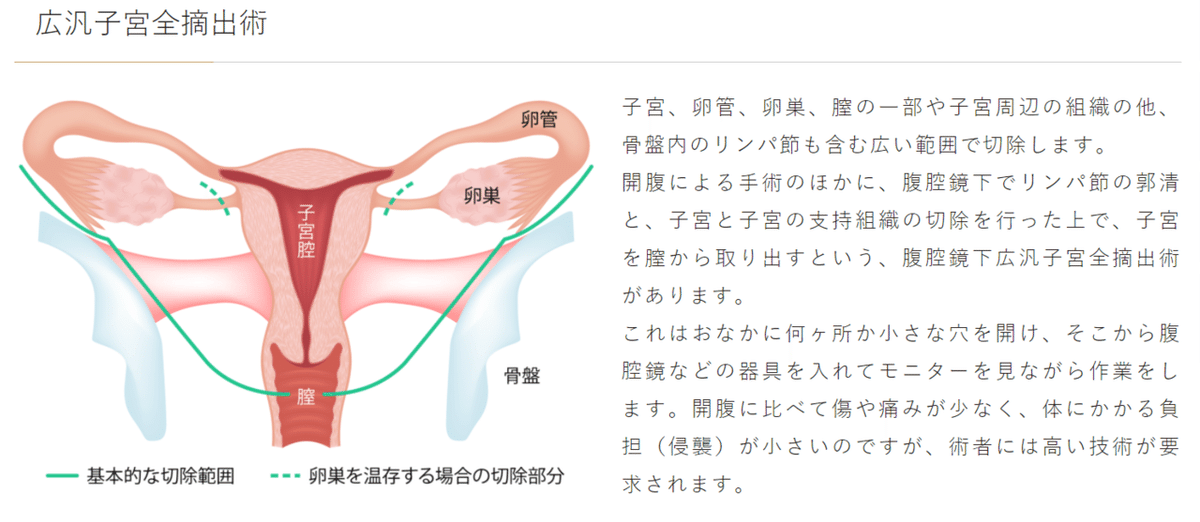
3.広汎子宮全摘術
子宮および子宮傍(結合)組織、膣壁および膣傍(結合)組織の一部を摘出し、骨盤内所属リンパ節を郭清する術式である。子宮傍(結合)組織は前方の膀胱子宮靭帯(前層および後層)、側方の基靭帯、後方の仙骨子宮靭帯、直腸膣靭帯に区分される。
諸種の術式のうち、欧米諸国ではWertheim術式、わが国では岡林術式を基本として変遷を経た術式が汎用されている。岡林術式の特徴は、膀胱子宮靭帯の前層を処理した後に、後層も切断して尿管と膀胱を完全に子宮・膣から分離して膣を十分に切除することにある。子宮頸癌に対する基本治療術式であり、一般に子宮頸癌ⅠB期とⅡ期の症例が適応となっている。一方、子宮体癌においては、深い頸部間質浸潤例に対して用いられることがある。
(*)膣傍(結合)組織
膣壁の各層は内側から、粘膜、筋層、腟傍結合組織(Paracolpium)となっている。つまり、膣壁の外層部分を膣傍結合組織という。かなり密な結合組織からできていて、そこには平滑筋線維が存在する。腟の下部は隣接する諸器官(膀胱、尿管、直腸)とかたく結合している。
中層は筋層(Tunica muscularis)であって、平滑筋線維の束が絡みあったものからなっている。内層すなわち粘膜(Tunica mucosa)は、その表面に多数の横走する稜状の高まり、すなわち腟粘膜ヒダ(Rugae vaginales)があって特徴的な形態を示している.
http://www.anatomy.med.keio.ac.jp/funatoka/anatomy/Rauber-Kopsch/2-23.html
--------------------------------------------------------------------------------------
以下は、子宮体がん治療ガイドライン 2018年版より抜粋。
子宮体癌の摘出術式を論ずる場合には、①各術式の内容自体に対する施設間差と、②各術式を適応とする症例選択の施設間差を考慮する必要がある。①に関して、本邦の広汎子宮全摘出術はかなり一致した術式で行われているが、拡大単純子宮全摘出術や準広汎子宮全摘出術などの術式は施設間で切除範囲や手技に差があると推測される。加えて、海外からの報告を参考にする場合には、本邦との術式の違いについて考慮する必要がある。欧米では子宮全摘出術をⅠ型からⅤ型に分類することが多いが、名称上は同じ術式であっても切除範囲や手技が本邦と異なることがあり、海外のエビデンスをそのまま国内に当てはめることには慎重でなければならない。②に関しては、2005年に行った婦人科悪性腫瘍研究機構(Japan Gynecologic Oncology Group:JGOG)の調査研究で子宮体癌に対する各施設での基本術式を調査したところ、「単純子宮全摘術を行う」、「拡大単純子宮全摘術を行う」および「術前の推定進行期により術式を変更する」と答えた施設が、それぞれほぼ1/3ずつであった。約70%の施設は「子宮体癌に対しては広汎子宮全摘出術を施行しない」と答えた。このように国内でも、どのような症例にどの術式を選択するかに関する施設間差は大きい。
子宮体癌Ⅰ期の再発のリスク因子としては、年齢、筋層浸潤の深さ、脈管侵襲、腫瘍サイズ、子宮頸部間質浸潤などがあるが、術前にⅠ期と考えられる症例に対する子宮の摘出術式は、国内外とも筋膜外単純子宮全摘術(筋膜内単純子宮全摘術もある)が標準とされているのが現状で(CQ01)、開腹術式に加えて術後のquality of life(QOL)が良好な鏡視下手術の適用も広まりつつある(CQ12)。傍大動脈リンパ節郭清(生検)を必要としない再発低リスクの術前推定Ⅰ期症例を対象に、本邦でも2014年4月に腹腔鏡下子宮悪性腫瘍手術が、2018年4月にロボット支援下子宮悪性腫瘍手術が保険適用となった。今後は、腹腔鏡あるいはロボットによる鏡視下手術が急速に増えてくると思われる(CQ12)。
術前にⅡ期と推定される症例の子宮の摘出術式に関しては、術後進行期との不一致例が少なからずあることに留意する必要がある(CQ02)。また、推定Ⅱ期症例が子宮傍(結合)組織浸潤を有する率は比較的低く、子宮傍(結合)組織の十分な切除を特徴とする広汎子宮全摘出術の適用に関しては最近、否定的な報告もある。以上から、術前推定Ⅱ期の子宮摘出術式としては準広汎子宮全摘出術を中心として、広汎子宮全摘出術に加え、筋膜外単純子宮全摘術、拡大単純子宮全摘術も考慮される(CQ02)。術前推定Ⅱ期に対する鏡視下手術に関してはまだ報告が少ない為、開腹手術と同等の根治性が証明されておらず、今後の検討が待たれる。
もう少し、術式について整理。婦人科疾患の診断・治療・管理より抜粋。
http://fa.kyorin.co.jp/jsog/readPDF.php?file=to63/61/11/KJ00005822376.pdf
腹式単純子宮全摘術(Abdominal Total Hysterectomy)
本術式は、婦人科手術の中で最も代表的な、最も数多く実施されている基本手術であり、婦人科医すべてが修得すべき術式である。基本は、子宮支持組織をできるだけ子宮近傍で切断し、膀胱を子宮腟翻転部下方まで剝離展開し、子宮を腟管から切断することにある。以前は、子宮頸部を残す姑息的術式として子宮腟上部切断術(supravaginal hysterecromy) が行われていたが、残存子宮頸部から子宮頸癌を発症(断端癌)する可能性があるので、特殊な場合を除き、現在ではほとんど行われていない。
筋膜外術式と筋膜内術式
単純子宮全摘術は、筋膜外術式と筋膜内術式(Aldridge 術式)に分類される。通常、腹式単純子宮全摘術とは筋膜外術式を指すが、子宮頸部のらせん状筋層の外側を縦走する筋層を残し、その内側で子宮を摘出する筋膜内術式も行われている。筋膜内術式は原則的に子宮悪性疾患には禁忌であるが、頸部周辺に強度の癒着がある例などに適している。
術式名について、もう少しだけ整理。単純子宮全摘出術と拡大単純子宮全摘術の違いや、準広汎(拡大)子宮全摘出術と拡大子宮全摘出術は同義語であることを理解しておく。
子宮摘出術式の定義と解説(ガイドライン旧版)
本ガイドライン(旧版)での子宮全摘出術はすべて腹式であり、以下に各術式を記載する。
https://minds.jcqhc.or.jp/n/med/4/med0050/G0000135/0011
単純子宮全摘出術
子宮支持装置と腟管を子宮付着部の近くで切断して子宮頸部を残さないように腟壁を多少なりとも切除する筋膜外術式である。
拡大単純子宮全摘出術
単純子宮全摘出術に加えて腟壁を1〜2cm切除する術式をいう。
準広汎(拡大)子宮全摘出術
膀胱子宮靱帯前層を分離切断して尿管を側方に避け、前子宮支帯と腟壁を子宮頸部からできるだけ離して子宮を摘出し、膀胱子宮靱帯後層の分離切断は施行しない。したがって、腟壁を1.5〜2cm余分に切除することが可能であり、単純子宮全摘出術に比し、基靱帯もより多く切断されるのが特徴。
拡大子宮全摘出術
準広汎子宮全摘出術と同義語として用いる。
広汎子宮全摘出術
膀胱側腔、直腸側腔を展開して前・中・後の各子宮支帯を分離切断して腟壁の一部および骨盤結合織を広く摘出し、かつ骨盤内所属リンパ節を郭清する術式である。すなわち、基靱帯は骨盤壁近くで切断し、膀胱子宮靱帯前層を分離切断し、尿管を剥離、側方に圧排して後層を分離切断し、仙骨子宮靱帯および直腸腟靱帯を切断した後に腟傍結合組織および腟壁の一部(少なくとも3cm)を十分に摘出する。
14.ロボット支援下 子宮悪性腫瘍手術(子宮体がんに限る)手術について
ここからは、子宮体がん手術について整理していく。初めに、保険適用範囲について。

2018年4月から子宮体がんの中でも危険度の低い、すなわち、がん細胞が子宮壁の中にまで浸潤していないタイプに対して、ロボット手術が保険適応となった(ロボット支援下 腹腔鏡下子宮悪性腫瘍術)。
つまり、子宮体がんの中でも、傍大動脈リンパ節郭清(生検)を必要としない(骨盤リンパ節だけは摘出する)、再発低リスクの術前推定Ⅰ期症例が対象となっている(通常の腹腔鏡下手術は、2014年4月から保険適用)。
また、高リスク体がんにおいては、いまだ保険適用には至っていない(完全な私費治療。保険も先進医療特約の適用範囲でもない)
--------------------------------------------------------------------------------------
次に、低リスク体がん(あまり浸潤していない大人しい組織型)についてまとめていく。
◆低リスク体がんの標準術式は・・・
『単純子宮全摘術』+『両側付属器(卵管と卵巣)摘出術』+『骨盤内リンパ節郭清術』

ロボット支援下手術のメリットとして、特に肥満・高齢の患者にとっては、手術成績よりも術後の合併症等のリスクが少ないという点で優れた術式となっている。
単純子宮全摘術とは?
浸潤が壁に達していない、危険度の低い子宮体がん(低リスク体がん)の場合、広汎性に拡がった子宮がんと違い、ギリギリで子宮のみを取り、膣と靭帯(基靭帯)を切除しない手術方式。
両側付属器(卵巣&卵管)摘出術とは?
子宮体がんの場合、卵巣・卵管が病巣のすぐ近くにあるため、子宮だけでなく両方の卵巣・卵管も摘出するのが一般的。
骨盤リンパ節郭清とは?
さらに、子宮周囲の骨盤内部リンパ節も切除。このようにがんの病巣周囲のリンパ節を全て切除する術式は「リンパ節郭清」と呼ばれる。これは、病巣からリンパ節への転移、リンパ節から全身臓器への転移を防ぐため、がんの切除術では一般的に行われる術式。
--------------------------------------------------------------------------------------
◆高リスク体がん(進行癌)の術式は・・・
『低リスク体がんの術式』+『傍大動脈リンパ節郭清』+『大網切除』
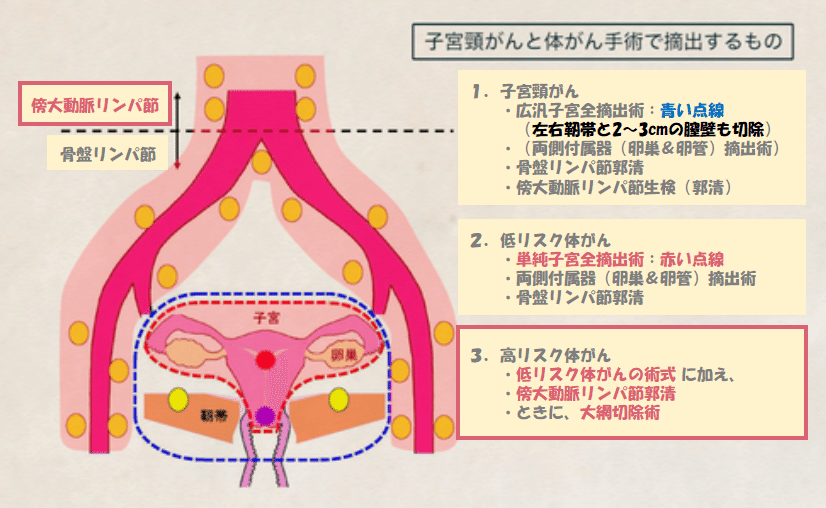
高リスク体がんでは、傍大動脈リンパ節郭清および、時に大網切除も必要となる。転移リスクが増すため、子宮周辺だけではなく骨盤リンパ節郭清に加え、傍大動脈リンパ節もしっかりと郭清することで、がん細胞の拡散を防ぐ。このことから、非常に大掛かりな手術となる。
また、高リスク体がん手術は、上腹部・下腹部両方からのアプローチとなる「デュアル・ドッキング手術」が行われる。この手術方式は患者にとって非常に恩恵が大きいため、出来るだけ早く保険適用が認められてほしい領域のひとつ。
傍大動脈リンパ節郭清とは?
高リスクな子宮体がんのケースでは、転移リスクがより大きくなるため、子宮周辺だけでなく、傍大動脈リンパ節も郭清することで、がん細胞の拡散を防ぐ。
大網切除術とは?
時に、腫瘍組織の状態で分類した時に悪性度の高いタイプ(G3:低分化型)の子宮体がんは、卵巣がんのように卵管から腹腔内へと拡がる場合がある。このようながんの拡がりを「播種」といい、がん細胞が腹腔内へ散らばるイメージでがんが転移していく。
この場合、胃から垂れ下がっている脂肪組織である「大網(*)」も同時に切除するべきだと言われている。大網は脂肪組織の塊で、腹腔臓器を覆っているカバーのような組織。リンパ節を多く含むため、リンパ節転移のリスクを未然に防ぐためにも、摘出が適当であるとされている。
(*)大網:卵巣がんの転移がよく起こる組織であり、手術時に切除する場合が多い。

--------------------------------------------------------------------------------------
(補足)
◆子宮頸がん手術(広汎子宮全摘術)の術式は・・・
『広汎子宮全摘出術(左右基靭帯と2~3cmの膣壁も切除)』+『両側付属器摘出術(卵巣と卵管)』+『骨盤リンパ節郭清』+『傍大動脈リンパ節郭清(生検)』
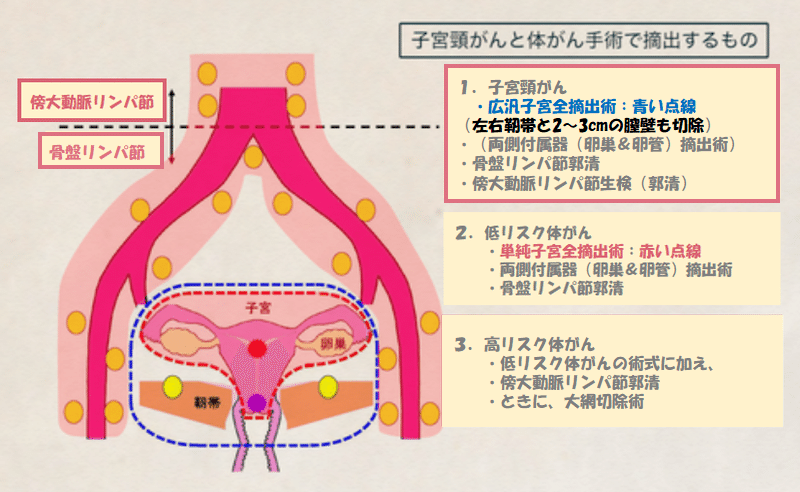
*子宮体がん手術との違いは、左右基靭帯および膣壁切除が伴う点。
--------------------------------------------------------------------------------------
保険適用に関する補足情報について、以下にまとめる。
(補足1)
子宮体がんからの転移に対する腹腔鏡下傍大動脈リンパ節郭清術(35,500点)に関しては、2020年4月から保険適用となっている。ただし、ロボット支援下手術は保険適用外。
K627-2 腹腔鏡下リンパ節群郭清術
1 後腹膜 40,670点
2 傍大動脈 35,500点
3 骨盤 41,090点
注 1及び3については泌尿器がん(1については精巣がんに限る)から、2については子宮体がんから転移したものに対して実施した場合に限り算定。
--------------------------------------------------------------------------------------
(補足2)
子宮頸がんに対して行われる腹腔鏡下広汎子宮全摘術は、2018年4月より保険適用。ロボット支援下においては先進医療となっている。

子宮頸がんのロボット支援下広汎子宮全摘術(先進医療)
子宮頸がんのロボット支援下 広汎子宮全摘術は先進医療であり、国内では限られた施設でしか受けることの出来ない治療となっている。患者が先進医療特約の付帯した医療保険を契約していない場合、入院費用は保険で賄われるが、手術料(約135万円)が別途必要になる。先進医療特約保険に入っていれば手術代金は無料となる。
先進医療とは?
厚生労働省が定める「高度な医療技術を用いた治療」のこと。高度の技術を要する外科療法や放射線療法、抗がん薬などの薬物療法、免疫療法など様々な治療法が含まれる。先進医療を行うには、医療技術の認定の他に、
実施機関として先進医療ごとに厚生労働省から認定を受けなければならない。つまり、どの医療機関でも先進医療を受けられるわけではない。
先進医療の費用負担は?
手術費用が自己負担となり、残りの入院費、検査料などが保険適応(3割負担)となる、いわゆる混合診療になる。(民間保険の先進医療特約に加入していれば、自己負担分の手術費用もカバーされる)
早期保険適用が望まれるロボット支援下広汎子宮頸部摘出術
さらに、子宮頸がん手術には、子宮全摘ではなく、将来の妊娠可能性を保持したままがんを切除する「広汎子宮頸部摘出術」という術式がある。『ロボット支援下広汎子宮頸部摘出術』は全く保険が認められておらず、入院費用から手術費用まで全額患者負担となり、約100万円の費用がかかる。
若い女性が将来の妊娠を可能とする広汎子宮頸部摘出術をロボット支援下で行うことは、恩恵が大きく、少しでも早い保険適用が望まれている。
15.子宮体がん術式の特徴(開腹、腹腔鏡、ロボット)
子宮体がんの手術療法には開腹手術と腹腔鏡下手術がある。子宮体がん症例では、リンパ節転移が広汎に起こり得るという特徴があるため、子宮全摘術に加え、他臓器への転移予防のため骨盤内や腹部大動脈などのリンパ節郭清(切除)を行う。
腹腔鏡手術のメリット
子宮周囲のリンパ節は腎臓の動脈付近に達するほど広がっているため、開腹手術の場合、リンパ節郭清を行うと下腹部からみぞおちに達するまでの長大な切開が必要となり、術創が非常に大きく体への負担もかかる。開腹手術で、徹底的にリンパ節郭清(リンパ節を摘出)を行っていた時代は、元気な患者でも10日~2週間は寝たきり状態になってしまっていた。そういったこともあり、子宮体がんのリンパ節郭清は低侵襲の腹腔鏡下手術で行うことで、驚くほどの回復力が見られるようになった(高齢の方でも、翌日には座って笑える程に回復)。また、出血量が非常に少ない点も大きなメリットであり、さらには、DPC制度下における入院日数の短縮化が、病院収益確保の点で恩恵も大きくなる。
後腹膜アプローチによるリンパ節郭清

リンパ節は体の深い位置にあるため開腹手術を行うと、かなり大きな傷になってしまうが、後腹膜(腹側部)からのアプローチにより簡単に患部・摘出部位に到達できる。腹腔鏡などを挿入するための数箇所の小さな傷のみで、傷痕が目立たず、治療後の回復も早いのが特徴。大きな切開は術後の痛み、回復の遅れ、癒着による腸閉塞を伴うため、積極的に腹腔鏡下手術を導入。これにより痛みの大幅な軽減、歩行・食事開始までの期間の短縮、出血量の軽減が可能となる。腹腔鏡は容易に体腔深部を観察でき、また映像を拡大して手術を行えるため、リンパ節郭清も開腹手術を上回る制度で行える。
ロボット支援下手術のメリット
[術者メリット]
・座りながらの遠隔操作により、肉体的にも視覚的にも術者負担が少なく集中力が持続できる。
・ロボット手術では直接立体視(3D)できる。通常の腹腔鏡下では2Dの映像を頭の中で立体化して行う必要あり。
・腹腔鏡手術よりも更に出血量が少ない。殆ど出血しないことも(術後採血の方が多いくらい)
・解剖上、子宮の前には膀胱、後ろには直腸、脇には尿管があり、臓器が非常に入り組んでおり、周囲の臓器を傷つけずに細かな部分に入り込める点がロボット手術のメリット。
・腹腔鏡下手術よりも小さな動きで広範囲な処置が行える点にある。腹腔鏡オペでは、鉗子の先が固定されているため、鉗子そのものを大きく動かす必要性がある。一方、ロボット手術では、ポート(トロカー)が支点になっており動かず、鉗子の先が360℃回転することで、変幻自在に繊細な作業が行える。
・更に、糸での縫合結紮手技には、非常に高い技術力が求められるが、ロボット鉗子の先は人間の手と同じように動かせるので、細やかに縫うことが可能(医師による技術の差を少なくできる)
[患者メリット]
・術後の炎症所見もあまり見られない。腹腔鏡手術と比較し、炎症反応(CRP値)が低い。
・合併症や感染リスクも減少。
ロボット支援下手術の適応外患者
・頭低位で行うため、脳動脈瘤がある方、眼圧が上がると困る緑内障の方には適さない。
合併症 その他
・一般的な合併症としては、リンパ節郭清によるリンパ浮腫・リンパ嚢腫が挙げられる。
・子宮体がんの進行例では、術後の再発予防のために、化学療法や放射線療法を施行する。これらは手術による体のダメージが軽減してから施行するので、短期間で回復が望める腹腔鏡下手術はより有用だと考えられている。
16.術後療法(化学療法、ホルモン療法)について
ここからは、術後療法についてまとめていく。子宮体癌治療の基本戦略は、可能な限り手術の実施であり、手術摘出物の病理組織検査によって再発リスクを推定することになる。
その結果、低リスクの場合には再発リスクは殆どないため手術で終了。その後、経過観察となる。しかし、再発リスクがある中・高リスクの場合には、術後療法が必要となる。

◆術後療法の比較(化学療法 vs 放射線療法)
術後療法は、国内では中・高リスクともに化学療法が中心となっているが、欧米では中リスクにおいて放射線療法が第一選択となっている。この背景には、放射線療法が受けやすい欧米施設の整備環境要因も大きく影響している。

ただ、化学療法と放射線療法の効果については、両者の比較も含め認識しておく必要がある。以下にて、両者の生存割合について調べた試験結果を記載する(JGOG2033試験)
5年生存割合調査。 上線:化学療法 下線:放射線療法

(結果)
5年生存割合は『85.3% vs 86.7%』で、ほぼ同等(若干、化学療法の試験成績が良好)。つまり、両者の効果に違いがないことが見えてくる。この試験結果をもとに、国内では中リスクに限らず、高リスクでも化学療法を取り入れている。
◆抗がん剤の変遷
子宮体癌に効果が高い抗がん剤は以下の3種類(系統)であり、赤字で記した5つの抗がん剤(子宮体癌治療の基本薬)がよく使用されている。

これまでの変遷を辿ってみると、ドキソルビシン(別名:アドリアマイシン)単独使用に始まり、その後(2005年頃?)、奏功割合1位、2位のシスプラチン(42%)とドキソルビシン(37%)を組み合わせたAP療法が主流となった。それから、AP療法にパクリタキセル(乳癌や卵巣癌でよく使用される)を足したTAP療法を試みた結果、高い効果は表れたものの、副作用として酷い痺れも出現してしまった。結局、この痺れが原因でTAP療法が広まることはなかった。
こういった状況もありAP療法が継続されていたが、しばらくして卵巣癌患者にも使用しているTC療法(パクリタキセルとカルボプラチン)が、なんとなく効果がありそうだということがわかってきた。今現在(2016年当時)は、国内・欧米ともにTC療法が主流となっている(効果が高く、毒性も少ない)。

(上図):右に行くほど毒性が強く、上に行くほど効果が高い
◆問題点
肝心な本来の標準的治療であるAP療法と、主流のTC療法との比較がなされないまま、なんとなく効果がありそうだと言われているTC療法が主流となっているのが現状であり、問題でもある。
そのため、「しっかりと両者の比較をした方がいいのでは?」という論調になり、2010年頃から、まずTC療法 vs TAP療法の臨床試験が行われた。その結果、効果は同程度、毒性が少ない点でTC療法となった。
次に、注目されているAP療法 vs TC療法の効果を比較検討するために、日本国内において下記臨床試験(JGOG2043試験)が行われている。結果は2017年頃に判明?。
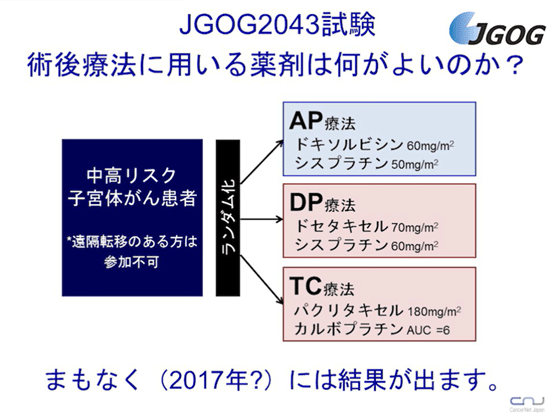
JGOG2043試験
中・高リスクを対象に、AP療法(本来の標準的治療)とTC療法(現在の主流)に期待がもてそうなDP療法を加えた臨床試験。
◆子宮体癌の期待薬 ”ベバシツマブ(商品名:アバスチン)”
子宮体癌の期待薬として注目されている分子標的治療薬のベバシツマブ(商品名:アバスチン)。その効果を示す臨床試験データを下記に2つ示す。ただし、アバスチンは2016年時点では、子宮頸がんと卵巣がんにしか保険適用されていないため、子宮体癌での保険適用が望まれている。
下図は、進行再発の子宮体癌患者に対する”TC療法” vs ”TC療法+ベバシツマブ”の比較試験の報告(2015年 アメリカ臨床腫瘍学会(ASCO)報告データ)

下図
薄紫線:TC療法+アバスチン
濃紫線:TC療法

上記研究結果から、腫瘍が進行するまでの期間は、TC療法+ベバシツマブ群で13カ月となり、TC療法単独の8.7カ月と比較し、かなり伸びていることがわかる。

また、生存期間においても、TC療法+ベバシツマブ群で23.5カ月と、TC療法単独の18カ月と比較し、伸びていることが分かる。
◆ホルモン療法
術後療法として忘れてはならないのがホルモン療法である。抗がん剤と比較し、その効果に懐疑的な意見はあるが、MPA(黄体ホルモン)においては抗がん剤に見劣りしない奏効率(25%)を示す。MPAは、国内で唯一保険収載されているホルモン剤。ヒスロン、プロベラとも呼ばれる。
MPA(Medroxyprogesterone acetate:MPA)とは・・・
・メドロキシプロゲステロン酢酸エステル。
・プロゲステロンタイプの(黄体)ホルモン薬剤のひとつ。
・商品名:ヒスロン、プロベラ

また、黄体ホルモン療法の奏効率を示したのが下図。黄体ホルモンレセプター(ホルモン受容体)がある人には、効果が高いということが分かっている(受容体検査はすぐに行える)。つまり、Grade1(組織分化度:類内膜癌/高分化型)でのMPA奏効率は37%と、かなり高い効果が期待できる。

17.最後に・・・
次回は、ロボット支援下腹腔鏡下膣式子宮全摘術(良性疾患)についてまとめていく予定です。
お読み頂きありがとうございます。もしよろしければサポートお願いしますm(__)m 頂いたサポートは、クリエイターとしての活動費(かけっこ教材などの運営費etc)に使わせていただきます!
