
【CBDの効果】てんかん、アトピー、皮膚炎、腰痛、頭痛、免疫疾患、糖尿病、癌などに関係する論文をレビューおよび評価
本記事では、以下の病気や症状に対するCBDの効果・効能について解説していきます。
●疾患:パーキンソン病、てんかん、皮膚炎、疼痛(痛み)、免疫暴走、炎症性腸疾患、糖尿病、高血圧、癌、その他の疾患
●CBDの副作用、用量設定、利用目的に関する概略
ここでは、エビデンスとなる臨床試験を実施した論文などを必要に応じて情報・知識として引用しています。そのうえで、信ぴょう性の高いCBDの効果・効能を考察し、まとめています。
前回の記事「【CBDの効果】論文によるエビデンスをもとに精神疾患への効果を解説(うつ病、双極性障害、不安障害、不眠症など)」の続編になりますので、まだ読んでいない方は最初の導入部分(無料公開部分)だけでも見て頂けると、今回の記事をスムーズに読み進められるかと思います。今回取り上げるてんかんや炎症などに対するCBDの効果についても言及しています。以下にもリンクを貼っておきます。
今回の内容は、上の記事の続きになります。
なお、前述した通り、精神疾患以外の疾患や症状:パーキンソン病、てんかん、皮膚炎、疼痛(痛み)、免疫暴走、炎症性腸疾患、糖尿病、高血圧、癌、その他の疾患、に対するCBDの効果を調査した臨床研究のレビューや考察に関して今回は取り上げていきます。
まず、目次を見て、ご自身の知りたいテーマがあるかをご確認ください。関連する内容を網羅的に取り上げているので、その他の内容も役立つ情報になるかと思います。
◆CBDと神経疾患

神経疾患に関して、パーキンソン病の前に、てんかんについて先に取り上げたいと思います。
なお、神経疾患の概要についても前回のnote「【CBDの効果】論文によるエビデンスをもとに精神疾患への効果を解説(うつ病、双極性障害、不安障害、不眠症など)」で解説しているので興味のある方はご覧ください。
・てんかん(けいれん、発作)
CBDはてんかん発作への有益な効果で大きなブレイクスルーがあり、日本でもCBDの難治性てんかんへの効果が注目されています。

てんかんとは、発作や意識障害を慢性的に繰り返す脳の病気で、脳内の神経細胞の過剰な電気的興奮によって症状が引き起こされます。てんかんは特に小児、思春期、高齢での発症率が高く、過半数が原因不明だと言われています。ただし、脳血管障害や脳腫瘍、認知症などが発症原因になることもあります。また、てんかんは自閉症などの発達障害とも医学的に類似した部分があり、けいれんによる発達障害の症状の悪化が懸念されます。ほかにも知的障害や運動障害、言語障害が見られることもあり、さらに、二次的併存症としてうつ病や不安障害などの問題も起きる恐れがあるとされています。てんかんの種類は非常に多く報告されていますが、特に重篤な脳機能障害をきたす、ドラベ症候群やレノックス・ガストー症候群などの難治性てんかんは、その過酷な臨床経過から破局てんかんとも呼ばれています。
背景
2013年にアメリカのテレビ局CNNが放映した番組『WEED』が全米を騒然とさせました。以下がその内容です。
この番組の主人公は、週に300回以上のけいれん発作に苦しみ、心肺停止にまで陥ったことのある女の子でした。彼女はドラベ症候群という難治性てんかんでした。強い副作用のある複数の薬を投与しても、どれも成果はありませんでした。そんななか、両親が藁にもすがる思いで手に入れた高濃度CBD品種の大麻を彼女に使用したところ、発作がほとんど治まったのです。
この事実は全米に影響を与え、大麻合法化の波を大きく後押ししていくことになります。このような影響もあり、その後、CBDのてんかんに対する有効性を調査するための大規模な臨床試験が行われるようになりました。
2018年6月には、米国食品医薬品局(FDA)が、ドラベ症候群(DS)とレノックス-ガストー症候群(LGS)の治療を目的とした、高度に精製された大麻由来のCBDの調剤(Epidiolex)を承認しました。
2019年3月には日本でも大麻由来のCBD製品が国内の臨床試験で使用できるようになりました。このようなてんかんに対する臨床試験がまとめられ、有効なデータが得られてくると、大麻取締法の改正にもつながってくると考えられます。
ここではCBDの有効性が認められた重要な臨床試験の研究報告を主に取り上げていきたいと思います。そのうえで、CBDの大規模臨床試験のその後と抗てんかん薬との併用による影響についても詳しくまとめていきます。
大規模臨床試験その1
2017年、ドラベ症候群の患者120人に対する「ランダム化二重盲検プラセボ比較対照試験(GWPCARE1試験)」が報告されました。
【引用文献:Trial of Cannabidiol for Drug-Resistant Seizures in the Dravet Syndrome. N Engl. J Med. 2017, 376, 2011.】
ドラベ症候群は全身けいれん発作などを繰り返す指定難病であり、高い死亡率を伴う難治性の小児てんかん障害です。ほとんどの場合、一歳までに発症し、その後も発作を繰り返します。この試験ではCBDオイルによって、てんかん発作の頻度が有意に減少し、発作が完全に止まった患者もいました。具体的には、応答率(=けいれん発作が50%以上減少した人の割合)について、プラセボ(応答率27%)と比較して、CBD治療群(20 mg / kg /日の投与で応答率43%)で有意に高い応答率を示しました。同様に、プラセボよりもCBDの有効性を支持する顕著な違いは、けいれん発作(発作頻度変化:CBD20 mg/kg vs プラセボで、-38.9% vs -13.3%)の頻度変化でも観察されました。
【設定】(※ここからの「設定」や「結果」は必要な箇所以外は読み飛ばしても問題ありません。)
ドラベ症候群と診断されていた参加者の年齢は2〜18歳(平均9歳)で52%が男でした。適格とされた参加者の120人はランダムでプラセボ群59人と10%CBDオイル群(=CBD群)61人に割り当てられました。安定している抗てんかん薬の摂取に加えて、それぞれプラセボもしくはCBDオイルが1日2回に分けて投与されました。使用されたCBDオイルは「エピディオレックス」という大麻草由来の10%CBDオイルで、ハイになる成分のTHCをほとんど含まないものでした。治療期間は14週間で、最初の2週間が用量漸増期間、その後の12週間が用量維持期間でした。CBD群では、最初の2週間で20mg/kg/dayまでCBDの用量を増やしました(エピディオレックスは2.5mg/kgから始めることが多い)。
なお、治療前の4週間のベースライン期間(参加者の選定のための期間)で、ひとつ以上の抗てんかん薬を服用して4以上のけいれん発作がある者を参加者として適格としました。
また、使用していた抗てんかん薬の種類において、それぞれ人数の割合は以下の通りでした。
クロバザム65%
バルプロ酸59%
スチリペントール42%
レベチラセタム28%
トピラマート26%
【結果】
評価は2、4、8、14週間後に実施されました。治療終了後には10日間の減薬期間があり、毎日10%ずつ10日間で用量が漸減されました。治療の早期中止者は、減薬期間の終わりに評価されました。なお、治療期間中にはCBD群61人のうち9人の離脱(うち8人は副作用が理由で離脱)、プラセボ群59人のうち3人の離脱(うち1人は副作用が理由で離脱)があり、治療期間終了時には全体で108人になりました。さらに、減薬期間においてCBD群で1人が減薬中に副作用のため離脱がありました。
結果の主要評価項目は治療期間中の1か月あたりのけいれん発作頻度におけるベースラインからの変化でした。けいれん発作頻度の変化はそれぞれCBD群で12.4回/月→5.9回/月(発作頻度の変化率:-38.9%)、プラセボ群で14.9回/月→14.1回/月(-13.3%)となり、けいれん発作ではCBDで明らかに有意な減少が見られました。
なお、維持期間の最初の月、つまり治療期間開始後2週間〜6週間で、けいれん発作頻度はCBD群で12.4回/月→5.0回/月、プラセボ群で14.9回/月→13.0回/月となりました。発作が完全に止まった者もCBD群のみで3人いました。また、けいれん発作が50%以上減少した人の割合(応答率)は、CBDおよびプラセボ群でそれぞれ43%と27%でした。
一方で、非けいれん発作ではプラセボと比較して有意差はありませんでした。もしくは、親が気づきにくく、カウントが正確でなかった可能性もあります。
副作用については以下のような症状がありました。
傾眠・眠気、食欲減退、下痢、疲労、嘔吐、倦怠感・無気力、けいれん、発熱、肝臓異常
CBD群61人、プラセボ群59人のうち、副作用があった人数は以下の表のようになりました。

最も多い「傾眠」ではほとんどの人が抗てんかん薬のクロバザムを利用していました。「肝臓異常」とは肝臓アミノトランスフェラーゼ酵素レベルの上昇を示しており、抗てんかん薬のバルプロ酸を利用していた人のみで見られました。しかし、服用を続けていると酵素レベルの増加はほぼ解消されました。すなわち、可逆性があり、肝臓に対する一時的な代謝ストレスの可能性あります。
抗てんかん薬には「肝障害、傾眠、無気力、睡眠障害、行動障害」などの副作用があり、このような副作用がCBDとの薬物間相互作用で助長された可能性があります。また、肝障害の代表的な症状には「腹痛、食欲減退、体重の変化、無気力・倦怠感、発熱、吐き気・嘔吐、かゆみ」などがあります。つまりどの副作用の症状もCBDと抗てんかん薬との薬物間相互作用(あるいは肝障害の相乗効果など)による影響が関与していると考えられ、純粋なCBDの副作用と言うことは難しいと言えます。
大規模臨床試験その2
さらに、最近の第III相RCT(ランダム化比較対照試験GWPCARE2)では、ドラベ症候群と診断された小児および若年成人の集団において、CBD 10および20 mg / kg /日の有効性と忍容性がプラセボと比較されました。
【引用文献:GWPCARE2 A Study to Investigate the Efficacy and Safety of Cannabidiol (GWP42003-P) in Children and Young Adults With Dravet Syndrome. ClinicalTrials.gov identifier: NCT02224703.】
世界中(38か所)から集められた198人のドラベ症候群の患者が、CBD 10もしくは20 mg / kg /日、プラセボをそれぞれ摂取する3つのグループにランダムで割り当てられ、14週間(2週間の滴定と12週間の維持)の治療が実施されました。最近リリースされた予備データでは、プラセボ(応答率26.2%)と比較して、両方のCBD治療群(10および20 mg / kg /日グループでそれぞれ応答率43.9%および49.3%)で有意に高い応答率(=けいれん発作が50%以上減少した人の割合)を示しました。同様に、プラセボよりもCBDの有効性を支持する顕著な違いは、けいれん(発作頻度変化:CBD10および20 mg/kg vs プラセボで-48.7%と-45.7% vs -26.9%)と発作全体(-56.4%と-47.3% vs -29.7%)の両方の頻度変化でも観察されました。

大規模臨床試験その3
2018年には、レノックス・ガストー症候群の患者225人に対する「ランダム化二重盲検プラセボ比較対照試験(GWPCARE3試験)」が報告されました。
【引用文献:Effect of cannabidiol on drop seizures in the lennox-gastaut syndrome. N Engl. J Med. 2018, 378, 1888.】
レノックス・ガストー症候群は重度のてんかん性脳症であり、8歳までに発症することが多く、その90%以上が成人になっても症状が続きます。特徴的なてんかん発作が何種類も発症し、知的障害もほぼ全例に出現する疾患です。結果について、レノックス・ガストー症候群に特徴的な転倒発作の頻度の変化率は、CBD20mg/kgを受けた患者の方がプラセボを投与された患者よりも有意に優れていました(-41.9%対-17.2%)。同様に、転倒発作の有意な応答率も見られました(CBD 20mg/kgで39%、プラセボで14%)。
【設定】
レノックス・ガストー症候群と診断されていた参加者の年齢は2〜55歳(平均15〜16歳)で57%が男でした。適格とされた参加者の225人はランダムでプラセボ群76人と、一日当たり10mg/kgまたは20mg/kgのCBDが投与される10%CBDオイル投与群73人または76人(それぞれCBD10群およびCBD20群)に割り当てられました。安定している抗てんかん薬の摂取に加えて、それぞれプラセボもしくはCBDオイル(エピディオレックス)が1日2回に分けて投与されました。治療期間は14週間で、最初の2週間が用量漸増期間、その後の12週間が用量維持期間でした。最初の2週間で、2.5mg/kgから始めて、1日あたり均等量ずつ増やしていき、10または20mg/kg/dayまで用量を増やしました。なお、CBD10群から6人がやむを得ず一時的に基準を超えた用量になりました。
なお、治療前の4週間のベースライン期間(参加者の選定のための期間)で、ひとつ以上の抗てんかん薬を服用して、毎週1週間のうち2以上のけいれん発作がある者を参加者として適格としました。
また、使用していた抗てんかん薬の種類において、それぞれ人数の割合は以下の通りでした。
クロバザム49%
バルプロ酸38%
レベチラセタム31%
ラモトリジン30%
ルフィナマイド29%
【結果】
評価は2、4、8、14週間後に実施され、治療終了後には10日間の減薬期間がありました。なお、治療期間中にはCBD20群76人のうち9人の離脱(うち6人は副作用が理由で離脱)、CBD10群73人のうち2人の離脱(うち1人は副作用が理由で離脱)、プラセボ群76人のうち2人の離脱(うち1人は副作用が理由で離脱)があり、治療期間終了時には全体で212人になりました。
結果の主要評価項目は治療期間中の1か月あたりの発作頻度におけるベースラインからの変化でした。結果は以下の通りです。
●転倒発作(脱力発作)頻度のベースラインからの減少率(中央値)
CBD20群41.9%
CBD10群37.2%
プラセボ群17.2%
・転倒発作頻度がベースラインから少なくとも50%減少した患者の割合
CBD20群39%
CBD10群36%
プラセボ群14%
・転倒発作頻度がベースラインから少なくとも75%減少した患者の割合
CBD20群25%
CBD10群11%
プラセボ群3%
●発作全体のベースラインからの減少率(中央値)
CBD20群38.4%
CBD10群36.4%
プラセボ群18.5%
●転倒発作以外の発作のベースラインからの減少率(中央値)
CBD20群54.6%
CBD10群61.1%
プラセボ群34.3%
◎介護者の全体的な印象で少なくとも改善したとみられた患者の割合
CBD20群57%
CBD10群66%
プラセボ群44%
これらの結果より、CBDがプラセボよりも明らかに転倒発作(脱力発作)の頻度を大幅に減少させることを示しました。しかもその他の発作頻度も大幅に減少させました。なお、発作が完全に止まった者はCBD群で8人、プラセボ群で1人いました。
副作用については以下のような症状がありました。
傾眠・眠気、食欲減退、下痢、嘔吐、発熱、肝臓異常
CBD20群82人、CBD10群67人、プラセボ群76人のうち、副作用があった人数は以下の表のようになりました。※ここでは、CBD10群の6人で一時的に用量が増えたことを考慮して、CBD10群の6人をCBD20群として数えています。

「肝臓異常」とは肝臓アミノトランスフェラーゼ酵素レベルの上昇を示しており、最大で正常範囲の3〜12倍でした。異常はCBD20群で11人、CBD10群で3人でみられ、抗てんかん薬のバルプロ酸を利用していた人がそれぞれの群で9人、2人いました。CBD服用群で肝酵素レベル上昇の肝障害を示したのは14人/149人なので、CBD投与者の9%でした。しかし、それぞれ治療期間中、もしくは減薬、断薬の段階で酵素レベルの増加がほぼ解消されました。すなわち可逆性があり、肝臓に対する一時的な代謝ストレスの可能性あります。さらに、これらの範囲は重篤な薬物誘発性肝障害の基準を満たしていませんでした。
前述したように、抗てんかん薬には「肝障害、傾眠、無気力、睡眠障害、行動障害」などの副作用が考えられ、このような副作用がCBDとの薬物間相互作用で助長される可能性があります。特にCBDは肝酵素阻害により抗てんかん薬のクロバザムの血中濃度を高めた可能性が高いと指摘しています。なお、患者の約半数がクロバザムを併用していました。また、肝障害の代表的な症状には「腹痛、食欲減退、体重の変化、無気力・倦怠感、発熱、吐き気・嘔吐、かゆみ」などがありますが、バルプロ酸とCBDの肝臓への副作用の相乗効果によって、一部でこれらの症状が生じている可能性があります。
【考察】
プラセボと比較したときのくすりの実力を示す指標にNNT(必要症例数)というものがあります。NNTの数字が意味するのは「ある効果を得る患者を1人増やすために、何人の患者を必要とするかを示すもの」です。
NNTの計算法は、試験薬による改善者の割合(改善したヒトの数の割合)からプラセボによる改善者の割合を引いた数字の逆数となります。例えば、転倒発作頻度が50%以上減った患者の割合で計算すると、この割合はCBD20群で39%、プラセボ群で14%という結果だったため、39%-14%=25%の逆数をとって1/0.25=4となり、CBD20群でNNTは4となります。つまり、CBD 20mg/kg/dayの服用で転倒発作頻度を50%以上減らす効果を得る患者を1人増やすためには、4人の患者を必要とすると言えます。もちろん、数字が小さいほど実力があり、プラセボとの差も大きくなります。同様に計算すると、CBD10群ではNNTは5となります。また、75%以上の発作頻度の減少だと、CBD20群でNNTは5、CBD10群でNNTは13となります。
NNTが4や5というと、素人には数字が大きいように見えるかもしれません。しかし、もちろん疾患にもよりますが、難治性てんかんの発作に対してこの4や5という数字は非常に素晴らしい結果と言えます。
異なる疾患で薬のNNTを比較するのは、かなり大胆なことではありますが、そういった論文を発表した研究者もいます。急性の症状に使用する薬はNNTが低くなりやすく、2〜3となります。やや治りやすい急性あるいは慢性の症状はNNTが4〜6くらいになります。アスピリンでの痛みの半減におけるNNTは4くらいとされています。これは意外に感じた方が多いのではないでしょうか。アスピリンはバファリンなどの成分としても有名です。そうです、私たちはプラセボ効果による影響を殆どの場合において受けているのです。強調しておきますが、難治性てんかんに対して従来の抗てんかん薬はほとんど効果を見込めませんでした。
ただし、NNTは完璧な指標ではありません。例えば副作用です。NNTが小さいとその分副作用が大きくなることがしばしばあります。つまり副作用に関する情報は欠けています。また、NNTだけではプラセボ効果の実力はわかりません。例えば、プラセボによって改善した人が50%いて、試験薬によって改善した人が70%いたとするとNNTは5です。一方で、プラセボによる改善が5%いて、試験薬による改善が25%でもNNTは5です。前者だと、精神療法や自然治癒による回復がありうるので、様子を見てみようということになるかもしれません。後者だと、薬で少しでも良くなる可能性があるならと薬を使用することになるかもしれません。このように同じNNTでも差があり、特に「副作用」と「プラセボの実力」の2点に関しては注意すべきでしょう。
大規模臨床試験その4
同様にLancetで報告されたGWPCARE4試験では、171人のレノックス・ガストー症候群の患者のうち86人にCBD 20 mg / kgが投与されました。
【引用文献:Cannabidiol in patients with seizures associated with Lennox-Gastaut syndrome (GWPCARE4): a randomised, double-blind, placebo-controlled phase 3 trial. Lancet 2018, 391, 1085–1096.】
前述のGWPCARE3試験の結果は、ここでのGWPCARE4研究によって、さらに裏付けられました。転倒発作頻度の変化率は、CBDを受けた患者の方がプラセボを投与された患者よりも有意に優れていました(-43.9%対-21.8%)。同様に、転倒発作の有意な応答率も見られました(GWPCARE4:CBD 20で43.9%、プラセボで21.8% ; GWPCARE3:CBD 10で36%、CBD 20で39%、プラセボで14%)。なお、応答率とは転倒発作が50%以上減少した人の割合を意味します。転倒発作に対する臨床的利益は、12週間の維持期間全体にわたって持続するように見えました。興味深いことに、ここでもCBDは非転倒発作にも効果的であることが判明し、さらに同様の傾向は「全発作」でも観察され、すべての種類の発作の治療におけるCBDの有効性を裏付けています。

大規模臨床試験のその後と抗てんかん薬との併用による影響
最近発表されたレビューでは、その後のてんかんにおけるCBD利用の課題や展望がまとめられました。
【引用文献:Cannabinoids in the Treatment of Epilepsy: Current Status and Future Prospects. Neuropsychiatr. Dis. Treat. 2020, 16. 381–396.】
上で紹介した大規模なドラベ症候群(DS)およびレノックス・ガストー症候群(LGS)におけるCBD臨床試験について、それらの延長試験が報告されていますが、臨床的利益は時間とともに持続するようであり、耐性は観察されなかったようです。
一方で、非常に物議を醸していたこととして、重要なRCT(ランダム化比較対照試験)への参加者の多くの割合(およそ50~65%)が、抗てんかん薬のクロバザムを併用しており、臨床的に関連している可能性があるという議論が挙げられます。実際、小児期発症の薬剤耐性てんかん(DRE)患者の集団における追加治療薬としてのCBDに関する最初のオープンラベル試験では、クロバザムを服用している被験者における発作頻度減少の応答率(運動発作:motor seizures)がそれ以外の被験者と比較して高い(51%対27%)ことを発見しました。その上、クロバザムの併用が運動発作頻度の減少を予測する唯一の因子であったことを示した調査結果もあります。発作の結果に対するクロバザムの影響が指摘されることにより、CBD単独の抗けいれん作用について疑問が投げかけられるようになりました。
しかし、GWPCARE3/4でのレノックス・ガストー症候群(LGS)患者に対して行われた事後分析で、クロバザムの存在に関わらずCBDはプラセボより有効であることが示されました。この結論は、CBDが投与された際のクロバザムによる影響を評価した最近のオープンラベル試験の結果とも一致していました。とはいえ、クロバザムとの併用が臨床的にプラスに働いている可能性を完全に否定することはできないため、解釈には注意しておかなければなりません。
副作用についてもいくつかレビューがあります。小児および成人の薬剤耐性てんかん患者に対するCBDのオープンラベル試験では、128/162(79%)が副作用を報告し、最も一般的なのは傾眠(25%)、食欲低下(19%)、下痢(19%)、疲労(13%)、けいれん(11%)でした。さらに、48人の参加者が深刻な有害事象を発症し、20人の症例(12%)でCBDに因果関係があるとみなされました。しかし、興味深いことに、有害事象のためにCBDを中止した患者はわずか3%であり、治療に関連する利点が欠点を上回った可能性を示唆しています。
3つの重要なRCTに参加したDSおよびLGS患者550人全体に関する最近のメタ分析では、プラセボ投与を受けて治療を中止したのは2.6%であったのに対し、CBDを摂取して治療を中止したのは11.1%でした。有害事象は、CBD群とプラセボ群のかなりの割合(それぞれ87.9%と72.2%)の患者から報告されましたが、ほとんどが軽度から中等度で、概して一過性のものでした。ある調査結果によると、最も一般的な有害事象は、傾眠(24.5%)、食欲の低下(20.1%)、下痢(18.2%)、およびトランスアミナーゼのレベルの上昇(16.1%)でした。トランスアミナーゼの上昇は、ほとんどが初期に見られ、一時的なものであり、その後に解消されました。興味深いことに、バルプロ酸を併用して服用している患者のみが顕著なトランスアミナーゼレベルの増加を引き起こす可能性があることが確認されています。また、傾眠のような有害事象はクロバザムを受けている被験者でより観察される可能性が高いように見えました。これらの結果は、抗てんかん薬とCBDの薬物間相互作用による副作用の発生を示唆しています。実際に最近の報告で、てんかんの研究を除外した場合、CBD治療に明らかに関連する有害な結果は下痢だけだったと報告されています。

さらに、DSおよびLGS以外の小児発症の薬剤耐性てんかんに苦しむ複数の患者が補助治療としてCBDを受けることができるようになりました。中でも、結節性硬化症(TSC)はこれまで最も広範囲に調査されています。結節性硬化症(TSC)とは、遺伝子TSC1、TSC2の産生タンパク質の機能不全により、てんかんや精神発達遅滞、自閉症、腎血管筋脂肪腫、リンパ脈管筋腫症、顔面の血管線維腫などの過誤腫を全身に生じる疾患です。
2〜31歳のTSCの診断を受けた18人の被験者が、CBD評価試験に登録され、6か月以上追跡されました。なお、患者の大半(14/18)は発達遅延を示しています。
【引用文献:Cannabidiol as a new treatment for drug-resistant epilepsy in tuberous sclerosis complex. Epilepsia 2016, 57(10), 1617–1624.】
CBDは5 mg / kg /日の初期用量で投与され、その後は最大25 mg / kg / 日まで投与されました。ただし、発作を十分に制御できない場合は最大用量の50 mg / kg / dayまで増加させることができました。12か月のフォローアップを達成したのは8/18人の被験者だけでしたが、全体的な平均発作頻度は経時的な減少傾向を示しました。発作の頻度変化は、他の焦点発作と比較して、特に強直間代発作(-91.4 % [対象は6人])、点頭てんかん(乳児けいれん)(-87.5% [対象は4人])および脱力発作(-86.5% [対象は4人])で顕著でした。さらに、3ヶ月での応答率は点頭てんかんと脱力発作で、より高かった(それぞれ75% [いずれも4人中3人])。クロバザムを併用した12/18人の患者のうち、58.3%(7人)が3か月の時点で治療に反応していました。さらに、認知および行動における改善がそれぞれ85.7% (14人中12人)および66.7% (9人中6人)の症例で報告されました。著者らは、CBDはTSC患者にとって忍容性があり効果的な補助的治療薬になる可能性があると結論付けました。しかし、付随する有害事象は最小限に抑えられましたが、最初の3か月間は完全に回避できませんでした。
さらに1〜65歳(平均14歳)の224人のTSC患者に対してRCT(GWPCARE6)が実施されました。
【引用文献:GW Research Ltd. A randomized controlled trial of cannabidiol (GWP42003-P, CBD) for seizures in tuberous sclerosis complex (GWPCARE6). ClinicalTrial.gov Identifier: NCT02544763.】
224人のTSC患者は、CBD 25 mg / kg /日(75人)およびCBD 50 mg / kg /日(73人)、プラセボ(76人)がそれぞれ投与される群に割り振られ、16週間の治療(4週間の滴定と12週間の用量維持)での安全性と有効性が評価されました。主な評価項目は全体的な発作頻度の変化でしたが、いくつかの副次的な評価項目には、さまざまな種類の発作(意識障害のある、またはない焦点発作、点起始両側強直間代発作、全般発作)における頻度の変化およびインスリン成長因子(IGF1)の血清レベルも評価されました。結果、発作頻度の低下率は、プラセボ(26.5%)と比較して、CBD 25グループ(48.6%)とCBD 50グループ(47.5%)の両方で有意に高かったことを発表しました。
また、Devinskyらは、CBD(> 20 mg / kg)を受けたCDKL5欠損症(20例)、アイカルディ症候群(19例)、ドーゼ症候群およびDup15q症候群(各8例)といった、特定のてんかん症候群と診断された55人の患者らのデータを分析しました。
【引用文献:Open-label use of highly purified CBD (Epidiolex®) in patients with CDKL5 deficiency disorder and aicardi, Dup15q, and doose syndromes. Epilepsy Behav. 2018, 86, 131–137.】
これらの分析では、12週間でけいれん発作の月間頻度の大幅な減少を示し(ベースライン時の中央値59.4回/月からフォローアップ時の22.5回/月まで)、48週間以上持続したことがわかりました。けいれん発作の応答率は12週間で50%、48週間で57%でした。ただし、これらの難治性症候群における補助薬としてのCBDの有効性について結論を出す前に、さらなる研究の実施が必要です。
<考察・まとめ>
まとめると、てんかんに対するCBDの有効性を裏付ける確固たる証拠は、ドラベ症候群(DS)およびレノックス・ガストー症候群(LGS)の重要なRCT(ランダム化比較対照試験)から得られました。これらの結果は、発作が50%以上減少した人の割合(=応答率)がおよそ36%~50%の範囲であり、けいれん発作/転倒発作からの解放(発作の解消)の割合が約5%であることを示しました。これは、てんかん性脳症でみられる治療抵抗性を考慮すると注目に値する結果です。CBDによる有害事象は主に中枢神経系の症状と消化管障害でしたが、それらの多くは軽度から中程度で、一般的に一時的なものでした。CBDを処方するとき、その限られた治療適応症、その起こり得る副作用、および同様に重要な薬物間相互作用(による臨床的効果の増強および有害事象の発生)を考慮に入れておく必要があるということが指摘されています。

最近、日本でもCBDサプリメントが薬剤耐性の早期乳児てんかん性脳症の治療に非常に効果的にはたらき、強直発作を解消することが確認された症例が報告されました。
【引用文献:Report of a 6 month old Asian infant with early-infantile epileptic encephalpathy whose seizures were eliminated by cannabidiol. Epilepsy & Behavior Reports 2020, 100373.】
乳児は、妊娠39週目の誕生から強直発作に苦しみ始め、すぐに入院しました。フェノバルビタール、ゾニサミド、ビタミンB6、クロバザム、レベチラセタム、トピラメート、フェニトイン、バルプロエート、高用量フェノバルビタール、ACTH療法の試験では発作を制御できませんでした。彼は130日齢で退院しましたが、平均して1日20〜30回の強直発作がありました。退院後も高用量フェノバルビタールによる薬物療法が続けられましたが、耐性によるものなのか、発作頻度は増加していきました。207日齢でCBDサプリメントの投与を開始し、219日齢に投与量18 mg/kg/日(150mg/日)まで増量しました(15% CBDオイル:Hemptouch® CBD 1500 mg / 10 ml)。すると、彼の発作頻度は減少していき、234日齢までに強直発作は完全に消失しました(下図)。フェノバルビタールとCBDを併用していましたが、およそ250日齢以降から徐々にフェノバルビタールを減量していき、およそ490日齢には発作が再発することなくフェノバルビタールを断薬することに成功し、CBD単剤療法に切り替えることができました。

また、重大な副作用が報告されることはありませんでした。CBDの治療の前に、彼は複数の標準治療を受けていましたが、明確な効果が現れていなかったため、彼の寛解が219日目に導入された高用量CBDによるものであったと言えます。薬剤耐性てんかんの治療におけるCBDの有効性は、ヨーロッパと米国での大規模な臨床試験で確認されていますが、日本では生後6か月の乳児での有効性を実証した報告はありません。この結果は、(日本あるいはアジアでも)CBDによって乳児の薬物耐性てんかんを効果的に治療できる可能性を示唆しています。
まとめると、CBDは、てんかん発作に対して明らかに有効であり、脳内の居所的に過剰な神経細胞の電気的興奮を和らげて落ち着かせることができる可能性が示されました。
・パーキンソン病 /ハンチントン病
CBDはパーキンソン病患者のQOL(生活の質や幸福度)を改善するという結果が報告されています。ここではパーキンソン病を主に取り上げますが、後ほどハンチントン病についても少しだけ触れます。
パーキンソン病は難治の神経障害のなかで最も患者の多い疾患です。この疾患では運動機能障害が特徴的な症状として現れますが、非運動症状も深刻なものが多くあります。パーキンソン病の発病の原因はまだはっきりとよく分かっていませんが、発症年齢は50〜60歳代で多く、男性よりも女性がなりやすいと言われています。
パーキンソン病の主な症状には以下の運動障害が挙げられます。
・手や足などのふるえ (振戦)
・筋肉の緊張や関節のこわばり (固縮)
・動作障害、動き出しの遅延 (寡動)
・身体が傾くと転倒しやすい状態 (姿勢反射障害)
これらにより歩行障害や動作の不自由化、コミュニケーション障害などが生じます。
また、以下の非運動症状も深刻です。
排泄障害(便秘、排尿困難、よだれ)、嗅覚低下、身体の痛み、睡眠障害、記憶障害、立ちくらみ、うつ、幻覚・妄想
これらは病気の経過年数によって、出現する症状が異なってきます。
ほかにも、ジスキネジア(身体の一部が勝手に動く)といった症状もあります。
従来の治療薬であるドーパミン作動薬は運動障害の主な緩和治療に使用され、疾患の初期段階で特に効果的です。ただし、パーキンソン病の進行は止められず、これらの薬物療法は症状を軽減させるその場しのぎの方法でしかありません。また、非運動症状はドーパミン作動薬では反応せず、悪化することすらあります。したがって、うつ病や不安症、精神病、認知症、疼痛などの非運動症状を改善できる、ドーパミン作動系システムとは異なるメカニズムを利用した治療法が必要とされています。
背景
大麻成分のカンナビノイドの一種であるCBDは従来とは異なる複数の作用機序が示されており、CBDの神経保護効果はアルツハイマー病(認知症)、パーキンソン病、ハンチントン病などの神経変性疾患に関する調査の対象となっています。このなかでもパーキンソン病に関するヒト臨床研究が最も進んでおり、パーキンソン病の新しい神経保護薬として有望視されています。
手が震えたり動作が遅れるといった、パーキンソン病に見られるような症状が続くと日常生活に支障がでたり、生活の質(QOL)の低下につながります。そのような症状に悩む方が実際に皆さんの身近にもいらっしゃるかもしれません。では、現時点で、パーキンソン病に対するCBDの効果にどのくらい期待ができるのでしょうか。
パーキンソン病に対するCBDの効果を調査した臨床試験をレビューしたところ、パーキンソン病患者の精神症状や睡眠の質、QOLなどがCBDの服用によって改善されていました。ただし、高用量のCBDの使用には注意が必要だということが示唆されていました。とはいえ、まだまだ研究が不足しており、CBDの効果を結論付けることまではできませんでした。

1985年に報告された症例では、CBD 200mgにおいてジスキネジア(意図せず出てしまう動き)の改善が報告されましたが、300mgを越える用量だとパーキンソン病の症状に悪影響を与えたという結果が見られました。
【引用文献:Neurology 1985, 35, 201.】
また、1986年に報告された予備的なオープンパイロット研究では、ジストニア運動障害の患者5人に標準的な薬剤とともにCBDが投与されました。ジストニアとは筋肉に勝手に力が入ってしまう運動障害で、神経変性疾患と関与しています。
【引用文献:Open label evaluation of cannabidiol in dystonic movement disorders. Int. J Neurosci. 1986, 30(4), 277‐282.】
6週間の治療期間でCBDの経口用量は100 mg /日から600 mg /日まで増量されました。ジストニアの改善は、すべての患者で観察されました。しかし、パーキンソン病の特徴が共存する2人の患者では、300 mg /日を超える用量のCBDが運動機能の低下と安静時振戦の悪化を引き起こしました。なお、CBDの副作用は軽度で、低血圧、口渇、立ちくらみ、鎮静などがありました。
2009年には、パーキンソン病患者に対するCBDの有効性を直接評価するために実施されたオープンラベルによる臨床試験の結果が報告されました。
【引用文献:Cannabidiol for the treatment of psychosis in Parkinson’s disease. J Psychopharmacol. 2009, 23, 979.】
この研究では、パーキンソン病と診断され、少なくとも3ヶ月間の精神病に悩まされていた6人の患者が試験対象に選ばれました。患者らは通常の治療に加えて、4週間の期間、1日あたり150〜400mgのCBDが投与されました。評価には、簡単な精神症状評価スケールやパーキンソン精神病アンケートが利用されました。結果はCBD治療で有意な精神症状の軽減が見られました。さらに、認知や運動機能に影響を与えず、悪影響は観察されませんでした。
2014年には4人のパーキンソン病患者の睡眠障害に対するCBDの影響がまとめられ、報告されました。この症例報告では、CBDの使用により、いずれの患者でもレム睡眠行動障害の頻度が迅速かつ大幅かつ持続的に減少しました。さらに副作用も見られなかったとのことです。
【引用文献:Cannabidiol can improve complex sleep‐related behaviours associated with rapid eye movement sleep behaviour disorder in Parkinson's disease patients: a case series. J Clin. Pharm. Ther. 2014, 39, 564.】

さらに同じ年の2014年に、パーキンソン病に対するCBDのランダム化比較対照試験が報告されました。
【引用文献:Effects of cannabidiol in the treatment of patients with Parkinson’s disease: An exploratory double-blind trial. J Psychopharmacol. 2014, 28, 1088.】
参加者はパーキンソン病に特有の運動障害があり、認知症または併存する精神症状が見られない21人の患者が選ばれました。患者らはプラセボ、CBD 75mg/day、CBD 300mg/dayの3つのグループに7人ずつ割り当てられました。結果、パーキンソン病患者の幸福と生活の質に関する評価尺度(PDQ39)において、CBD 300mg/dayのグループでプラセボのグループと比較して有意に改善しました。では、どの程度変化があったのでしょうか。
【設定】
参加者は45歳以上の特発性パーキンソン病患者で、少なくとも30日間の抗パーキンソン薬の安定用量での使用が認められた者に限りました。21人の患者はプラセボ群、CBD75群、CBD300群の3つのグループに7人ずつランダムに割り当てられました。プラセボ群、CBD75群、CBD300群にはそれぞれプラセボ、CBD 75mg/day、CBD 300mg/dayがカプセルとして経口投与されました。治療期間は6週間でした。
パーキンソン病症状における治療前後の評価には、PDQ-39やUPDRSといった評価尺度が用いられました。PDQ-39は、活動性、日常生活動作(ADL)、情緒的健康、スティグマ、社会的支援、認知、コミュニケーション、身体的不快感に関わるそれぞれの項目で構成された評価尺度です。なお、スティグマとは、他者や社会集団によって個人に押し付けられたネガティブなレッテルを指し、偏見的な思考です。また、UPDRSは(1)知的活動・挙動・気分、(2)日常生活活動、(3)運動テスト、(4)合併症の4つのパートで構成された評価尺度になります。
【結果と考察】
6週間の治療前後における評価尺度のスコア変化の結果は以下のようになりました。※スコアが高いと病気の症状がより深刻と言えます。

プラセボ群と比較してCBD300群でPDQ-39(機能と幸福度の評価尺度)のスコアに有意な改善が見られました(p=0.03)。PDQ-39の項目の中の、活動性、日常生活動作、情緒的健康の3つで用量依存的な改善の傾向が見られました(それぞれ p=0.11, 0.02, 0.06)。用量依存的とは、用量を増やすに従い効果が高まるというような規則性が見られることです。特に日常生活動作に関してはCBD300群でプラセボ群と比較して統計的に有意な改善でした(p=0.02)。また、スティグマについてはCBD75群と比較してCBD300群で統計的に有意な改善が見られました(p=0.04)。
CBDは抗不安薬、抗うつ薬、抗精神病薬、鎮静剤のような特性を持つことが研究により報告されています。したがって、情緒的健康や日常生活活動の改善はこのようなCBDの特性に関係していると考えられます。
ただし、ベースラインにおけるプラセボ群のPDQ-39合計スコアが23.8と低いのはバイアスになる可能性がかなり高いように思えます。なぜならばプラセボ群でスコア低下のハードルが高くなってしまうからです。なお、CBD300群のベースラインにおけるPDQ-39合計スコアは47.3でした。これだけ見るとかなり怪しい結果に思えます。項目ごとのベースラインにおける詳細なスコアは論文内に見当たらなかったため、どの項目にこのバイアスが強い可能性があるか判断できませんでした。このことから、この研究を引用する場合は解釈にかなり注意が必要ということが分かりました。

なお、平均年齢や疾患の種類も関係しているかもしれませんが、この結果を見る限り十分な効果を得るためのCBDの用量は300mg付近かそれ以上の量であるかのように思えます。ただし、前述したように、1985年および1986年に報告された研究では、300mgを越える用量だと運動症状に悪影響を与えたという結果が見られているため、用量は慎重に決定されなければなりません。
一方で、パーキンソン病症状の評価尺度であるUPDRSのスコアはグループ間で統計的に有意な差はありませんでした。CBDは多くの部位で作用し、局所的な抗炎症作用、酸化ストレスの抑制、グリア細胞活性化の抑制、グルタミン酸ホメオスタシスの正常化といった効果によって神経保護に寄与しうると報告されています。CBDにこのような神経保護作用の可能性が示されているにもかかわらず、UPDRSスコアではグループ間で有意な差は見つかりませんでした。 原因のひとつとして、研究に登録されたサンプルが小さすぎたため、分析の範囲が制限され、明確な結論が得られなかったということがあります。なお、CBDの神経保護効果は動物モデルで報告されていますが、人間では簡単に測定できないため、この点に関しては評価の弊害となっています。
2020年には、パーキンソン病患者のスピーチテストよって引き起こされる不安と振戦に対するCBD投与の影響を調査した研究が報告されました。
【引用文献 :Effects of acute cannabidiol administration on anxiety and tremors induced by a Simulated Public Speaking Test in patients with Parkinson’s disease. J Psychopharmacol. 2020, 34, 189.】
パーキンソン病(PD)患者の不安の徴候および症状に対するCBDの影響を評価するために、疑似公開スピーチテスト(SPST)によって引き起こされる患者の不安感と振戦に対する300 mg用量のCBD単回投与の影響が調査されました。試験はランダム化二重盲検プラセボ比較対照クロスオーバー試験の形式で行われ、PDの合計24人の患者が参加しました。 CBDまたはプラセボを服用した後、参加者はSPST(スピーチテスト)を受け、テスト中に心拍数、全身血圧、振戦の頻度と振幅、さらにVAMSによる不安レベルのスコアが記録されました。結果、CBDはSPSTによって実験的に誘発された不安を有意に軽減し、不安を誘発する状況下では振戦の振幅も有意に低下させました。
<考察・まとめ>
以上、これらのすべての結果から、パーキンソン病に対するCBDの有効性を結論付けるのは難しく、CBDは神経障害に対して直接的に効果を示したというよりかは、精神症状や睡眠を改善して結果的に患者の生活の質(QOL)を向上させたという印象でした。また、長期的なCBDの使用を調べた研究もなかったため、CBDがパーキンソン病の進行を妨げるかどうかなどについては可能性がありますが、まだよくわかっていません。今後はより大規模なランダム化二重盲検プラセボ比較対照試験が必要でしょう。
ハンチントン病について
一方で、ハンチントン病もパーキンソン病と同様の神経変性疾患です。ハンチントン病は遺伝性の神経変性疾患で、舞踏運動などの不随意運動(意図なく体が動いてしまう運動)、精神障害、行動異常、認知障害などの症状を特徴とします。これらの症状は脳の大脳基底核や大脳皮質が萎縮してしまうために生じます。
1991年、ハンチントン病におけるCBDの対照臨床試験が報告されました。
【引用文献:Controlled clinical trial of cannabidiol in Huntington's disease Author links open overlay panel. Pharmacology Biochemistry and Behavior 1991, 40, 701.】
有望な予備調査結果に基づいて、ハンチントン病(HD)の患者15人の症状に対するCBDの有効性と安全性について評価されました。6週間の期間で経口CBD(10 mg / kg /日:1日平均用量が約700 mg)とプラセボ(ごま油)の効果が、ランダム化二重盲検クロスオーバー設計で確認されました。しかし、舞踏運動の重症度とその他の治療結果、臨床検査テスト、安全性結果などに対するCBDとプラセボの効果に有意な違いは示されませんでした。
◆CBDと皮膚や筋肉の炎症
日本でも様々な種類のCBD製品が見られようになりました。例えば、オイルやvape以外にもCBDロールオンやクリーム、バームなどの肌・皮膚に塗るタイプのものなどです。軟膏やバームなどの経皮薬物製剤は、口に入れる経口剤よりも多くの利点があります。経皮投与は初回通過における代謝効果を回避できるため、薬物の生物学的利用能(吸収率、利用率)が改善します。さらに、経皮投与では、高い薬物血中濃度で起こる悪影響を最小限に抑えながら、適用部位で長期間にわたって薬物を一定に放出できるため、患者の薬物療法の有効性と安全性を向上させることができます。したがって、医薬品の局所塗布は、炎症や筋肉痛などへの適用に最適です。
大麻成分のカンナビノイドの経皮吸収は痛みや炎症症状の軽減に有効であることが報告されています。さらに、カンナビノイドの中でも、比較的に水となじみやすい(極性の高い)化学構造を持つCBDは、皮膚吸収の改善に有利であるはずです。実際にCBD経皮吸収は、ヒトにおけるTHCの経皮投与よりも10倍高いと報告されています。また、THCの安全な代替薬としてCBDは期待されています。CBDは痛みや炎症を含む多くの病状の治療に影響を与える可能性のある物質であり、炎症誘発性サイトカインの放出を減少させる効果を示すことが前臨床研究により確認されています。
・皮膚炎に対するCBD塗布

皮膚炎に対するCBD塗布に関しては、CBDの有用性は示されていますが、それ単体のみではアトピーなどの皮膚炎を十分に回復させるのは難しい可能性があります。しかし、皮膚炎(ニキビ、肌荒れ)の状況によってはCBDのみで症状が改善した例もあります。
背景
皮膚炎に対する従来のステロイドなどの治療法には、繰り返し刺激される組織への副作用など、いくつかの課題があります。近年、皮膚癌なども含めた皮膚疾患の治療に大麻成分のカンナビノイドが注目されるようになりました。この大麻成分のカンナビノイドが抗炎症効果を示し、癌細胞の急増殖を阻害することが報告されたからです。
ヒトの皮膚にある感覚神経や様々な種類の細胞には、カンナビノイドが作用するカンナビノイド受容体が発現しており、表皮の恒常性維持の調節や痛みの感覚の調節、皮膚の炎症の調節、皮膚付属器の調節に関わるとされています。すなわち、ヒトに備わっているカンナビノイドが関わるシステム(内因性カンナビノイドシステム)は痛みやかゆみ、表皮の恒常性、皮膚炎の促進と抑制に関連する機能があることがわかってきました。皮膚疾患では、皮膚癌、アトピー性皮膚炎、アレルギー性皮膚炎、皮膚が硬くなる強皮症、ニキビなどにおいても研究が進んでいます。これらはカンナビノイドの皮膚への塗布が新しい治療手段になる可能性を示唆しています。
CBDやTHC、CBN、CBGなどのカンナビノイド(大麻の成分)は抗炎症作用があり、皮膚疾患のケアに重要な役割を果たす可能性があると言われています。例えばアトピーでは、表皮にある角化細胞(ケラチノサイト)に過増殖が生じると言われていますが、CBDやCBN、CBGなどは角化細胞の過剰増殖を抑制することが報告されています。なかでもCBDは安全性の高い有益なカンナビノイドの一種として注目されています。CBDはTHCなどと比べると刺激性が低く、皮脂腺の活動を抑え、抗炎症作用や抗菌作用を示すため、ニキビの治療に有望です。また、乾燥や日焼けの予防にも期待されています。CBDは乾燥して痒くなる前の予防や悪化の抑制にも有望かもしれません。しかし、このようにCBDは様々な効能の可能性が指摘されているにもかかわらず、これまで皮膚疾患に対するCBDの効果を経過観察したヒト臨床試験はほとんど報告されていませんでした。
2019年に慢性的な皮膚疾患(アトピー、乾癬、ニキビなど)に対するCBDゲル(軟膏)の効果を調査した非対照臨床試験が報告されていました。
【引用文献:A therapeutic effect of cbd-enriched ointment in inflammatory skin diseases and cutaneous scars. Clin. Ter. 2019, 170(2), e93-99.】
この研究では、1日2回、患部にCBD軟膏を局所投与する(局部に塗る)と3ヶ月でどのような変化(効果)が現れるかを調査しました。結果はCBD軟膏の局所治療がアトピー性皮膚炎、乾癬およびそれらの瘢痕(痕跡)、ニキビ、漿液性(=ジクジクした)皮膚の炎症に改善をもたらしました。さらに副作用は報告されず、筆者は安全性の高い手段だと述べています。ただし、この研究の解釈には注意が必要です。まず、使用したCBD軟膏にはCBD以外の有効成分(脂肪酸など)も含まれています。また、他にも注意点があります。それらの点も含めてこれから詳しくみていきましょう。
乾癬とは、皮膚に赤い発疹ができ、次第にその表面にフケのような粉が付着し、ポロポロ剥がれ落ちるような症状を言います。
【概要とサンプル】
この臨床試験の参加者は20人(20〜80歳)で、少なくとも6ヶ月は皮膚疾患に悩んでおり、適切な治療を求めていました。20人のうち5人がアトピー性皮膚炎、5人が乾癬、10人が皮膚炎による染みおよびニキビの慢性患者でした。使用されたCBD軟膏はヘンプタッチ社のCBDが豊富に含まれるオーガニックスキンケア軟膏であり、オーガニック由来の成分を多数含んだものと説明されています。試験中、このCBD軟膏を3ヶ月の期間、朝と夕方に1日2回使用するように指示されました。この期間、他のスキンケア製品の使用を禁じられました。
また、試験は比較になる対照群を置かない非対照試験でした。そのため、どの程度CBDが効果に寄与しているのかは不明であり、解釈にはかなり注意が必要です。とはいえ、ヘンプ、CBDを用いた皮膚炎に対する先駆けたヒト臨床試験として、今後に繋がる研究であることには間違いないでしょう。
評価指標には皮膚水和レベル(Skin hydration level)、経表皮水分蒸散量(TEWL)、皮膚の弾力性、外観およびアンケートが利用されました。これらはいずれも、治療前およびCBDによる治療3ヶ月後について評価され、結果が示されました。皮膚水和レベル、TEWL、皮膚弾力性に関しては額、右頬、左頬、首の右側部、首の左側部の5箇所について測定されました。皮膚水和レベルの測定では皮膚角質層の水分の量(結合能力)が、TEWLの測定では体内から表皮層を通って空気中に蒸散される水分の量がそれぞれ測定されます。
【結果】
試験の結果を示します。皮膚水和レベルは各部位でおよそ5〜7%上昇しました(下図)。

経表皮水分蒸散量(TEWL)は各部位でおよそ17〜28%上昇しました(下図)。
※これに関して、筆者は改善したと主張しています。ところが、TEWLの上昇は皮膚バリアを減少させていると考えられるため、改善なのかは疑問です。

また、皮膚弾力性は各部位でおよそ17〜27%上昇しました(下図)。
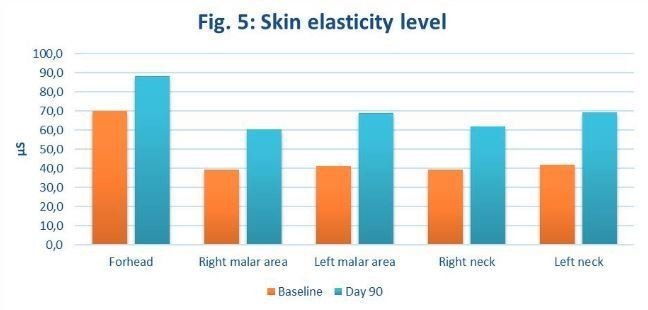
外観変化の評価では3ヶ月の治療前後における無加工の写真で比較されました。以下は3ヶ月のCBD治療で皮膚の染み・痕跡の改善が示された画像です。


また、以下の画像では、嚢胞(液状成分)を皮膚から取り除く外科手術後の傷痕がCBD治療後に改善されたことが示されています。

さらに、CBD軟膏の利用で発疹(丘疹)が20%、吹き出物(膿疱)が31%減少したと報告されました。また、乾癬の深刻度の指標となるPASIスコアにも改善が見られたと報告されました。これらの結果から、筆者らはCBD軟膏が皮膚疾患に苦しむ患者のQOLを有意に改善させたと結論づけています。
【考察】
今回紹介した臨床試験では、比較対象が欠如していました。CBDを排除した軟膏との比較がないということは決定的な欠陥と言わざるを得ません。さらにこの論文には、使用した軟膏におけるCBDの含有量および他の成分の含有比率、患者ごとの詳細なデータ、評価方法の詳細・TEWLの結果への言及などが見つかりませんでした。また、皮膚の水和量や弾力性の改善は、軟膏に含まれたリノール酸やオレイン酸などの脂肪酸によるものである可能性があります。したがって、脂肪酸などの有効成分が合わさることで、CBDの角化細胞の増殖抑制効果が十分に発揮され、乾癬などに治療効果を示した可能性があります。
これらのことから、この改善したという結果の解釈には十分注意しなくてはなりません。ポジティブに捉えるのであれば、CBDの皮膚炎に対する効果の可能性が支持され、今後の臨床試験の土台になりうると考えられます。その際にはプラセボなどとの比較や、より堅牢な臨床試験が求められます。
また、2018年、表皮水疱症による水ぶくれや皮膚・粘膜のただれにCBDオイルが効果を示したと主張する3つの症例が報告されました。
【引用文献:Self-initiated use of topical cannabidiol oil for epidermolysis bullosa. Pediatr. Dermatol. 2018, 35(4), e224–227.】
表皮水疱症は表皮を接着させるタンパク質が遺伝的に欠落することで、表皮が容易に剥がれて、水ぶくれ(水疱)や皮膚・粘膜のただれを生じる疾患です。この疾患はかゆみや痛み、行動制限、再発性の感染症を引き起こすため、管理が難しいと言われています。現在、表皮水疱症の治療法は創傷ケアや鎮痛の管理、栄養サポート、理学療法、社会的サポートなどに限られています。CBDは抗炎症作用と鎮痛作用が認められていることから、表皮水疱症に対するCBD局所投与の効果は注目されます。研究で報告された3つのいずれの症例でもCBDの利用により、創傷治癒が速くなり、水ぶくれが減り、痛みが改善したと報告しました。
【概要と結果】
症例1: 生後6ヶ月の子供
1つ目の症例の患者は、潜性的栄養失調による表皮水疱症と診断された生後6ヶ月の子供でした。初期の創傷ケアにはワセリン軟膏やエミューオイルなどが利用され、感染症治療や除菌のためにムピロシンが断続的に用いられました。また、モルヒネやジフェンヒドラミンを投与されていました。モルヒネによる不十分な鎮痛作用や持続的な水ぶくれを理由に、両親はCBDスプレーの使用を開始しました。1日2、3回患部に噴霧したところ、水ぶくれが大幅に減少し、傷が速く治癒するようになり、モルヒネをやめることができました(下図 A:before, B:after)。

症例2: 3歳の少女
2つ目の症例の患者は、痛みを伴う足裏の角化症により歩行が制限され、表皮水疱症(EB simplex)と診断された3歳の少女です。ケアにはワセリン軟膏とココナッツオイルの混合物、酸化亜鉛とアラントイン6%クリームが使用され、抗菌剤としてバシトラシンが用いられました。その後、母親は水疱にエミューオイルとCBDオイルのブレンドを使用し始め、その結果、水疱が減りました。顔の水ぶくれの治癒時間も大幅に短縮されました。結局、角化症にCBDを適用すると歩行に伴う痛みが軽減され、水ぶくれが減ったことを主張しました(下図A:before, B:after)。

症例3: 10歳の少年
最後の3つ目の症例の患者は、年齢を重ねるにつれて首、腕、足裏に水疱が頻出し、表皮水疱症(EB simplex)と診断された10歳の少年です。痛みを伴う角化症により車椅子の援助が必要であり、創傷ケアには皮膚軟化剤と市販の局所抗生物質が利用されていました。また、ナプロキセンやガバペンチンも処方されました。両親はCBDオイルとクリームを水ぶくれ(水疱)に使用し始めたところ、水疱が大幅に減少しました。これにより、ナプロキセンとガバペンチンを中止することができ、歩行が増えるようになりました。
【考察】
患者は3人とも医師の推奨なしにCBDオイルによる治療を開始しました。2人はCBD局所投与を開始した後、経口鎮痛薬をやめることができました。また、すべての患者で水疱が減り、活動性水疱の活動時間が短縮されました。有害作用の報告もありませんでした。ただし、表皮水疱症の信頼できるエビデンスを提供するには、今後ランダム化二重盲検比較対照試験が必要です。
実際にこれらの観察研究には当然、固有のバイアスがあります。例えば、改善を示した時の方がそうでない時よりもCBDの使用を明かす可能性が高いため、結果を過大評価してしまうということです。他にも比較対照がないため、どの程度がプラセボ効果・自然治癒なのかわかりません。また、この研究からもわかるように、他のオイルやクリームとブレンドすることで、もしくは他の薬と併用することで改善効果が十分に発揮されている可能性があります。いずれにしても、今後さらに大規模な研究が求められます。
体験談
CBDのみの塗布にも期待が寄せられていますが、やはりカンナビノイドやテルペンなどの大麻成分のアントラージュ効果(相乗効果)が注目されています。つまり、THCとCBDの組み合わせやCBN、CBG、大麻由来のテルペンにおけるそれぞれの効果を見ることで、皮膚癌なども含む各皮膚疾患に対する最も効果的なブレンドを見出すことができるようになるかもしれません。実際に、アトピーなどの皮膚炎にはTHCの存在も重要だという体験談が多く見られます。例えばTHCと組み合わせたCBDには、以下のような体験談がありました。※Twitterより引用
アトピー性皮膚炎にはCBDだけでは効果は感じられませんでした。しかしCBDに対してTHC含有量を徐々に増やした所THC:CBD=3:7位だと症状が快方へ向うと自身の人体実験で感じられました。でもTHC率は検査ができないんで(設備無い/安定供給無い)、ざっくり計算です。また割合は個人によると思います。
さて3週間ほどTHCとCBDのクリームを手のアトピーに塗ったところ、ゆっくりではありますが、着実に治ってきてます。首には効き目が薄いのかそこまで実感はできず。もう20年は戦ってるアトピーは悪化するばかり、今度こそ治る、、、?
前述した臨床研究でも、利用されたのはCBDだけでなく、脂肪酸などの有効成分と組み合わさった軟膏でした。これらのことを考えると、皮膚炎に関してはCBDだけでなく、他の成分との相乗効果も重要である可能性が高いと言えるでしょう。
ただし日本では現在、大麻やTHCは医療機関でも法律上の問題により基本的に利用できません。THCは日本で利用できないことを考えると、ヘンプシードオイルとCBDを組み合わせたような、他の麻由来の成分をブレンドしたクリームやバームを購入する、もしくは作るのが効果的なのかもしれません。
また、CBDの作用する受容体が皮膚にどれくらい豊富にあるかは部位によるので、効果が現れやすい部分とそうでない部分があるといえます。CBDの関わる受容体は、皮膚において、毛の生える部分や皮脂が分泌される部位、汗が分泌される部位に多いと考えられています。いずれにせよ、濃度や希釈剤の種類、組成など、効果に及ぼしうる様々な要因があるため、なかなか試行錯誤なしに判断するのが難しいのが現状です。
・疼痛や筋緊張に対するCBD塗布

腰痛・頭痛・肩凝り・神経痛などに関しては、CBDオイルやクリームの塗布で症状が改善するという証拠が臨床研究でも報告されてきています。
背景
大麻成分のカンナビノイドの経皮吸収は痛みの軽減に有効であるということを前述しました。例えば、ラットに関する調査研究の結果では、カンナビノイド受容体が筋肉痛障害における鎮痛療法の標的になることを示唆していました。さらにCBDの、「塗る」などの局所投与は、脳脊髄炎や多発性硬化症などの慢性疾患のケアに効果的である可能性が示唆されています。しかし、現時点での痛みに対するCBD塗布の効果を調査したヒト臨床研究は限られています。
最近、疼痛患者の痛みの緩和のために、CBD製剤を皮膚に塗布する経皮投与試験が実施されました。対象は慢性的な顎(あご)の痛みやしびれに苦しむ顎関節症と診断された60人の患者でした。
【引用文献:Myorelaxant Effect of Transdermal Cannabidiol Application in Patients with TMD: A Randomized, Double-Blind Trial. J Clin. Med. 2019, 8(11), 1886.】
顎関節症とは顎(あご)の痛みや口が開けづらいなどの症状がある顎の関節と筋肉の病気です。顎関節症の患者60人はランダムにCBD群とプラセボ群に分けられ、2週間、1日2回CBD製剤を痛みのある咀嚼(そしゃく)筋部位の皮膚表面に塗布するように指示されました。咀嚼筋にCBD製剤を適用すると、患者の筋活動(筋肉の緊張)は低下し、その痛みが大幅に軽減され、咀嚼筋の状態が改善されることがわかりました。痛みの尺度において、プラセボ群では10%の改善であったのに対し、CBD群では70%も改善し、明らかに有意なCBDの有効性を示しました。
【研究背景】
持続する筋収縮の増加をもたらす歯ぎしりは、顎関節症(TMD)に繋がる重要な危険因子です。歯ぎしりを誘発する原因として、自律神経系内の交感神経と副交感神経におけるバランスの調節不全が考えられます。歯ぎしりは、歯の摩耗と咀嚼筋の痛みの主要な原因の1つと考えられてます。睡眠時の歯ぎしりは成人の約13%に発生する可能性があり、小児期には頻度が最も高く14〜20%であり、年齢とともに減少し、高齢者では3%程度と報告されています。歯ぎしりによって誘発される咀嚼筋の筋筋膜性疼痛(MFP)は一般的な障害で、筋肉にかかる過度のストレスや疲労などにより痛みやしびれを引き起こす症状を言います。このような筋膜痛(筋筋膜性疼痛:MFP)の症状は筋肉の損傷によるものです。そのため、咀嚼筋の筋緊張を軽減し、筋膜痛を治療する革新的な方法が求められています。そこで、著者らは、CBDの筋弛緩作用が筋膜痛患者の筋緊張を有意に緩和できるか調査するために、CBDクリームの臨床試験を実施することにしました。
【設定】
顎関節症と診断された平均年齢23歳の60人の患者が、ランダムにCBD群30人とプラセボ群30人に分けられました。CBD群で使用されたCBD製剤(軟膏)のCBD含有量はおよそ1.46%でした。患者は、2週間、1日2回CBD製剤を咬筋(咀嚼筋のひとつ)の部位の皮膚表面に塗布するように求められました。
なお、カンナビノイドの塗布による潜在的な欠点は、局所的なアレルギー反応の可能性や、皮膚への浸透性の低さですが、これはコレステロール軟膏を媒体として利用することで、低アレルギー性および皮膚を介して浸透を容易にする特性を持たせることができます。
2週間の治療前後で、咬筋の活動度合をみる表面筋電図(sEMG)およびVAS(ビジュアルアナログスケール)の痛みの強度が測定されました。sEMGの分析では安静時および収縮時の咬筋張力(咀嚼筋の緊張度合)が測定されました。
【結果】
試験の結果、sEMGからわかる咬筋の活動(筋緊張)はCBD群でのみ有意に減少し、プラセボ群と比較してもその減少は有意なものでした(減少の割合:右側の咬筋11%[CBD群] vs 0.23%[プラセボ群]、左側の咬筋12.6%[CBD群] vs 3.3%[プラセボ群])。VASの痛みの強さはCBD群で大幅に低下しました(低下の割合:70.2%[CBD群] vs 9.8%[プラセボ群])。

上図のように、プラセボ群での痛みの強度におけるスケールでは5.1から4.6への低下だったのに対し、CBD群でのスケールは5.6から1.7に低下し、統計的に有意な変化でした。
結論として、咬筋にCBD製剤を適用すると、咬筋のsEMG活動と痛みの強さが減少し、MFP患者の筋肉の状態が改善されることがわかりました。
さらに、神経因性疼痛患者に対するCBDオイルの局所投与(患部への塗布)の有効性を調査するためにランダム化プラセボ比較対照試験が別の研究で実施されていました。
【引用文献:The Effectiveness of Topical Cannabidiol Oil in Symptomatic Relief of Peripheral Neuropathy of the Lower Extremities. Current Pharmaceutical Biotechnology 2020, 21, 390.】
末梢神経障害における疼痛は患者の生活の質に大きな影響を与える可能性があります。カンナビノイドは慢性の非癌性疼痛に対する治療効果が示されてきています。末梢神経障害の患者29人(平均68歳)のうち、15人が0.3% CBDオイルを治療薬に用いるCBD群に、14人の患者がプラセボ群に無作為に割り当てられました。 4週間の試験後、神経障害性疼痛スケール(NPS)におけるベースラインからの平均変化を評価したところ、プラセボ群と比較しCBD群で、激しい痛み、鋭い痛み、寒さ、かゆみの感覚が統計的に有意に減少しました。忍容性は良好でした。結論として筆者らは、CBDオイルを塗布すると、末梢神経障害患者の痛みやその他の不安感を大幅に改善でき、従来の治療法と比較して、より効果的な代替手段になる可能性があると報告しました。
体験談
私はアレルギー性皮膚炎やアトピー性皮膚炎、頭痛、腰痛、肩こりなどに悩まされていました。ここではこれらの症状にCBDオイルの塗布がどのような効果をもたらすかを検証してみた結果を報告します。もちろん、効果や体感には個人差があるのでご了承ください。ただし、リアルな体験として参考になるかと思います。※実践する際は全て自己責任の上で行いましょう。

普段、私は6.6%濃度のCBDオイルを舌下投与で利用していました。舌下投与でCBDオイルを利用していたのは、不安やうつ、睡眠障害にも悩まされていたからです。1日当たり3~7mgのCBDの舌下投与を1ヶ月半継続しても皮膚炎や痒みの改善はありませんでした。また、肩こりなどに関しても改善しているのか、因果関係があるのか、不明でした。これはあまり効いていないか、もしくは異なる用量などで継続が必要だったのかもしれません。一方で、そもそも塗る方が効果を実感できるのではないかとも思っていました。そこで、まずは直にCBDオイルを塗る方法に注目しました。なお、今回直塗りに利用したオイルも6.6%濃度のCBDオイルです。さらに、CBDバームとの比較もしました。
【結果】
CBDオイルを直接、患部に塗ってみて得られた効果について結論から言うと、頭痛や腰痛・肩こり・筋肉痛には効果てきめんでした。これはかなりの驚きでした。なぜなら、期待を大きく裏切るレベルで効いたからです。オイルを塗った瞬間にすぐ効果を感じました。一方で、皮膚炎やかゆみに対しての効果は微妙でした。※おそらく個人差あり。
では、具体的な効果と私が実践したオイルの塗り方について説明します。
後頭部が重い頭痛の時では、首の後ろから後頭部の間あたりにオイルを1〜2滴ほど塗りました。指にオイルを1滴のせて、患部でのばして塗りました。案外1滴でも延ばせば広い範囲に塗ることができます。これで頭が軽くなり、痛みも明らかに緩和しました。鬱や過眠で起こる頭痛にも効果があり、鬱症状も緩和されたように感じました。なお、濃度が濃いと刺激が強い可能性があるので、最初は薄めてからの使用か薄いオイルの使用がよいかもしれません。腰痛・肩凝り・筋の痛みでCBDを塗る際の塗り方も同様です。いずれにもよく効き、整体でほぐしてもらったかのように軽くなりました。ただし、アレルギー反応も他の物質と同様に起こりうるので、デリケート部分に関しては、薄めたオイルやCBDバーム・クリームなどから始める方がよいでしょう。また、紹介した論文にもあったように、コレステロール軟膏を媒体として利用したCBDバームを用いるなどの工夫で劇的に良くなる可能性もあります。
結局、CBDオイルの患部への直塗りが良いか否かは、CBDオイル濃度とその用途、あなたの体質や状態によります。ただ、肩こりなど筋肉の緊張をほぐす効果は非常に有益に感じたので、特に急性の筋の痛みや腰痛、頭痛には直塗りもありかと思いました。ただし、基本的には低い濃度から少しずつ濃度を上げていく方法が推奨されていますので、留意してください。
【考察】
一方で自作の1%CBDバームでも頭痛や腰痛・肩凝り・筋肉痛に対して明らかに有益な効果がありました。オイルの直塗りと比較して、ニオイやオイルのベタベタが気にならないことが大きな利点です。さらに、刺激も弱いためアレルギー反応も起こりにくいと推測できます。しかも、オイルよりも手軽で使い勝手が良いです。激しいスポーツをしている時にも有効性を感じており、今では運動をする時にはバームを持ち歩いてます。CBDバームはCBDオイルがあれば自分で作れるので試してみてください。濃度も自由に決められてオススメです。つまり、CBDオイルを買っておけば経口摂取も経皮投与も試すことができます。とはいえ、まずは市販のバームやクリームから試すのが最も無難かもしれません。
比較した結論としては、デリケートな部分においてはCBDオイルの直塗りから試すよりも、CBDバームから試していく方が無難かもしれません。ですが、腰痛や頭痛が辛いという場合は、オイルを軽く塗ってみて、まず効能の感覚を知るのは良いかもしれません。
◆免疫暴走による炎症 (拒絶反応)
CBDは移植後の免疫暴走・拒絶反応や痛みの抑制に効果を示しており、白血病の治療にも効果が期待されています。

背景
一般的に大麻は強力な抗炎症作用と免疫抑制作用を幅広く備えています。このような幅広い作用の延長上で、大麻は成人の慢性疼痛(慢性的な痛み)の治療に使用できる可能性が示されています。医療用大麻の有効性と安全性に関して米国神経学会が実施した系統的レビューでは、著者らは大麻成分のカンナビノイドが多発性硬化症の患者の痙縮と痛みを伴うけいれんを軽減するのに効果的であると述べています。また、カンナビノイドは12〜15週間から最長1年間の治療で痛みを軽減するのに効果的だと報告しています。
実際に治療目的で使用されるカンナビノイドベースの薬物はすでに世界中にいくつかあります。ナビロン(別名:セサメット、成分:合成THC)は、化学療法による重度の吐き気と嘔吐の治療のためにカナダ保健省によって承認された経口薬です。ドロナビノール(別名:マリノール、成分:THC)も経口剤で、重度の化学療法による吐き気や嘔吐、後天性免疫不全症候群に伴う体重減少の治療にも承認されています。サティベックス(別名:ナビキシモルス、成分:THC:CBD = 1:1)は、多発性硬化症と難治性のがん性疼痛を有する成人患者のけいれんまたは神経因性疼痛の補助治療薬であり、口腔粘膜投与剤として用いられます。ところが、THCの精神作用は、臨床での使用を制限します。CBDはTHCとは異なり、「ハイ」になるような精神活性作用はありませんが、抗炎症や筋弛緩作用が示されてきているため、関連した研究がいくつか行われてきています。
2018年には腎臓移植患者の慢性疼痛(持続的な痛み)に対するCBDの改善効果の可能性が報告されました。
【引用文献:Chronic Pain Treatment With Cannabidiol in Kidney Transplant Patients in Uruguay. Transplantation Proceedings 2018, 50, 461.】
臓器の移植後に問題となるのは、外部から取り込んだ臓器に対する過剰な免疫反応(拒絶反応)です。この研究は、腎臓移植患者の慢性疼痛や免疫暴走に対するCBDの効果を評価することを目的としています。腎臓移植患者における慢性疼痛は、非ステロイド性抗炎症薬に関連する腎毒性のため、主要な治療上の問題となっています。58〜75歳(平均64.5歳)の7人の腎臓移植患者に対して50~300mg/日のCBDを3週間の期間で投与したところ、2人の患者は完全な痛みの改善があり、4人は最初の15日間に部分的な反応があり、1人には変化がありませんでした。この追跡調査中、CBDの忍容性は良好で、重篤な副作用はありませんでした。
【研究背景】
臓器移植後の拒絶反応・免疫暴走に対する治療法は1980年代以降から大きな進歩はありません。移植後に対応が必要とされる免疫抑制のための薬物投与によって、感染症と癌の発生率が高くなることがあります。また、慢性疼痛は、もう1つの課題であり、基礎疾患または他の併発疾患に関連しています。腎臓移植患者は、腎毒性のために非ステロイド性抗炎症薬の使用を制限する必要があります。そのようななか、最近では、慢性疼痛治療における内因性カンナビノイドシステムの調節が注目されています。しかし、カンナビノイドと免疫抑制剤との潜在的な薬物間相互作用には十分注意しなくてはなりません。
【設定】
この研究で使用された試験薬は1mlあたり50mgのCBDを含むCBD:THCが30:1のCBDオイルです。
具体的には以下のことを評価することがこの研究の主な目的となります。
・CBDと免疫抑制剤(タクロリムスやシクロスポリン等)との薬物間相互作用
・腎臓移植患者におけるCBD安全性プロファイル
・疼痛管理におけるCBDの効果
・腎臓移植患者におけるCBD忍容性
腎臓移植を受け、慢性的な痛みの治療を求めていた58~75歳の7人の患者を評価しました。CBDの初期用量は100 mg / 日で、300 mg /日まで段階的に増加しました。
【結果と考察】
治療を受けた7人の患者を患者1~7とします。吐き気が持続したため、患者1は4日目にCBDの用量を50mg /日に減らしました。ただし、この患者は以前から他のいくつかの薬物に対して同様に消化不良・吐き気がありました。
免疫抑制剤であるタクロリムスやシクロスポリンとCBDとの相互作用についても調査されました。3週間の治療を受けて、タクロリムスの血中濃度は患者2で低下しましたが、患者3や患者5で濃度が増加したため、タクロリムスの投与量を減らしました。シクロスポリン療法の患者6と患者7は、安定したシクロスポリン濃度を示しました。
CBDによる疼痛管理の結果は2人の患者で最適であり、4人は最初の15日間で部分的な応答があり、1人では変化がありませんでした(表1+2:痛みの指標スコア)。
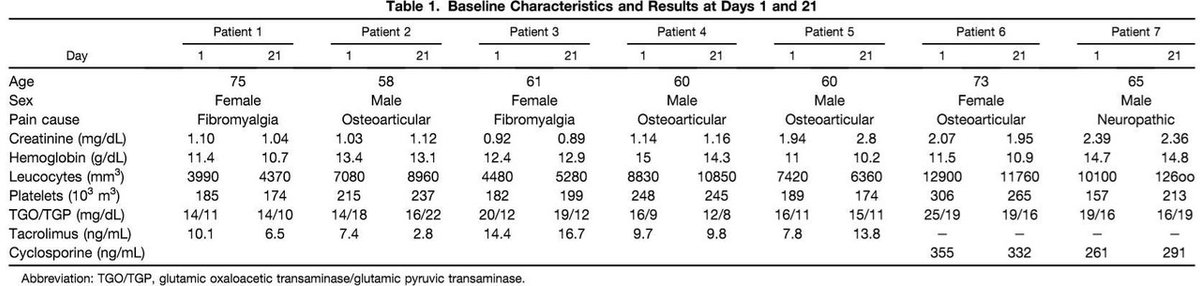

患者6と7には最適な疼痛制御反応があり、1人は骨関節痛ともう1人は神経障害性疼痛でした。両方の患者は、免疫抑制療法においてシクロスポリンで治療されていました。患者1、3、4、および5は、痛みが部分的に改善しました。患者5は、より低いCBD用量で最も良い結果を示しましたが、CBD用量を増加すると痛みが増加しました。この結果はCBDには顕著な適量範囲が存在することを裏付けています。
CBDは忍容性が良好で、報告された副作用は軽度であり、それらのすべてが神経系または消化器系に関連していました。ほとんどの有害事象はCBD投与量を増やした直後に発生しており、免疫抑制剤との併用による薬物間相互作用が副作用の原因として考えられます。ただし、CBDと免疫抑制剤の間の臨床的に関連する薬物動態学的相互作用について結論を出すには、より多くの患者でのより長いフォローアップが必要です。また、この研究の結果からも、併存疾患があり他の治療薬を服用しているような患者には特に血中濃度のモニタリングと最適な用量の調整を必要とすることが分かりました。
腎臓移植のように、外部から移植された臓器が自己の免疫反応により攻撃される反応を拒絶反応といいますが、リンパ球などの免疫を担う細胞が移植された場合、逆に移植された免疫細胞が正常な自己の臓器を異物と認識して攻撃してしまいます。これによる疾患が移植片対宿主病(GVHD)です。
急性GVHDの予防および症状緩和にCBDの抗炎症・免疫抑制効果が有効かどうか評価するための試験が実施され、2015年に報告がありました。なお、移植から発症するまでの時期が100日以内の場合を急性GVHDと呼びます。
【引用文献:Cannabidiol for the Prevention of Graft-versus-Host-Disease after Allogeneic Hematopoietic Cell Transplantation: Results of a Phase II Study. Biology of Blood and Marrow Transplantation 2015, 21, 1770.】
患者には同種造血細胞の移植を受けている48人の成人が登録されました。これらGVHDが懸念される患者にCBD 300 mg /日を、移植の7日前から治療30日目まで経口投与したところ、過去に標準治療のみを受けた対照群と比較して中等度~重度の急性GVHDを発症するリスクが約70%低下 [ハザード比0.3(p = 0.0002)]しました。CBDと標準的なGVHD予防の組み合わせは、急性GVHDの発生率を減らすための安全で有望な治療法であると結論付けられました。
【研究背景】
実験的なマウスモデルでは、マリファナの主な精神活性成分であるTHCがGVHDの予防と治療の両方に効果的であることが示されました。にもかかわらず、THCの望ましくない「ハイ」になる精神活性効果は、GVHD予防のための利用の検討をためらう原因になっています。対照的に、CBDはTHCのような精神活性効果をもたらさず、長期間にわたって摂取された場合でも人間によって十分に許容されるため、臨床研究と治療的利用の両方の可能性があります。
【設定】
CBDは標準治療に追加の薬物療法として、移植の7日前から治療30日目まで1日2回150 mgの固定用量で経口投与されました(300 mg /日)。治験薬のCBDは、2.5%の濃度でオリーブオイルに溶解されていました。
参加者である48人の患者は従来通りのGVHDの予防に、抗炎症・免疫抑制のための薬物であるシクロスポリンとメトトレキサートが利用されました。
※なお、CBD治療を受けた48人の患者のうち38人(79%)は急性白血病または骨髄異形成症候群であり、35人の患者(73%)は骨髄破壊的前処置がされました。ドナーは28人が同種の血縁のものでした。血縁関係のないドナーから移植された患者には、低用量の抗T細胞グロブリンが投与されました。また、支持療法として、すべての患者は感染予防および肝臓における血管の病気の予防のために、それぞれフィルグラスチムおよびウルソデオキシコール酸の投与による薬物療法が実施されました。
【結果と考察】
急性GVHDにおける症状の重症度を示す指標として、グレードI〜IVの段階があり、数字が大きいほど重症度が高くなります。この研究の主要な評価項目は、100日目までのグレードII〜IVおよびグレードIII〜IVの急性GVHDの累積発生率でした。他の評価項目には急性および慢性GVHDの累積発生率、非再発死亡率、再発率、および生存率がありました。
CBDを摂取している間(すなわち、治療30日目まで)に急性GVHDを発症した患者はいませんでした。CBD中止後には、 1人がグレードIの急性GVHDを発症し、7人がグレードII~IVの急性GVHDを発症しました。また、4人の患者がグレードIII〜IVの急性GVHDを発症しました。
100日目までのグレードII~IVおよびグレードIII~IVの急性GVHDの累積発生率は、それぞれ12%と5%でした(下図)。一方で、101人の過去の対照患者の100日目までのグレードII~IVおよびグレードIII~IVの急性GVHDの累積発生率は、それぞれ46%と10%でした。

グレードII〜IVの急性GVHDの発症までの期間の中央値は60日でした(範囲、41〜150)。対照群で急性GVHDを発症までの期間の中央値は20日(範囲、9〜137)で、CBDグループと比較して有意に短かったです(20対60日、P = .001)。
急性GVHDによって炎症の症状が出た箇所に関して、CBDで治療された患者は対照群と比較して、皮膚、上部消化管、および下部消化管での発症頻度が低くなりました。なお、消化管は口から肛門までの食物が通る管で、食道、胃、小腸、大腸などを指します。
移植後100日での非再発死亡率は8.6%でした。ただし、急性GVHDの発生率に対照群と差があるにもかかわらず、移植後1年での非再発死亡率に有意な差はありませんでした(CBD治療グループ13.4%vs対照グループ20%、P = 0.95)。
今回の患者(中央値56歳)、ドナー(同種の血縁の割合)、および移植特性(骨髄破壊的条件付け、73%)を考慮すると、これら急性GVHDの発生率や 非再発死亡率は非常に低い値で抑えられたと言えます。
移植後100日以上生存した患者(n = 41)の間で、慢性GVHDが15人の患者で発生し、8人の患者で中等度~重度の慢性GVHDに分類されました。1年後の中等度~重度の慢性GVHDの累積発生率は20%で、18か月時点の中等度~重度の慢性GVHDの累積発生率は33%でした(下図)。

慢性GVHDには好ましい移植片対腫瘍効果が関連しており、この発生率の低下が非再発死亡率の増加に関与することが示されています。したがって、将来の取り組みは移植片対腫瘍効果を軽減することなく、臨床的に有害なタイプの慢性GVHD(すなわち、中等度および重度のグレード)の、より効果的な予防に向けられるべきです。なお、患者の30%で粘膜炎や吐き気の副作用によりCBDを平均して86%の用量に減らしましたが、大きな問題は見られなかったようです。
この研究でCBD治療を受けた患者で見られた急性GVHDと中等度から重度の慢性GVHDの低い発生率は、マラビロックやボルテゾミブ、ボリオノスタットのような新規の薬剤で治療された患者の比較的に最近の第I / II相試験で明らかになったGVHDの発生率と同程度の大きさでした。
CBDは安全で忍容性が高く、現在の試験の有望な結果に照らして、CBDへの長時間の曝露が遅発性のGVHDをさらに低減できるかを調査すべきでしょう。さらに、CBDは前臨床試験などで骨髄性およびリンパ性白血病細胞のアポトーシス(細胞死)を誘発することが示されています。また、CBDへの長時間の曝露は、好ましい抗白血病効果を明らかにする可能性があります。
結論として、この研究はGVHDの予防におけるCBDの潜在的に有望な役割を初めて示しました。これらの有望な結果はランダム化二重盲検プラセボ比較対照試験で検証されるべきです。
◆炎症性腸疾患
CBDは炎症性腸疾患の発病や病態の進行を抑制する可能性が指摘されていますが、現時点では効果を示した決定的なヒト臨床試験は報告されていません。

炎症性腸疾患は腸に炎症が起こる病気ですが、発病の原因の特定が困難なものには、主に潰瘍性大腸炎とクローン病の2種類に分類されることが多いです。潰瘍性大腸炎は大腸の粘膜にびらんや潰瘍がみられ、炎症の部位が大腸に限局しています。一方でクローン病は腸だけでなく、それ以外の消化管でも炎症が起こり、潰瘍が飛び飛びにできます。いずれの疾患も下痢や血便、腹痛などが症状として現れます。
背景
大麻成分のカンナビノイドの投与は炎症および腸運動の減少を含む腸に対する有益な効果と関連しています。実際に、大麻は炎症性腸疾患の症状を改善するということが報告されています。あるプラセボ対照試験では、大麻喫煙が難治性クローン病患者に有意な臨床反応を引き起こした例もあります。一方で、主要なカンナビノイドのひとつである、乱用の危険性が無いCBD(カンナビジオール) は、抗炎症作用および免疫調節作用を有することが示されてきています。
最近、CBDが炎症性腸疾患の発症や進行を抑制する可能性を示す試験の結果が報告されました。
【引用文献:Palmitoylethanolamide and Cannabidiol Prevent Inflammation-induced Hyperpermeability of the Human Gut In Vitro and In Vivo—A Randomized, Placebo-controlled, Double-blind Controlled Trial. Inflammatory Bowel Diseases 2019, 25, 1006.】
この研究でCBDはヒトの腸管の透過性を低下させることが分かりました。腸の透過性の亢進は炎症性腸疾患の発症および病態の進展に関与していると考えられています。なぜなら、種々の炎症誘発物質は腸内の上皮層を透過すると、粘膜内にある炎症担当細胞を慢性的に刺激するからです。この研究で示されたCBDによる腸管の透過性の低下は、実際に腸から採取したヒトの結腸粘膜を用いた実験やヒト臨床試験(ランダム化二重盲検比較対照試験)などで確認されました。なお、ヒト臨床試験では600 mgのアスピリンを服用したヒトのラクツロースとマンニトールの吸収に対するCBDの効果を評価しました。体内で、アスピリンはラクツロースとマンニトールの吸収の増加を引き起こしましたが、CBDによって吸収が減少しました。

潰瘍性大腸炎(UC)患者に対する、CBDが豊富な大麻抽出物の有効性、安全性、忍容性が評価され、2018年に結果が報告されました。
【引用文献 A Randomized, Double-blind, Placebo-controlled, Parallel-group, Pilot Study of Cannabidiol-rich Botanical Extract in the Symptomatic Treatment of Ulcerative Colitis. Inflammatory Bowel Diseases 2018, 24, 714.】
左側または広範囲の潰瘍性大腸炎(UC)をもつ18歳以上の患者がCBD投与群とプラセボ群にランダムで割り振られ、10週間治療されました。結果は、治療終了後の寛解率が、CBD群(28%)とプラセボ群(26%)で有意な差はありませんでした。しかし、興味深いことに他の評価スコアではCBD群で有意に改善され、生活の質が向上しました。ただし、使用されたCBDが豊富な大麻抽出物にはTHCが含まれていたため、副作用による離脱が増えてしまい、結果に悪影響を与えた可能性があります。また、患者らは潰瘍性大腸炎(UC)の標準治療薬である5-アミノサリチル酸が安定投与され、その追加でCBDもしくはプラセボが投与されました。この場合はすでに標準的な薬物療法が施されているため、試験薬に対する反応も小さくなることが多く、効果を見るときに不利になります。また、薬物間相互作用も関与してくる可能性があります。薬物間相互作用で効果や副作用が増幅する可能性も考慮しなくてはなりません。これは、統合失調症やてんかんなどにおける臨床試験も同様です。
【研究背景】
潰瘍性大腸炎(UC)は慢性の再発性炎症性腸疾患(IBD)です。このような活動性腸疾患は通常、直腸出血と下痢を引き起こし、多くの場合、痛み、疲労、体重減少も引き起こします。慢性腸炎になると腸がんを発症するリスクも高くなります。軽度から中程度のUCの第一選択療法は5-アミノサリチル酸(5-ASA)であり、最近ではさらにいくつかの薬物療法が確立されてきています。軽度から中等度のUCにおいて処方される5-アミノサリチル酸は、患者の約50%の寛解を誘発および維持するのに効果的であるとされています。ただし、一部の患者は現在の標準的な治療法に耐性があり、代替治療を必要とする軽度から中程度のUCを持っています。
前臨床研究では、CBDが潰瘍性大腸炎(UC)の治療に有効である可能性が示唆されています。具体的には腸の炎症の減少や炎症性運動亢進の抑制など、炎症を起こした腸で有益な効果を発揮することが示され、マウスの実験でも大腸炎を予防することが示されています。また、CBDとTHCの組み合わせが炎症性腸疾患の改善に相乗効果をもたらす可能性があるという証拠があります。ラットでの研究で、最適用量におけるTHCとCBDの組み合わせは、炎症を軽減するだけでなく、機能障害の発生も低下させました。したがって、5-ASA(5-アミノサリチル酸)療法に難治性であることが証明された軽度から中程度の潰瘍性大腸炎(UC)の患者において、CBDが豊富な大麻抽出物の有効性と安全性が調査されました。
【設定】
このランダム化二重盲検プラセボ比較対照試験は、5-ASAに難治性であることが証明された軽度から中程度のUCの患者に対して、CBDが豊富な大麻抽出物の有効性と安全性を評価しました。60人の患者はランダムにCBD群29名とプラセボ群31名に割り当てられ、50mgのCBDが豊富な抽出物を含むカプセル、または賦形剤のみを含むプラセボカプセルが投与されました。これらは、朝と夕食の30分前に、1日2回経口摂取されました。最初の2週間は用量漸増期間であり、その間に1日2回、最大許容用量である250 mg(500mg/日)まで増量し、残りの8週間、この用量を維持するように患者らは指示されました。
【結果と考察】
投与は両グループで同様に開始されましたが、用量漸増期間中に分岐し、CBD群の患者は平均してプラセボ群よりも3分の2の数のカプセルしか服用しませんでした(下図)。

結局、1日当たり10カプセル(500mg)まで増量せよとの指示でしたが、CBD群で平均して1日当たり6カプセル(300mg/日)、プラセボ群で9カプセルの服用になりました。39人の患者が最後まで試験を受けました。
中止した患者は合計21人で、CBD群では13人が有害事象、プラセボ群では7人が有害事象、1人が他の理由により離脱しました。これにより、CBD群で、患者のCBDへの曝露の平均日数(48日)がプラセボ群の平均日数(61日)と比較して短くなりました。なお、本来の暴露日数は10週間なので70日です。ここでの有害事象はCBD治験薬に少量のTHCが含まれていることが影響している可能性が高いです。
この探索的研究では、患者の41%が治験薬CBDへの曝露が不十分でした。そのため、指示を順守した患者に見られる可能性のある正確な治療効果を見逃さないようにするために、追加の分析を行い、その結果が評価に盛り込まれました。
主要評価項目は、治療終了時の寛解期の患者の割合であり、10週間の治療後のMayoスコア(Mayo score)が2以下であれば寛解とされました。なお、Mayo Score(メイヨースコア)とは、排便回数が寛解期に比べてどの程度増えているか、直腸からの出血はあるか(血便スコア)、内視鏡による大腸の所見(内視鏡スコア)、そして、医師による全般評価(PGAS)という4項目で構成されたもので、それぞれに4段階(0~3点)でスコアを付け、その合計(0~12点)で評価します。点数が低いほど軽症です。
結果は治療終了時に両方のグループでほぼ等しいレベルでの寛解が見られ、統計的には有意な差はありませんでした。ただし、平均Mayo合計スコアはプラセボ群と比較してCBD群でより低下の傾向がありました。内視鏡スコアはCBD群で21人中14人(66.7%)の患者が改善を示し、プラセボ群での26人中10人(38.5%)の患者の改善と比較して、高い割合となりました(P = 0.054)。医師による全般評価の重症度スコア(PGAS)について、治療前では約75%が「中程度」または「重度」の重症度と評価され、2つの治療グループ間でほとんど差がありませんでした。治療の終わりまでにCBD群で改善が観察され、その時点でおよそ80%が疾患の重症度を「正常」または「軽度」と評価されましたが、プラセボグループではおよそ50%でした。
他の評価項目は、炎症性腸疾患の生活の質をはかる指標となるアンケート(IBDQ)スコア(これはスコアが高いほど健康)です。このIBDQを使用して評価された、患者が報告した生活の質は、医師の見解と一致していました。 IBDQ(腸症状、全身症状、感情状態、および社会的機能の4つで構成されるアンケート)の結果は、両方の治療グループでスコアが改善(増加)しました(下図)が、プラセボ群と比較してCBD群で強い改善の傾向がありました。

今回の結果から、CBDが消化管運動における疾患活動性スコアの改善をもたらす可能性が示唆されます。内視鏡スコアなどで見られるCBD群でのより大きな改善は、真の抗炎症効果のマーカーとして機能しうるため、有望です。
なお、少なくとも一つ以上の有害事象(副作用)が見られた患者の割合はプラセボ群で48%、CBD群で90%でした(下表)。特に、吐き気、めまい、傾眠、精神障害がCBD群で、より高い発生率で発生しました。一方で大腸炎、腹痛などの疾患の進行に関連しうる有害事象は、CBD群(10%)よりもプラセボ群(42%)でより多く見られました。有害事象の大部分は重症度が軽度または中程度でした。
報告された深刻な有害事象について、 CBD群の3人(10%)が重度の神経系における副作用を発症し(1人が注意力障害、1人がめまい、1人がめまい、関節の腫れ、筋肉のけいれん)、プラセボ群の1人(3%)が重度の消化管における有害事象を発症(出血性下痢)しました。
ところが、重篤な有害事象が3つ、すべてプラセボ群で報告されました。2つは潰瘍性大腸炎、1つは胸痛でした。これはプラセボ群内での腸疾患の悪化を示唆しています。
プラセボ群と比較してCBD群で約2倍の患者が有害事象のために治験薬を中止しました(CBD群13 [45%]患者およびプラセボ群7 [23%]患者)。CBD群で治療中止の原因となった有害事象は主に目まいなどの神経系関連のものでしたが、ほとんどの患者でその後、解消されました。一方、プラセボ群で治療中止を引き起こした原因となる有害事象は胃腸障害であり、特に大腸炎/ 潰瘍性大腸炎でした。
この試験で使用された、CBDが豊富な大麻抽出物カプセルは高度に精製されておらず、CBDに加えて他の多くの化合物(特にTHC は4.7%まで)を含んでいました。したがって、たとえば200 mgのCBDを服用している患者は9 mg以上のTHCを服用しています。CBD群で報告されたかなりの数の副作用が、このTHC含有量に起因している可能性があります。めまい、吐き気、注意力の乱れなどのこれらの影響は、治療コンプライアンスの低下と治療グループの離脱率の上昇に貢献した可能性が高いです。今後は精製されたCBDの使用がこの試験中に指摘された有害事象をどのように変化させるかを見るべきでしょう。
さらに有害事象で興味深いことは、プラセボ群では、大腸炎(重度の出血性下痢、大腸炎、または潰瘍性大腸炎)の悪化を示唆する患者が9人いたのに対し、CBD群ではそのような患者は2人だけでした。これは、潰瘍性大腸炎の症状に対するCBDの治療効果を示唆する可能性があります。
この研究は、潰瘍性大腸炎におけるCBDが豊富な大麻抽出物の効果を評価する最初のランダム化二重盲検プラセボ比較対照試験です。おそらくTHCの含有により忍容性が低くなりましたが、CBDが豊富な大麻抽出物が忍容性のある患者に治療効果をもたらした可能性があることを示唆しました。これらの調査結果は注意して解釈する必要がありますが、将来の研究で処方、滴定、忍容性の改善を目的としたCBD臨床試験を検討することを奨励しています。
さらに、ランダム化プラセボ比較対照試験で、クローン病に対するCBDの効果を評価した研究が2017年に報告されました。
【引用文献:Low-Dose Cannabidiol Is Safe but Not Effective in the Treatment for Crohn’s Disease, a Randomized Controlled Trial. Digestive Diseases and Sciences 2017, 62, 1615.】
18〜75歳の中等度のクローン病患者20人がランダムにCBD群とプラセボ群に割り振られ、10mgの経口CBDまたはプラセボを1日2回投与されました。8週間の治療後、プラセボと比較してCBDでの有意な症状の改善はありませんでした。これは、クローン病に対するCBDの効果の欠如が原因である可能性もありますが、設定されたCBDの用量が明らかに低すぎること、または他のカンナビノイドとの必要な相乗作用が欠如していることが効果を観察できなかった原因である可能性もあります。したがって、この試験のみでは結果を結論づけることはできないと言えます。
【結果と考察】
募集した20人の患者のうち19人が研究を完了しました。平均年齢は39±15歳でした。評価はクローン病活動指数(CDAI)を用いて行われました。この指数は低いほど症状が軽度であることを示し、150以下で寛解とみなされます。CBD摂取前の平均のクローン病活動指数(CDAI)は、CBDおよびプラセボ群でそれぞれ337±108および308±96でした。 8週間の治療後、CBD群とプラセボ群のCDAIはそれぞれ220±122と216±121になり、CBD群で117の低下、プラセボ群で92の低下を示しました。低下の変化数ではCBDのほうが大きかったようですが、統計的に有意な差ではなかったようです。しかし、これは、サンプルの規模を大きくし、CBDの用量を増やして臨床試験を行えばポジティブな結果が得られる可能性がまだ十分に考えられるということを示しています。なお、副作用は観察されませんでした。
また、この研究における患者はステロイド(11人の患者)、チオプリン(14人)、またはTNF拮抗薬(11人)による標準的な治療に反応しませんでした。このような治療に抵抗性のある患者であるにもかかわらず、今回のCBD投与量は10mg/回という低用量でした。これは用量が低すぎる印象があります。そのため、さらなる臨床研究が必要です。
◆その他の疾患 (糖尿病、高血圧、癌など)

糖尿病・肥満
2型糖尿病は最も一般的な糖尿病であり、すい臓でつくりだされるインスリンがうまく働かなくなることで血糖値が上がる病気です。2型糖尿病では、インスリンの量が十分ではない(インスリン分泌不全)か、作られたインスリンが十分作用しません(インスリン抵抗性)。原因には加齢や遺伝、肥満体などが挙げられます。糖尿病になると、食物の正常な代謝ができなくなり、疲労感や皮膚の乾燥、感覚麻痺、頻尿、治癒力の低下などの症状が起こります。CBDとTHCVは、動物モデルにおける脂質や糖代謝に影響を与える、向精神作用(陶酔作用)を持たないカンナビノイドとして注目されています。
2型糖尿病の62人の患者に対してCBDおよびTHCVの有効性を調査したランダム化二重盲検プラセボ比較対照試験の結果が2016年に報告されました。
【引用文献:Efficacy and Safety of Cannabidiol and Tetrahydrocannabivarin on Glycemic and Lipid Parameters in Patients With Type 2 Diabetes: A Randomized, Double-Blind, Placebo-Controlled, Parallel Group Pilot Study. Diabetes Care 2016, 39(10), 1777-1786.】
この研究では、インスリン非治療の2型糖尿病患者62人が、以下の試験薬が使用される5つの治療群に無作為に分けられました:CBD(100 mg 1日2回)、THCV(5 mg 1日2回)、 比率1:1のCBDとTHCV(5 mg / 5 mg、1日2回)、比率20:1のCBDとTHCV(100 mg / 5 mg、1日2回)、プラセボ。各治療群でそれぞれ対応する試験薬が13週間投与されました。主要の評価項目はHDLコレステロール濃度の変化でしたが、治療で血漿中のHDLには影響が見られませんでした。しかし、他の評価項目において、THCVはプラセボと比較して有意な改善効果が得られました。一方で、CBDは有意な影響を与えませんでした。しかし、動物モデルや他の疾患の研究で使用された用量を考慮すると、より高用量のCBDであれば効果を示していた可能性があります。また、CBDは非肥満糖尿病マウスの糖尿病の発生率を下げ、自己免疫性糖尿病の発症を阻止することが報告されています。結論として、THCVは2型糖尿病の血糖コントロールにおける新しい治療薬となる可能性がありますが、CBDの有効性に関しての結論を出すには更なる調査が必要です。
高血圧 (動脈硬化、心筋梗塞、脳梗塞など)
高血圧の初期の症状としては頭痛やめまいなどが挙げられます。しかし、高血圧によって血管に負担がかかり動脈硬化が進行すると、狭心症、心筋梗塞、脳出血、脳梗塞などのリスクが高まります。高血圧を引き起こす要因としてはストレスや過労、肥満、食生活の乱れ、アルコールの過剰摂取、運動不足、睡眠障害、老化などが考えられます。前臨床試験では、カンナビジオール(CBD)が血圧(BP)を急激に低下させることが示されているため、CBDの高血圧に対する効果は注目されています。
最近、健康な男性の血行動態(血圧)に対する、7日間のCBD投与の影響を調査したランダム化比較対照試験が報告されました。
【引用文献:The effects of acute and sustained cannabidiol dosing for seven days on the haemodynamics in healthy men: A randomised controlled trial. British Journal of Clinical Pharmacology 2020, 86, 1125.】
この研究ではCBD投与がヒトの血行動態に及ぼす影響が評価されました。ランダム化二重盲検プラセボ比較対照並行試験で、26人の健康な男性がCBD(600 mg)群またはプラセボ群に13人ずつ割り振られ、7日間それぞれ経口投与を受けました。血圧などの心血管パラメーターは、安静時において急性投与後と反復投与後に評価されました。結果、プラセボと比較して、CBDは急性投与後(=単回投与後)で安静時の平均動脈圧(=動脈内の血圧:-2 mmHg)を大幅に低下させましたが、反復投与後では低下させませんでした。ストレスに応じて、CBDを摂取した被験者は、急性および反復投与後における最大血圧(=収縮期血圧:それぞれ、-6 mmHgおよび -5.7 mmHg)が低下しました。また、7日間のCBD摂取により、内頸動脈径が増加(=動脈血管が拡張:+0.55 mm)しました。CBD群での反復投与により、1日目と比較して、7日目までに動脈硬化が減少(=脈波伝播速度が低下:-0.44 m / s)し、血管の内皮機能が改善(=血流依存性血管拡張反応が増加:+ 3.5%)しました。結論として、CBDは、単回投与後に安静時の血圧を低下させますが、7日間の治療後に効果が失われます(=耐性を獲得します)。ただし、ストレス中での血圧低下は持続しました。さらに、CBD反復投与後の動脈硬化の減少と内皮機能の改善は、血管疾患のある集団に対してさらなる調査を促す発見と言えるでしょう。なお、被験者は高血圧で動脈硬化が進行した患者ではないため、そのような患者が対象であれば、より良い結果が出る可能性もあります。

癌(脳腫瘍など)
癌を治すにはCBD単体では難しいような印象があり、THCなどの他のカンナビノイドとの混合物として使用することが重要である可能性があります。しかし、CBDだけでも癌の進行を阻害する働きがあると言われています。動物実験でもCBDと抗がん剤を併用することで、すい臓がんのマウスにおいて寿命が三倍に伸びたという結果が報告されています。実際に、CBDがヒトの癌細胞の増殖を抑制した可能性が示唆されたという症例もあります。ただし、このような効果はエビデンス力としてはまだ低いままです。
悪性脳腫瘍患者9人の、CBDによる併用治療に関する症例集積報告の投稿が2019年にありました。
【引用文献:Concomitant Treatment of Malignant Brain Tumours With CBD - A Case Series and Review of the Literature. Anticancer Res. 2019, 39(10), 5797-5801.】
脳腫瘍についての前臨床研究では、腫瘍抑制剤としての潜在的なCBDの役割が指摘されています。ここでは、合計9人の脳腫瘍患者の症例が報告されており、患者らは切除手術とそれに続く放射線化学療法という標準治療に追加でCBDが1日あたり400 mg投与されました。グレードIVの多形性膠芽腫(=最も多くみられる脳の悪性腫瘍)は致命的な疾患であり、生存期間の中央値は約14〜16か月です。また、切除手術とそれに続く放射線化学療法による治療は数か月ほどしか生存期間を延長しません。ところが、この報告書の提出までに、1人を除く患者8人が、平均生存期間22.3か月(範囲= 7〜47か月)で、予想されるよりも長く生存しています。この結果からCBDが脳腫瘍に対して効果的に働いている可能性があります。
さらに、同じ2019年、肺がん患者がCBDを使用した症例も報告されました。
【引用文献:Striking lung cancer response to self-administration of cannabidiol: A case report and literature review. SAGE Open Medical Case Reports 2019, 7, 1–4.】
81歳の肺がん患者の男性は最初の診断から9か月間で癌が大きくなっていったにもかかわらず、そのさらに4か月後の診断 (最初の診断から13か月後の診断) では明らかに癌が小さくなっていました(下図)。患者は2か月前に2%CBDオイル(最大12 mg/日)を使用し始め、1か月間服用を続けたこと以外は特に何も変えたことはなかったと医師に伝えました。なお、この患者は生活の質に悪影響を与える可能性のある治療を望まないという理由で標準的な治療を断り、検査のみを受けていました。

眼圧症 (緑内障)
緑内障は、目と脳をつなぐ視神経が障害され、徐々に視野が狭まってくる病気です。緑内障の進行を妨げるためには、眼圧を下げることが大切です。眼圧は10~20 mmHgが正常範囲とされていますので、20 mmHgを大きく超えるような眼圧が続くと、視神経が障害される可能性が高くなります。緑内障の原因ははっきりとはわかっておらず、眼圧以外にも「視神経が弱い」、「血流が少ない」などの原因が考えられていますが、確実な証拠は見つかっていません。
CBDおよびTHCの舌下投与が眼圧に及ぼす影響を調査するためにパイロット研究が実施されました。
【引用文献 Effect of Sublingual Application of Cannabinoids on Intraocular Pressure: A Pilot Study. Journal of Glaucoma 2006, 15, 349-353.】
低用量のTHCとCBDの口腔粘膜投与の眼圧(IOP)に対する効果および安全性、忍容性を評価するために、大麻ベースの医薬品抽出物を使用して、ランダム化二重盲検プラセボ比較対照クロスオーバー試験が行われました。高眼圧症または初期の緑内障(開放隅角緑内障)の6人の患者は、5 mgのTHC、20 mgのCBD、40 mgのCBD、またはプラセボの舌下投与を受けました。主要な評価項目はIOPで、そのほかには、視力、バイタルサイン、向精神効果が評価されました。5 mg THC舌下投与の2時間後、プラセボと比較して有意にIOPが低くなりました(23.5 mm Hg対27.3 mm Hg、P = 0.026)。IOPは、4時間後に元のベースラインのレベルに戻りました。一方、CBDではIOPが減少することはありませんでした。さらに、より高用量のCBD(40 mg)では、投与後4時間でIOPが23.2 mm Hgから25.9 mm Hgに一時的に上昇しました(P = 0.028)。バイタルサインと視力で顕著な変化はありませんでした。1人の患者で、THC投与後に軽度のパニック症状を経験しました。結論として、THC 5 mgの単回投与により、IOPが一時的に低下し、ほとんどの患者で忍容性が良好でした。したがって、THCは緑内障の症状の改善に有効だと考えらえれます。一方、20 mgのCBDの舌下投与はIOPを低下させませんでしたが、40 mgのCBDは一時的なIOPの上昇をもたらしました。そのため、CBDは緑内障の症状を悪化させる可能性があるため注意が必要です。
一方で、両目のまぶたが自分の意思とは無関係にこわばってしまい目を開けることができなくなってしまう、メージュ症候群という病気があります。CBDの眼圧を高める効果は、このような症状を改善する可能性があるということを示す症例が報告されています。
【引用文献:Treatment of Meige's syndrome with cannabidiol. Neurology. 1984, 34, 147.】
メージュ症候群の原因は、大脳基底核や脳幹の働きに異常が起こり、まぶたの痙攣やこわばりといったような病状を引き起こすことに起因すると考えられています。したがって神経変性疾患と関係しています。初期の症状では、まばたきが多くなる、目が開けにくくなる、まぶしく感じるなどの症状が表れます。症例報告では、メージュ症候群の患者にCBD (7 mg/kg/日)を投与したところ、けいれんの頻度と重症度が改善されたと報告されています。
その他の疾患

強迫性障害に関してはプラセボと比較した単回投与の対照試験が最近報告されていましたが、プラセボと比較して有意な改善は見られなかったようです。ただし、この試験では大麻使用歴のある者を集めているため、単回投与だけでは反応が弱かった可能性などがあり、結論づけられるほどのものではありませんでした。
【引用文献:Acute effects of cannabinoids on symptoms of obsessive‐compulsive disorder: A human laboratory study. Depress Anxiety 2020 May 7.】
その他の疾患や症状:片頭痛(偏頭痛)、線維筋痛症、リウマチ、過敏性腸症候群、吐き気、認知症(アルツハイマー病)、多発性硬化症、ALS、筋ジストロフィーなどにおける、ヒトに対するCBD単体のランダム化比較対照試験(RCT)のようなエビデンス力の高い試験は私の知る限り報告されておらず、よくわかっていないというのが現状です。このように効果が不明瞭である理由には、前臨床試験の段階で決定的な効果が見られていないためヒトに対する試験に踏み込むことができない、もしくは対象の疾患の被験者を集めにくい、研究の進行が追い付いていない、経済的に厳しいなどのことが考えられます。
ただし、ここで挙げられた疾患に対しては、動物実験などの研究でCBDのポジティブな結果が報告されています。これはエンドカンナビノイドシステムの調節がこれらの疾患に関与しているからです。例えば、慢性的な片頭痛の患者では健康な人と比較してエンドカンナビノイドが不足していたという研究結果が報告されています。したがってCBDは片頭痛の阻害・予防効果などに期待されています。また、これらの疾患の中には、CBDとTHCの組み合わせが最も適切であるものも多いだろうと予想できます。癌や疼痛(痛み)に関してもTHCの存在が重要かもしれないと言われています。したがって、これらに対してはCBD単体よりも大麻での使用が好まれることが多々あるようです。

一方で、明らかにCBDではなくTHCで効果を示している疾患例としては、食欲不振や疲労、緑内障、睡眠時無呼吸症候群などがあります。
なお、ここで挙げられなかった症状:花粉症、鼻炎、生理痛、肺炎、喘息、免疫不調などは「改善したかも」という話は聞いたことがありますが、非常にあいまいなもので、明らかにエビデンス力に欠けています。また、抗炎症作用は免疫抑制作用と同じことなので、例えば肺炎について、高用量のCBDは肺炎患者の炎症を和らげる可能性はありますが、健康な人に投与して肺炎を予防できるかどうかは疑わしく、感染症のリスクを高めるかもしれません。あるいは、適量が重要になってくるのかもしれません。いずれにしても解釈には注意が必要です。
◆CBDの副作用・用量設定・利用目的について
CBDは安全性および忍容性が高いというのは事実です。一方で、気を張るほどの副作用が全くないというのは嘘です。確かに多くの人にとって、CBDで得られる利点が副作用 (有害事象) という欠点を上回っています。しかし、CBDで起こりうるリスクを避けるための正しい知識を身につけることは利用するうえで必須と言えるでしょう。
ではまず、重要な副作用やリスクについて以下に列挙します。
●肝臓障害・薬物間相互作用 →薬の飲み合わせ、用量に注意
●下痢・腹痛などの胃腸障害 →薬で胃腸障害が出たことのある人は注意
●生殖毒性・催奇形性の疑い →妊婦は使用しない
●眼圧の上昇 →緑内障患者には悪化の危険性あり
●血圧の抑制 →低血圧の人は注意
●血液凝固の抑制 →血友病患者は注意
●鎮静・頭痛などの神経障害 →用量に注意
●アレルギー反応 →体質、用量に注意
●感染症の注意 →体質、用量に注意 (抗炎症=免疫抑制)
これらについて文献や研究論文を交えて詳しく解説するのは、また別の機会にするとして、ここでは簡潔に触れるだけにとどめておきます。
まず重要なのは、急性的な副作用はどれも軽度で一時的なものがほとんどであるということです。例えば、肝酵素レベルの上昇、下痢、鎮静、眼圧上昇、血圧低下などは生じても一時的であり、安定用量に達すると問題がなかったという報告がほとんどでした。明らかに高用量すぎる時などは問題が生じる可能性はありますが、自分に適した用量の範囲内で使用していた場合は問題にならないでしょう。実際、忍容性などを考えると他の薬と比べても安全性が高いという事実があります。
ですので、特に注意すべきことに絞って考えていきましょう。特に注意すべきことなのは(1)薬の飲み合わせと(2)用量コントロール、(3)利用者の状態であると言えます。
(1) 薬の飲み合わせについて、他の薬との同時使用を避け、その薬の種類を確認しつつ医師と相談して用量を調整することが必要です。相互作用が不明瞭な場合は血中濃度のモニタリングが必要になってくるでしょう。
(2)用量コントロールに関して、基本的にCBDは少量から始めて様子を見ながら徐々に増量していくということが大切です。なぜなら、CBDが効果的に効くかどうかは、個人差があり、かつその時の状況によっても変わってくるためです。
(3)利用者の状態に関して、妊婦や緑内障患者、低血圧症の人、腹痛・アレルギー反応が出やすい人は使用にはリスクがあることを理解しておかなければなりません。
このようにCBDを使用するうえでのリスクに関してはしっかりと理解して適切に利用することで、安心して健康的な利用ができると言えるのでしょう。
比較的、健康な人がサプリメント・健康補助食品としてCBDを摂取する場合の用量は1日10~20mg程度を使用する人が多いように感じますが、数mg以下でも十分に効果を感じる人もいるため、1~2mgから始めても良いかもしれません。人によって適量に20倍の差があるという報告もあります。なお、繰り返しになりますが、研究論文の臨床試験で使用されるCBDの用量は多めに設定されることが多いということに注意してください。いずれにしても少量から始めて適量を見つけることが大事です。

一般に、どのような症状にCBDがよく利用されているかについては、世論調査により以下のものが多いことが判明しているようです。
・痛み、不快感
・不安、うつ
・睡眠障害
・ストレス、イライラ
実際にこれらが改善されると生活の質(QOL)が向上し、1日の日常生活活動が充実するようになると言えます。こういった効果が多くの人に支持されていることから、CBDを信頼して愛用する人が増えてきているのでしょう。
また、最近ニュージーランドで疼痛患者、精神疾患患者、神経障害患者のいずれかに該当する400人を対象にCBDオイルを処方し、生活の質(QOL)の変化を評価する調査が実施されました。
【引用文献:Cannabidiol prescription in clinical practice: an audit on the first 400 patients in New Zealand. BJGP Open 2020, 4 (1).】
ニュージーランドのカンナビスケアを受診し、CBDの処方箋を求めたすべての患者(n = 400)を対象に、3週間の10%CBDオイル使用による生活の質の変化、患者から報告された満足度、副作用の発生率、用量設定レベルが評価されました。フォローアップは253人の患者(63.3%)で完了し、110人の患者(27.7%)が生活の質をはかるEQ-5D-5Lアンケートに回答しました。EQ-5D-5Lは、EQ-5D-5L記述システムとEQビジュアルアナログスケール(EQ-VAS)で構成される2つの部分からなるツールです。患者は、全体的な健康の質を表すEQ-VASスコアで平均13.6ポイントの改善(P <0.001)を報告しました。アンケートに回答した患者のうちの非がん性疼痛患者と精神疾患患者は、日常活動能力、痛み・不快感、うつ・不安症状が有意に改善しました(P <0.05)。また、睡眠と食欲の改善も報告されています。110人の患者のCBD投与量は40~300 mg/日の範囲でした。大きな悪影響は報告されませんでした。この研究は、処方された一部の患者でのみ自己申告によって評価されているため、バイアスがあることを考慮しなければなりませんが、痛み・不快感、不安・うつ、睡眠などの改善は世論調査で判明したCBDがよく利用される目的とつじつまが合います。
________________________________________
以上になります。いかがだったでしょうか。
CBDの副作用や用量設定、薬物動態などに関する詳細な記事は続編として、また別の機会で取り上げようと思います。
今後も情報発信を続けるために、ロキは皆様の応援や支持をお待ちしております。もしも、記事が気に入ってくださった方は、↓から「サポートをする」、「フォロー」、「拡散」などをよろしくお願いします!
また、Twitter、Facebook をお持ちの方は是非シェアして感想をいただければ嬉しいです!Twitterやyoutubeのフォローも是非よろしくお願いします。
また次回のノートをお楽しみに!
ここまで見ていただきありがとうございました。________________________________________
以下のテーマを取り上げた記事を更新しました。興味のある方は是非、覗いてみてください。
◆CBD製品における合成品と天然抽出物の比較【リスクとメリット】
◆CBD製品の具体的な生産方法(製造過程)【大麻からの抽出と化学合成】
◆オレンジCBDとは何か
◆合成CBDの歴史と最新の研究【化学合成と生物学的技術】
◆カンナビノイド製品における不純物の検出方法や組成分析技術【GCやHPLC】
この記事が気に入ったらサポートをしてみませんか?
