
どうして結晶はきれいな形なのか:結晶の平衡形
自然鉱物や雪とかの幾何学的な結晶の形ってきれいですよね。私は自然の神秘を感じますが、これも物理を使って理論的に説明することができるんです。
前回、結晶の表面から原子が手を伸ばす数(表面エネルギー)が小さくなるために、多面体形状の結晶が生まれるという話を紹介しました。
今回はなぜあのようなきれいな多面体になるのかについて、難しい数式などは使わずに簡単に紹介したいと思います。
結晶の平衡形”ウルフ多面体”
厳密な話をすると水晶のように私たちの身近にみられる多面体結晶は平衡形とは異なり、成長形と呼ばれる形になります。
ですが、今回は最初の入りということで少しやさしめな平衡形から入りましょう
そもそも平衡というのは何なんでしょうか?理系の人にはなじみの単語だと思います。一般的には平行の方が有名ですもんね。
平衡というのは、結晶表面から入っている原子の数と出ていく原子の数が同じときのことを言います。
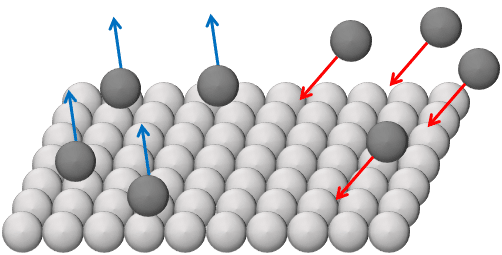
こちらのイラストでは4つの原子が入ってきて、逆に4つの原子が出ていっています。同じ原子でなくてもいいわけですね。
(リアルの結晶とは異なりますが、平衡のイメージはこんな感じ)
つまり、平衡状態というのは、結晶の表面への原子の出入りが等しく見えるということです。ですが、それでは結晶は成長しません。
なぜなら増えた分だけ減ってしまいますからね。
そのため結晶が成長するためには原子は入り続けないといけません。そのため、結晶の平衡形というのは、同じ数の原子で最も安定な形は何ですか?と聞かれたときの形です。または非常に平衡に近く結晶成長するときの形となります。
少し脱線しましたが、結晶の平衡形はどうやって決まるのでしょうか。
これは最初に書いた表面エネルギーとの関係性で決まります。
ここからは少し難しくなりそうなので、ざっくりと行きましょう。
基本的な原理原則は表面エネルギー(原子が伸ばす手の数)が小さくなるように、結晶面が現れます。

[1]より引用
でも、こうやって見てみると特定の面だけが出ているわけではないですよね。
これはいくつか理由があります。まず結晶の体積はあらかじめ決まっているので、特定の面だけ出ていれば全体として安定か(エネルギーが低いか)と聞かれるとNOです。
つまり、結晶全体で見たときにもっともエネルギーが小さくなるように最適な結晶面が出てくるわけです。詳細はウルフの定理、ウルフプロットとググってみてください。
加えて、原子は隣り合う原子とだけ手を伸ばしてるわけではありません。すなわち、ちょっと離れた(第2近接、第3近接)位置にいる原子ともうっすら手をつないでいるのです。
ここまで全部考慮すると上のイラストのような多面体が現れるわけですね。
ちなみに、結晶の平衡形のことをウルフ多面体といいます。ウルフというとオオカミっぽいですが、人の名前です。このウルフさんの研究によってこの分野は少し発展しました。
最後に
再度、注意しておきますが、今回紹介したのはあくまで平衡形であって、私たちが普段見かける雪の結晶などとは違います。平衡形は特殊な環境で作られた小さな粒子などで見られることがある状態です。
とはいえ、結晶の形というのは熱力学的に求められるこの平衡形と環境的な要因で決まる成長形の組み合わせによって決まります。
もう少し勉強が進んだら、結晶の成長形についても紹介したいと思います。
[1] Combination of (100), (110) and (111) facets in MgO crystals shapes from dry to wet environment
この記事が気に入ったらサポートをしてみませんか?
