
ノーベル賞クリスパー・キャス9の知財
今年のノーベル賞について知財分析してみます。
今年のノーベル賞はカリフォルニア大学バークレー校のジェニファー・ダウドナ教授(Jennifer Anne Doudna)とスウェーデンのウメオ大学のエマニュエル・シャルパンティエ教授、現在はマックス・プランク研究所って跳ねましたね(Emmanuelle Marie Charpentier)が選ばれました。MIT のフェン·ザン教授の所属するブロード社との特許紛争でも有名な「クリスパー・キャス9(CRISPR-Cas9)」です。
このCRISPR-Cas9システム、Clustered Regularly Interspaced Short Palindromic Repeats CRISPR-AssociatedProteins 9の略ですが(規則的な間隔で並んでひと塊をなす、回文構造をなす反復配列)と訳します。
1986年に大腸菌で初めて発見された反復クラスターが基になります。ここには当初は日本人も関わって居ましたが今回受賞ならず残念です。
クリストファー·プレストン著の合成テクノロジーが世界をつくり変えるの説明が分かりやすくp143を引用すると
ハーバードとMITの研究者が単純な細菌という枠を越えた複雑な生物のゲノムにこの(切り出した断片を別のもっと望ましい配列に置き換える)知見を応用する方法を突き止めた。植物や昆虫はもちろん哺乳類にも使えるような、きわめて効率の高いゲノム編集技術が基本的に実現されたのだ。CRIRPR の活用により、ゲノムを正確な位置で切り出し、その取り除いた部分を、有用な働きをさせるべく選んだ遺伝子配列に置き換えられるようになった。
とのことです。
改編版のひとつでは、遺伝子を切り取る代わりに、遺伝子のオン/オフを切り替えたり、遺伝子に刺激を加えたりおとなしくさせたりして、遺伝子の発現を調整できるまでになったそうです。
「CRISPR」はある特定のDNA配列のことです。
「Cas9酵素」はDNAを切断する酵素です。
「ガイドRNA」は特定のDNA部位を探し出します。
このゲノム編集では「CRISPR」をもとに切断したい部分にとりつくいわば目印となる配列を作ります。この目印となる配列をめがけて、「Cas9」が到達し、DNAを切断します。
この研究には、ごく微量のDNA試料で、配列解析が可能で高感度の検出を短時間で行うことができるポリメラーゼ連鎖反応(PCR:Polymerase Chain Reaction)技術が貢献しています。
って何処かで聞いたと言うか、コロナ禍で耳タコの言葉が出てきますな。
PCR法は、遺伝子操作実験を圧倒的に簡便化し、初心者でも遺伝子操作実験ができるようになったそうです。やったことはないですが日本ではインフルエンザ試薬が発達してわざわざ遺伝子から解析する必要性が少なくて装置が少なかったとお聞きしました。
CRISPR-Cas9の基本特許
CRISPR/Casに関する基本特許について、列記します。
フェン・ジャンのブロード(Broad )社
米国仮出願61/736,527
真核生物における人工型の概念に関する特許(米国特許第8,697,359号)
分割出願多数のため、これだけがという訳では無いですが色々持ってますね。ここ所属の発明者はノーベル賞の対象外でした。
後で述べますが、ノーベル賞を受賞したバークレーと揉めていることを嫌気したのかもしれません。
カリフォルニア大学バークレーBerkeley
米国出願13/842,859、61/65,2086
対象が限定されない人工型の概念に関する特許
分割出願を活用して要素技術の特許化し,2018年6月に1件の特許(米国特許第10,000,772 号)
先ほどありましたブロード(Broad )社の方が後願なのですが、
US早期審査制度(いわゆるファーストトラック)を利用していち早く,真核生物における天然型及び人工型の概念に関する特許(米国特許第8,697,359号)を取得しました。
バークレーとしては、これもUS特有のインターフェースで先発明による異議申し立てを行いました。自分たちのは人以外が対象で、ブロード側は人も含む真核生物だったので潰すしかライセンスを考えると障害にしか感じ無かったのでしょう?
ノーベル賞の受賞者を見てもどちらが優位かはわかりますね。バークレー側の初期の講演では人への、真核生物への転用は分からないと言ってたので、ブロード側は残念でしようが。
一度目のインターフェアレンスについては18年9月、控訴裁判所は米国特許裁判と上訴委員会の判決を維持すると決定を下し、チャン博士の特許権が認められたが、翌19年にも2度目のインターフェアレンスがあり争いにはまだ決着が付いていません。
ノーベル賞側も辛く
「 該接触は、インビボのヒト細胞ではなく、ヒト生殖細胞ではなく、およびヒト胚細胞ではない細胞内で行われ、」
という限定が日本の特許では行われています。

二四から四八塩基スペーサーが付与する塩基配列特異性
これ以外にも基礎出願と呼べそうな他社の出願はあり、公報番号だけ列記します。
Toolgen 韓国
米国仮出願61/717,324
Vilnius大学 リトアニア
米国仮出願61/613,373
Cas9 の由来,in vitro での使用及び二重鎖分解へ限定し,天然型CRISPR-Cas9に関する特許(米国特許第 9,637,739 号)
シグマアルドリッチ社 アメリカ
(米国出願14/649,777、61/734,256)
セレクティス社
(米国特許9,458,439 号)
論文を最初に出したのはダウドナ
では人体にCRISPR-Cas9が使用可能としたのは誰!?
この分野の歴史
60年代には品種改良のため、放射能を照射して突然変異種をどこか自然に任せて作っていました。例;20世紀ナシ
70年代には遺伝子組み換えにより別の遺伝子を挿入することが可能となりました。例:青いバラ
1970 年代後半には、Boyer らが設立したGenentech 社が合成ヒト遺伝子を組み込んだ大腸菌を使用し、糖尿病治療用のインスリンを量産します。その後、遺伝子組み換えされたマウスを良く見た記憶が有りませんか?「アルジャーノに花束を」
1987年,大阪大学の中田篤男・現名誉教授と,当時タカラで勤務していた石野良純・現九州大学教授のグループが,大腸菌のゲノムに同じ配列が何度も繰り返し現れることを発見。これがCRISPRの基礎でもあり石野さんはノーベル賞かも?と期待されていました。
宝酒造株式会社ってバイオに強いのですが、ノーベル賞とってたら痛快だったはず、残念!
ハサミの技術についても第3世代のCRISPR/Cas9以外にも蓄積が有るので簡単に見ていくと
第1世代 1996年 ZFP⇒ZNF キメラヌクレアーゼ ジョンホプキンス大学
Zincフィンガーを結合されたヌクレアーゼ(FOK1)を利用して片鎖を切断します
ZFN(Zinc Finger Nuclease)は US6013453号Sangamo Therapeutics(米国)が製造、研究用のSigma Aldrich(米国)が有名
標的認識技術区分別では、「ZFP」ではSangamo Therapeutics(米国)とUniversity of California(米国)、京都大学が上位3位にランクインしており既存のゲノム編集ツールの権利化状況として、ZFNの研究利用はSigma Aldrich(2015年11月にMerck(ドイツ)により買収)、商業利用はSangamo Therapeutics(米国)が世界的な基本特許の権利を有している
MITのUS789538号なども有名です。
第2世代 2000年 TALEN TALEヌクレアーゼ ユタ大学
食物細菌キサントモナスの転写因子TALEタンパク質由来の結合ドメインを結合させたヌクレアーゼ(FOK1) US8470973号、WO2011072246号
TALEN( Transcription Activator-Like Effector Nuclease)Cellectis(フランス元Institut Pasteur)、US8586363号ミネソタ大学、アイオワ大学
TALENについては、治療分野に関してはCellectis(フランス)が、治療分野以外はThermo Fisher Scientific(米国)が世界的な基本特許の権利を有している
90年代にDNAの特定の配列に結合するすが登場し,ピンポイントで切断する道が開けた
ちょっと古いが特許庁の資料がまとまっています。
細菌が有害ウイルス感染をしのぐと、有害なDNAの短い配列を、敵に関する一種の生化学的な記憶として保存できる。この相手を認識し取り除いて無害化するプロセスを利用するのが第三世代の特徴です。
まとめ
上で述べたようにCRISPR/Casシステムについては、米国はUniversity of Californiaのバークレーグループ(原核生物)とBroad Institute(真核細胞)の両方に特許が与えられました。
日時的には
ダウドナ教授(バークレー校)らは、2012年6月サイエンス誌に発表した(掲載号は8月)。そして、これに先立つ同年5月25日に米国にて仮出願をした。
他方で、フェン·ザン博士(ブロード社)らは、同年12月12日に「CRISPR/Cas9」に関して米国に仮出願をし、その後2013年10月15日に優先権主張出願をし、早期審査を経て特許が付与されました。一部は残って要るので敗けでは無いですが、バークレーの方が優勢なのは確かなところです。
クリスパー配列は繰り返し単位の中に逆向きの二回対称配列を切り分けるハサミ✂️はこの分野の発展に寄与していて、ノーベル賞の授与も妥当なんてしようね。
2019年にはブロード研究所の十二の特許権とCVC社の十の特許権の争いもある。
シングルガイドRNAの優先権争いだそう。
今後もCRISPR/Casシステムを巡る知的財産の争いが今後も繰り返されるだろうし、アメリカを中心にライセンスで稼ぐのだろうね。
ちなみに国ごとにその基本特許の権利者が異なる状況が起きています。勿論日本にも出願を移行しており、出願や裁判は係属中でもあるのですが、日本発も期待したいです。
以前研修で見せて頂き勉強になった発明者ネットワークのつながりの図です。

個人的感想
個人的には最もまとまっていた記事はこちら
四十の手習いでこの分野の勉強を初めてはや数年、難しいですよね。
高校の教科書を取り寄せて読んでたらPCR法が載ってて、しかもパン酵母を利用した組み換えDNA実験まで有るんですよね。時代は変わった!
また、知財についても、モデルナ社がコロナ禍なのでワクチンについて自社の特許紛争を行わない旨を宣言しました。
日本でもトヨタとキャノンが旗振り役となってコロナ関連の特許自由実施を宣言しました。置いてかれてはイメージにと、ホンダなど各社手を上げました。
知財の扱いも難しいですよね。出願要らないと言うか、訴訟しないとテスラに言われると他はうちずらいです。
これはトヨタの燃料電池車も同じですが。
元に戻ってバイオでも研究と製品化ではフェーズや参加企業も異なり、悪者に成らない方法を模索しています。
とろーるなら楽なんだろうな。
勉強したならノーベル賞も解るだろうと言われたので追記
【出願】 14/685,502(2015/04/13) 【公開】 2016/0130608 (2016/05/12)
【特許】 10,000,772 (2018/06/19)
【発明の名称】 Methods and compositions for RNA-directed target DNA modification and for RNA-directed modulation of transcription
【出願人/権利者】 NATIONAL INSTITUTES OF HEALTH (NIH), U.S. DEPT. OF HEALTH AND HUMAN SERVICES (DHHS), U.S. GOVERNMENT;THE REGENTS OF THE UNIVERSITY OF CALIFORNIA;UNIVERSITY OF VIENNA
【発明者】 Doudna Jennifer A.;Jinek Martin;Charpentier Emmanuelle;Chylinski Krzysztof
対応JP登録6343605B2
公開2件JP2018138054A、JP2020039351A
56段落32ページにわたる関連出願・文献が載っています。
図もFig57Bまで
ファミリー特許群は
US201261652086P
US201261716256P
US201361757640P
US201361765576P
US2013032589W

登録クレーム

代表図です。
PAM でマーキングしたターゲットDNAから所望の場所を刈る技術です。
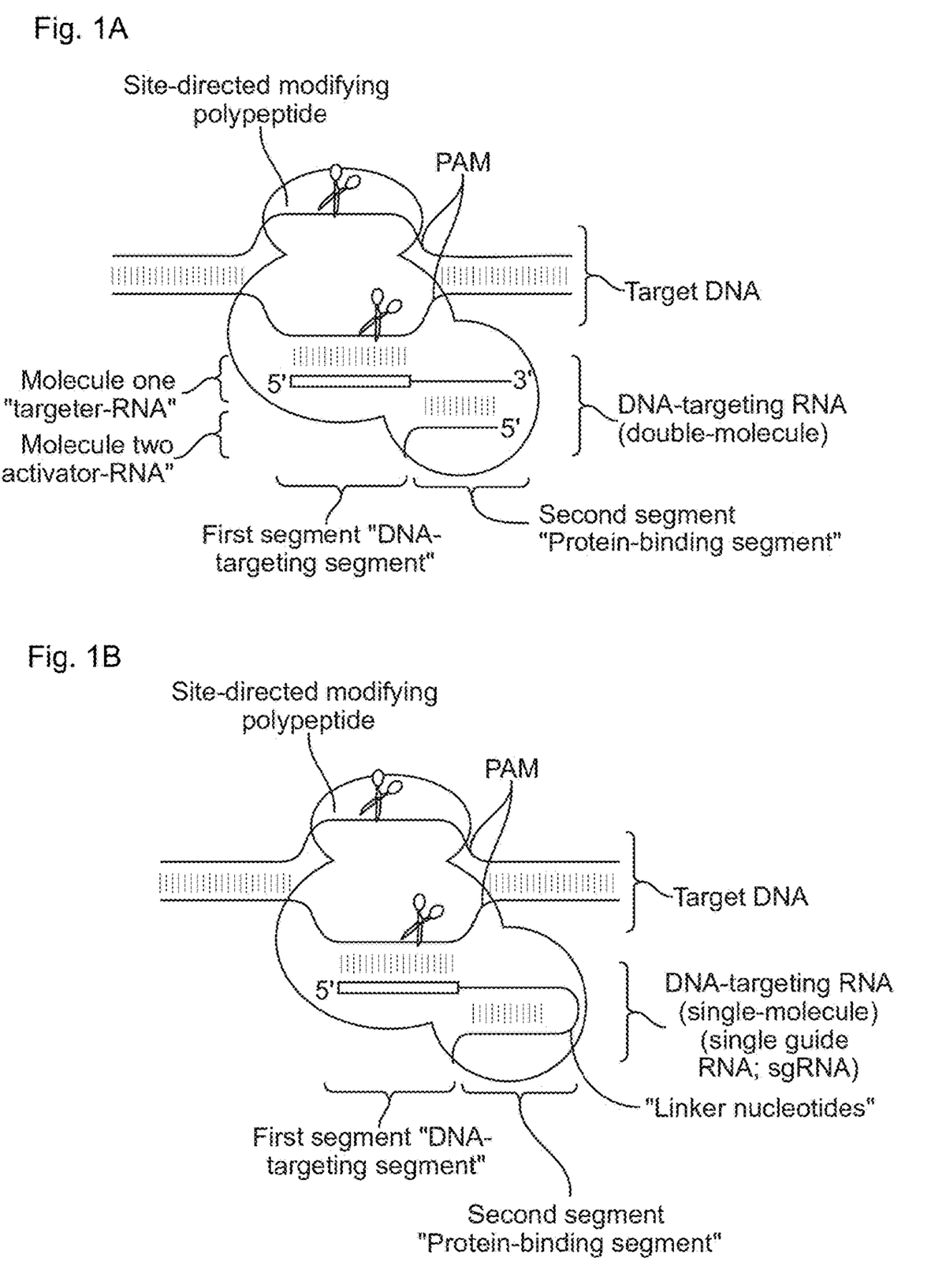

対比のために競合特許も
2019/06/24にDeclaration of Interference、つまりインターフェアレンスにより無効化されようとしています。
【出願】 14/54,414(2013/10/15) 【公開】
【特許】 8,697,359 (2014/04/15) 【優先権】
【発明の名称】 CRISPR-Cas systems and methods for altering expression of gene products
【出願人/権利者】 NATIONAL INSTITUTES OF HEALTH (NIH), U.S. DEPT. OF HEALTH AND HUMAN SERVICES (DHHS), U.S. GOVERNMENT;THE BROAD INSTITUTE, INC.;MASSACHUSETTS INSTITUTE OF TECHNOLOGY
【発明者】 Zhang Feng
対応日本の特許はファミリーだけでこれだけ登録しています。
JP6552965B2
JP6545621B2
JP6203879B2
JP6420273B2
JP6395765B2
JP6625971B2
JP6495395B2

対応日本のクレーム1だと
【請求項1】
目的ゲノム遺伝子座における標的配列の操作により生物または非ヒト生物を改変する方法において、
A)-I.CRISPR-Cas系キメラRNA(chiRNA)ポリヌクレオチド配列であって、
(a)真核細胞中の標的配列にハイブリダイズし得るガイド配列、
(b)tracrメイト配列、および
(c)tracr配列、
を含むポリヌクレオチド配列、および
II.CRISPR酵素をコードするポリヌクレオチド配列であって、場合により少なくとも1つ以上の核局在化配列を含む配列[(a)、(b)および(c)は、5’から3’配向で配置されており、
転写されると前記tracrメイト配列が前記tracr配列にハイブリダイズし、かつ
前記ガイド配列が前記標的配列へのCRISPR複合体の配列特異的結合を指向し、および
前記CRISPR複合体は、(1)前記標的配列にハイブリダイズされる前記ガイド配列
、および(2)前記tracr配列にハイブリダイズされる前記tracrメイト配列と複合体形成している前記CRISPR酵素を含み、かつ前記CRISPR酵素をコードするポリヌクレオチド配列は、DNAまたはRNAである]、
または
(B)I.ポリヌクレオチドであって、
(a)真核細胞中の標的配列にハイブリダイズし得るガイド配列、および
(b)少なくとも1つ以上のtracrメイト配列を含むポリヌクレオチド、
II.CRISPR酵素をコードするポリヌクレオチド配列、および
III.tracr配列を含むポリヌクレオチド配列[転写されると前記tracrメイト配列が前記tracr配列にハイブリダイズし、かつ前記ガイド配列が前記標的配列へのCRISPR複合体の配列特異的結合を指向し、および
前記CRISPR複合体は、(1)前記標的配列にハイブリダイズされる前記ガイド配列、および
(2)前記tracr配列にハイブリダイズされる前記tracrメイト配列と複合体形成している前記CRISPR酵素を含み、かつ前記CRISPR酵素をコードするポリヌクレオチド配列は、DNAまたはRNAである]
を含む天然に存在しないまたはエンジニアリングされた組成物を送達することを含む、方法。
つらいってことで絵を見ます。


国際調査結果は論文に書いてあるそうな

この記事が気に入ったらサポートをしてみませんか?
