88)ブドウ糖から脂肪酸への代謝シフトが健康寿命を延ばす
体がみるみる若返るミトコンドリア活性化術88
ミトコンドリアを活性化して体を若返らせる医薬品やサプリメントを解説しています。
【脂肪酸はミトコンドリアでβ酸化によって分解される】
β酸化(ベータさんか)とは脂肪酸を酸化して脂肪酸アシルCoA(fatty acyl-CoA; 脂肪酸と補酵素Aのチオエステル)を生成し、そこからアセチルCoAを取り出す代謝経路のことです。脂肪酸アシルCoAのβ位において段階的な酸化が行われることからβ酸化と名付けられました。
β酸化は4つの反応の繰り返しから成り、反応が一順するごとにアセチルCoAが1分子生成され、最終生産物もアセチルCoAとなります。生成されたアセチルCoAはTCA回路(クエン酸回路、クレブス回路)に送られ、酸化的リン酸化を経てATP産生に使われます。動物細胞では脂肪酸からエネルギーを取り出すための重要な代謝経路です。
脂肪酸のβ酸化はミトコンドリアで行われますが、長鎖脂肪酸はカルニチンが無いとミトコンドリアに入れませんが、中鎖脂肪酸はカルニチンの助けなしにミトコンドリアに運ばれ、β酸化で代謝されます。(下図)
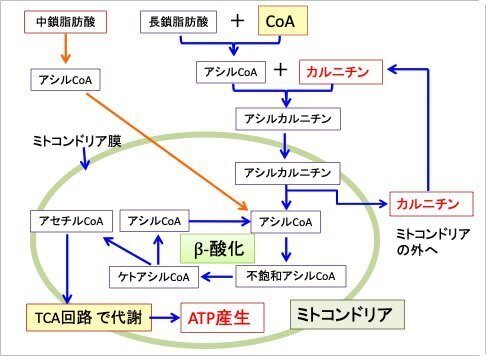
図:脂肪酸はミトコンドリアでβ参加によってアセチルCoAを生成する。長鎖脂肪酸はカルニチンが無いとミトコンドリアに入れない。一方、中鎖脂肪酸はカルニチンの助けなしにミトコンドリアに運ばれ、β酸化で代謝される。
【脂肪酸のβ酸化のレベルが寿命に影響する】
寿命延長の達成で最も再現性のある方法はカロリー制限です。栄養障害を起こさずに食事からの摂取カロリーを30~40%程度減らすと寿命延長効果があることは、酵母から線虫、ハエ、マウス、霊長類に至る多くの生物種において確認されています。さらに、カロリー制限は老化を遅延し、がんを含めた老化関連疾患の発症を遅らせる効果も確かめられています。
カロリー制限すると脂肪の燃焼が亢進します。このとき、カロリー制限がAMP活性化プロテインキナーゼ(AMPK)を活性化し、活性化したAMPKが脂肪酸のβ酸化を亢進するということになっています。糖質制限などによるインスリン/インスリン様成長因子シグナル系の抑制も脂肪酸β酸化を促進します。
カロリー制限やAMPK活性化などで脂肪酸のβ酸化が亢進されますが、脂肪酸のβ酸化の亢進自体がカロリー制限と類似のメカニズムで寿命延長効果を示すことが報告されています。以下のような報告があります。
Overexpression of Fatty-Acid-β-Oxidation-Related Genes Extends the Lifespan of Drosophila melanogaster(脂肪酸β酸化に関連する遺伝子の過剰発現はショウジョウバエの寿命を延ばす)
Oxid Med Cell Longev. 2012; 2012: 854502.
この研究グループは、ショウジョウバエの突然変異系統(ミュータント:変異体)を使って、寿命に関連する遺伝子の研究を行っています。ある遺伝子が過剰発現していることによって寿命が延長したショウジョウバエの突然変異系統を解析して、寿命延長効果のある遺伝子を幾つか発見しています。その中に、脂肪酸のβ酸化に関連する遺伝子のfatty-acid-binding protein(脂肪酸結合蛋白) と dodecenoyl-CoA delta-isomerase があったということです。
つまり、脂肪酸のβ酸化に関与する遺伝子が過剰に発現したショウジョウバエの突然変異系統は正常と比べて寿命が延びるという結果を報告しています。
コントロールの正常のハエの平均寿命が32日に対して、fatty-acid-binding proteinの遺伝子が過剰に発現しているハエの平均寿命は58日、dodecenoyl-CoA delta-isomerase遺伝子が過剰に発現しているハエの平均寿命は42日でした。
また、正常なハエでは、カロリー制限によって寿命が31.4%延長したのに対して、脂肪酸β酸化関連の遺伝子が過剰発現しているハエでは、カロリー制限による寿命延長が減少していました(12%と15%)。これは、脂肪酸β酸化関連遺伝子の過剰発現による寿命延長作用のメカニズムはカロリー制限による寿命延長作用のメカニズムと共通していることを意味しています。
つまり、カロリー制限を行わないでも、脂肪酸のβ酸化を促進することはカロリー制限と同じ寿命延長効果を再現できることを示しています。
ただし、カロリー制限の寿命延長効果が脂肪酸β酸化の亢進でゼロになったわけではなく、約半分に減少した程度なので、カロリー制限による寿命延長作用にはβ酸化亢進以外のメカニズムも関与していると考察しています。
さらに、酸化ストレスや飢餓に対する抵抗性が高まっていることを示しています。つまりβ酸化の亢進したハエでは、パラコートを使った酸化障害やエサを減らすことによる飢餓によって死亡する率が減少することが示されています。さらに、このような効果のメカニズムとしてFOXOシグナル伝達系が活性化されていることが示されています。
そして、この論文の結論は「脂肪酸のβ酸化に関与する遺伝子の過剰発現はカロリー制限と同じような機序で寿命を延ばし、そのメカニズムとして転写因子のFOXOの活性化の関与が示唆された」ということでした。
【FOXOとは】
長寿になるには、様々なストレスに対する抵抗性が高くなっている必要があります。医学の発達によって80歳代での死亡が多くなっていますが、100歳を超えるような超高齢になるには、それなりの理由があるはずです。FOXOは様々なストレスに対する抵抗力を高める作用を担っており、カロリー制限における寿命延長や老化性疾患の抑制において重要な役割を果たしていることが知られています。
FOXOは「Forkhead box O」の略で、DNA結合ドメインFOX(Forkhead box)をもつForkheadファミリーのサブグループ“O”に属する転写因子です。哺乳類ではFOXO1,3,4,6の4種類が存在、線虫ではDaf-16、ショウジョウバエではdFOXOとそれぞれ1種類のみ存在し、栄養飢餓時に活性化される転写因子です。
転写因子というのは特定の遺伝子の発現(DNAの情報を蛋白質に変換すること)を調節している蛋白質で、FOXOはストレス応答、代謝制御、細胞周期、アポトーシス、DNA修復などに関連する多くの遺伝子の発現誘導を促します。がん抑制遺伝子としての性格ももっており、FOXOの活性化は抗がん作用があります。
FOXOはインスリン-PI3K-AKTシグナルによって負に制御されています。つまり、PI3K-AKTシグナルが活性化されるとAKTによって直接的にリン酸化され、FOXOの核外移行を促進することでその転写活性は抑制されます。
一方、栄養飢餓状態ではPI3K-AKTの不活性化に伴いFOXOの活性化が誘導されることになります。つまり、カロリー制限や糖質制限やAMPK活性化などによる寿命延長や抗がん作用に関与する転写因子として重要な役割を担っています。
脂肪酸のβ酸化の亢進がどのようなメカニズムでFOXOを活性化するかは現時点では不明です。しかし、何らかの機序で、脂肪酸の燃焼(β酸化)の亢進はFOXOの活性化を介して寿命延長と抗がん作用を発揮する可能性が示唆されます。
【脂肪酸のβ酸化を亢進するケトン食】
ケトン食が健康寿命を延ばすことが動物実験で報告されています。例えば、以下のような報告があります。
A ketogenic diet extends longevity and healthspan in adult mice(ケトン食は成体マウスの寿命と健康寿命を延ばす)Cell Metab. 2017 Sep 5; 26(3): 539–546.e5.
【要旨】
栄養失調のないカロリー制限は、寿命を延ばすことが示されている。これは糖代謝から脂肪酸のベータ酸化へのシフトと関連している。この研究の目的は、低糖質食を使用してこの代謝シフトを模倣し、マウスの寿命と健康寿命に対するこれらの食事の影響を検討した。
C57BL/6 マウスは、生後12 か月の時点でケトン食、低炭水化物、または対照食に割り当てられ、1か月または 14か月の食事介入後に自然な寿命を延ばすか、生理学的機能についてテストされた。
ケトン食は、コントロールと比較して寿命と生存期間の中央値を大幅に増加させた。老齢マウスでは、ケトン食を摂取したマウスのみが生理機能の維持を示した。ケトン食はタンパク質のアセチル化レベルを増加させ、組織依存的に mTORC1 シグナル伝達を調節した。
以下のような報告もあります。
Ketogenic diet reduces mid-life mortality and improves memory in aging mice(ケトン食は中年の死亡率を低下させ、老齢マウスの記憶を改善する)Cell Metab. 2017 Sep 5; 26(3): 547–557.e8.
この論文では、雄マウス(C57BL/6)を使って、ケトン食が健康寿命に影響するかどうかを検討しています。ケトン食を隔週で周期的に行ったマウスでは、中年期の死亡率を減らしましたが、最大寿命は延長しませんでした。
この周期的ケトン食は、高齢マウスの記憶力を改善すると同時に、複合的な健康寿命の測定値をわずかに改善しました。
遺伝子発現解析により、体中の組織で、インスリン、ラパマイシン標的タンパク質(TOR)、および脂肪酸合成経路の発現レベルが低下し、PPARα標的遺伝子の発現亢進が認められました。
全体として、ケトン食が老化マウスの生存率、記憶力、および健康寿命を改善することを示しています。
「ケトン食」というのは、体内でケトン体が多く産生されるように考案された食事です。古来、さまざまな疾患に絶食療法が行われており、特にてんかん発作が絶食によって減少することは古くから知られていました。そして、「脂肪を多く炭水化物の少ない食事をと摂れば、絶食と同等の効果が得られる」という考えのもとに、1920年代に米国のメイヨークリニックでケトン食療法(ketogenic diet)が発案されました。
ケトン食というのは、絶食療法の代わりとして考案されたものですが、糖質制限食よりも、脂肪の燃焼亢進作用が高いことが報告されています。
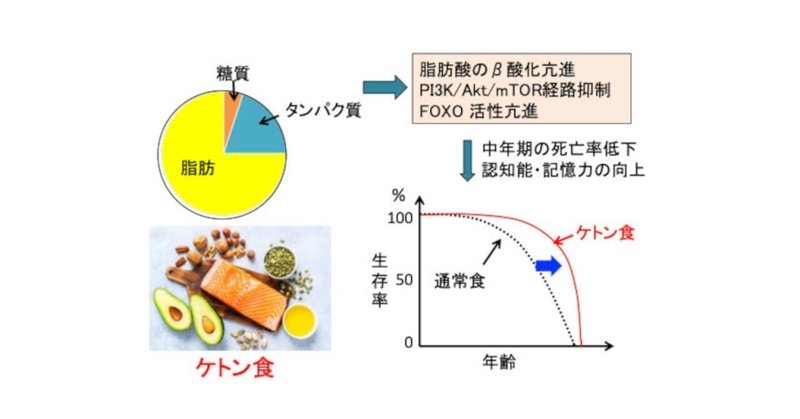
ケトン食はエネルギー産生を糖質主体から脂肪酸主体にシフトさせることによって、健康寿命を延長し、認知機能を良くすると考えられています。

図:脂肪が多く、糖質の少ないケトン食は、脂肪酸のβ酸化を亢進し、PI3K/Akt/mTORシグナル伝達系を抑制し、転写因子のFOXOの活性を亢進する。その結果、中年期の死亡率を低下し、認知機能と記憶力を向上する。
この記事が気に入ったらサポートをしてみませんか?
