
妊娠初期にワクチン打つと自然流産と比較して7から8倍の流産リスクが上がるとの論文
科学、公衆衛生政策、および法律
第4巻:130-143 2021年11月
クリニカル&トランスレーショナルリサーチ
迅速なコミュニケーション
純粋・応用知識研究所(IPAK)の
and Applied Knowledge (IPAK)
パブリック・ヘルス・ポリシー・イニシアティブ(PHPI)
妊娠中の自然流産とCOVID-19 mRNAワクチンの使用に関する政策
Aleisha R. Brock1, Simon Thornley2
概要
ニュージーランド、米国、オーストラリアなどでは、COVID-19に対するmRNAワクチンの妊娠中の使用は、一般的に安全であると考えられている。しかし、この考えを裏付けるためにCDCがスポンサーとなって発表されたShimabukuroらの論文(2021年)をよく見てみると、特に妊娠初期に感染した場合には、ほとんど保証されていないことがわかります。この研究では、計算対象となった女性の大半が、アウトカム期間が定義された後(妊娠20週)にmRNA製品に曝露されているため、妊娠初期の自然流産のリスクに関連する誤った安心感を与える統計値が提示されています。
この論文では、これらの誤りに注目し、妊娠20週以前にワクチンに曝露されたコホートに基づいて、この転帰のリスクを再計算しました。再解析の結果、自然流産の累積発生率は、原著者の結果の7~8倍であることがわかりました。
(p < 0.001)であり、この期間の妊娠損失の典型的な平均値よりも7~8倍高いことがわかりました。これらの結果を受けて、信頼性の低い疑わしいデータを用いて重要な政策決定がなされています。我々は、COVID-19を予防するためのmRNAベースのワクチンに妊娠初期の女性が曝露することの安全性について、これらのデータを用いて行われた主張は正当ではないと結論づけ、それらの政策決定を見直すことを提言する。
Copyright © The Authors - Published Under the Creative Commons License Share/Alike (See https://creative commons.org/licenses/)
Correspondence: s.thornley@auckland.ac.nz
キーワード
COVID-19; 妊娠; 有害事象; 自然流産
1 Dr Aleisha Brock Ph.D., MVS, BSc. Dr Aleisha Brock Ph.D., MVS, BSc., Whanganui, New Zealand. E-mail: aleisharbrock@protonmail.com
2 Dr Simon Thornley Ph.D., MPH(Hons), MBChB. オークランド大学 疫学・生物統計学部 上級講師 Park Rd, Grafton, New Zealand E-mail: s.thornley@auckland.ac.nz
Sci, Pub Health Pol, & Law Critical appraisal of VAERS Pharmacovigilance - Oct. 2021
目次
1 はじめに 131
2 研究の探求と考察 131
3 さらなる議論 135
4 結論 137
5 編集者による注釈 137
6 編集者の参考文献 137
7 著者の参考文献 138
8 付録の表 142
1 はじめに
ニュージーランド[1]、アメリカ[2]、オーストラリア[3]などの国では、COVID-19に対する保護を目的としたmRNAワクチンを妊娠中に使用することは、妊婦とその胎児にとって安全であると報告されています。ここでは、これらの懸念を概説し、妊娠中の女性にこれらのワクチンを無制限に使用することに疑問を呈します。
著者らは、2020年12月14日から2021年2月28日まで(11週間)のv-safe登録データを分析し、結果が記録されている827件の妊娠(登録された3,958件のうち)を対象とした。データは、米国の3つのワクチン安全性監視システム(v-safe after- vaccination health checker、v-safe registry、Vaccine Adverse Event Reporting System(VAERS))から収集した。米国疾病予防管理センター(CDC)のv-safeレジストリは、COVID-19ワクチン接種プログラムのために開発されたCDCのスマートフォンをベースにした新しいアクティブサーベイランスシステムで、参加者にテキストメッセージを送信して、健康状態を評価するオンライン調査への回答を促し、ワクチン接種後の副反応の報告を12カ月間奨励しています。
最終接種から12カ月後まで、ワクチン接種後の副反応の報告を促します。著者らは、妊娠中のmRNAワクチンの使用を妨げる明らかな安全性シグナルはないと結論づけています。この結論は、自然流産の累積発生率が12.6%(104/827)であり、過去の研究と同様であると考えられることから、さらに正当化されました。しかし、島袋氏らは、「参加者は妊娠第1期の最もリスクの高い時期の後にワクチンを接種した可能性があり、非常に早い時期の妊娠の喪失が認識されない可能性があるため、自然流産を報告した妊娠者の割合は、(ワクチン接種後の)真の割合を反映していない可能性がある」と正しく認識しています[4]。
しかし、この計算の分母となった827人の女性を詳しく調べてみると、700人から713人の女性が、結果を記録するための期間(妊娠20週まで)が経過した後にワクチンにさらされていることがわかりました。したがって、これらの数値を再分析すると、自然流産の累積発生率は82%(104/127)から91%(104/114)となり、原著者らの結果よりも7~8倍高くなります。
この論文の情報をもとに、女性が初めてワクチンにさらされた妊娠期間を導き出し、mRNA製品を投与された後に自然流産の危険性がある女性のおおよその数を算出しました(妊娠20週以前にさらされた女性)。生児が誕生したのは712人(724人、うち多胎児は12人)で、700人(98.3%)が妊娠第3期にワクチンに初めて曝露され、妊娠26週以前に曝露された女性は12人だけでした。この研究では、さらに多くの女性が20週以前にワクチンを接種していましたが、これらの女性の妊娠の結果はほとんど入手できず、研究の時間枠内で生児を出産することはできませんでした。このコホートの入手可能な結果では、第1期および第2期の女性のうち、それぞれ約8%(96/1,132)および約0.8%(14/1,714)の結果しか把握できませんでした。
2 現在の推奨事項を示すために使用された研究の調査と考察
現在の推奨事項
131
Sci, Pub Health Pol, & Law Critical appraisal of VAERS Pharmacovigilance - October.2021
図 1. 島袋ら(2021)が使用した曝露コホートと転帰コホートの比較[4] 曝露の4つのコホートが報告された:受胎前後(最終月経の30日前から14日後まで),第1期(受胎から14週まで),第2期(14週から28週まで),第3期(28週から出産まで)。2つのコホートのアウトカムが報告されました:20週前に受けた最初のmRNAワクチン、および妊娠20週以降に受けた最初のmRNAワクチン。乳児は周産期(出生~28日)に28日間追跡されました。
さらに混乱を招いたのは、曝露と転帰の期間がいくつか重なって報告され、女性のコホートを定義するために使用されたことです。ワクチンへの曝露は、3学期(妊娠前後、第1、第2、第3)で定義されました。転帰は、妊娠20週以前に初めてmRNAワクチンにさらされた女性、および妊娠20週以降に初めてさらされた女性と定義した。乳児は、周産期(出生~28日)の28日間、追跡調査を行った(図1)。
これらの解析では、mRNA注射が妊娠20週以前、または妊娠20週以降に行われた女性の総数が論文に明記されていないため、範囲が示されている。本文および表に記載されている情報から、以下のように理解しています。
1. 少なくとも114人の女性が妊娠20週以前に初めて妊娠した(妊娠損失として報告された)。
a. そのうち、96人が妊娠第1期(妊娠14週までの妊娠)であった。
b. 残りの18人の妊婦は、第2期の前半に被曝したものと思われる。妊娠14週目から20週目まで。
2. 第3期(妊娠28週から出産まで)に、700人の妊婦が初めてmRNAの注射にさらされたと報告されている。
3. 3.第2期(妊娠14週から28週まで)にmRNAに曝露された残りの13人の女性は、妊娠喪失のタイプ(自然流産または死産)を定義するための20週目のカットオフの前後でmRNAに初めて曝露されたとはさらに分類できないため、この不確実性を反映して範囲が報告されています。
島袋ら(2021年)[4]が行った安全性に関する包括的な結論は、彼らの研究の限界を考慮すると、説得力がありません。これらは以下の通りです。
1. 研究デザインの問題は以下の通りです。
a. 未露光の妊娠を用いていない。
b. コホートの94%が医療従事者であった。
c. V-safe登録の妊婦のうち、妊娠登録にも登録されていたのは15%未満であった。
2. 2.最初の20週での妊娠喪失について、累積発生率の計算に誤った分母が使用されていた。この計算には、アウトカム(自然流産)が定義された後に初めて注射にさらされたコホートが含まれていました。この点については、McCulloughらが考察しています[5]。
132
Sci, Pub Health Pol, & Law 自然流産と COVID-19 mRNA ワクチンに関する政策 - 2021年11月
3. など、提言を批評するのに必要な必須の記述統計を開示していない。
a. 最初のmRNAワクチン接種が妊娠20週前と後に行われた女性の生児数。
b. これらのグループの総妊娠数。
4. 4.曝露と転帰は、互換性のない2つの妊娠の尺度、すなわち、3学期(第1、第2、第3)と妊娠期間(20週未満、または20週以上)を用いて提供された(図1)。
5. 1回目と2回目のmRNAワクチン接種のタイミングがなく、結果も示されていない。さらに、妊娠転帰が製品の種類への曝露によって異なるかどうかを判断するための分析結果も提供されていませんでした。ファイザー/バイオンテック社の「BNT162b2」またはモデナ社の「mRNA-1273」のいずれかの製品への曝露によって、妊娠結果が異なるかどうかの分析は提供されていない。
6. 6.曝露後14日以内に発生した有害事象を含めるかどうかは規定されていない。
7. 7.自然流産リスクの過去の比較には、臨床的に認識されていない妊娠を含む推定値である26%という高いベースラインレートが使用されており、本研究で使用された定義(臨床的に認識された妊娠)とは大きく異なっています[5]。 臨床的に認識された妊娠の比較可能な推定値は、8%から15%の範囲です[6-8]。 ここでは、臨床的に認識された自然流産率である11.3%(マニトバ州でn=79,978人の女性を対象に実施された研究による)を使用しています[7]。
8. 自然流産の過小評価の可能性。自然流産は、妊娠に関連する有害事象の中で最も頻繁に報告されていました。しかし、自主的な報告システムは遅れがちであることが知られています。この記事で使用されている2021年2月28日までのVAERS報告は
今回の記事で使用した2021年2月28日までのVAERS報告は、イベント発生日ではなく報告を受けた日に基づいており、報告数が少ない可能性が高いと考えられます。
データの詳細について
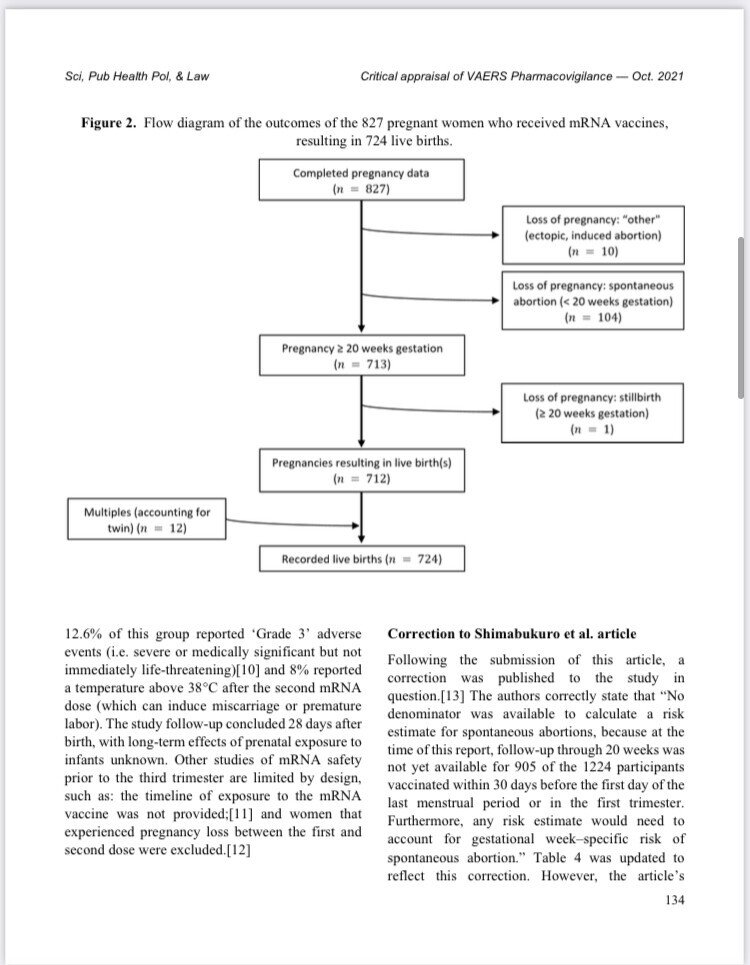
この研究には限界がありますが、著者が提示しなかったいくつかの情報を得ることができます。フロー図(図2)は、本研究に参加した827人の妊婦の転帰を示しており、その結果、724人の生児が誕生しました(12人の多胎児を含む)。図2を用いて、各曝露群の総数をある程度の不確実性をもって推定することができる(範囲が示されている;表1参照)。しかし、表1と原著論文[4]の表4を組み合わせて、妊娠中のmRNAワクチン使用と妊娠転帰(表2)との関連性をコホート別に調べました。
その結果、少なくとも81.9%(≧104/127)が20週以前のmRNA曝露後に自然流産を経験し、自然流産の92.3%(96/104)が妊娠13週以前に発生していることがわかりました(表4、脚注)。 [これは、妊娠20週以前にmRNAワクチン接種を受けた人に観察された妊娠喪失の割合が81.9~91.2%(n=114~127)と非常に高く、他の研究のベースライン推定値(11.3%、n=79,978[6]、p<0.001)とは有意に異なり、予想よりも7~8倍高かった(p<0.001)ということになります。) 妊娠20週以前に初めてmRNAワクチンを接種した人の妊娠損失の発生率に、ベースラインと比較して差がなかったという著者の解釈には疑問が残ります。
一見すると、今回発表された研究は、妊娠第3期にmRNAワクチンを接種しても安全であることを示しており、29週からの接種を検討した別の研究でも支持されています[9]。 しかし、McCulloughらが強調しているように[5]。
133
Sci, Pub Health Pol, & Law Critical appraisal of VAERS Pharmacovigilance - Oct. 2021
図 2. mRNAワクチンを投与された827名の妊婦の転帰を示すフロー図で、724名の生児が誕生しています。
このグループの12.6%が「グレード3」の有害事象を報告した 島袋らの論文の訂正
イベント(すなわち、重度または医学的に重要であるが、直ちに生命を脅かすものではない)[10]を報告し、8%が2回目のmRNA投与後に38℃以上の体温(流産または早産を誘発する可能性がある)を報告しました。この研究の追跡調査は生後28日目に終了しており、出生前の暴露による乳児への長期的な影響は不明です。妊娠第3期以前のmRNAの安全性に関する他の研究は、mRNAワクチンへの曝露のタイムラインが提供されていない、[11]、1回目と2回目の投与の間に妊娠喪失を経験した女性が除外されているなど、デザイン上の制限があります[12]。
本論文の投稿後、当該研究の訂正版が発表されました[13]。著者は、「本報告書の時点では、最終月経開始日前30日以内または妊娠第1期にワクチンを接種した1224人のうち905人について、20週までの追跡調査がまだ行われていなかったため、自然流産のリスク推定値を算出するための分母がありませんでした」と正しく述べています。さらに、どのようなリスク推定も、自然流産の妊娠週特異的なリスクを考慮する必要があります。" 表4はこの修正を反映して更新されました。しかし、この論文の
134
Sci, Pub Health Pol, & Law Spontaneous Abortions and Policy on COVID-19 mRNA Vaccines - Nov.2021
抄録、結果、考察では、20週以前にmRNAに曝露された人に観察された12.6%の自然流産率がバックグラウンドの範囲内であることなど、本研究の当初の知見が記載・考察されており、修正を考慮して更新されていません。このため、修正された結果の表と本文の間に不連続性が生じています。著者は、妊娠中のmRNA製品の使用に関する安全性のシグナルはないという声明を引き続き支持します。
3 その他の議論
Shimabukuro et al, は、妊娠中のCOVID-19病の罹患率と死亡率が増加すると報告されており、そのため、初期のワクチン試験から妊婦が除外されていたため、妊娠中のmRNAワクチンの広範な使用に関する現在の国際的な推奨を正当化するために使用されています。 [しかし、最近行われた2つの研究では、このようなリスクの増加は観察されませんでした[15,16]。むしろ、妊娠中の重症患者の入院率および死亡率は、同じコホートの一般人口のそれと同程度であることが観察されました[15]。また、妊娠中の女性の院内死亡率は、COVID-19およびウイルス性肺炎で入院した非妊娠患者よりも低かったのです[16]。
これらの疫学的知見の基礎となる生物学的経路が解明されました。研究者たちは,SARS-CoV-2が宿主細胞に侵入し,アンジオテンシン変換酵素2(ACE-2)受容体と,ヘプタッドリピートドメインであるHR1とHR2を用いたスパイク(S)タンパク質S2サブユニットを介して融合することを発見した。 [13,14] Pfizer/BioNTech社のBNT162b2ワクチンやModerna社のmRNA-1273ワクチンは、このスパイク(S)タンパク質をコードしており、ヒトの細胞内に送達されて翻訳されるように設計されています[19] SARS-CoV-2によって引き起こされる凝固障害は、ZhangらによってhACE-2コンピテントマウスで調べられ[20]、Grobbelaarらによってin vitroで調べられました[21] SARS-CoV-2のスパイク(S)タンパク質のhACE-2への結合は、SARS-CoV-2のスパイク(S)タンパク質とhACE-2のコンピテントマウスとの間で行われました。
(S)タンパク質のhACE-2コンピテントマウスへの結合が確認された。SARS-CoV-2とスパイク(S)タンパク質を投与すると、hACE-2トランスジェニックマウスにおいて、血小板が刺激されて凝固因子が放出され、炎症因子が分泌され、白血球と血小板の凝集体が形成された[20]。 生体内では、COVID-19患者のスパイク(S)タンパク質の循環が凝固亢進に寄与している。スパイク(S1)タンパク質のみの存在下では、全血の主要な超微細構造の変化(in vitroで指摘された血小板の過活性化)を通じて、健全な血流が阻害される可能性があるという知見が得られています[21]。
COVID-19に感染した妊婦42名のうち5名に子癇前症様症候群が認められ,重症肺炎を併発した前向き観察研究がある[22]。 mRNAワクチンにコード化されたスパイク(S)タンパク質とSARS-CoV-2ウイルスとの関係を考えると,ワクチン接種を受けた女性に子癇前症様症候群が発生する生物学的メカニズムがあると考えられる。
初期の臨床試験では妊娠中の女性が除外されていたため、mRNAワクチンが胎児や女性の生殖能力に与える影響について、動物実験(雌ラット)を用いて報告されました。ファイザー・バイオンテック社のラットを用いた研究では、曝露された動物やその仔の生殖能力に問題はないと報告されています。しかし、この研究をより詳細に検討した結果、着床前喪失率が約2倍(対照群4.09%に対し、9.77%)に増加したが、その結果は過去の対照データの範囲内(5.1~11.5%)であると報告された。さらに、胎児の胃捻転、口・顎の奇形、右側大動脈弓、頸椎の異常の発生率は低く、これも過去の対照データの範囲内であったと報告されています。この研究では、BNT162b2 mRNAの胎盤移行は評価されていない[23]。 同様に、Modernaの研究では、以下の研究において、妊娠、胚・胎児の発育、分娩、出生後の発育に有害な影響がないことが示されている。
135
Sci, Pub Health Pol, & Law 自然流産とCOVID-19 mRNAワクチンに関する政策 - Nov. 2021
ネズミで実施された研究[24]では、ネズミの研究と最初の臨床試験中に妊娠した人の情報が、臨床医によって、mRNA技術が有害である生物学的にもっともらしい理由がないという信念と合わせて、妊娠中および授乳中の安全性を保証するために信頼されていました[14]。
妊娠中や授乳中のmRNAワクチン接種の効果に対する懸念には、以下のような問題がありますが、これらに限定されるものではありません。
mRNAとスパイクタンパクの伝達
子宮内での発育や授乳中の乳児への影響が不明であることから、mRNAやスパイクタンパクが胎盤を越えて母乳を介して伝達されることが懸念されます。Mattarらが15人の妊婦と5人の授乳中の女性にファイザー・バイオンテック(BNT162B2)のmRNAワクチンを1回接種して実施した研究では、接種後0~7日目の水性または液体の母乳画分(n=5)にmRNAスパイクコード領域の増幅は検出されませんでした[25]。 ただし、スパイクタンパク自体の存在は検査されていません。この研究の著者は、サンプル数が少なく、研究期間が曝露後1週間しかないことを考慮して、注意を促しています。この研究とは対照的に、VAERSのような任意の報告システムには、血栓性血小板減少性紫斑病(TTP)、胃腸障害、発疹、アナフィラキシー反応、死亡などの報告が多数寄せられています(例えば、VAERS ID26: 例えば、VAERS ID26:1166062、927664、939409、954010、1166062、1224688、1254975、1272428、1343886、1395088、1415059、1445743、1031318、1113464、1182232)ワクチンを接種したばかりの母親の母乳に暴露した後に発生しています。
シンクチン-1の阻害
注射によって破壊される可能性のある他のメカニズムには、細胞融合および胎盤形成に不可欠なレトロウイルス由来の融合タンパク質であるシンキュティン-1(syn1)があります[27] mRNAにコード化されたスパイク(S)
タンパク質HR1(またはHR1a28)またはHR2が不用意にsyn1を阻害する能力を持ち、胎盤の付着に必要な細胞融合が妨げられ、その結果、妊娠が失われるかどうかを調べる必要があります。ファイザー社とモデナ社が実施した生殖能力や発育への影響を調べるためのげっ歯類の研究は、マカクのような旧世界の霊長類では、ヒトと同様のsyn1およびsyn2タンパク質を持っていますが、ラットでは持っていないので、繰り返し行う必要があるかもしれません。syn1に対する自己抗体の存在がMattarらによって調査され、Syn1に対する自己抗体のベースラインからの変化がファイザー・バイオンテック製品の初回投与に曝された15人の妊婦すべてに生じたが、その変化は生物学的に有意とみなされるほど高くないと判断された[25]。 サンプルサイズが小さいことから、これらの知見はさらなる調査が必要であることを示しているのかもしれない。さらに、観察研究において、SYN1の発現変化は、子癇前症、溶血、肝酵素の上昇および血小板低下症候群、子宮内発育制限および妊娠糖尿病と関連している[29-31]。
Synctyin-1は、配偶子の融合にも必要であり(精子[32]および卵母細胞[33]に存在するsyn1およびACET2受容体)、さらに、精巣34および卵巣にも存在します[33,35] 食品医薬品局(FDA)に提出されたComirnaty(Pfizer/BioNTech mRNA vaccine) Package Insertにおいて、メーカーは、男性の生殖能力の潜在的な障害は評価されていないと述べています(15ページ)。 [36] mRNAワクチン接種前(2~7日間の禁欲後)と、2回目のワクチン接種後70日後に男性45名を対象に、mRNAワクチン接種が精子の数と運動性に与える影響について、単一施設での前向き研究が実施されました。精子パラメータへの有意な悪影響は報告されませんでした。しかし、この研究では、このコホートにおける融合性の可能性(syn1は精子頭部の先体にある)やsynctyin抗体レベルを評価しておらず、さらなる研究が推奨されています[37]。
136
Sci, Pub Health Pol, & Law 自然流産とCOVID-19 mRNAワクチンに関する政策-2021年11月号
4 結論
私たちは、ニュージーランドを含む多くの国際的なワクチン使用ガイドラインに急遽取り入れられた、妊娠初期のmRNAワクチンの使用を支持する島袋ら[4]の研究の結論に疑問を持っています[1]。 第3期コホートにおける曝露が、妊娠中の曝露の影響を代表するものであるという仮定には疑問があり、サリドマイドのような薬剤に関する過去の経験を無視しています[38]。 第1期および第2期に使用した場合の製品の安全性の証拠は、これらのコホートを少なくとも周産期まで追跡調査するか、または妊娠中に接種した母親から生まれた赤ちゃんの長期的な安全性を決定するまでは確立できません[38]。さらに、本製品の製造元であるファイザー社は、これらの保証に反して、次のように述べています。「妊婦に投与されたComirnatyに関する利用可能なデータは、妊娠中のワクチン関連のリスクを知らせるには不十分である」、「Comirnatyがヒトの母乳中に排泄されるかどうかは不明である」、「母乳で育った乳児に対するComirnatyの影響を評価するデータはない」(14ページ)と述べています[39]。
mRNAワクチンの展開の性質上、医療従事者は、本製品の安全性をさらに判断するために、妊娠中の問題を報告する必要があります。H1N1pdm09を含むインフルエンザワクチンへの曝露(2010-11年および2011-12年)と自然流産との間に関連性がある可能性が示されているように、妊娠中のワクチン投与には注意を払う必要があります。 [40] ここで提示された証拠を考慮して、我々は、妊娠中(カテゴリーX)[41]および授乳中の人へのmRNAワクチンの使用を直ちに中止することを提案します。また、これらのグループにおける不妊、妊娠、生殖への安全性と長期的な影響に関するより説得力のあるデータが確立されるまで、一般集団における子供または妊娠可能な年齢の人へのmRNAワクチンの使用も中止することを提案します。
5 エディターズノート
編集部注1:本報告書は、著者とは関係のない査読者によって査読された。このプロセスはシングルブラインドで行われました(著者は査読者が誰であるかを知りません)。
編集部注2:2021年6月24日、島袋博士は、米国のAdvisory Committee on Immunization Practices(ACIP)においても、Vaccine Safety Datalinkのデータを発表し、COVID-19ワクチンに起因すると思われる重篤な有害事象や死亡例をシステムが捉えていない(ゼロ)と結論付けました。2021年6月10日、島袋医師は、ワクチン・関連生物製剤諮問委員会(VRBPAC)に対し、VSDのデータを用いて心筋炎のリスクが増加しないことを報告しました。これらの発表の直後に、米国FDAはファイザー/ビオンテックのBnt162b2/Comirnatyワクチンによる心筋炎および心膜炎のリスクに関する勧告を発表しました。ACIPに提示された情報は、ワクチンの推奨を決定する上で重要なものでした。私は、本誌の最近の論説で「ファーマコビジランス」の不在と失敗を取り上げました。
6 編集部からの引用
島袋哲也 2021.COVID-19 ワクチンの安全性に関する最新情報。Vaccines and Related Biological Products Advisory Committee (VRBPAC). June 10, 2021. https://www.fda.gov/media/150054/download Accessed Oct.23, 2021.
島袋、T. 2021. COVID-19 ワクチンの安全性の更新 予防接種実施諮問委員会(ACIP)。https://www.cdc.gov/vaccines/acip/meetings/d ownloads/slides-2021-06/03-COVID- Shimabukuro-508.pdf Accessed Oct.23, 2021.
137
Sci, Pub Health Pol, & Law 自然流産とCOVID-19 mRNAワクチンに関する政策 - 2021年11月
7 著者の参考文献
1. The Immunisation Advisory Centre(予防接種諮問センター)。COVID-19教育。2021. COVID-19 vaccines in pregnancy and breastfeeding. https://covid.immune.org.nz/faq/covid-19- vaccines-pregnancy-and-breastfeeding Accessed Jul.31, 2021.
2. 米国疾病管理予防センター(CDC). 2021. COVID-19 Vaccines during pregnancy or breastfeeding. https://www.cdc.gov/coronavirus/2019- ncov/vaccines/recommendations/regnancy.ht ml Accessed Aug.3, 2021.
3. Australian Government Department of Health. 2021. COVID-19 vaccination decision guide for women who are pregnant, breastfeeding or planning pregnancy. https://www.health.gov.au/resources/publicatio ns/covid-19-vaccination-shared-decision-making-guide-for-women-who-are-pregnant-breastfeeding-or-planning-pregnancy Accessed Jul.31, 2021.
4. 島袋TT、Kim SY、Myers TR、他。2021年。妊娠中の人におけるmRNA Covid-19ワクチンの安全性に関する予備的知見。New England Journal of Medicine 384(24): 2273-82. https://www.nejm.org/doi/full/10.1056/nejmoa 2104983
5. McCullough PA, Bernstein I, Jovanovic S, McLeod D, Stricker RB. 2021年、7月30日。Lack of compelling safety data for mRNA COVID vaccines in pregnant women/ https://trialsitenews.com/lack-of-compelling- safety-data-for-mrna-covid-vaccines-in- pregnant-women/
6. Dugas C, Slane VH. 2021, Jun 29. Miscarriage(流産)。StatPearls。トレジャーアイランド(フロリダ州)。StatPearls出版。pmid: 30422585. https://www.ncbi.nlm.nih.gov/books/NBK5329 92/
7. Strumpf E, Lang A, Austin N, et al.2021. 流産の有病率と臨床的・社会的・医療的予測因子。BMC Pregnancy and Childbirth 21(1): 185. doi: 10.1186/s12884- 021-03682-z. https://bmcpregnancychildbirth.biomedcentral. com/articles/10.1186/s12884-021-03682-z
8. R Linnakaari, N Helle, Mentula, er al. 2019. Trends in the incidence, rate and treatment of miscarriage-nationwide register-study in Finland, 1998-2016. Human Reproduction 34(11): 2120-8. https://academic.oup.com/humrep/article/34/11 /2120/5611272
9. Zdanowski W, Waśniewski T. 2021. ポーランドの医療従事者における妊娠中のCOVID-19ワクチン接種後の臍帯血中のSARS-CoV-2スパイクタンパク抗体価の評価。予備的な結果。Vaccines 9(6): 675. doi: 10.3390/vaccines9060675. https://www.mdpi.com/2076-393X/9/6/675
10. U.S. Department of Health and Human Services. 2010. https://evs.nci.nih.gov/ftp1/CTCAE/CTCAE_4 .03/CTCAE_4.03_2010-06-14_QuickReference_8.5x11.pdf Accessed Jul.31, 2021.
11. Kadali RA, Janagama R, Peruru SR, et al.2021. 妊娠中の女性におけるCOVID-19メッセンジャーRNAワクチンの副作用。詳細な自己申告の症状を持つ医療従事者を対象としたクロスセクション研究。American Journal of Obstetrics and Gynecology 225(4): 458-460. doi: 10.1016/j.ajog.2021.06.007. https://www.ncbi.nlm.nih.gov/pmc/articles/PM C8189739/
12.Peretz SB, Regev N, Novick L, et al.2021. BNT162b2 mRNA COVID-19を接種した妊婦の短期成績
138
Sci, Pub Health Pol, & Law 自然流産とCOVID-19 mRNAワクチンに関する政策 - 2021年11月
ワクチンを使用しています。Ultrasound in Obstetrics & Gynecology 58(3): 450-456. doi: 10.1002/uog.23729. https://obgyn.onlinelibrary.wiley.com/doi/10.1 002/uog.23729
13.島袋TT、金SY、マイヤーズTR、他 2021年、10月14日。妊娠者におけるmRNA Covid-19ワクチンの安全性に関する予備的知見。訂正版です。ニューイングランド・ジャーナル・オブ・メディシン 384(24): 2273-82. https://www.nejm.org/doi/full/10.1056/NEJMx 210016
14. Riley LE. 2021年。妊娠中の女性におけるmRNA Covid-19ワクチンの安全性。ニューイングランド・ジャーナル・オブ・メディシン 384(24): 2342-2343. doi: 10.1056/ NEJMe2107070. https://www.nejm.org/doi/full/10.1056/nejme2 107070
Erratum in: New England Journal of Medicine 385(16): 1536. doi: 10.1056/NEJMx210017. https://www.nejm.org/doi/10.1056/NEJMx210 017
15. Knight M, Bunch K, V ousden N, Morris E, Simpson N, Gale C, O'Brien P, Quigley M, Brocklehurst P, Kurinczuk JJ; UK Obstetric Surveillance System SARS-CoV-2 Infection in Pregnancy Collaborative Group(英国産科サーベイランスシステムSARS-CoV-2感染症共同グループ)。2020. 英国でSARS-CoV-2感染が確認されて入院した妊婦の特徴と転帰。National population-based cohort study. BMJ 369: m2107. doi: 10.1136/bmj.m2107. https://www.bmj.com/content/369/bmj.m2107
16.Pineles BL, Goodman KE, Pineles L, O'Hara LM, Nadimpalli G, Magder LS, Baghdadi JD, Parchem JG, Harris AD. 2021. COVID-19による入院中の妊娠中および非妊娠中の患者のコホートにおける院内死亡率。Annals of Internal Medicine 174(8): 1186-1188. doi: 10.7326/M21-0974. https://www.acpjournals.org/doi/10.7326/M21- 0974
17.Xia S, Zhu Y, Liu M.ら、2020年。2019-nCoVの融合メカニズムとスパイクタンパク質のHR1ドメインを標的とした融合阻害剤. Cellular & Molecular Immunology 17: 765-7.
18.
doi: 10.1038/s41423-020-0374-2
https://www.nature.com/articles/s41423-020- 0374-2
Xia X. 2021. SARS-Cov-2のスパイクタンパク質のドメインと機能について、ワクチンデザインの観点から考察する。Viruses 13(1): 109.
doi: 10.3390/v13010109. https://www.mdpi.com/1999-4915/13/1/109
19.Lokossou AG, Toudic C, Barbeau B. 2014. Implication of human endogenous retrovirus envelope proteins in placental functions. Viruses 6(11): 4609-27.
20.
doi: 10.3390/v6114609.
https://www.mdpi.com/1999-4915/6/11/4609
20. Zhang S, Liu Y, Wang X, Yang L, Li H, Wang Y, Liu M, Zhao X, Xie Y, Yang Y, Zhang S, Fan Z, Dong J, Yuan Z, Ding Z, Zhang Y, Hu L. 2020. SARS-CoV-2は血小板のACE2と結合し、COVID-19の血栓症を増強する。Journal of Hematology & Oncology 13(1):120.
doi: 10.1186/s13045-020-00954-7.
https://jhoonline.biomedcentral.com/articles/10 .1186/s13045-020-00954-7
Grobbelaar LM, Venter C, Vlok M, Ngoepe M, Laubscher GJ, Lourens PJ, Steenkamp J, Kell DB, Pretorius E. 2021. SARS-CoV-2のスパイクタンパク質S1は、線溶に抵抗性のあるフィブリン(オゲン)を誘導する。COVID-19におけるミクロクロット形成への影響。Bioscience Reports 41(8): BSR20210611.
doi: 10.1042/BSR20210611.
https://pubmed.ncbi.nlm.nih.gov/34328172/
Mendoza M, Garcia-Ruiz I, Maiz N, Rodo C, Garcia-Manau P, Serrano B, Lopez-Martinez RM, Balcells J, Fernandez-Hidalgo N, Carreras E, Suy A. 2020. 前置血栓症様症候群
21.
22.
139
Sci, Pub Health Pol, & Law 自然流産とCOVID-19 mRNAワクチンに関する政策 - 2021年11月
重度のCOVID-19によって誘発される。前向きな観察研究である。BJOG 127(11):1374-1380. doi: 10.1111/1471-0528.16339. https://obgyn.onlinelibrary.wiley.com/doi/10.1 111/1471-0528.16339
23.欧州医薬品庁(European Medicines Agency)。2021年、2月19日。アセスメントレポート: Comirnaty. https://www.ema.europa.eu/en/documents/asse ssment-report/comirnaty-epar-public-assessment-report_ja.pdf
24. European Medicines Agency. 2021, Mar.1. EU Risk Management Plan for COVID-19 mRNA vaccine Moderna. https://www.ema.europa.eu/en/documents/rmp -summary/spikevax-previously-covid-19-vaccine-moderna-epar-risk-management-plan_ja.pdf
25.Mattar CNZ, Koh W, Seow Y, et al. 2021. BNT162B2 COVID-19 mRNAワクチン接種後の抗シンサイチン抗体レベル、および妊孕性と母乳育児の懸念への対応。 medRxiv preprint: 2021, May 25.
doi: 10.1101/2021.05.23.21257686.
https://www.medrxiv.org/content/10.1101/202 1.05.23.21257686v1
26.国立ワクチン情報センター. 2021. VAERSデータベースの検索。https://medalerts.org/vaersdb/
27.Guo L, Gu F, Xu Y, Zhou C. 2020, Nov.17. 妊娠外胚葉におけるsyncytin-1のコピー数の増加は、胚盤胞の着床と関連する。PeerJ Life & Environment 8: e10368. doi: 10.7717/peerj.10368. https://peerj.com/articles/10368/
28. Gallaher B. 2020, Feb. Response to nCov2019 against backdrop of endogenous retroviruses. https://virological.org/t/response-to-ncov2019- against-backdrop-of-endogenous- retroviruses/396 Accessed Aug.3, 2021.
29. Langbein M, Strick R, Strissel PL, et al. 2008. Impaired cytotrophoblast cell-cell fusion is associated with the reduced Syncytin and increased apoptosis in patients with placental dysfunction(胎盤機能不全患者における細胞芽細胞の融合障害はSyncytinの減少およびアポトーシスの増加と関連する)。Molecular Reproduction & Development 75(1): 175-83. doi: 10.1002/mrd.20729. https://onlinelibrary.wiley.com/doi/10.1002/mr d.20729
30.Lokossou AG, Toudic C, Barbeau B.2014. Implication of human endogenous retrovirus envelope proteins in placental functions. Viruses 6(11): 4609-27.
doi: 10.3390/v6114609.
https://www.mdpi.com/1999-4915/6/11/4609
31.Soygur B, Sati L, Demir R. 2016. Altered expression of human endogenous retrovirus syncytin-1, syncytin-2 and their receptors in human normal and gestational diabetic placenta(ヒト正常および妊娠糖尿病胎盤におけるヒト内因性レトロウイルスsyncytin-1, syncytin-2およびその受容体の変化)。Histology and Histopathology 31(9): 1037-47. doi: 10.14670/HH-11-735. https://pubmed.ncbi.nlm.nih.gov/26875564/
32.
33.
Köhn FM, Müller C, Drescher D, et al. 1998. アンジオテンシン変換酵素(ACE)およびアンジオテンシンのヒト精子機能への影響。Andrologia 30(4-5): 207-15.
doi: 10.1111/j.1439-0272.1998.tb01162.x.
https://onlinelibrary.wiley.com/doi/10.1111/j.1 439-0272.1998.tb01162.x
Rajput SK, Logsdon DM, Kile B, et al.2021. ヒトの卵・接合体・胚は、重症急性呼吸器症候群コロナウイルス2の感染に必要な受容体アンジオテンシン1変換酵素2と膜貫通型セリンプロテアーゼ2タンパク質を発現している。F&S Science 2(1): 33- 42. doi: 10.1016/j.xfss.2020.12.005. https://www.sciencedirect.com/science/article/ pii/S2666335X20300616
34. Verma S, Saksena S, Sadri-ArdeKani H. 2020. 精巣におけるACE2受容体の発現:コロナウイルス感染症における意義 2019年
140
Sci, Pub Health Pol, & Law 自然流産とCOVID-19 mRNAワクチンに関する政策 - 2021年11月
病因を明らかにする。生殖の生物学 103(3): 449-51. doi: 10.1093/biolre/ioaa08 https://academic.oup.com/biolreprod/article/ 103/3/449/5840520
35.Virant-Klun I, Strle F. 2021. ヒト卵母細胞はACE2とBSGの両方の遺伝子と対応するタンパク質を発現している:SARS-CoV-2の感染は可能か?Stem Cell Reviews and Reports 17(1): 278-84. doi: 10.1007/s12015- 020-10101-x. https://link.springer.com/article/10.1007%2Fs1 2015-020-10101-x
36.米国食品医薬品局(Food and Drug Administration)。2021, Aug. Package insert - Comirnaty. https://www.fda.gov/media/151707/download Accessed Aug.31, 2021.
37. Gonzalez DC, Nassau DE, Khodamoradi K, et al. 2021. COVID-19 mRNAワクチン接種前後の精子のパラメータ。JAMA 326(3):273-274. doi: 10.1001/jama.2021.9976. https://jamanetwork.com/journals/jama/fullarti cle/2781360
38. Vargesson N. 2015. サリドマイドによる催奇形性:歴史とメカニズム。Birth Defects Research (Part C) 105(2): 140-56. doi: 10.1002/bdrc.21096. https://onlinelibrary.wiley.com/doi/full/10.100 2/bdrc.21096
39. Pfizer. 2021年、8月23日。Pfizer-BioNTech COVID- 19 ワクチン COMIRNATY® が 16 歳以上の個人を対象に米国 FDA の完全承認を取得。
https://www.pfizer.com/news/press- release/press-release-detail/pfizer-biontech- covid-19-vaccine-comirnatyr-receives-full Accessed Sep.5, 2021.
40. Donahue JG, Kieke BA, King JP, DeStefano F, Mascola MA, Irving SA, Cheetham TC, Glanz JM, Jackson LA, Klein NP, Naleway AL, Weintraub E, Belongia EA. 2017. 自然流産と、2010-11年および2011-12年のH1N1pdm09を含む不活化インフルエンザワクチンの接種を受けたこととの関連。Vaccine 35(40):5314-5322.
doi: 10.1016/j.vaccine.2017.06.069.
https://www.sciencedirect.com/science/article/ pii/S0264410X17308666?via%3Dihub
41. New Zealand Medicines and Medical Devices Safety Authority (MEDSAFE). 2013, Jun. 6. 妊娠中の医薬品と使用。https://medsafe.govt.nz/profs/PUArticles/June2 013MedsInPregnancy.htm Accessed Aug. 5, 2021.
141
Sci, Pub Health Pol, & Law 自然流産と COVID-19 mRNA ワクチンに関する政策 - 2021 年 11 月
8
補足表
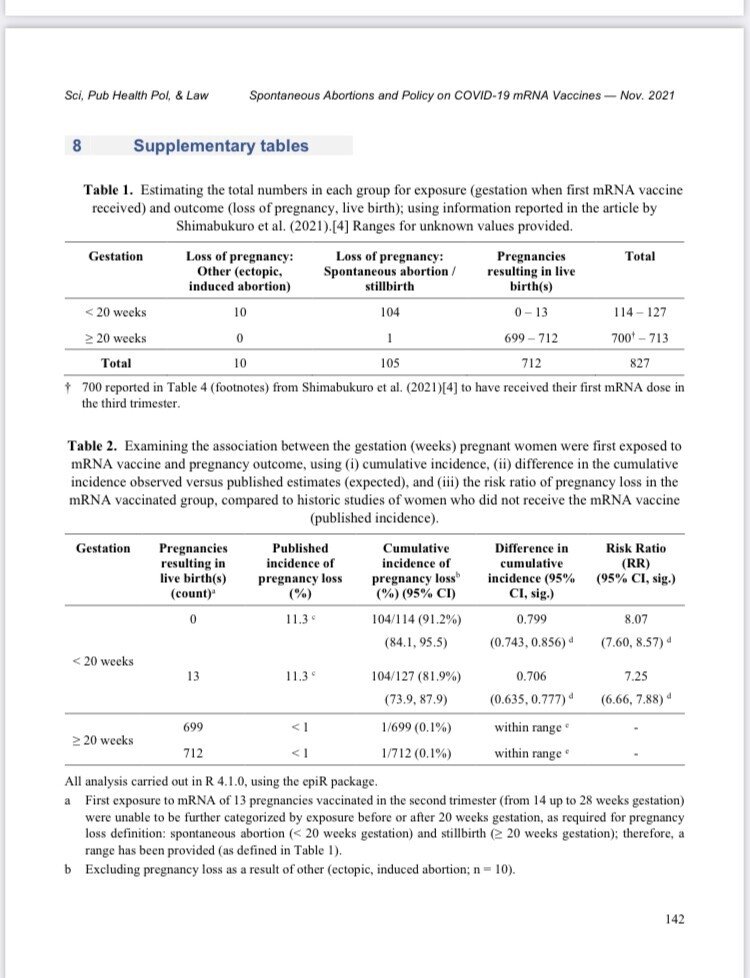
表 1. 曝露(最初にmRNAワクチンを接種した時の妊娠期間)と転帰(妊娠喪失、生児)について、各群の総数を推定する。
島袋ら(2021)の論文で報告された情報を用いて、各群の総数を推定した[4]。 不明な値については範囲を示した。
妊娠期間
< 20週 ≧ 20週 合計
妊娠の喪失 その他(子宮外妊娠、人工妊娠中絶)
10 0 10
妊娠の喪失。自然流産/死産
104 1 105
生児を出産した妊娠
0 - 13 699 - 712 712
712 712 合計
114 - 127 700† - 713 827
†
Shimabukuroら(2021)[4]の表4(脚注)に報告されている700人は、第3期に最初のmRNA投与を受けている。
表2. 妊婦がmRNAワクチンに初めて曝露された妊娠期間(週)と妊娠転帰との関連を、(i)累積罹患率、(ii)公表された推定値に対する観察された累積罹患率の差(期待値)、(iii)mRNAワクチンを接種しなかった女性の歴史的研究(公表された罹患率)と比較したmRNAワクチン接種群の妊娠減少のリスク比を用いて検討した。
妊娠期間
< 20週未満
≥ 20週以上
生児を出産した妊娠(数)a
0
13
699
712
妊娠損失の公表された発生率(%)
11.3 c 11.3 c
< 1
< 1
累積
妊娠損失の発生率b (%) (95% CI)
104/114 (91.2%) (84.1, 95.5)
104/127 (81.9%) (73.9, 87.9)
1/699 (0.1%) 1/712 (0.1%)
累積罹患率の差(95%CI、sig.)
0.799 (0.743, 0.856) d
0.706 (0.635, 0.777) d
範囲内 e 範囲内 e
リスク比(RR)(95%CI、sig.)
8.07 (7.60, 8.57) d
7.25 (6.66, 7.88) d
- -
すべての解析は,R 4.1.0で,epiRパッケージを用いて行った。
a 妊娠第2期(妊娠14週から28週まで)にワクチンを接種した13人の妊娠者のmRNAへの初回曝露量
は、妊娠損失の定義(自然流産(妊娠20週未満)および死産(妊娠20週以上))に必要な、妊娠20週以前または以後の曝露によってさらに分類することができなかったため、範囲が示されている(表1に定義されている)。
b その他(子宮外妊娠、人工妊娠中絶、n=10)による妊娠喪失を除く。
142
自然流産と COVID-19 mRNA ワクチンに関する政策 - 2021 年 11 月
c カナダのマニトバ州で実施されたn=79,978人の女性を対象とした研究に基づき、臨床的に認められた自然流産のベースラインを11.3%に設定した[7]。
d 妊娠20週未満にmRNAを投与した場合に観察された妊娠喪失(observed)と、公表されている発生率(expected)との間に、統計的に有意な関係(sig.<0.001)があることを示す。
e 700人が最初のmRNA投与を妊娠第3期に受けたが、曝露後の出産までの期間については示されていない。
143












この記事が気に入ったらサポートをしてみませんか?
