
週刊レキデンス ~第18回~ スタチンの開発
「SGLT-2i が令和のスタチンとなるか」と言われて久しいですが、さてスタチンのインパクトたるものは一体どういうものなのでしょうか? 一体なぜスタチンはこの世にインパクトを与えた薬剤となったのでしょうか?その謎を探るべくまずは開発経緯から見ていきましょう!!
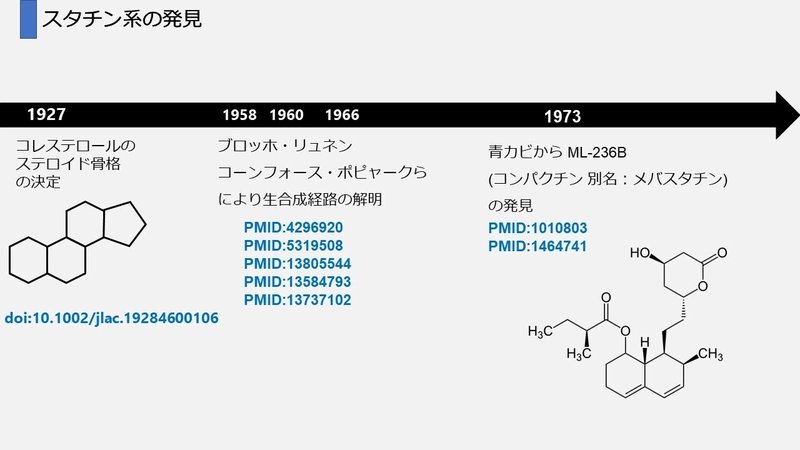
スタチン系の発見
スタチン系の一番初めに開発(正しくは発見)されたのは、「コンパクチン 別名メバスタチン」、 発見したのは遠藤章(1933年11月14日 -)です。
遠藤は三共(現 第一三共)で、1973 年青カビの培養液からコレステロール合成阻害剤 ML-236B(コンパクチン)を発見しました。
彼がコレステロール関連薬の開発を行った背景には、1966年当時留学していた米国の死亡原因第1位だった心血管疾患が大きく関わっていたようです。
もちろん当時は心血管イベントの真骨頂とも言える高血圧の治療もまだ発展途上でした。高血圧によって死亡率が高まることを人類が認識したのは、フラミングガム研究以降です。(1)(2)
ステロイド骨格の決定
そのフラミンガム研究の結果が発表されるずいぶん前の事、オットー・パウル・ヘルマン・ディールス(Otto Paul Hermann Diels、1876年1月23日 - 1954年3月7日)はコレステロールのステロイド骨格が 6-6-6-5環で構成されていることを決定づけました。 オットーは、あの Diels–Alder 反応を発表した人物です。この反応を用いて炭化水素をセレンにより脱水素させ、炭化水素C18H16を導きステロイド骨格を決定づけしたのです。(3)
コレステロール生合成経路の解明
コレステロールの生合成に関しては、主に次の 4 名 コンラート・エミル・ブロッホ(Konrad E. Bloch.1912年1月21日–2000年10月15日),フェオドル・フェリックス・コンラド・リュネン(Feodor Felix Konrad Lynen, 1911年4月6日 - 1979年8月6日), ジョン・コーンフォース(John Cornforth.1917年9月7日–2013年12月8日), ジョージ・ポピャーク(George Popják.1914年5月5日-1998年12月30日) の功績によって解明され(4)、1964 年にブロッホとリュネンはノーベル生理学・医学賞を受賞しています。
つまり、遠藤の研究当時既に HMG-CoA 還元酵素の存在は明らかになっており、そこで彼はこの酵素をターゲットにしたのです。(5)(6)(7)(8)(9)
HMG-CoA還元酵素のへ理由
彼が酵素をターゲットにした理由がもう2つあります。それにはフレミングに対する憧れと彼のそれまでの研究背景です。幼少期にフレミングの伝記を読み創薬による社会貢献への気づきと、大学卒業後に三共へ入社した後、果汁とワインのペクチンを分解する菌類のペクチナーゼの研究を行い、学位を取得しています。 つまり酵素への研究は自然な入り口だったのかもしれません。(10)
この様な背景から、フレミングと同様に、1973 年 7 月 青カビ(Penisillium citrinum pen-51)から ML-236B (コンパクチン 別名:メバスタチン)を発見しました。これが後のスタチン系と呼ばれるHMG-CoA還元酵素阻害薬の第 1 号です。(11)(12)
コンパクチン(メバスタチン)の運命はいかに
そこからのコンパクチンの運命は波乱万丈です。
①コンパクチンを健常ラットに投与しても血中コレステロールが低下しない。
②英国もコンパクチンを発見するが、ラットに効かないため中止。
③諦めずに研究を続けると、ニワトリ、イヌ、サルに投与でコレステロールが下がる。
④肝毒性の疑いが出現、再び中止の危機に
⑤家族性高コレステロール血症ホモ接合体を除く患者に投与でコレステロール低下
⑥イヌの長期毒性試験で発がん性が見つかる、再々中止の危機に
⑦メルクはコンパクチン開発中止し、1987年ロバスタチンの開発
三共はコンパクチン開発中止し、プラバスタチンを開発
(13)
結局、遠藤が発見したコンパクチンは商業化までは辿り着きませんでしたが、後のスタチン系開発に大きな一手を示したのです。
参考
1. DAWBER TR,et al.Am J Public Health Nations Health. 1959 Oct;49(10):1349-56.PMID:13814552
2. Kannel WB,et al.Dis Chest.1969 Jul;56(1):43-52.PMID:5789839.
3. Diels O., Alder K. Synthesen in der hydroaromatischen Reihe. Liebigs Ann. Chem. 1928;460:98–122. doi: 10.1002/jlac.19284600106.
4. Endo A.Proc Jpn Acad Ser B Phys Biol Sci. 2010;86(5):484-93.PMID:20467214
5. Lynen F.Wien Klin Wochenschr.1966 Jul 8;78(27):489-97. German.PMID:4296920.
6. Bloch K.Science. 1965 Oct 1;150(3692):19-28.PMID:5319508
7. BUCHER NL,et al.Biochim Biophys Acta. 1960 Jun 3;40:491-501.PMID:13805544.
8. CORNFORTH JW,et al.Br Med Bull. 1958 Sep;14(3):221-6.PMID:13584793
9. POPJAK G,et al.Adv Enzymol Relat Subj Biochem. 1960;22:281-335.PMID:13737102
10. https://www.igaku-shoin.co.jp/paper/archive/y2014/PA03080_01
11. Endo A, J Antibiot (Tokyo). 1976 Dec;29(12):1346-8.PMID:1010803
12. Endo A.J Lipid Res. 1992 Nov;33(11):1569-82. PMID:1464741
13. 遠藤章 日農医誌 64巻6号 958-965 2016.3 https://doi.org/10.2185/jjrm.64.958
この記事が気に入ったらサポートをしてみませんか?
