エタノール(CH₃CH₂OH)
「この世には2種類の○○しかいない。●●か、●●以外か。」という言い回しがあります。アルコールにもこの言い回しを当てはめると、「この世には2種類のアルコールしかいない。飲めるアルコールか、飲めるアルコール以外か。」ということになるのかもしれません。
一般的にアルコールといえばエタノール(CH₃CH₂OH, 図1)や、それが含まれる酒類のことを指しますが、化学でのアルコールはヒドロキシ基(-OH)を持つ有機化合物のことを指します。

よって、メタノール(CH₃OH, 図2左)やイソプロピルアルコール((CH₃)₂CHOH, 図2右)などの俗に言う工業用アルコール¹⁾もアルコールの仲間になりますが、これらを飲んではいけません。最悪の場合、命を落としてしまいます。“飲めないアルコール”であるこれらをエタノールに混ぜて飲用不可にしたものを変性アルコールと呼び、変性アルコールは工業用に購入したエタノールを酒類などへ使用する不正を防止するための手段の1つです。前置きが長くなりましたが、今回は“飲めるアルコール”²⁾であるエタノールについて紹介したいと思います。

エタノールの製造方法には大きく分けて2種類³⁾あり、製造方法によって使用用途が異なります。石油由来のエチレンから合成されたエタノールは化学工業用、植物由来のデンプンや糖を発酵させて製造されたものは飲用をはじめとした種々の用途に用いられます¹⁾。さらに前者の方法は、硫酸を用いた間接水和法と、触媒を用いてエチレンに直接水を反応させる直接水和法の2種類⁴⁾に分けられます。
間接水和法を式1に示しました。式1だけ見ると、エチレンに酸を作用させてカルボカチオンを発生させたところに水を付加するという反応機構が思い浮かぶかもしれません。しかし、実際は多段階反応であり、間接水和法はエチレンに硫酸を付加させることで硫酸エステルを形成した後、それを加水分解する方法になります。
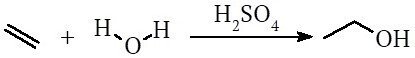
それぞれの素反応の考えられる反応機構を式2-式4に示しました。式2はエチレンかが硫酸からの水素イオン(プロトン, H⁺)によりカルボカチオン(C+)を発生する機構を示したものです。多くの化学反応は、電子豊富な部分から電子が欠乏する部分へ矢印を引き、電子の流れを示すことで機構を表すことができます。

カルボカチオンは正の電荷を持つため電子不足であり電子豊富な試薬(求核試薬)から攻撃を受けます。この場合は硫酸が求核試薬として働きます(式3)。こうしてエチレンと硫酸が反応して中間体の硫酸エステルが生成します。

続いて、硫酸存在下なので硫酸エステルが水素イオンで活性化され、硫黄原子上で酸による求核アシル置換反応に類似する反応が起こります。これにより、硫酸エステルが加水分解することで、エタノールが生成し、硫酸が再生すると考えられます。
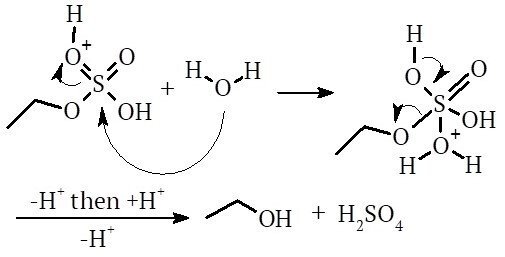
この手法には、入手が容易で安価な硫酸を用いて反応を進行することでエタノールが得られるメリットがあると考えられます。
一方で、間接水和法は触媒を用いて直接エチレンに水を付加する手法です(式5)。リン酸をシリカゲルに担持した触媒⁵⁾が用いられています。間接水和法は強酸である硫酸を用いないため、生産設備の腐食などの問題が軽減されるというメリットがあると考えられます。この手法では、間接水和法と同様の式2に示したカルボカチオン中間体が発生し、そこに水が付加してエタノールが生成する機構が考えられます。

次に、糖(グルコース)からの発酵による酵素分解からエタノールを合成する手法を紹介します(式6)⁶⁾。実際は多段階反応ですが、素反応の詳細を省略してまとめると以下のようになり、1分子のグルコースから2分子のエタノールと2分子の二酸化炭素が生成します。

ところで、酒屋でアルコール度数96%のお酒が売られていることがあります。なぜ96%で100%ではないのでしょうか?「どうせなら100%を目指せばよいのに…」と思ったことがある方もおられるかもしれません。それは、高度数のアルコールを蒸留して精製する際に、水とエタノールが一緒に蒸気として出てきてしまうからです(詳しくは“共沸”で調べてみてください。)。決してメーカーが残りの4%分のアルコール分を出し惜しんでいるわけではありません。96%以上のさらに純度が高いエタノールを得るためには、脱水剤(酸化カルシウム, いわゆる消石灰(CaO))と加熱撹拌して水分の大部分を取り除いた後、残った微量の水分をさらに金属カルシウム(Ca)などの強力な脱水剤で取り除くか、ベンゼンなどを混合して再び蒸留し、それら(水とベンゼンの共沸混合物)と共に水分を取り除く方法があります⁷⁾。
エタノールの使用は多岐にわたっているため、代表的な事柄だけを挙げました。身近に存在する物質ですが少しでも化学に興味を持ってもらえれば嬉しいです。
【参考文献と注釈】
1) 一般的にはメタノールやイソプロピルアルコールも工業用アルコールに含めるかもしれませんが、アルコール事業法の区分によると工業用アルコールとは90度以上の濃度のエタノールのことを指します。アルコール事業法についての詳細は以下のサイトをご覧ください。
化研テック株式会社, 工業用アルコールとは ~ アルコールとエタノール②, https://www.kaken-tech.co.jp/trouble/alcohol_ethanol-2/ (2023年12月15日閲覧)
2) 化学でのアルコールの定義に沿うのであれば、他にも飲食物に使用可能なアルコールはあります。代表例を挙げるならば、食品添加物として使用されているグリセリンや、糖類であるグルコース(ブドウ糖)やスクロース(砂糖の主成分)は分子内にヒドロキシ基を含むためアルコールの1種と言えます。
3) 石油由来のエチレンから製造するか植物由来のデンプンや糖から発酵を用いて製造するかで分けているのを見ると“化学的に合成されたもの”と”天然由来で合成をしていないもの”で分けたくなるかもしれませんが、それは正しくありません。発酵も細菌や酵母などの微生物を利用した化学反応だからです。また、微生物だけでなく植物も化学反応を利用して生命の維持や成分の合成を行っており、それを人間が利用しているのです。
4) 日本合成アルコール株式会社, 製造方法概要 | 日本合成アルコール株式会社, https://www.j-s-a.co.jp/pro/outline.html (2023年12月16日閲覧)
5) 日本合成アルコール株式会社, 製造方法概要 | 日本合成アルコール株式会社, https://www.j-s-a.co.jp/pro/outline1.html (2023年12月16日閲覧)
6) Try IT, 【高校生物】「アルコール発酵」 | 映像授業のTry IT (トライイット), https://www.try-it.jp/chapters-15009/sections-15053/lessons-15081/point-2/ (2023年12月16日閲覧)
7) 長倉三郎ら 編, 岩波 理化学辞典 第5版, 岩波書店, 2005年, エチルアルコール(電子辞書版)
