
中2理科の化学反応式を【理解】する(12) 化学変化と熱の出入り その2
この記事は前回の続きです。
前回のおはなし
まとめページ↓
温度と濃度の関係
さて,今もし中学生にわかるように熱と温度の違いを説明するとしたら,どうしたらよいだろう?教科書には載っていません。検索にも頼らず,中学生の立場に立って自分の頭だけを使ってなんとか考えてみよう。
熱と温度の性質には,次のような違いがあります。今,コップに入った50℃のお湯100 gが2個あったとします。二つを混ぜると200 gのお湯ができますが,温度は50℃のままですね。質量は足すことができるのですが,温度は足し算できないのです。

では熱はどうでしょうか?200 gのお湯を室温から50℃にするのに必要な熱は,100 gのお湯を室温から50℃にするのに必要な熱の2倍になります。風呂を沸かす時,水の量が2倍になると電気代も2倍になりますからね。
熱は足すことができる。温度は足し算できない。これをもっと理解するために,似た例がもう一つ思い当たります。それは果汁入りジュースの量と濃度の話です。
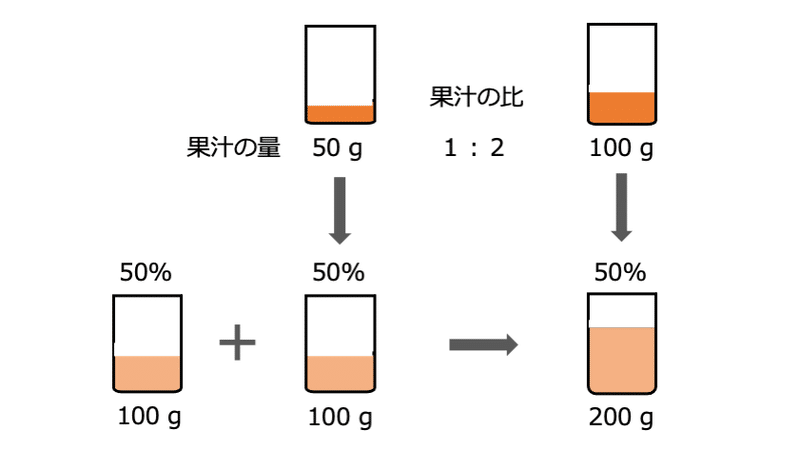
今,果汁50%のオレンジジュースが100 gあるとします。この50%というのは質量%濃度と呼ばれるもので,中1理科で学びます。果汁50%とは,ジュース100 gの中に果汁50 gが溶けている,という意味です。
もし,このジュース2本を混ぜたらどうなるでしょうか?ジュースの量は2倍,溶けている果汁の量も2倍になりますが,濃度は50%のままでしょう。温度と濃度はよく似ていると思いませんか。
ここまで考えると,熱とは何か流体のようなものであり,物質の中の熱の「濃さ」のようなものが温度である,というイメージが出てきます。
熱は物質か? ー熱素(カロリック)説ー
18世紀に酸化還元反応を酸素を使って説明したラヴォアジェも,熱とは何らかの物質からなる元素(熱素,カロリック)であると考えました。これを熱素説と言います。それでは,熱素説を他のいくつかの変化でもつじつまが合うかどうか,試してみましょう。
小4「すがたを変える水」で,水を熱すると水蒸気に変わると学びました。状態変化でも,水が熱素と結びつくことで状態が変化したと考えることができそうです。
氷(固体) + 熱素 → 水(液体)
水(液体) + 熱素 → 水蒸気(気体)
そうすると,酸素も熱素を含んでいるために気体でいられることになります。
酸素(固体) + 熱素 → 酸素(気体)
一方,これまで検討してきた酸化反応はどう説明されるでしょうか。金属酸化物とは金属に酸素が結びついたものですから,以下の式で表現されます。
金属 + 酸素(固体) → 金属酸化物
金属酸化物には熱素が含まれていないので,固体のままでいられるわけです。そこで、酸化反応の反応式は以下のようになります。
【酸化】 金属 + 酸素(気体) → 金属酸化物 + 熱素 (発熱)
酸素が持っていた熱素が物質の外に出ることで,金属酸化物の中に酸素がギュッと凝縮される。化学変化と状態変化を同時に説明できています。なんだか,最近高校化学で廃止された熱化学方程式の原型を見ているようですね。
しかし,以上の話は現代の理科の教科書には全く載っていません。なぜでしょうか?
熱素説は否定されている
もし熱素が何らかの元素であるとすると,熱素は元素記号で表され,対応する原子が想定できるはずです。しかし水をいくら温めても(つまり,水に熱素をいくら注入しても)質量の変化はありません。
そうすると熱素は質量ゼロであると考える他ありません。もし原子論的な見方で考えようとすると,熱素の原子も質量ゼロになります。質量のない原子は,その存在を天秤を使った実験で証明することができず,単なる想像上の存在になってしまいます。
それでも熱素の存在を守りたいのであれば,熱素とは原子ではない「何か」と考えざるを得ません。熱素は質量を持たず,どのような物質にも浸透し,その物質の温度を上昇させます。このような,質量ゼロの仮想流体を不可秤流体と呼びます。
こうなると,「世界は原子と真空のみ」とする原子論的世界観は崩壊します。そういうわけで,熱素説は現代では否定されています。その結果,原子論的世界観を反映した化学反応式に,熱は含みません。
正式には,熱を仕事に変換する機械(エンジン)の研究によって,熱は物質ではなく,エネルギーの移動方法であることがはっきりしました。捨て去られた考え方である熱素説を現代の教科書に載せるわけにはいきません。
したがって,教科書にはさりげなく「熱が・・・」と書かれるだけで,その正体には決して言及しようとしない。そのように私には読めます。
先生や教科書は熱素説を公的に教えられない
ここまで考えて,私はこのあたりに小・中理科における「エネルギー」概念の起源がありそうだと思いました。つまり,理科におけるエネルギーの最初のイメージは,熱の感覚から得られる概念としての不可秤流体ではないかと思ったのです。
本当は,熱もエネルギーも実体はなく,最終的には粒子の運動として理解されますが,その途中段階で「熱は物質ではない」などという否定型の言葉を使って熱を定義するのは適切ではありません。
「ピンク色の象を想像しないでください」という言葉を聞いて,象を想像しない人などいません。私は,まず最初に熱を「質量のない仮想的な流体」であると想像しなければ,熱の理解はその先一歩も進めない,と思うのです。
電流によって発生する熱の量についても同じです。中2理科「電流とそのエネルギー」においては,以下の式を学びます。
電熱線から出る熱量[𝐽] = 電力[𝑊] × 時間[秒]
何のイメージもなく,式だけで意味を理解するのは難しくないですか?電力と熱量を,共にエネルギーという名の流体としてイメージして初めて,理解できるようになるのだと思います。
熱素説は教科書に載せることができない。先生も表立っては教えられない。そのようなジレンマの中で,結局中学生には数式の計算方法だけを教え,テストに出して終わりにせざるを得ない状況になってはいないでしょうか。
実体的な見方と量的な見方
小中の理科では様々な種類の「エネルギー」を扱いますが,それらは流れたり貯まったりするという,流体のような性質を持っています。小学校における電流も,電線の中を流れる流体としてイメージされますし,電球からは光が「流れ」出るように思えます。
炎が出す熱は,実は有機物の酸化反応から出たものであり,これも一種の流体として解釈されます。そして,もしもエネルギーが不生不滅の性質(保存性)を持つのであれば,熱エネルギーに変わる前に有機物の中に貯まっていた状態のエネルギーが思考によって想定されます。それを理科では化学エネルギーと呼んでいるのではないか。
そうすると,中学理科の段階では2種類の世界観が共存していることになります。一つは原子論的世界観であり,もう一つはエネルギー的世界観です。どちらも現実世界を解釈する,異なったものの見方です。
理科では原子論的世界観を「実体的な見方」,エネルギー的世界観を「量的な見方」と呼んで区別しているようなので,私独自の大袈裟な言い回しである「なんとか的世界観」は今後やめたほうがいいのかなと,今ちょっと迷っています。
いずれにせよ,この推測が当たっているかどうかは,もう少し教科書を読み進めていく中で明らかになっていくでしょう。ではまた。
次のお話し↓
参考書籍
この記事が気に入ったらサポートをしてみませんか?
