
NMRスペクトルによる有機化合物の構造解析入門②~NMRの原理~
はじめに
どうも、無名博士の墓です。
引き続き見てくださり大変ありがとうございます。
今回から本格的に解説をはじめていきますが、その前に前回のおさらいを。
~前回のおさらい~
NMRとはNuclear Magnetic Resonanceの略で日本語では核磁気共鳴といいます。核磁気共鳴とは、水素などの、特定の原子の原子核が持つ磁石のような性質に由来する現象です。

この核磁気共鳴現象を検出することで化合物の構造を調べる手法を核磁気共鳴分光法といい、一般にNMRといった場合核磁気共鳴分光法のことを指します。
核磁気共鳴現象が最初に観測されたのは今から80年程前であり、今では有機化合物だけではなく、高分子化合物の解析にも利用されるほか、医療現場ではMRIとして応用されています。
そしてここではNMRスペクトルによる有機化合物の構造解析法について解説していきます。
なお、溶液NMR法による低分子化合物の解析について解説する予定ですので、固体NMR法や高分子の解析を期待していた方がいましたらすみません。
以上が前回のおさらいです。
そして今回はNMRの原理について解説していきたいと思います。
NMRスペクトルを理解する上でもある程度原理を知ることは重要です。
一応原理が分からなくてもスペクトルを解析すること自体はできなくはないのですが、ある程度原理を分かっていた方が理解の助けになりますからね。
それでは初めて行きましょう。
取り敢えず実物を見てみよう
まず初めに、実際のNMRスペクトルを見てみましょう。

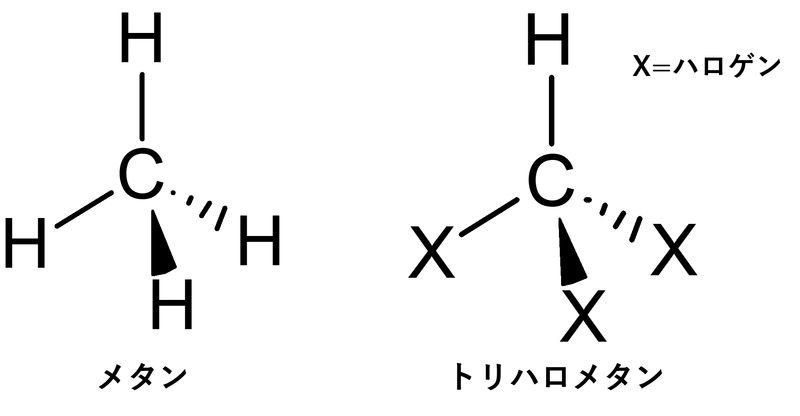
こちらはサスペンスでお馴染み(?)の化合物、クロロホルムの1H(プロトン) NMRスペクトルとなります。1H NMRとは、文字通り化合物中の軽水素(1H)を検出した1H NMRスペクトルになります。一本のピークが確認できますね。このピークがクロロホルムの構造式中にある1個の水素に由来しています。横軸の単位はppmです。右から左に向けて数値が大きくなります。このスペクトルにおいて、クロロホルム中の水素原子(1H、プロトン)はどうやら7.26 ppm付近にピークが出現するみたいですね。因みに、クロロホルムのように、メタン分子の4つの水素原子のうち3つがハロゲン元素で置換された化合物のことをトリハロメタンと総称します。
ここで同じトリハロメタンの仲間であり、塩素の代わりに臭素が結合したブロモホルムの1H NMRスペクトルも見てみましょう。

ピークの位置はだいたい6.8ppmくらいでしょうか。クロロホルムと比べると若干低い値ですね。ではヨウ素が3個結合したヨードホルムではどうでしょう。

4.9 ppmにピークがありますね。クロロホルムやブロロホルムと比べて随分値が小さいです。
ここでトリハロメタンの種類の違いとピーク位置の違いとの間にはどのような関係がありそうか考えてみましょう。周期表を見てみますと、どうやらピークの位置は各トリハロメタンに結合していたハロゲン元素の電気陰性度の強さと関係がありそうですね。

電気陰性度とはとある分子内のとある原子がどの程度電子を引っ張る力を持っているかを示したものです。周期表の右上に位置する元素ほど電気陰性度が強い傾向にあります(但し希ガスは除く)。従ってヨウ素、臭素、塩素の順に電気陰性度は強くなり、各トリハロメタンのNMRスペクトルのピーク位置の値は、結合しているハロゲンの電気陰性度の強さに比例して大きくなったように考えられますね。
それではこちらのスペクトルはどうでしょう。

こちらはベンゼンのスペクトルになります。水素が6個あるはずですがピークは1本だけですね。対称性の高い構造なのが関係しているのでしょうか。そしてピークの位置は7.33 ppmとクロロホルムよりも大きな値となっています。しかし、ベンゼンは水素と炭素のみからなる化合物で、いずれも電気陰性度は塩素よりも弱いはずです。電気陰性度だけを考えればクロロホルムよりもピーク位置の値は小さいものになると予想されます。ですが実際はそうなっていません。ベンゼンのような芳香族化合物にはNMRのピーク出現位置を左右する電気陰性度とは別の要因があるのでしょうか。
最後にこちら、クメンという化合物の1H NMRスペクトルを見てみましょう。

クメンはベンゼン環にイソプロピル基が結合した芳香族化合物になります。7ppm付近のピークはベンゼン環部分のプロトンに由来しますが、幅広でギザギザした形状になっていますね。1 ppm付近の2本のピークはメチル基のプロトン由来です。2.88 ppmにあるピラミッド状の多重線になったピークはメチンのプロトンに由来するのですが、このピークの形は何に由来するのでしょうか。また、それぞれのピークの強度というか大きさというかが、明らかに異なっていますよね。ベンゼン同様、炭素と水素のみでできた化合物にもかかわらず、各ピークの位置も非常にばらついており、やはり電気陰性度だけではピークの出現位置の説明が難しそうです。
とまあこんな感じで、NMRスペクトルのピークの位置や形状を決める要因が幾つか存在しそうであることは実感していただけましたでしょうか。
NMRスペクトルを特徴づける様々な要因について知り、その原理を理解すれば、解析がそこまで難解なものとは感じなくなるはずです。
ではここからはいよいよ本日の本題、NMRの原理についての解説に移りましょう。
NMRとは分光法の一つである
核磁気共鳴分光法(NMR)という名称からもわかる通り、NMRは分光法の一つです。
分光法とは、測定対象の物質が透過・吸収・散乱する”電磁波”を観測することで対象物質の定量や定性、構造解析を行う実験手法のことをいいます。したがって、まずはNMR(核磁気共鳴分光法)がどのような分光法なのかについて見ていきましょう。
分光法で用いられる「電磁波」とは、簡単に表現すると紫外線や赤外線などの目に見えない波長域も含めた”広義における光”のことです。少し厳密にいうと電場と磁場の振動(波)が空間を伝播していく物理現象のことをいいます。

電磁波はその波長の長さによっていくつかの種類に大別されます。

最も短い波長帯の電磁波はガンマ線やx線などで、一般に放射線と呼ばれる類のものになります。
そこからもう少し長い波長帯の電磁波は日焼けと殺菌でおなじみの紫外線と呼ばれるものであり、紫外線よりまた更に長い波長帯の電磁波は可視光、すなわち私たちが普段目にしている光になります。この紫外線~可視光にかけての波長域を利用し、特定の成分について定性・定量分析を行う分光法に、紫外可視分光法(UV-Vis、紫外吸収分光法)があります。紫外線や可視光を吸収する性質のある官能基(発色団)を検出できるため、有機化合物の構造解析にも時折利用されます。他にも光学活性物質などの測定に使われる円二色性スペクトル(CD)や旋光分散法(ORD)でもこの波長域が用いられます。
可視光よりもさらに長い波長の電磁波を赤外線といいます。こちらも赤外分光法(IR)として有機化合物の構造解析にはNMRと共によく用いられます。
赤外線より長い波長帯には、電子レンジやWi-fiなどに使われるマイクロ波があります。そして、NMRに使われる電磁波は、そのマイクロ波よりも更に長い波長域の、ラジオ波と呼ばれる電磁波になります。文字通りラジオの配信などに使われています。そういう意味では核磁気共鳴分光法というのは”ラジオ波分光法(注:うp主の造語です)”と解釈することもできますね(ちょっと強引な議論かもしれませんが・・・)。しかし、このように考えるとNMRもれっきとした分光法の一つなのだなと実感することができるのではないでしょうか。
核スピンと共鳴のメカニズム
分光法の定義からも分かるように、NMRとは原子核がラジオ波と呼ばれる電磁波を吸収・放出する過程を観測した分光法といえます。
それでは、このラジオ波がどのようにして核磁気共鳴現象を引き起こすのでしょうか。ここでカギとなるのが前回も登場した”ある種の原子の原子核が持つ磁石のような性質”です!
なおここからの解説では、説明を容易にするために敢えて古典物理学的な表現を採用しています。予めご了承ください。
さて、原子核は陽子と中性子から構成されています。

陽子が正の電荷を持つため、原子核自体も正電荷を持っています。また、原子核はその状態で常に自転しています。よって、原子核では自転による電荷の移動が常に生じていることになり、これは電流が絶えず流れて続けている状態だといえます。

そして原子核の周囲にはこの電流に由来する磁場が発生しているのです。これが磁石のような性質の正体です。このとき自転する原子核の角運動量のことを核スピンといい、磁石としての強さのことを核磁気モーメントμ で表します。(なお、前回の動画でも登場した核磁気共鳴最初の観測者I. I. Rabiはこの核磁気モーメントを測定することを目的にして実験していました)。

そんな原子核に対し、磁石を近づけるなどして外部静磁場の中に置くと、核磁気モーメントの向きは方位磁石のように静磁場に対して決まった方向を向くようになり、その状態で歳差運動するようになります。

歳差運動というのは倒れかけのコマのように回転体の回転軸が円を描く運動のことです。よくジャイロスコープ(地球ゴマ)の動きが歳差運動の例として取り上げられますね(ただし原子核の場合は磁気モーメントが歳差運動している)。
原子核の歳差運動の周波数(単位時間当たりで1周する回数)はラーモア周波数と呼ばれています。そして原子核はこのラーモア周波数と同じ周波数のラジオ波と共鳴を起こします。これが核磁気共鳴の正体です。
つまり、原子核の歳差運動に対して、それと同じ周波数のラジオ波を照射すると、核磁気共鳴が起きるという訳です。そのためラーモア周波数のことを共鳴周波数ともいいます。
共鳴周波数は下図に示した簡単な式から導くことができます。

注目してほしいのはB0です。B0は外部静磁場の強度、即ち原子核に近づけた磁石の強さを示しています。原子核の歳差運動というのは常に固有の周波数を持つものではなく、近づけた磁石の強さに依存して変化する値なのです。そのためNMR装置のスペック(分解能)は搭載する磁石の強さによって決まるのです。ちなみにNMRスペクトルの横軸は共鳴周波数に対応した値となっています。単位がHzではなくppmなのは、使用したNMR装置に搭載された磁石の強さ(外部静磁場強度)で横軸の値が変動してしまわないようにするためです。ラーモアの式からも分かる通り、共鳴周波数は外部磁場強度、つまり磁石の強さによって変わってしまいます。測定した装置によってピーク位置の 値が変わってしまったら不便極まりないので、それを避けるために外部静磁場とは無関係な値に変換してあるのです。

さて、原子核を静磁場中に置くと磁気モーメントが磁場に対して一定方向を向き、歳差運動することを説明しました。
このとき磁気モーメントが静磁場に対して“方位磁石のように”一定方向を向くといいましたが、実際は少し異なります。というのも、原子核は静磁場に対して複数通りの方向を向くからです。これは核スピンが外部磁場に対して複数の状態をとることができるのに由来するのですが、その状態の数は以下の式で求められます。

Iは核スピンを特徴づける量子数で、文字通り核スピン量子数と呼ばれる値です。
ここからはプロトン(質量数1の水素)を例にして解説を進めていきましょう。
プロトンの核スピン量子数は1/2という値をとるので、式に代入すると2となります。従ってプロトンは外部静磁場に対して2通りの状態をとることがでるのです。

具体的には磁場と同じ方向を向き、エネルギーが低く安定なαスピンと、真逆の方向を向き、エネルギーが少し高くて不安定なβスピンです。このように、核磁気モーメントを持つ原子核が静磁場中で幾つかのエネルギー状態に分裂することをゼーマン分裂といいます。
なお、原子核の中には核スピン量子数が0であるものもあり、このような原子核はNMRを測定することができません。具体的には陽子と中性子の数がそれぞれ偶数個だとスピン量子数が0になります。代表的な例が炭素12です。炭素全体のほぼ99%を占める安定同位体で、原子核は陽子6個と中性子6個から構成されています。だから有機化学では炭素ではなく1H NMRが一番よく使われるのです(炭素のNMRを測定したいときは同位体の炭素13を測定するため、感度が悪い)。
さて、プロトンの原子核では、ゼーマン分裂が生じると、安定なαスピンの方が不安定なβスピンと比べて少し多く存在するようになります。この少し多い分のαスピンをボルツマン過剰分といいます。

ここへβスピンとαスピンのエネルギー差に相当するエネルギーを持ったラジオ波(ラジオ波磁場)を照射すると、ボルツマン過剰分のαスピンがβスピンへと励起します。この時のエネルギー差ΔEは、実は先ほど出てきたプロトンの共鳴周波数νとプランク定数と呼ばれる量子力学でよく出てくる数値の積に相当します。

ラジオ波照射を止めると励起した分のβスピンは徐々に元のαスピンへと戻ります。

この過程を緩和といい、この際に励起していたプロトンの原子核から放出された信号を検出したものがFIDになります。
FIDは横軸が時間のデータなので、コンピューターでフーリエ変換という処理を行い、横軸を共鳴周波数に変換したものが最初にお見せしたNMRスペクトルになります。

ちなみにエネルギー差ΔEはとても小さいものですので、NMRは他の分析法と比べると特に感度が低いことで知られています。その為、NMRスペクトルを得るには比較的大量の試料が必要になるのです。
化学シフト値と化合物の構造
ではここでもう一度NMRの原理の最も基本となるラーモアの式を見てみましょう。

NMRスペクトルはこの式に相当する電磁波を外部磁場中で照射して核磁気共鳴を起こさせ、その際に得られる信号を測定したものになります。
ですので、もしすべての化合物中のプロトンが全くこの式の通りに共鳴周波数を示すのであれば、得られるNMRスペクトルは全て同一のものとなるはずですよね。クロロホルムのピークが7.2 ppmに出現するのであればブロロホルムもヨードホルムも同様に7.2 ppmにピークが出るはずです。ベンゼンやクメンの全てのプロトンのピークも7.2 ppmにひとまとまりになって出現するのではないかと考えられます。化合物の種類や結合位置が違っても、同じプロトンである以上、同じ式で共鳴周波数が求まるはずだからです。
しかし実際は化合物の種類や化合物中におけるプロトンの結合位置によってピークの出現する場所は大きく異なっています。この違いはいったい何に由来するのでしょう?
ここで重要になってくるのが遮蔽と化学シフトです。
実は外部磁場の強度と実際に原子核に作用する正味の磁場の強度は、化合物中で原子核が置かれた環境によってわずかに異なります。
皆さんは中学校の理科の授業で電磁誘導について習ったのを覚えていますでしょうか。コイルに磁石のN極を近づけるとコイルに電流が流れ、磁石とは逆方向の磁場が生じる現象です。これと同じようなことが原子にも起こります。

原子核に磁場を近づけると、原子核の周囲にある電子から誘起電流が生じて外部磁場に逆らう方向へ誘起磁場が発生します。
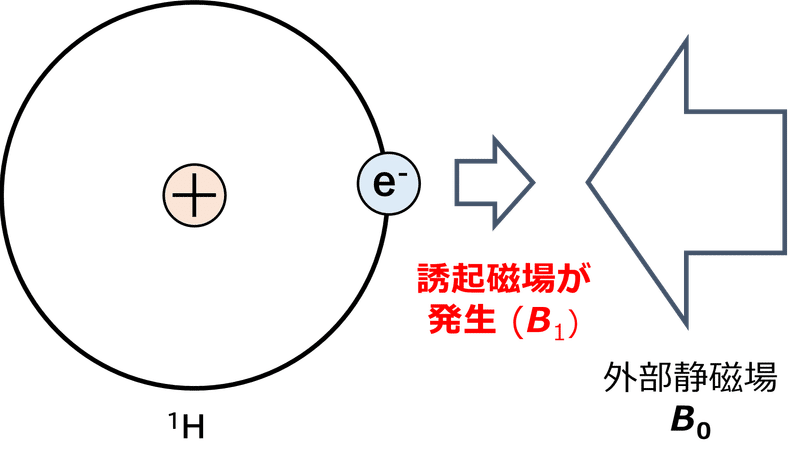
そのため、原子核には外部磁場の強度から電子で発生した誘起磁場を差し引いた分の強さの磁場が実際には作用していることになります。

この現象を遮蔽といいます。そして遮蔽の度合いは原子核周辺の電子の密度の違いによって左右されます。
これがトリハロメタンの1H NMRスペクトルでピークがそれぞれ異なった位置に出現する理由です。要は電気陰性度の高いハロゲン元素が結合している化合物ほど、電子がハロゲン側に強く引っ張られてしまうため、この電子による電磁誘導の影響を受けにくくなってしまったという訳なのです。
電子密度の違いは、電気陰性度(電子を引っ張る力)などの化学的な要因によって決まります。そのためNMRスペクトルの横軸のあたいは「化学的要因でShiftする値」ということで化学シフト値、またはケミカルシフト値と呼ばれます。

化学シフト値を決める要因には電気陰性度のほかに、磁気異方性効果というものがあります。化合物の二重結合や三重結合のπ結合に由来するπ電子が外部磁場に対して誘起磁場を生じるとき、π結合を構成する原子やその周辺に対しては外部磁場と同じ方向に誘起磁場が作用します。π結合を持った化合物では外部磁場に誘起磁場を加算した磁場が作用していることになるのです。よってベンゼンやクメンの化学シフト値は磁気異方性効果によって説明することができるのです。
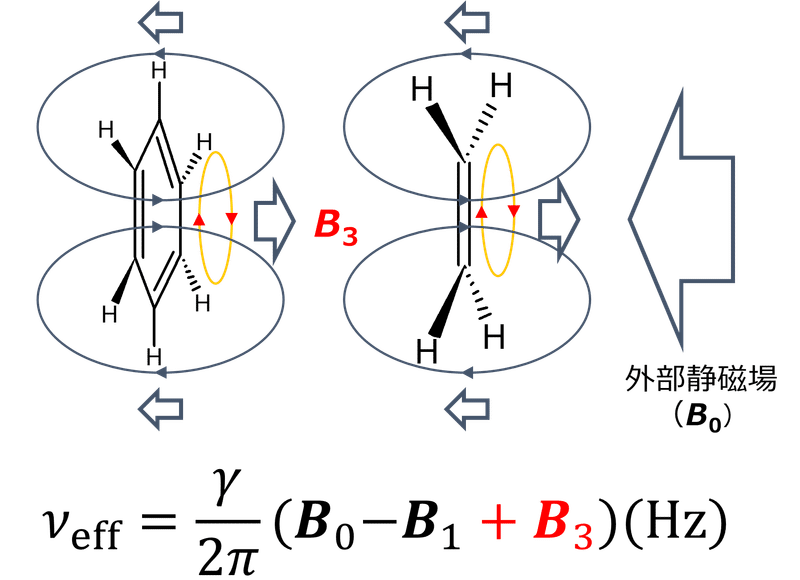
化学シフト値は化合物中の構成原子の置かれた環境を色濃く反映していることから構造解析において非常に有益な情報を与えてくれるのです。では電気陰性度や磁気異方性効果が具体的にどの程度化学シフト値に影響をおよぼすのか。これについては次回詳しく解説していこうと思います。
おわりに
NMRの仕組みを総括すると下図の通りになります(かなり端折ってますが)。

今回はここまでとなります。長時間お付き合いいただきありがとうございます。
次回
次回は1H NMRスペクトルの解析法の解説をしていこうと思います。
引き続きよろしくお願いいたします。
参考文献
執筆に当たり、以下の文献を引用しました。
SDBSWeb : https://sdbs.db.aist.go.jp (National Institute of Advanced Industrial Science and Technology, 2023/5/21
また以下の文献を参考にしました。
J. Clayden, N. Greeves, S. Warren著, 野依 良治, 奥山 格, 柴崎 正勝, 檜山 爲次郎 監訳, ウォーレン有機 第2版, 東京化学同人(2015)
M. Hesse, H. Meier, B. Zeeh 著, 市川 厚 監修, 野村 正勝 監訳, 馬場 章夫, 三浦 雅博 訳, 有機化学のためのスペクトル解析法 第2版 ―UV,IR,NMR,MSの解説と演習―, 東京化学同人(2010)
R. M. Silverstein, F. X. Webster, D. J. Kiemle, D. L. Bryce著, 岩澤 伸治, 豊田 真司, 村田 滋 訳, 有機化合物のスペクトルによる同定法 (第8版) ―MS, IR, NMRの併用―、東京化学同人(2016)
T. D. W. Claridg著, 竹内 敬人, 西川 実希 訳, 有機化学のための 高分解能NMRテクニック, 講談社(2004)
川端 潤, ビギナーズ有機構造解析, 東京化学同人(2005)
楠見 武德, テキストブック有機スペクトル解析 ―1D,2D NMR・IR・UV・MS―, 東京化学同人(2015)
田代 充, 加藤 敏代 著, (社) 日本分析化学会 編集, 分析化学実技シリーズ機器分析編3 NMR, 共立出版(2009)
福士 江里 著, よくある質問 NMRスペクトルの読み方, 講談社(2009)
執筆に当たり以下の素材を利用しました。
makewordart(ワードアート風3D文字)
https://www.makewordart.com/
TogoTV © 2016 DBCLS TogoTV, CC-BY-4.0 https://creativecommons.org/licenses/by/4.0/deed.ja
かわいいフリー素材集いらすとや(棒磁石のイラスト, レントゲン写真を見せるお医者さんのイラスト, ラジオのイラスト, 原子のイラスト)
https://www.irasutoya.com/
化学の迷路(周期表)
http://chem.chu.jp/topic/perio.html
ニコニコモンズ [nc119883 (Wi-fi), nc197167 (ハザードシンボル), nc190959 (電流走る) ]
https://commons.nicovideo.jp/
この記事が気に入ったらサポートをしてみませんか?
