高校無機化学#7(17族)~ハロゲン化水素③~
②HCl
(製法)
まず、HClの製法から。

この反応は、3つあるうちの「揮発性酸遊離反応」の2つ目である。(1つめは、#5で勉強した、HFの製法の反応である。)
では、揮発性酸遊離反応のポイントである、「濃硫酸を加えて加熱」の意味を考えよう。HCl, H2SO4はともに強酸であるから、加熱なしでは平衡反応となってしまい上の弱酸遊離反応は右に進まない。

そこで、加熱をすることにより、HClは揮発させ反応系から取り除き、ルシャトリエの原理により、反応を右に進めることができる。濃硫酸は不揮発性なので、反応系から取り除かれない。(これがポイント!)
※1つ注意。下の画像を見てほしい。部分点は出るかもしれないが、、
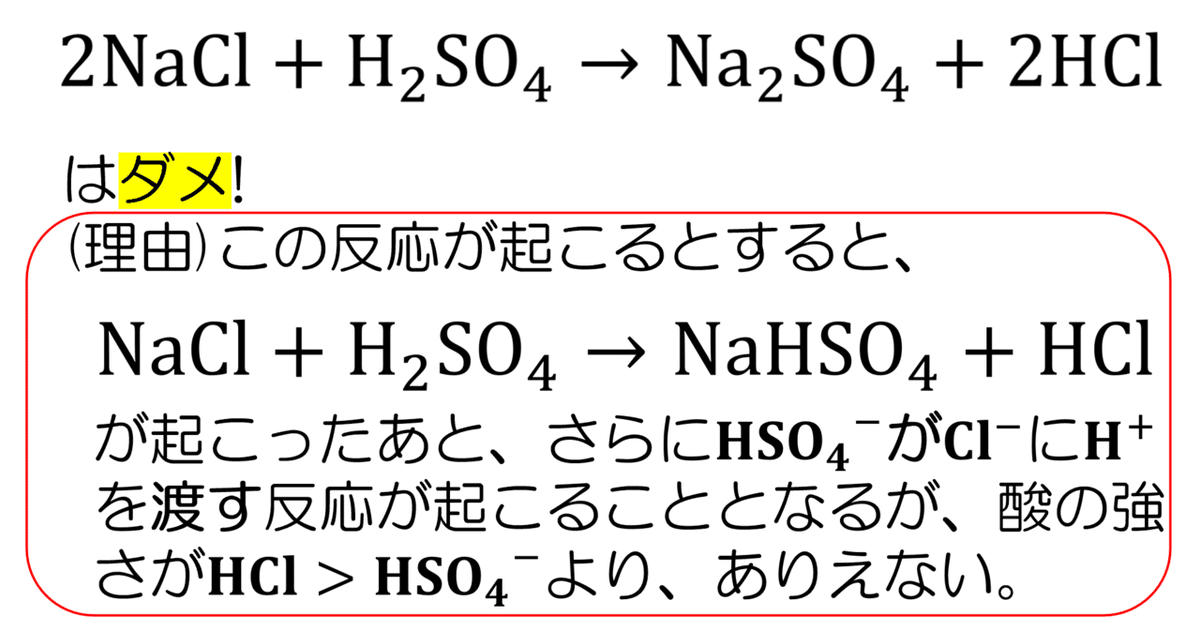
(反応)
HClは強酸であり、塩基と反応する。HClは、NH3と反応させてNH4Clの白煙を生じることで確認する。

③HBr, HI
HBr, HIはこれといって重要なことはない。どちらも、強酸であることは知っておいてもいいかもしれない。
あと、HIに関して、
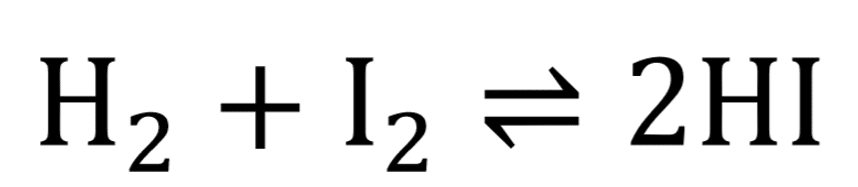
この反応は平衡の問題でよく題材とされる。問題集を見れば、1題はあると思う。
今回は、楽でした。お疲れ様です。
この記事が参加している募集
この記事が気に入ったらサポートをしてみませんか?