
77)老化は病気なのか?
体がみるみる若返るミトコンドリア活性化術77
ミトコンドリアを活性化して体を若返らせる医薬品やサプリメントを解説しています。
【老化は成長の延長】
生まれてから生殖年齢に達するまで、生き物は成長します。この成長過程において、成長ホルモンやインスリンやインスリン様成長因子や、PI3K/AKT/mTORシグナル伝達系や性ホルモンなど様々な因子が成長を促進します。
成長が終了したあとは、成長に関わってきた全ての因子が老化を促進し、がんの発生を促進する方向で作用します。
性成熟を促進する女性ホルモン(エストロゲン)や男性ホルモン(アンドロゲン)はそれぞれ乳がんと前立腺がんの発生と進展を促進します。
生殖活動を犠牲にすれば生物の寿命が延びることはショウジョウバエやネズミの実験で示されています。人間でも去勢によって寿命が延びることが報告されています。
カロリー制限や去勢や遺伝子改変によって生殖活動を弱めると寿命が延び、これは「生殖と寿命のトレードオフ」と呼ばれています。トレードオフ(trade-off)とは、一方を追求すれば他方を犠牲にせざるを得ないという状態 ・関係のことです。
生殖活動を高めると寿命が短くなるという関係があると言うことです。逆に言うと、生殖活動を弱めれば、長生きできるということです。セックスは寿命を短くするという考えですが、それを支持する根拠は多数あります。
性ホルモン以外にも、成長ホルモンやインスリン、インスリン様成長因子、上皮成長因子など体の成長を促進する様々な因子は、成熟年齢を過ぎると、老化とがんの発生・進展を促進します。
老化は成長の延長であり、成長を促進する因子は、多くの場合、老化も促進します。生殖が終了した後は、そのまま老化を促進させる方が種の繁栄には都合が良い(若い世代に生きる場所と食料を与える方が種の繁栄には有利)ので、多くの生物は、成長に関わる因子がそのまま老化を促進し、生殖の終わった個体の死を早めているのです。
サケ科の魚のように、排卵や排精の直後に死亡したり、カマキリの雌が交尾中に雄を食べてしまうように、生殖が終了すれば直後に死ぬ生き物もあります。
アンチエイジングの領域では、ヒト成長ホルモンや性ホルモンの補充によって若返りを目指す治療が行われています。実際に、中年以降の人に成長ホルモンを注射すると、老化の症状を逆行させる様々な効果が現れます。筋肉量が増え、脂肪組織が減り、筋力や体力が増し、男性の性的能力が向上します。
しかし、中年以降の成長ホルモンの注射は、がんの発生や成長を促進する可能性が高く、そして寿命を短くする可能性が指摘されています(現段階では人間においてはまだ証明はされていません)。
マウスの研究では成長ホルモンの産生や受容体に異常がある場合は寿命が延びることが示されており、人間でも成長ホルモンが過剰に分泌される先端肥大症や巨人症ではがんの発生率が高く、寿命が短くなることが知られています。
閉経後の女性に女性ホルモン(エストロゲン)を補充すると、骨粗しょう症の減少や性欲の増加や若返り効果が得られますが、乳がんを促進し、寿命に対してもマイナスに働くことが指摘されています。
男性ホルモン(テストステロン)の場合も同様で、一時的には年老いてきた男性の衰えを回復させる効果はありますが、長期にテストステロンを補充すると生存に及ぼす影響は最終的にはマイナスになることが示されています。
インスリンは性ホルモンの産生と活性を高めます。中年以降はインスリンを高めない方が寿命を延ばす効果が得られます。つまり糖質制限が寿命を延ばす根拠です。
「生殖と寿命のトレードオフ」の存在意義はまだ良く判っていません。「地球上には空間的にも食料供給にも限界があるので、生き物に寿命がなければ、いずれ生物は全滅するので、寿命や老化が必然的に存在する」という考えがあります。空間や食糧供給に限界がある状況では、繁殖力が強いほど早く死なないと種の保存ができないということになります。実際に繁殖能の高いマウスは短命で、成熟のプロセスがゆっくりで繁殖率が低い動物(ゾウや人間など)は寿命が長いのも「生殖と寿命のトレードオフ」の1例だと考えられています。
以上のような考え方は、「老化は生きる上で避けて通れない変化」ということを意味します。加齢とともに体の機能が低下するのは、「生物として避けられない運命」であり「遺伝的に決められた必然の生理現象」というのが一般的な考え方です。
しかし、アンチエイジング(抗老化)の研究領域では「老化は病気」という考え方で、老化を治療の対象にする考え方が主流になっています。
長寿研究の第一人者デビッド・A・シンクレア博士が、著書の『LIFESPAN 老いなき世界』の中で「老化は人間の運命ではなく『病気』であり、治すことができる」と言っています。
【加齢と炎症と慢性疾患】
加齢とともに、関節炎、2型糖尿病、心血管疾患、腎臓病、アルツハイマー病、パーキンソン病、黄斑変性、虚弱(frailty)、呼吸器疾患、ある種のがんなど様々な慢性疾患の発症頻度が高まってきます。
このような加齢関連疾患の発症に慢性炎症が関わっていることは広く認識されています。
加齢が慢性炎症を引き起こして加齢関連疾患の発症を促進し、慢性炎症はさらに老化を促進し、加齢関連疾患をさらに悪化させます。このように、加齢と慢性炎症と加齢関連疾患との間には強い関連があり、悪循環を形成しています。
すなわち、慢性炎症を引き起こしている原因を除去することによって、老化や加齢関連の慢性疾患の発症や進展を遅延させることができ、老化そのものを治療の対象にできます。(下図)
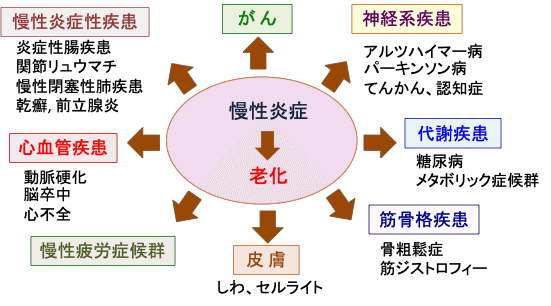
図:慢性炎症は老化や様々な加齢関連の慢性疾患の発症を引き起こしている。(参考:Prev Med. 2012 May; 54(Suppl): S29–S37.)
【加齢とともに炎症性サイトカインの血中濃度が高くなっている】
加齢は細胞のダメージの蓄積とダメージ関連分子パターン(damage-associated molecular patterns: DAMPs)を除去する内因性メカニズムの疲弊と考えられます。
ダメージ関連分子パターン(DAMPs)というのは、細胞傷害に伴って放出される細胞内分子で、組織の炎症を引き起こします。このDAMPsの処理能力が低下すると慢性炎症が持続します。
生体は「自己にない分子パターンを認識する」というメカニズムで細菌やウイルスや真菌などの病原体を認識して免疫を発動させます。これを「病原体関連分子パターン(pathogen-associated molecular patterns: PAMPs)」と言います。
また、細胞傷害に伴って放出される細胞内分子を「危険シグナル」として認識して炎症反応を発動させます。これをダメージ関連分子パターン(damage-associated molecular patterns: DAMPs)と総称しています。これらは、周囲の組織や細胞に危険を知らせるアラームのような役割を担っています。
壊死した細胞、細胞外に漏出したATP、高血糖、セラミド、アミロイド、尿酸結晶、コレステロール結晶など様々なDAMPsが加齢とともに増加します。これらのDMAPsは、マクロファージなどの組織に常在する自然免疫に関与する細胞によって認識され、慢性の炎症を引き起こし、これが加齢や加齢関連疾患の原因になっています。(下図)
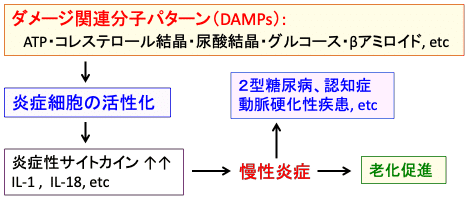
図:細胞ダメージに伴って漏出したATPや、コレステロール結晶や尿酸結晶や高血糖やβアミロイドなどの自己由来成分はダメージ関連分子パターン(damage-associated molecular patterns: DAMPs)となって、マクロファージなどの組織に存在する炎症細胞を活性化し、IL-1βやIL-18などの炎症性サイトカインの産生を高め、慢性炎症を引き起こす、慢性炎症は老化を促進し、2型糖尿病や認知症や動脈硬化性疾患など様々な加齢関連疾患の発症と進展を促進する。
中枢神経系におけるミクログリア、肝臓のクッパー細胞、骨の破骨細胞、腎臓のメサンギウム細胞などの組織に常在する貪食細胞は、傷害された組織の修復や再構築を行うためにサイトカインを産生し、臓器機能の恒常性維持に重要な役割を果たしています。
しかし、加齢関連のDAMPs(ダメージ関連分子パターン)による組織マクロファージの持続的な活性化は、組織の炎症性のダメージと機能異常を進行させるメカニズムになっています。組織常在のマクロファージの活性化だけでなく、組織の白血球浸潤も加齢関連疾患の発症に関与しています。
現在では、加齢と炎症と慢性疾患の関連は確立されています。男女とも65歳以上では炎症性サイトカインのIL-6やTNF-αやIL-18の血清中濃度が上昇していることが報告されています。これらのサイトカインは、アルツハイマー病や虚弱(frailty)を含む様々な加齢関連疾患の発症に密接に関連していることが明らかになっています。
加齢に伴う炎症性サイトカインの増加は「inflammaging(炎症加齢)」という用語が提唱され、加齢関連疾患の発症を促進し、寿命を短くする原因として重視されています。
多臓器における加齢関連炎症の存在は、特別な疾患が存在しなくても、臓器機能の低下を引き起こしています。炎症によって産生が高まる活性酸素は細胞や組織に酸化傷害を与えることによって細胞や組織の老化を促進し、機能を低下させます。
炎症性の免疫応答は、成長期においては感染症から個体を守ってくれますが、年齢が進み生殖年齢が終了したあとの身体に対しては、炎症性細胞の働きは臓器機能を低下させ、寿命を短くする方向で作用します。
つまり、炎症応答というのは、感染症から身体を守るという働きがある一方、身体の老化を進行させているというトレードオフの関係が存在するのです。
炎症加齢仮説(Inflammaging theory)では、生理的加齢あるいは病的加齢はともに、自然免疫システムによって産生される炎症起因性のサイトカインによって進行されると考えています。この炎症加齢仮説が正しければ、自然免疫の応答経路を制御することによって、加齢による臓器機能の低下を弱めることができる可能性があります。
病原菌による感染症から防御するために急性炎症のメカニズムは必要ですが、炎症応答を制御するメカニズムは加齢とともに異常をきたしています。その結果、慢性的な軽度の炎症が多くの加齢関連疾患の発症に関与しています。
【慢性炎症は免疫力を低下し、老化を促進する】
老化というのは、加齢に伴って個体の生存に必要な様々な生命機能が低下していく現象です。加齢に伴って免疫系が老化(機能低下)する結果,免疫系本来の非自己を排除する機構と炎症反応を制御する機構が低下し,その結果、高齢者では易感染性や炎症の持続(慢性炎症)が引き起こされます。
加齢に伴う免疫系の老化を特徴づける現象として「免疫老化(Immunosenescence)」と「炎症加齢(Inflammaging)」があります。
「免疫老化」は免疫系本来の役割である「非自己を排除する機能」が加齢に伴って低下することを指し、高齢者で認められる易感染性の原因となっています。
「炎症加齢」は炎症反応を制御する機構が加齢に伴って低下する結果、慢性的に炎症が持続することによって老化が促進されることです。
「Inflammaging」はinflammation(炎症)+aging(加齢)から作られた用語で、炎症が老化や、老化に伴う様々な疾患と密接な関係があることから生まれた造語です。
加齢に伴って免疫機能は個体・細胞レベルで低下していますが、一方で高齢者の血中において インターロイキン6(IL-6)や 腫瘍壊死因子α(TNFα) などの炎症性サイトカイン、C-反応性タンパク質(CRP)や種々の補体分子などの炎症性タンパク質が慢性的に増加しています。
このような血中の炎症性物質の増加に加えて、高齢者では自己抗体の保有率が上昇しています。老化に伴う慢性炎症状態が様々な老化関連疾患の発症を促進しています。
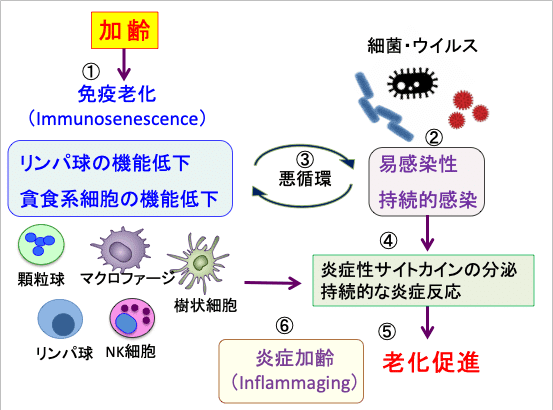
図:加齢に伴ってリンパ球(T細胞やB細胞など)や貪食細胞(マアクロファージ、樹状細胞など)の免疫細胞の機能が低下し(①)、この免疫老化(Immunosenescence)によって、感染症に罹りやすくなり、さらに感染が持続しやすくなる(②)。持続的感染はさらに免疫機能を低下させ、悪循環を形成して免疫老化が進行する(③)。持続的感染は持続的な炎症反応(慢性炎症)を引き起こして、炎症性サイトカインの分泌が亢進する(④)。このような慢性炎症状態は組織障害を介して細胞や組織の老化を促進する(⑤)。このような慢性炎症の持続によって老化が促進される現象を炎症加齢(Inflammaging)という(⑥)。
体の若返りが可能な理由の一つは、老化に伴う臓器機能の低下に、幾つかの生体内成分の減少や増加が関与していることです。
2 匹のマウスの脇腹の皮膚を縫い合わせる並体結合(parabiosis)という手法を用いて、若い個体と老齢個体を並体結合し、両者の血液を一緒に循環させて1ヶ月ほどすると、老齢個体が若返りの兆候を示すことが報告されています。
老化によって低下していた骨格筋の筋力が増加し、神経幹細胞の増殖能が促進されて認知機能が良くなり、心臓や肝臓や膵臓などの臓器機能が改善することが認められています。
逆に若いマウスは老化の徴候が進行することが示されています。
これは、加齢とともに老化を促進する「老化因子」が次第に増加し,体を若い状態に維持する「若返り因子」が加齢とともに減少することが老化の原因である可能性を示唆します。
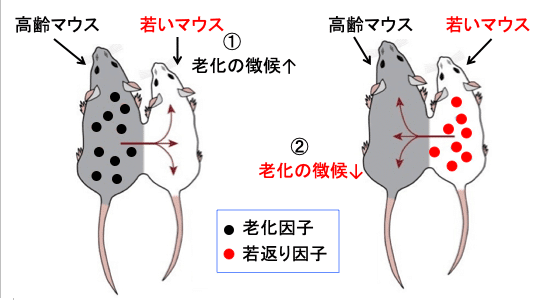
図:高齢マウスと若いマウスの脇腹の皮膚を縫い合わせる並体結合によって両者の血液循環を共有させると、高齢マウスの老化因子によって若いマウスの老化の徴候が促進される(①)。一方、高齢マウスは若いマウスの若返り因子によって老化の徴候が減少する(②)。
体内の生命活動に必須の補酵素のニコチンアミド・アデニン・ジヌクレオチド(nicotinamide adenine dinucleotide:NAD+)はそのような若返り因子の一つとして研究されています。
NAD+は加齢とともに減少し、NAD+を増やす方法は老化の徴候を低下させることが明らかになっています。NAD+の前駆物質であるニコチンアミド・モノヌクレオチド(NMN)やニコチンアミド・リボシド(NR)をサプリメントとして補充すると体内のNAD+の量を増やし、免疫老化と炎症加齢を抑制し、免疫機能を若い人のレベルに回復させることが可能になります。
さらに加齢に伴って慢性的に血中に増えてくる炎症性サイトカイン(IL-6やTNF-α) やC-反応性タンパク質(CRP)や補体分子などの炎症性タンパク質を減少させることは老化を抑制し、体の若返りに有効です。
実際、COX-2阻害剤などの抗炎症剤が老化抑制に効果が期待できる可能性が報告されています。食事でも、抗炎症作用のある野菜の多い食事が老化を抑制し、体内の炎症を促進する肉や精製糖質の多い食事は老化を促進します。
炎症を阻害する食品成分や食事法として、ケトン食、オメガ3系不飽和脂肪酸、カロリー制限が報告されています。実際に、動物実験モデルではケトン体とカロリー制限が寿命を延長することが報告されています。
ケトン体のβヒドロキシ酪酸とアセト酢酸は、グルコースに変わるエネルギー源となることによって飢餓時の生存を助ける働きがあります。肝臓や筋肉の貯蔵グリコーゲンが枯渇すると、肝臓は脂肪酸を燃焼(分解)してβヒドロキシ酪酸を産生します。カロリー制限や強度の運動や低糖質ケトン食によって、βヒドロキシ酪酸の血中濃度は上昇します。
ケトン体が炎症を抑制する作用があることは実験的に多くの研究で確かめられています。
人間とマウスのマクロファージを用いた実験でβヒドロキシ酪酸は炎症細胞の活性化を阻害しました。
オメガ3系多価不飽和脂肪酸が抗炎症作用を示すことは多くの研究で確かめられています。マクロファージや単球におけるIL-1β分泌を、ドコサヘキサエン酸(DHA)が減少させることが報告されています。一方、動物性脂肪などに含まれる飽和脂肪酸やオメガ6系不飽和脂肪酸の多い食用油は末梢血の単球を直接活性化することが報告されています。
油脂には健康に良い油脂と悪い油脂があることを知ることが重要です。最近の研究でも、バター、ラード、赤身肉などに含まれる飽和脂肪酸が、早死リスクを上昇させることが、30年間に及ぶ研究で明らかになっています。その一方で、飽和脂肪酸を魚油やオリーブオイルなどの不飽和脂肪酸に切り替えることで、健康上の大きな恩恵が得られることが報告されています。ω3系不飽和脂肪酸やオリーブオイルは多く摂取するほど健康作用が高まる様です。
以上のように、老化は食事やサプリメントや医薬品で治療できることが明らかになり、「老化は病気」という考え方が主流になりつつあります。ただし、老化を病気として治療することが「生物としての人類」の繁栄につながるかは疑問も多くあります。
