
人工イクラとpH
人工イクラはアルギン酸ナトリウムがカルシウムイオンによってゲル化したものです。
通常、人工イクラを作るとき、アルギン酸ナトリウム水溶液と乳酸カルシウム水溶液を使います。
食用色素で着色した1%のアルギン酸ナトリウム水溶液を、1%の乳酸カルシウム水溶液中に滴下します。
液面から5cm程度の高さから滴下すると、綺麗な球状のゲルが出来ます。

スプーンですくって慎重に水溶液を落とすと、少し大きめの人工イクラを作ることも出来ますね。

太いスポイトを使ったときも、大きな人工イクラを作ることが出来ます。
ただ、スプーンを使った方が手軽ですね。
色を上手く調整出来れば、本物のイクラのようなゲルになります。
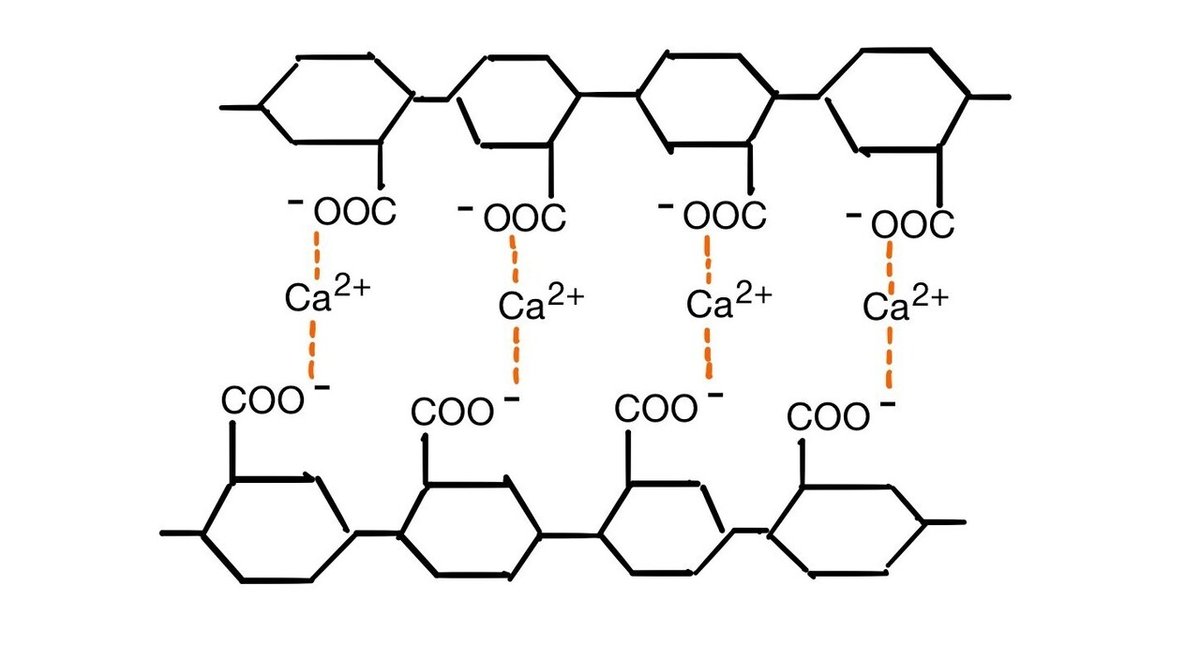
この図のように、カルシウムイオンがアルギン酸のカルボキシル基を橋架けし、ネットワークを作ります。
*アルギン酸は簡略化した構造です。
では、強いアルカリ性を示す水酸化カルシウム水溶液を使うとどうでしょうか?
乳酸カルシウムとおなじように、カルシウムイオンを持っています。
水酸化カルシウムは水に溶け難いため、1%未満の濃度でも溶け残ります。
そのため、白く濁った水溶液になります。

ここに、1%のアルギン酸ナトリウム水溶液を滴下します。
一見、人工イクラができたように見えます。
しかし、ゲルを水溶液からすくい上げてみると、柔らかい上に形はバラバラです。

ゲル化が不十分なんですね。
そこで、クエン酸を加えて混ぜます。

すると、溶け残っていた水酸化カルシウムが溶け、無色透明になります。
1%のアルギン酸ナトリウム水溶液を滴下すると...

今度は球状のゲルが出来ました!
酸性になることでカルシウムイオンが水中に放出され、アルギン酸ナトリウムがゲル化し易くなったんです。
塩基性の状態でもカルシウムイオンによる橋架けは起きますが、酸性条件の方が、より多くのカルシウムイオンが架橋剤として働きます。
また、クエン酸には金属イオンを補足するキレート作用があります。
そのため、クエン酸に補足されたカルシウムイオンは架橋剤として働きません。
従って、出来た人工イクラは柔らかく、潰れやすいものになります。
ちなみに、アルギン酸ナトリウム水溶液は、酸を加えてpHを小さくするとゲル化します。
クエン酸を少量加えて混ぜると、少しずつゲル化し、以下の写真のような柔らかいゲルが出来ます。

これは、アルギン酸に付いているCOO-がCOOHになり、静電反発がなくなるために起きる現象です。
中性付近や塩基性だと、カルボン酸はCOO-の状態になっているので、負の電荷どうしの反発で分子鎖は広がっています(当然ですが、対イオンとしてナトリウムイオンや水素イオンが近くに存在しています)。
COOHになると反発がなくなり、アルギン酸の分子鎖は水素結合などで凝集して弱いネットワークを作るんです。
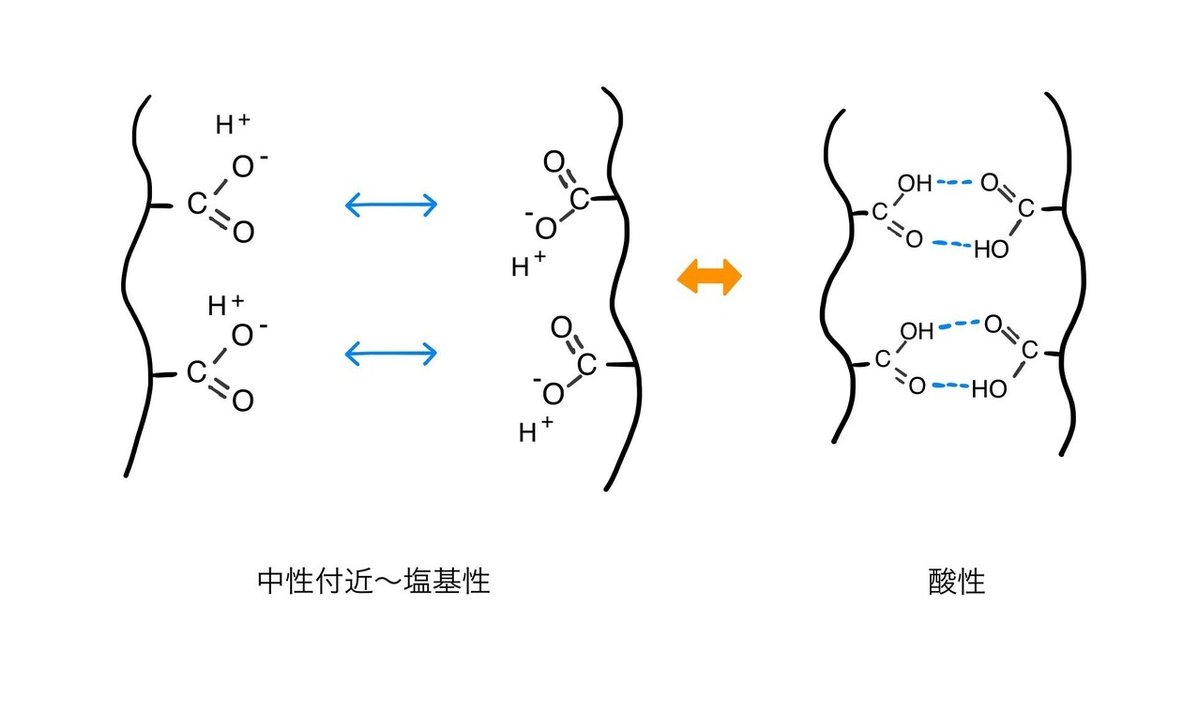
人工イクラのように球状のゲルを作るのは難しいですが、こんな方法でもアルギン酸ナトリウムのゲルを作ることが出来ます。
よく使われる乳酸カルシウム水溶液で人工イクラを作るときも、pHによってゲル化のし易さやゲルの硬さが変わります。
余談ですが、スポイトが無くても人工イクラを作ることが出来ます。
ビーカーなどから少しずつ滴下すれば球状のゲルができます。

スポイトを使う時と同じく、液面から5cm以上離れたところから液滴を落とせば大丈夫です。
慣れれば、スポイトを使う時よりも楽に人工イクラを作ることが出来ます。
人工イクラは乳酸カルシウム水溶液に滴下して1~2分程度でできますが、指で簡単につぶすことができます。
これを一晩漬けておくと、中心部までゲル化するので、指で強く押しても潰れなくなります。
変形はしますが、潰れません。
硬いもので強い圧力をかければ流石に潰れます...

人工イクラを作るときに試してみて下さい。
読んでいただけるだけでも嬉しいです。もしご支援頂いた場合は、研究費に使わせて頂きます。
