
「反応膜を浸しておくだけ!」 植物の原理でトリチウムを実用的に分離・回収 (基礎編)
研究の背景と概要
すべての植物は葉緑体の中で、光合成のために水を酸化分解する触媒として酸化マンガンをつかっています。フォワードサイエンスラボラトリ(FSL)は、酸化マンガンの結晶構造を制御することで発現する種々の機能性に関する研究を長年続けてきました。一連の研究から得られた成果は、国内外の学会や査読付きの学術誌において公表されています。このたび、それら研究成果のひとつとして、室温の水中から極低濃度のトリチウムを選択的に分離・回収する技術を開発するに至りました。
トリチウムは大気や水中に水分子の同位体異性体(HTO)として存在します。HTOは、物理化学的性質が通常の水分子(H2O)と似ているために分離が容易ではありません。これまで、室温下でHTOを水や空気中から選択的に分離回収する技術は全く存在しませんでした。さらに、トリチウム濃度が10000 Bq/mL以下の超低濃度の場合には、トリチウムを分離することが不可能であるとさえ考えられてきました。
本技術をもちいた実験結果の例として、福島原発事故汚染水のトリチウム濃度と同レベルの濃度であるトリチウム濃度が4000 Bq/mL(11.17 ng/L相当)の試験水から、室温下でトリチウムを分離効率2.66×10^6 Bq/m^2hで除去することができることを実証しました。この分離効率は、酸化マンガンを含む反応膜の単位面積(m^2)・単位時間(h)あたりに水中から除去できるトリチウムの量をベクレル(Bq)単位で表しています。また、除去されたトリチウムは反応システム内の小型キャッチャー容器に回収されるため、環境中に拡散することもありません。本技術は、処理前の汚染水に含まれていたトリチウムを同キャッチャー容器の極少量の水やシリカゲルに移動させる仕組みです。これは、元の汚染水の容積を約100万分の1に減容することに相当します。
同分離効率の値が実際にどのくらいの性能に相当するのかをわかりやすく説明するために、福島原発事故現場に敷設されたタンク群に保管されている莫大なトリチウム汚染水の全量に対して適用を想定した効果を試算してみました。その結果、同反応膜(面積1m^2)を1万枚(総面積10000 m^2)使えば、約6年間で汚染水全量中のトリチウムを全量分離回収できるという、極めて期待が持てる性能が試算されました。
また、同分離効率は反応膜を適切に設計することで増加することがわかっています。このため、さらに短期間でトリチウムを効率よく分離できる浄水プラントが実現します。浄水プラントの規模にしたがって必要な処理時間は短縮できます。したがって、今後、処理対象水の量と質(他核種の濃度・油や界面活性剤の濃度など)、および処理期限など設計に必要な情報が充分に開示されれば、最適なコストパフォーマンスを考慮した浄水プラントの設計・施工が可能になります。
研究の経緯
ここで、「酸化マンガンの結晶構造を化学的に制御するトリチウムの分離」とは、具体的にどのような技術なのか、研究の経緯を追いながら述べてみたいと思います。この記事では内容が少しだけ専門的ですので、福島原発事故汚染水に対する適用について主に知りたい方は、本手法を適用した浄水処理プラントを提案しましたので、以下のURLからご確認下さい。
(掲載先の情報)政府刊行物 として全国官報販売協同組合から発刊されている、月刊JETI (ジェティ) 2022年9月号
https://www.gov-book.or.jp/book/detail.php?product_id=376409
古屋仲秀樹:スピネル酸化マンガンを用いた三重水素の分離技術, Japan Energy & Technology Intelligence, Vol. 70, No. 9, 109-113, (2022).
ガラスや水銀などは、物質を構成する原子のならび方がランダムであることからアモルファスという特殊な物質であることが知られています。しかしながら、酸化マンガンなどの一般的な物質のほとんどは、物質を構成する原子のならび方に規則性が存在し、その規則性には物質に応じていくつかの種類が存在します。この原子がならぶ規則性の違いが結晶構造の違いとして分類され、空間群という指標で識別されます。今回、トリチウムの分離に使われた酸化マンガンは、空間群が Fd3mの結晶構造にあたります。この結晶構造を有する酸化マンガンは、スピネル型の結晶構造をもつ酸化マンガンとして知られており、1970年代頃から世界中の多くの固体物理や電気化学の分野の研究者によって物性と機能性が報告されてきた物質です。特に、同酸化マンガンの結晶内におけるリチウムイオンと水素イオンの交換性と拡散性に関しては、電池としての応用に対する期待もあって数えきれないほどの報告が存在します。高名なJ. B. Goodenough博士らもリチウムイオンの挿入によって結晶の膨らみや縮みを表す指標である格子定数が大きく変化し、電池材料としての性能に影響することを報告しています。私共も2003年に水素イオン化した同酸化マンガンを乾燥処理することで、結晶内の水素イオンが水(H2O)として表面から蒸散することを報告しています[1]。これが今回、同酸化マンガンに取り込まれたトリチウムイオンが水分子(HTO)として蒸散することに気づく手がかりになりました。
図1に、同酸化マンガン表面の透過型電子顕微鏡写真を載せました。図中、長さの縮尺を表すバーは 25 Å (オングストローム=10^-10 m)の長さを示し、同酸化マンガン1粒子の表面を構成する原子群の観察に適した高解像度であることがわかります。

図1 スピネル型酸化マンガン表面の透過型電子顕微鏡写真 ref. [1]
酸素とマンガンの原子が規則的に配列して表面を構成している。水中において同表面に存在する無数の細孔から、水素イオン、重水素イオン、トリチウムイオン、およびリチウムイオンが結晶内に取り込まれる。同結晶の格子定数は、主にイオン半径が大きいリチウムイオンの含有量に応じて増減し、トリチウムイオンの吸着/脱着には、それぞれ適した格子定数が存在する。本技術は、室温の水中で同結晶の格子定数を制御することによって、トリチウムイオンの吸脱着反応を実現している。
また、私共は同酸化マンガンの結晶構造に特別な原子間距離を有した酸素ペアがネットワークを構成していることを報告しました[2]。同ネットワークの存在が結晶を構成する酸素イオンに強い水素結合[3](弱い共有結合ともいわれる)によって水素イオンが吸脱着する原因になっています。一般に、結晶内で水素イオンを束縛する結合力が強すぎると水素イオンの吸着が一過性になり、脱着させることが困難になってしまいます。したがって、結晶を構成する酸素イオンが強い水素結合で水素イオンと結合する物性は、水素イオンとの吸着反応と脱着反応を両立させるために不可欠といえます。同ネットワークを通じて結晶内の局所におけるイベントである水素イオンとの結合が、情報として1粒子の表面にかぎらず、粒界を通じて接する全粒子の表面に伝わる効果が考察できました。
2012年当初、本研究における課題は、そもそもトリチウムイオンが水素イオンや重水素イオンと同様に、スピネル型の酸化マンガンの結晶に吸着して取り込まれるかどうか?を確認することでした。幸いにも京都大学放射性同位元素総合センターの協力が得られ、水素イオン化した酸化マンガンの粉末をトリチウムを含む試験水に懸濁させた際のトリチウム濃度の変化を調べる機会を得ました。具体的には同センターの放射性物質をあつかう施設において、RI管理区域内の実験室および測定装置として液体シンチレーションカウンターを利用することができました。
結果は、水素イオン化した酸化マンガンを懸濁した後、15分程度でトリチウム濃度が初期濃度の30%ほど減少することがわかりました。しかし、40分も経つと初期濃度近くに戻ってしまうという実用性に乏しい一時的な吸着反応でした。仮に、同酸化マンガン表面におけるトリチウムイオンの吸着が水素イオンとのイオン交換によって生じたのであれば、トリチウム濃度が初期濃度近くに戻った原因は、酸化マンガンの表面が含有する水素イオン量の不足によると考えました[4]。
上記の水素イオン不足を解消するために、課題は如何に粉末状の酸化マンガンに対して水素イオンを供給しながらトリチウムとのイオン交換を継続させるか?でした。
まず、酸化マンガン粉末を市販の導電性塗料と混合して厚み1mm程度の膜状に成形し、これを焼成することで固化しました。固化した膜の正面をトリチウムを含む試験水に接触させ、背面の膜表面には希酸を配置・接触させる反応系を設計・製作し、実験してみました。
この実験に供した反応系は、焼成によって膜表面に生じる細孔を通じて酸化マンガン粉末に希酸由来の水素イオンを供給するアイデアでしたが、結果的に、時間の経過とともに同膜の細孔を通じて希酸と試験水が混じり合うことが判明し、さらなる改良が必要になりました。
この頃までの状況は、 https://vimeo.com/120439648 に公開の動画で観ることができます。
改良策として、希酸との接触面には水素イオン導伝材であるナフィオン@(デュポン社の登録商標)を塗布・乾燥して反応膜を補強し、さらに希酸の量も必要最少限ですむ反応系を設計・製作しました。この新しい反応系を用いて試験水に適用した結果、粉末状の酸化マンガンを用いた際にみられた一時的なトリチウム濃度の低下は発生せずに、継続的なトリチウム濃度の低下が観察されました。さらに吸着トリチウムを極少量のキャッチャー物質(例えば、H2Oやシリカゲル)に回収する仕組みを追加考案し、同仕組みを組み入れた反応系によってトリチウムの継続的な分離と回収が実現しました。
多くの改良を施した同反応系によって得られた実験結果の一例として、トリチウム初期濃度3863.8 Bq/mLの試験水に適用した実験では、実験開始から120時間が経過してもトリチウム濃度は低下しつづけ、同時に試験水中の濃度低下量に相当する全量の約88.8%がキャッチャーに回収できました[6]。
しかしながら、同実験から新たな課題も見つかりました。一つ目は、トリチウムの吸着が活発に生じるように試験水のpHを弱酸性からアルカリ性に調整するためのアルカリ試薬を添加した瞬間、反応膜からマンガンイオンが溶出してスラッジが試験水中に発生することでした。本実験は、試験水の容量が200mL程度の小規模な実験なので発生する沈殿物のスラッジも少量なのですが、規模が大きい実際の水処理プラントで同様に発生すると処理コスト的にも大きな問題になってしまいます。二つ目は、反応系を長時間運転した際にトリチウム濃度の減少速度が低下することでした。
これらの新たな課題の対策として、試験水にアルカリ試薬を添加する操作に先立って、試験水に一定割合で極少量の塩化リチウムを添加してみました。その効果は絶大で、試験水中のスラッジ発生が完全に抑制されることがわかりました [7]。さらに、同添加はトリチウム濃度の減少速度を保つことにも有効でした。これらの知見は、同反応系を運転する際のメンテナンスにおける重要なポイントであり、反応膜の高寿命化と性能維持に寄与することになりました。
トリチウム分離・回収の原理
スピネル型酸化マンガンを含有する反応膜を用いてトリチウムを分離・回収する原理と手順を図2で説明します。同図は反応膜を試験水側から見た正面図であり、背面に希酸を配置することで同反応膜に水素イオンを供給しています。図中、反応膜に含まれる酸化マンガン粒子の格子間隔が気中と水中では異なることをグリットのサイズの違いで表現しています。すなわち、水中ではトリチウムイオンの吸着に適した格子間隔をもつ酸化マンガン粒子が機能し、気中ではトリチウムイオンの脱着に適した格子間隔をもつ酸化マンガン粒子が機能することによって、水中と気中でそれぞれトリチウムの吸着と脱着が生じるというしくみです。
同考察は、粉末の同酸化マンガンを試験水に適用した際に、酸化マンガンの結晶の格子定数(a)が8.037<a<8.040 Åの範囲にある際に高いトリチウムの吸着能が実験で確認され、また格子定数が8.036Åと値が低く結晶が縮んだ状態ではトリチウムの吸着がほとんど生じないという実験結果[5]に基づきます。
図2の下に記述した(1)〜(3)の手順にしたがってトリチウムの分離・回収が進みます。また、反応容器内において反応膜が気液と接している長さ(蒸散長)を適切に設計することで、反応膜から気中に蒸散する水の同位体異性体(HTO)の量を増加させることが可能です。これは、反応系の生成物であるHTOを反応膜から効率的に蒸散させることによって、水中のトリチウムの吸着速度が向上することを意味します[8]。
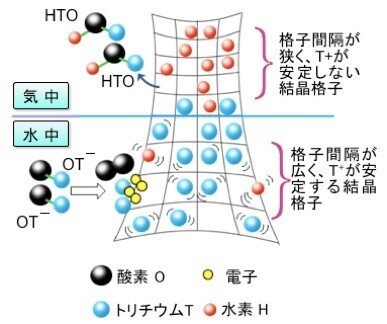
図2 水中からトリチウムが分離・回収される原理と手順
(1)水中で、トリチウムを含む水酸化物イオン(OT-)が反応膜の表面に吸着。
(2)吸着OT-が酸化マンガン表面で分解、トリチウムイオン(T+) として酸化マンガンの結晶に取り込まれる。この結果、水中のトリチウム濃度が減少する。
(3)気中で、反応膜の表面からトリチウムイオン(T+)がトリチウムを含む水分子(HTO)として反応容器内部のヘッドスペースに蒸散する。この蒸散 HTOを反応容器のヘッドスペースに導入した気流にのせてキャッチャー容器に回収する。
極低濃度トリチウムの分離・回収を実現したスキーム
本トリチウムの分離現象は、図3の右下に示した様に、見かけ上は反応膜の表面における酸(H+)とアルカリ(OT-)の中和に基づく単純な化学反応とみなせます。しかしながら、実験結果においてトリチウムに対する高い選択性が生じていることを考慮すると単純な中和反応では分離現象を説明できません。このため本分離現象の本質は、水分子の同位体異性体(HTO)が水中のブラウン運動衝突により自然解離することで生じる水酸化物イオンの同位体異性体(OT-)が、酸化マンガン表面で選択的に酸化分解される複雑な触媒反応であると考えられます。
また、通常の水分子(H2O)に比べてHTO分子は、その分子構造上の非対称性によって解離しやすいのかもしれません。したがって、トリチウムイオン(T+)の方が水素イオン(H+)よりも取り込まれやすい酸化マンガンの表面においては、OT-の方がOH-よりも優先的に反応すると考えられます。結果として、水中濃度が極低濃度であってもトリチウムに対する選択的な分離が生じていると考察しています。
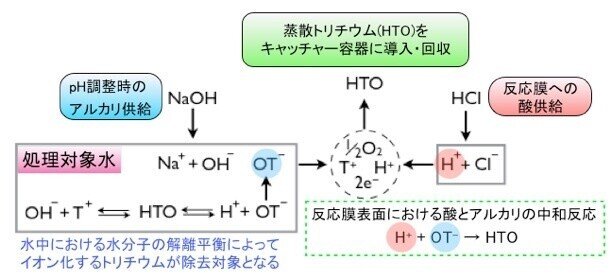
図3 トリチウムの分離・回収スキーム
おわりに
このnoteでは、水分子の酸化分解反応をうまく利用することで、水中のトリチウムを効率よく分離できることを紹介しました。本手法は、原理的に付加的な電気や熱エネルギーを必要とせず、長期間にわたって運用される水処理施設のコストを最小限におさえることを可能とします。現在、早期に実用化するための取り組みを続けています。
引用文献
[1] H. Koyanaka, O. Matsubaya, Y. Koyanaka, and N. Hatta, Quantitative correlation between Li absorption and H content in Manganese Oxide Spinel λ-MnO2, J. Electroanalytical Chemistry, 559, Nov p.77-81, (2003)
[2] E. Libowitzky, Correlation of O-H Stretching Frequencies and O-H⋅⋅⋅O Hydrogen Bond Lengths in Minerals, Monatshefte fur Chemie 130, 1047-1059, (1999)
[3] H. Koyanaka, Y. Ueda, K. Takeuchi, and A. I. Kolesnikov, Effect of crystal structure of manganese dioxide on response for electrolyte of a hydrogen sensor operative at room temperature, Sensors & Actuators: B, 183, pp. 641-647, (2013)
[4] H. Koyanaka and H. Miyatake, Extracting tritium from water using a protonic manganese oxide spinel, Separation Science and Technology, 50, 14, 2142-2146, (2015)
[5] 古屋仲秀樹, 福谷哲, 宮武秀男, プロトン含有酸化マンガンのトリチウム吸脱着能に対するスピネル型結晶格子定数の影響, 電気化学会第86回大会, 予稿集 2H07, (2019)
[6] H. Koyanaka and S. Fukutani, Tritium separation from parts-per-trillion-level water by a membrane with protonated manganese dioxide, J. Radioanalytical and Nuclear Chemistry, 318, 175-182, (2018)
[7] H. Koyanaka, S. Fukutani, and H. Miyatake, Tritium separation from heavy water using a membrane containing deuterated manganese dioxide, J. Radioanalytical and Nuclear Chemistry, 322, 1889-1895, (2019)
[8] 古屋仲秀樹, 酸化マンガン触媒の水素イオン同位体効果による水中からのトリチウムの分離, 第122回触媒討論会, 予稿集1J20, (2018)
この記事が気に入ったらサポートをしてみませんか?
