
ピアノ調律師のための「錆を化学的に知る」
弦、フレーム、チューニングピン、キーピン、レール、スプーン、蝶板、ペダル...ピアノには多数の金属が使われています。そして金属とは切っても切れない「錆」
金属が錆びるのは酸化するからという程度の認識くらいで、ふと実は錆のメカニズムを正確には把握していないなあと言うことに気づきました。より的確で無駄のないメンテナンスをするためにも、こういったピアノに関する事象を化学的に知っておく必要があると最近は感じています。
と言うことで、こちらの本を読んでみました。
化学的な基礎知識が中学校の理科で止まっている僕にとって最初ははなかなか難しく...Aを知ることでBがわかり、Bの知識でCを知り、CがわかったことでAが本当の意味でわかる...という感じですかね。3周くらい読んでやっと全体がつかめた気がします。
この記事では本を読んで得た知識をまとめています。ピアノのメンテナンスに具体的に役立つ内容と言うよりも、錆を化学的に理解することを目的にしています。化学的に理解していればメンテナンス時の見方が変わるのはもちろん、錆や金属に関する他の資料を読んだ際の理解度がさらに高くなるのではと考えています。
化学の知識はほぼ皆無と言える自分の備忘録としてまとめていますので、全く0の状態からでも読めばわかるようになっていると思います(それゆえに説明不足な部分があったらすみません)。ピアノ調律師向けですが、そうでない方にもご参考になれば幸いです。
「錆」とはなにか
金属が錆びる現象を専門的には腐食と言います。
腐食とは金属が環境の物質と酸化反応して、溶けたり金属以外の物質に変わることで金属が失われる現象で、その結果生成される錆などの物質を腐食生成物と言います。
錆とは腐食で一部が失われた金属に、固体の腐食生成物が付着したものです。
もともと自然界の金属は安定した化合物の状態で鉱石の中に存在しているものがほとんどです。それを精錬によって結合している原子や分子を取り除くことで金属を取り出しているため、金以外の金属は不安定な状態と言えます。
腐食と言うと金属が劣化していく現象のように感じますが、金属が腐食して腐食生成物になろうとするのは、安定して自然に還っていく、摂理とも言えるようです。だからこそ工業製品としての金属は長く安全に使い続けるために、それを防ぐ工夫が必要なんです。
物質の最小単位である「原子」
腐食を化学的に知るためには物質を一番小さい単位まで分解して考える必要があります。
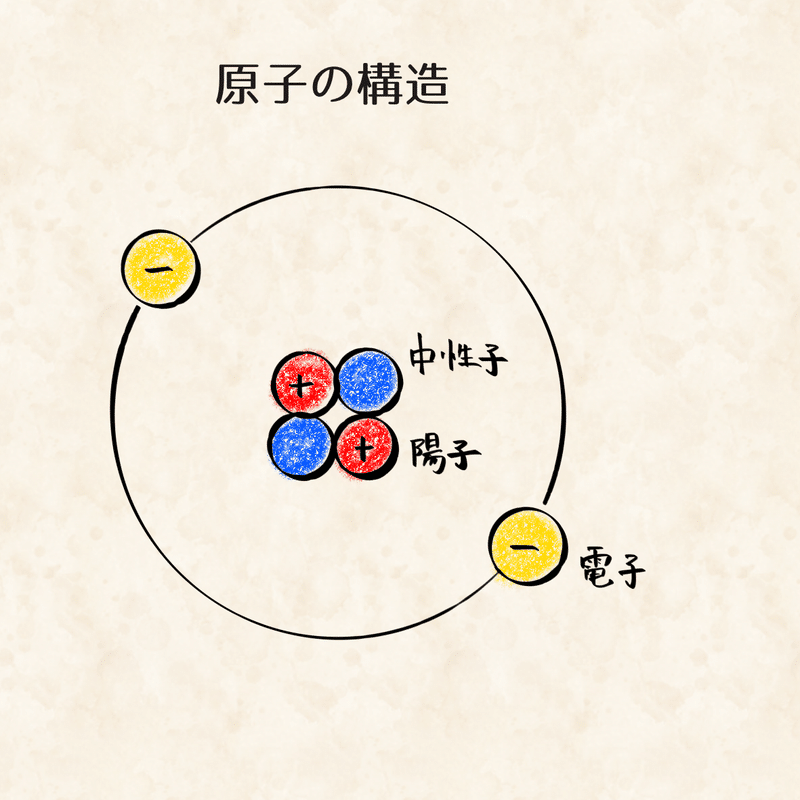
物質の最小単位は原子です。原子は陽子と中性子で構成される原子核と、その周囲の軌道を回っている電子でできています。陽子はプラスの電荷、電子はマイナスの電荷を持ち、それぞれの電荷の量は同じで打ち消し合っているため、原子自体は電気的に中性の状態です。
原子の「イオン化」
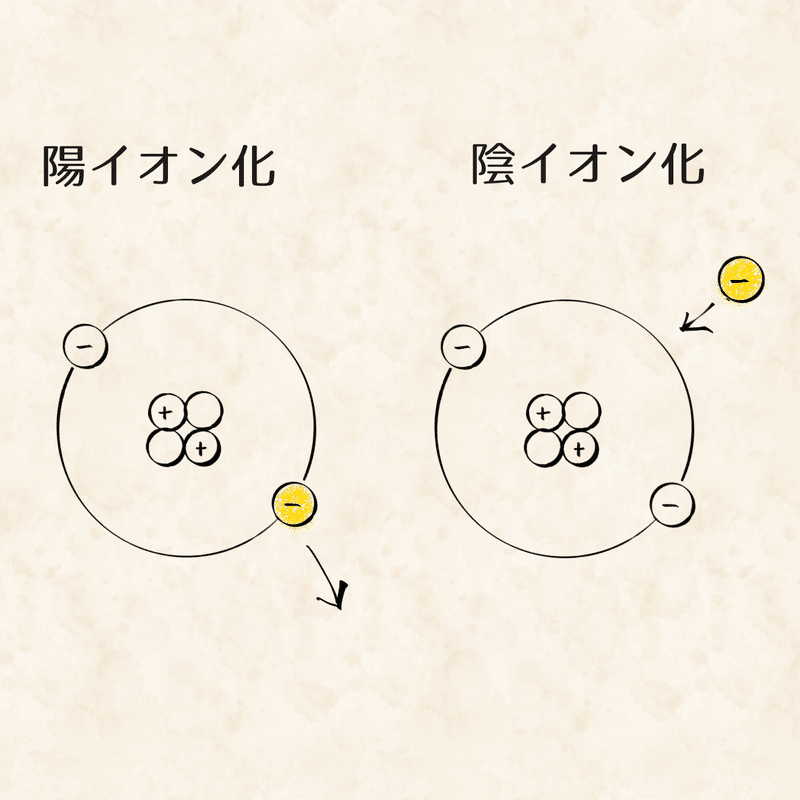
原子からは電子が減ったり増えたりすることがあり、この現象をイオン化と呼びます。
原子はもともと電気的に中性ですが、電子が減ると陽子が多い状態となり、原子全体ではプラスの電荷となります(陽イオン化)。逆に電子が増えた場合、マイナスの電荷が多い状態となります(陰イオン化)
金属の「構造」
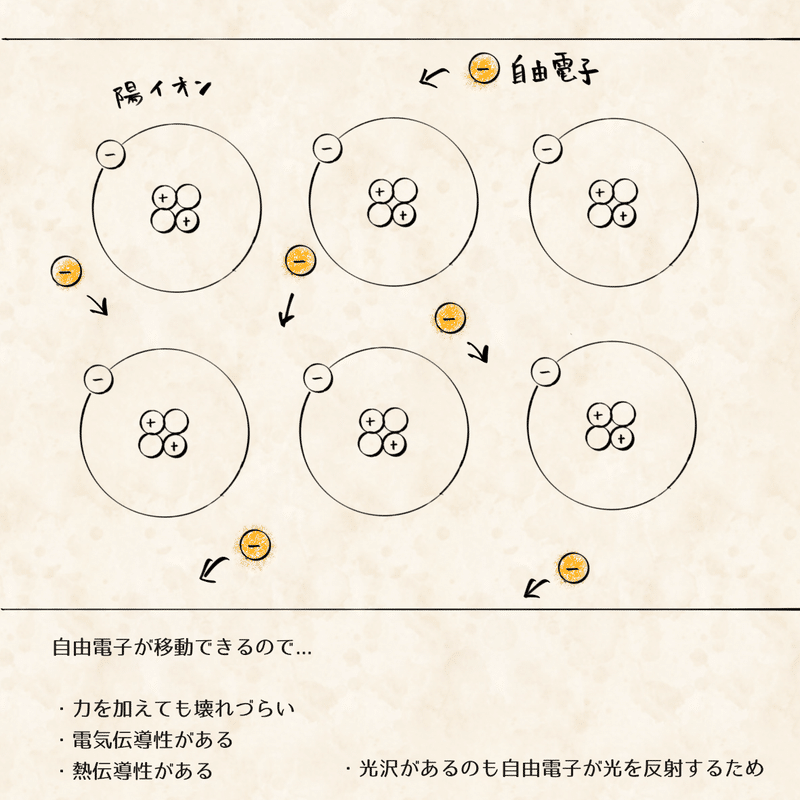
金属は金属原子同士が結合してできています。
金属原子は電子を放出しやすく陽イオン化しやすい性質があります。放出された電子が自由に動き回る自由電子となり、それが陽イオン化した原子同士を繋ぐことで固体としての金属となっています。
金属の特徴である展延性、電気伝導性、熱伝導性、光沢はこの自由電子のおかげなんです。
「電位」の差
電位と言う電気的な位置エネルギーの高さを示すものがあり、電流は電位の高い方から低い方へと流れます。金属にはそれぞれ固有の電位があり、電位が高い方を貴な金属、低い方を卑な金属と呼びます。この電位の差が腐食の反応には重要です。
腐食の起こる「メカニズム」
ここからやっと腐食の話です。一般的な腐食は電気化学反応(電子の授受が行われる化学反応)によって起こります。
その中でもピアノに関係のあるのは湿食という現象。(他には乾食というものがあり、これは火を使うような高温の環境で起こる腐食です)
湿食に必要なものは4つあり...
・金属原子(電位が高いもの)
・金属原子(電位が低いもの)
・水(液体である必要がある)
・酸化物(水の中の溶存酸素が代表的)
これらが合わさると電子の授受が行われ、金属原子がイオン化され腐食が起こります。
単純化したわかりやすい実験として、炭素鋼と白金を導線で繋ぎ、食塩水につけてみます。
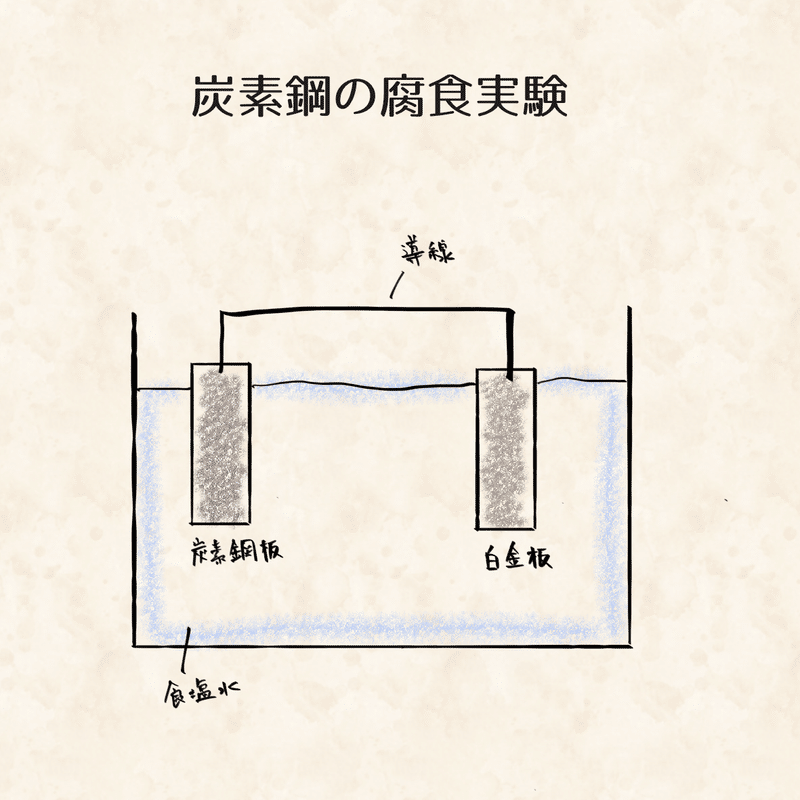
すると電気回路が構成され、炭素鋼(卑)から白金(貴)へ電子が移動し腐食が起こります。具体的にどういうことが起こっているかというと
①炭素鋼から鉄原子が鉄イオンとなって食塩水に溶け出します。(鉄が失われていく)
②炭素鋼から道線を伝わって移動してきた電子を、白金が食塩水と接している面で水と酸素が受け取って水酸化物イオンを生成します。
③ 1で生じた鉄イオン(陽イオン)と、2で生じた水酸化物イオン(陰イオン)がイオン結合(陽イオンと陰イオンが結合する現象)して水酸化第一鉄と言う、腐食生成物ができます。それが酸化して水酸化第二鉄(赤錆)になり、以降様々な化学反応が生じて赤錆としての化合物が生成されていきます。
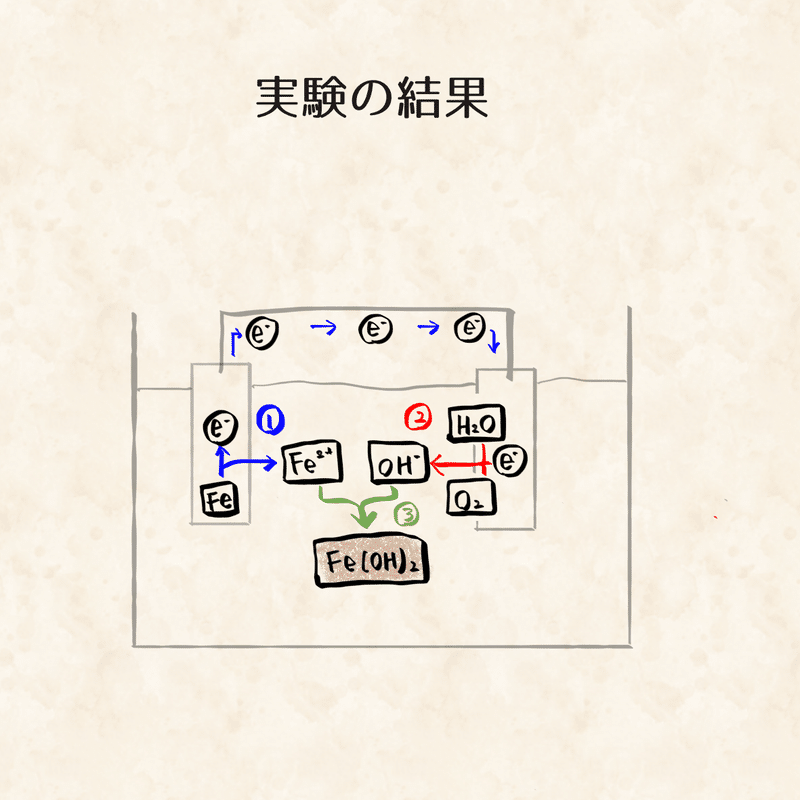
身近なものでは、乾電池の内部で起こっている反応と同じことが起こっている状態です。
「単独の金属」の腐食
上記の実験ではわかりやすく電位の差がある2種類の金属で腐食を起こしていますが、もちろん腐食は単独の金属でも起こります。
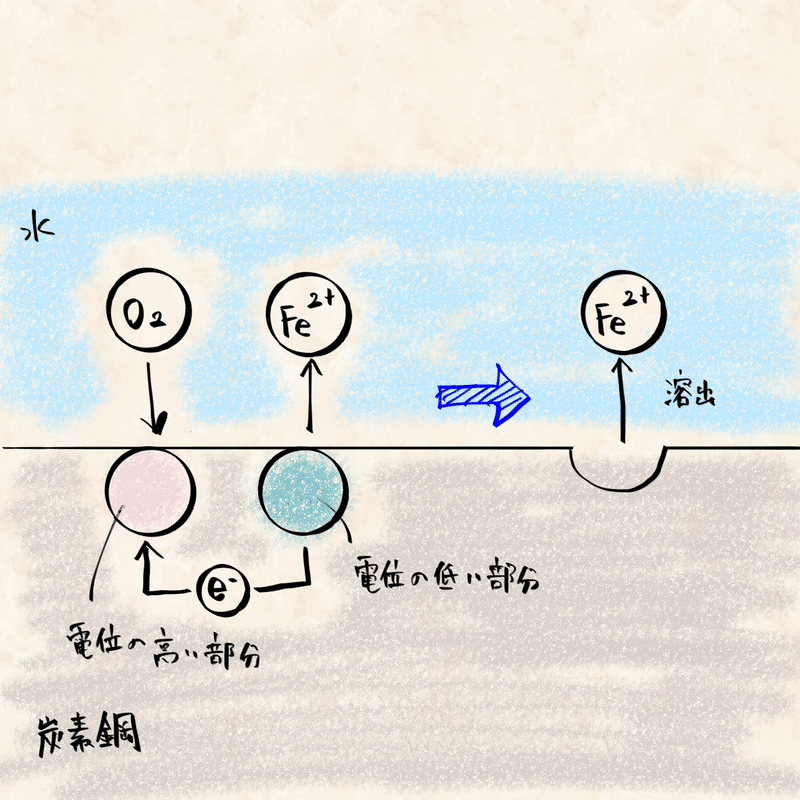
同じ金属内でも金属原子は全てが均一な状態とは限らず、各原子の状態の差が電位の差になって現れることがあります。金属の表面には、電位の異なった原子がランダムに存在している状態です。
そこに水と酸素が存在すると、実験と同じく電位の低い原子から高い原子へ電子が流れ、腐食が起こります。
反応に必要な「酸素」について
酸素は水に溶けた溶存酸素の状態である必要があります。酸素の濃度が高いほど、または水の中を移動する拡散速度が早いほど腐食は早まります。
水温が上昇すると濃度は低下しますが、拡散速度は早くなっていきます。水温80℃までは酸素濃度の低下の影響より拡散速度が速くなる影響のほうが大きいため、腐食速度は早まります。逆に水温が100°Cに達すると酸素濃度が0になるため腐食速度は一気に落ちます。
反応に必要な「水」について
大気中で水を供給しているのは水蒸気です。しかし水蒸気のままでは腐食は起こらず、水蒸気が結露して水になる必要があります。(ただし結露が起こっていなくても、大気中にある程度水蒸気があれば、金属表面は目に見えない水の膜に覆われていることが多いようです。)
空気は温度ごとに含むことのできる水蒸気の量に限界があり(飽和水蒸気量)その量に対する今現在の水蒸気量の比率を相対湿度と呼びます。いわゆる湿度計に表示される湿度のことです。
水蒸気を含んだ空気が冷やされることにより、相対湿度100%を超え含みきれなくなった水蒸気が空気中に水となって現れる現象が結露です。
もちろん部屋の温度が下がることによって結露は起こりますが、部屋の温度低下で生じた水が金属表面の水膜となることは少なく、どちらかと言うと冷えた金属を暖まった部屋に移動させた場合などに、金属と接している部分の空気が冷やされて水膜となることが多いようです。
腐食を促進するもの「塩害」
結露は湿度100%以下でも起こることがあります。
ひとつは塩化ナトリウム、塩化マグネシウム、塩化カルシウムなどの塩化物イオンが金属に付着した場合です。
汗や指紋にも含まれている塩化ナトリウムが金属表面に存在すると相対湿度76〜78%で結露が起こります。さらに塩化カルシウムや塩化マグネシウムの場合は湿度30%前後というかなり低い湿度で結露が起こります。

これらの塩化物イオンは腐食を促進してはいますが、腐食の化学反応には含まれません。塩など自体が腐食するわけではなく、あくまで腐食を促進するもの(腐食促進物)です。
腐食を促進するもの「毛細管」
もうひとつ腐食を促進するのは毛細管の作用です。
孔径がナノ単位の微細な穴の中では水の表面張力が起こり、平面よりも飽和水蒸気量が下がり相対湿度100%以下で結露が起こります。(毛細管凝縮)
ダストと呼ばれるPMなどの物質や工場・建設現場の粉塵、砂などの粒子状物質が金属表面に付着すると毛細管のような隙間ができ、毛細管凝縮が起こります。ダスト自体が多孔質であればその作用はさらに強くなります。

また、金属表面にできた錆自体が多孔質の場合もあり、それによっても毛細管凝縮が起こることもあります。いわゆる錆が錆を呼ぶ状態です。
「応力」と金属の破断
物体に外部から力が作用した際には物体内部に応力という、元の状態を保とうとする抵抗力が生じます。外力と内力は物体が壊れない限り釣り合っているので、外からの力が強いほど応力も強くなります。引っ張られた際に生じるものを引っ張り応力、圧縮された際に生じるものを圧縮応力と呼びます。
金属に与えている引っ張り応力を少しづつ大きくしてくと、ある大きさになったときに金属が破断します。この破断する瞬間の応力を引っ張り強さと呼びます。
引っ張り強さ以下でも応力を繰り返し加え続けると金属疲労という破断に至ります。とうぜん応力は小さいほど破断に至るまで繰り返すことのできる回数は増えていき、 ある応力以下になると、何度応力を与えても金属疲労が起こらなくなる強さがあります。この応力の強さを疲労限と呼びます。
腐食が進める「破断」
しかし、その金属が腐食環境にある場合は同じ応力でも耐えられる回数が少なくなり、疲労限自体も無くなることがあります。こうした腐食による影響を腐食疲労と呼びます。
そもそも物体が壊れる原因のはじまりは主に物体に生じた亀裂です。通常は亀裂が進んでも亀裂の先端が丈夫な部分に到達すればそれ以上進まず破断しませんが、腐食が同時に進行していると丈夫な部分を弱らせるため、亀裂の成長が止まらず破断します。

腐食の「環境要因」
金属の置かれた環境によっても腐食の速度、程度は変化します。環境は大きく4つに分けられます。
臨海大気
海に近いエリアの大気で、塩化物イオンなどが多く、湿度が低くても結露が起こり水膜が形成されやすくなります。
工場大気
工場から排出される石油系燃料由来の硫黄酸化物(亜硫酸ガスが水に溶け硫酸イオンを生成する)の濃度が高く、特に硫酸イオンは塩化物イオンほどではないが腐食を促進します。(特に銅の腐食性生物である緑青には硫酸イオンが含まれていることが多い。)ダスト濃度も高くなっています。
都市大気
自動車の排気ガスに由来する窒素酸化物の濃度が高くなっています。窒素酸化物は太陽光などで酸化し硝酸を生成し、腐食を促進します。エコ自動車や規制により昔に比べれば改善傾向にはあるようです。
田園大気
もっとも清浄な大気で、環境要因での腐食性は低い環境です。

腐食を防止する「不動態化」
ステンレス鋼が腐食しないのは、表面を薄い被膜に覆われているためです。この被膜によって金属表面が環境から遮断されるため、腐食反応が起こらなくなります。この被膜は不動態皮膜と呼ばれ、鉄に添加されたクロムが酸化した薄くて透明な腐食生成物です。つまり、腐食によって腐食から守られている状態です。
不動態皮膜は常に溶解と生成を繰り返し新陳代謝をしています。また部分的に破損しても、水と酸素が存在していれば瞬時に皮膜が修復されるため、長期間耐食性を発揮することができます。

自然な腐食生成物による「保護皮膜」
自然に発生した腐食生成物が腐食から守ってくれることもあります。
流通している10円玉の銅の表面は緻密な酸化銅に覆われ、変色はしていますがそれ以上の腐食から守られています。銅葺き屋根を覆っている緑青にも同様の効果があります。
鉄の黒錆は耐食性を発揮しますが、赤錆は緻密でなく水と酸素を遮断できないため、腐食が継続します。
こうした腐食生成物による皮膜が不動態皮膜と違う点は、被膜が形成されるまでの時間と厚さにあります。
不動態皮膜は瞬時に厚さ1〜3nmの被膜が生成され耐食性を発揮するのに対し、自然な腐食生成物による皮膜は少しずつ厚さが増していき、500〜1000nmに達したところでやっと十分な耐食性が発揮されます。また、一度損傷すると再生には長い時間が必要となります。
「メッキ」による防食
まったく腐食が起こらないようにすることが防食の理想ですが、現実的には難しいです。そこで金属には腐食速度を抑えるためにさまざまな防食処理が施されています。塗装やフィルムなどで覆ったり、メッキを施したりと防食には様々な方法がありますが、ピアノに代表的なものはチューニングピンやセンターピンへのニッケルメッキがあります。

メッキとは材料の表面に金属の薄膜を被覆することです。ここで気をつけないといけないのが、材料となる金属と、メッキ層となる金属の電位差です。
通常メッキ層には貴な金属を使用することが多いため、メッキ層に孔などがあると貴な金属(メッキ層)と卑な金属(材料)が環境にさらされた状態で触れることになるため電位差による反応が起こり、異種金属接触腐食という腐食が起こりやすくなります。
「環境制御」による防食
金属が接している環境から腐食性物質を除去して腐食を防ぐ方法もあります。効果が高いのは水か酸素の除去です。
ある程度閉鎖された空間であれば水の除去は比較的かんたんで、相対湿度55%以下にすれば結露を防ぐことができます。ただ温度差による結露には注意が必要です。ピアノの部屋の湿度を50%前後にすることは、錆づらくするという点でも効果的です。
酸素の除去は小さな密閉空間であれば脱酸素剤などで可能ですが、もちろん人のいる空間では不可能です。

「インヒビター」による防食
環境に薬剤を添加することでの防食も可能です。いわゆる防錆剤がこれにあたり、インヒビター(阻害するもの)と呼ばれます。
気化性防錆剤や防錆油などのインヒビターは一時的な防食のために使用される防錆資材に分類され、必要がなくなったときには比較的容易に取り除けるというメリットがあります。
金属表面に塗ることで効果を発揮する防錆油には石油系の鉱物油や溶剤にインヒビターが添加されています。一般的には吸着型インヒビターのスルホン酸塩、カルボン酸塩、エステル類、金属石鹸類、脂肪酸類などが使用されます。
気化性防錆剤は常温で消化性や気化性のあるインヒビターで、容器や包装内の密閉空間に入れたり、防食対象に散布して使います。アミン類の亜硝酸塩、炭酸塩、カルボン酸塩などが使用されます。
まとめ
錆と金属について調べると、金属の、人工物であるがゆえの頑丈さと脆さを強く感じます。乱暴にまとめるとするならば、調律師ができることはピアノの掃除をしっかりすること、所有者ができることは結露しない環境づくりかなと思いました。
冒頭にも書いたとおり、金属がどのような構造で腐食とはどのような反応が起こっているのか、科学的に知っているかどうかでその後の勉強にも違いが出てくると思います。実際にこの本を読んでから、保管してある錆についての別の資料を読んだところ以前読んだときとは理解度が全く違いました。
この本、カラーの図と説明でものすごくわかりやすく当然この記事よりはるかに詳しく知れますので、興味のある方はぜひ読んでみてください。
もし記事が参考になりましたらスキを押して頂けると励みになります!
