コロナウイルスとの生活(治療薬,ワクチン)
Сергей Нетесов,«Наука из первых рук» № 3(88), 2020 より
■治療薬はどうか?
残念ながら、2020年1月以降、治療用抗体を含む新薬の模索が続いていますが、COVID-19に対してウイルス特異的効果が証明された有効な薬剤はまだありません。
米国食品医薬品局(FDA)で事前承認を受けている製品は、RNAポリメラーゼのウイルス酵素阻害剤であるレムデシビルのみです。エボラの治療のために開発されたこともありましたが、その効果はあまり期待できませんでした。
SARS-CoV-2による肺炎患者の第1陣が、早くも2020年2月に中国で正式に服用を開始したが、その時点では効果が証明されていません。しかし、後にアメリカで行われた2つの臨床試験では、重症期間が15日から11日に短縮され、致死率が20~25%低下するという結果が出ています。しかし、他の2つの臨床試験では、これらの結果は確認されていません。レムデシビルは現在、米国ではCOVID-19治療薬として承認されていますが、ロシアでは登録されていません。
他の薬の有効性も研究されています。インターロイキン-6(IL-6)阻害剤は、免疫反応や急性炎症反応を調整する低分子で、患者の免疫系が「制御不能」のときに、いわゆるサイトカインの嵐を防ぐのに役立ちます。そのような薬には、モノクローナル抗体に基づくトシリズマブが挙げられる。イタリアの医師によると、それは肺炎を予防することで病気の経過を改善し、病気の初期段階で有効です。
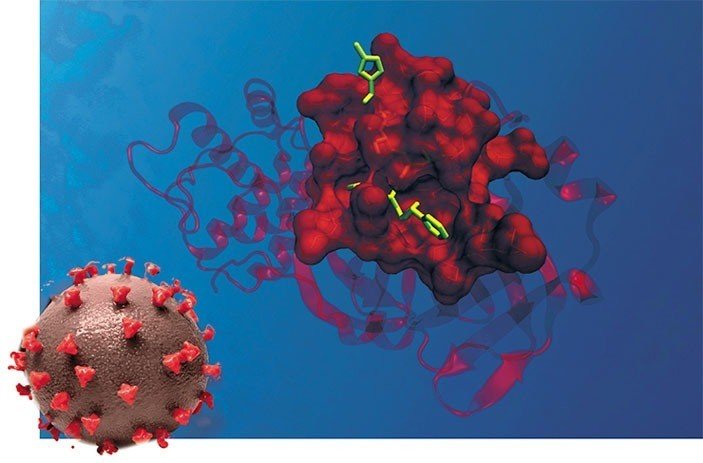
SARS-CoV-2ウイルスプロテアーゼの主酵素と潜在的阻害剤の組み合わせの分子モデル.X線構造解析による.
写真:ツヴィティリオ・クロメナーレ
左:SARS-CoV-2ウイルス粒子.芸術的な構成.写真:NIAID
英国の医師によると 、抗炎症作用と免疫抑制作用を持つ合成グルココルチコステロイドであり、古くから知られているはるかに安価な薬剤であるデキサメタゾンは、サイトカインの嵐を抑制し、重篤な疾患の死亡率を低下させることができます。英国では、この薬は非常にうまく機能しましたが、COVID-19の軽度の症例では、その使用は禁じられています。
抗マラリア薬ヒドロキシクロロキンと抗生物質アジスロマイシンの組み合わせも、ウイルスによる肺炎の治療にテストされました。前者は肺の炎症反応を抑え、後者は付着細菌感染を予防すると考えられていました。しかし、この組み合わせの第一成分の効果のなさを指摘する多くの出版物があり,テストに終止符が打たれました。さらに、ヒドロキシクロロキンとアジスロマイシンは、それ自体で心血管合併症による死亡のリスクを高める可能性があり、このような問題を抱える人々は特にコロナウイルスに対して脆弱です。
免疫不全状態の重症インフルエンザの治療薬として、2015年に日本でアビガンという名前で登録されたファビピラビルをベースにした薬剤に大きな期待が寄せられました(催奇形性効果のため、妊婦には使用できません)。この物質は、レムデシビルのようなRNAポリメラーゼの阻害剤であり、ヒトウイルスではなくRNA含有ウイルス酵素のみに作用する。2020年2月に中国でCOVID-19患者を対象とした臨床試験が開始され、3月に薬効が発表されましたが、その後の説明はありませんでした。
ファビピラビル/アビガンのライセンスは2019年に失効しており、2020年夏にはロシアのメーカー3社からコロナウイルス感染症治療薬として位置づけられている「コロナビル」「アビファビル」「アレプリビル」の3つのファビピラビル系薬剤が国内向けに発売されています。9月には、これらの処方薬がロシアの最低生活レベルに匹敵する価格で小売販売されました。
その有効性については、最近日本でコロナウイルス患者を対象としたファビピラビルの臨床試験の第3フェーズが完了し、平均的な重症度で、摂取により病気の期間が14.7日から11.9日に短縮されることが示されました。これらのデータは、ロシアのパイロット研究の結果と一致しています。中程度および軽度の疾患では、ファビピラビルは「臨床的回復期間を約3.5日短縮し」、鼻腔からのウイルス排除を加速し1~3日短縮することができます。全治療には、体重に応じて40錠1.5~2パックが必要です。

赤外線非接触温度計を使用して人々の健康状態をチェックします。インド。写真:グウィディオンM.ウィリアムズ
■ワクチン接種を受けるや否や?
2020年8月末現在、世界で約160の候補ワクチンが開発されており、そのうち約50は臨床試験のさまざまな段階にあり、そのうち9つはフェーズ3にあります。この段階では、通常、多施設で慎重に管理された研究で、安全性を判断し、実際の流行における薬剤の予防効果を評価するために、大規模な患者グループ(少なくとも1〜3千人)の参加を得て実施されます。
同時に、ロシアと中国の2つのワクチンは、フェーズ3の臨床試験が終了するまで、国レベルでの限定的な使用が許可されました。これは前例のないケースです。
まず、これは、コロナウイルススパイクタンパク質の遺伝子が挿入されたゲノムに第5血清型のアデノウイルスをベースにした中国企業CanSinoBiologicsのワクチンです。フェーズ3の臨床試験は、サウジアラビアの保健省と協議して、サウジアラビアの何万人ものボランティアを対象に8月に開始されました。しかし、早くも2020年6月25日、中国国防省は、一部の軍隊の医師にワクチン接種のために、このワクチンを1年間使用することを正式に承認しました。これが任意接種なのか強制接種なのかは不明です。今日、このワクチンが、アデノウイルスワクチンの中で最も「先進的」なワクチンです。
2つ目の「冬ツバメ」は、M.V.ロマノソフ記念・モスクワ疫学・微生物学研究センターとモスクワ疫学・微生物学研究センターが共同開発した2成分ワクチン「スプートニクV」です。このワクチンは、モスクワの疫学・微生物学研究センター(Gamaleya Research Center for Epidemiology and Microbiology)とロシア国防省の48中央研究所が共同で開発しました。また、コロナウイルス蛋白質遺伝子Sを組み込んだアデノウイルス(第5、26回ヒト血清型)をベースにするこのような方法論に基づいて、この研究センターでは、これまでに我が国のエキゾチックエボラおよび中東呼吸器症候群に対するワクチン候補が開発され、フェーズ1およびフェーズ2の臨床試験に合格しています。
このような組換えワクチンはすべて、比較的無害なウイルスをベースにしており、これらのウイルスは、人体内での繁殖能力を弱める(減衰させる)か、あるいは奪うかのいずれかです。実際、このようなウイルスは、DNAやRNAワクチンの場合のように、病原体の遺伝物質を細胞に送達し、特異的な免疫応答を誘発するためのベクターとなります。このようなウイルスが細胞に入ると、そのDNAが放出されて細胞核に入り、そこでメッセンジャーRNAが合成され、コロナウイルスの表面Sタンパク質を含むウイルスタンパク質が組み立てられます。これらのタンパク質が細胞膜に組み込まれると、細胞は免疫原性になります。つまり、体内で特定の免疫を形成することができます。
スプートニク Vワクチンの特定のアデノウイルスベースに関しては、これらのウイルスが人体での増殖能力をどのように失ったかについての情報はありません。
「スプートニクV」の正式登録は、2020年8月11日に発表されました。これは、臨床試験のフェーズIIIの開始とフェーズ1〜2の結果の公開のほぼ1か月前です。その後、この登録は条件付きで、2021年1月1日まで有効であることが発表され、最終的な登録は、最大4万人が参加することになっているテストの完了後に行われます。

マスクの少女(「サイエンス・ファースト・ハンド」第3号(88)、2020年)写真:ニックアンダーソン
2020年の夏に、コロナウイルススパイクタンパク質をコードするメッセンジャーRNAに基づくさらに2つのワクチンがフェーズ3の臨床試験用にリリースされました。1つは米国の革新的なバイオテクノロジー企業であるModerna社が、もう1つはドイツのBionTech社、米国のPfizer社、中国のFOSUN Pharma社が共同で開発しているワクチン、そして中国で国有製薬企業の参加を得て開発された不活化ウイルスSARS-CoV-2をベースにした3種類のワクチンです。
これとは別に、Sタンパク質遺伝子が挿入された組換えワクチンも注目に値します。これもアデノウイルスに基づいて作成されていますが、ヒトではなくチンパンジーに基づいています。オックスフォード大学(英国)で、英スウェーデンの製薬大手AstraZenecaと共同で開発されました。ステージ3の臨床試験は、8月初旬にブラジル、米国、南アフリカで開始されました。これらのテストのいくつかはロシアで実施される予定との情報があります。
なぜ開発者の中には、組み換えワクチンの基礎としてサルアデノウイルスや希少なヒトアデノウイルスの血清型を選ぶ人がいるのでしょうか?実は、最近の研究によると、かなりの割合の人がすでに共通の血清型5に対する抗体を持っている可能性があるということです。例えば、このような抗体は、がん研究プロジェクトの一環として中国で調査された人の67%、中国の青海省の子供の75%以上、米軍の新兵の4分の1にも見られた。また、このアデノウイルスをベースにしたワクチンが、以前に接触したことのある人にどの程度効果があるかは不明です。
ワクチン製造の世界的リーダーの育成に関連し最低限の宣伝と「PR」をしているのは:米国に本社を置く国際的なバイオ製薬企業メルク・シャープ&ドーム、英国グラクソ・スミスクラインに本社を置く国際的な企業、免疫生物学的製剤の多国籍メーカーであるフランスのサノフィ・パスツール
ロシアでは、さらにいくつかの候補ワクチンが様々な拠点で開発されており、その中には、Rospotrebnadzorの国立ウイルス学・バイオテクノロジー研究センター「Vector」(Koltsovo、ノボシビルスク州)、A.A. Smorodintsevインフルエンザ研究所(サンクトペテルブルグ)、M.P. Chumakov免疫生物学的製剤の研究開発のための連邦研究センター(モスクワ)などが含まれています。また、ロシアでワクチンを生産するために、外国の開発者との交渉が進んでいます。ということで、2021年には選択肢が出てきます。
■ワクチンの2ショット
「スプートニクV」の使用説明書には、臨床試験のフェーズ1の結果から、発生頻度の点で有害事象(AE)は、頻繁かつ非常に頻繁に発生していると見なせます。ワクチン接種後、次のAEが記録されました:一般的な障害と反応注射部位:高体温、痛み、浮腫、ワクチン接種部位のかゆみ、無力症、倦怠感、発熱、ワクチン接種部位の皮膚温度の上昇、食欲減退。神経系障害:頭痛、下痢。呼吸器系、胸部および縦隔器官からの障害:中咽頭の痛み、鼻のうっ血、喉の痛み、鼻漏。現在の臨床試験でワクチンの投与量を減らすことにより、これらの現象を減らすことができる可能性があります。
実際のワクチンの保護効果は、20年9月に始まったフェーズ3の臨床試験で検討されるためまだ評価されていません。この場合は破られましたが臨床試験のフェーズ3は通常のアルゴリズムで行います。フェーズ2の試験では、通常、薬剤の投与量が変化するが、既に公表されているスプートニクVの臨床試験結果では、そのようなデータは得られていません。
ワクチン「Gam-COVID-Vac」(「ScienceFirstHand」No.3(88)、2020)
フェーズ3に関しては、独自の規則があります。各テスト参加者には「幸福」の特別な日記が与えられ、セラピストが割り当てられます。すべてのテスト参加者は少なくとも4つのグループに分けられ、そのうちの1つはワクチンの代わりにプラセボを投与され、もう1つは同様のワクチン製剤、3つ目はワクチン自体、4つ目は可変用量などです。スプートニクVの場合、前例のないことに直面し、臨床試験のフェーズ3の開始を待たずに、2020年9月8日、ロシア保健省は、ワクチンの最初のバッチを民間循環に放出する許可を発表し、地域を含むリスクグループからの集団の大量ワクチン接種が計画されています。
ちなみに、「スプートニクV」の指示には、子供だけでなく、主なリスクグループである60歳以上の人(75歳以上の人の死亡率は20~30%)にもワクチンを使用してはいけないと書かれています。
以下略・・・・・
■氷山の水面下にあるもの・・・・・
■文献・・・・・
この記事が気に入ったらサポートをしてみませんか?
