100年前の「スペインかぜ」パンデミック
<第6回>
インフルエンザウイルスによる歴史的なパンデミックが、1918〜1919年にかけて流行した「スペインかぜ」だ。スペインは発生国でもないし、最大の流行国でもなかったが、ヨーロッパは第一次世界大戦の真っただなかで、参戦国では報道統制により感染者や死者の報告が公表されなかった。それに対して中立国であったスペインでは統制がなかったため、まるでスペインだけで流行していたように見えた。それで、スペインにとっては不名誉なことだが、こう呼ばれるようになったのだ。
最初のアウトブレイクが起こったのは、アメリカだった。1918年3月4日、アメリカ・カンザス州のファンストン陸軍駐屯地で1人の兵士が発熱、頭痛、首や背中の痛みを訴えて駐屯地内の病院を受診した。これがスペインかぜの最初の記録とされている。この時点で同駐屯地内にはすでに多数の感染者が出ており、さらにふえつづけたため、駐屯地内に航空機用格納庫を利用した緊急病棟を建設しなければならなかった(写真)。

出典:National Museum of Health and Medicine
その前年に第一次世界大戦参戦を決定したアメリカは、招集兵が滞在し訓練する施設として、全土に40か所の駐屯地を設けた。ファンストンはそのなかでも最大規模の駐屯地だった。ヨーロッパに渡る前には、東部にある別の駐屯地で一時的に過ごすこともあって、そこでも感染が広がった。兵士たちは駐屯地から戦場であるヨーロッパに送られたが、そのなかにはスペインかぜに感染した兵士が少なからずいた。
密閉状態でおおぜいの兵士がひしめきあう輸送船の船倉は、インフルエンザウイルスにとって願ってもない環境だった。兵士たちが降り立ったフランスの港で感染が広がり、さらにそこから前線へと伝わるのに、わずか数週間しかかからなかった。第一次世界大戦は1918年11月に休戦したが、そのかんにウイルスは変異を繰り返し、それぞれの国に帰還する兵士がそのウイルスを持ち帰ることになった。こうしてスペインかぜは世界中に広がった。
スペインかぜには、大きく分けて3つの波があった。第1波は、アメリカの駐屯地からヨーロッパに感染が広がった1918年の春から夏にかけて。第2波は、変異した強毒性ウイルスが世界中にまん延した18年8月後半から年末にかけて、第3波は休戦後の1919年年明けから夏にかけてである。日本の第3波は遅れて1920年1月に発生した。結局、パンデミックの終了までに、世界全体で約5億人がスペインかぜに感染し、1740万人〜1億人(研究によって幅がある。表参照)が死亡した。世界保健機関(WHO)は、当時の世界人口(約18億人)の25〜30%がこの感染症に罹ったと推測している。死者1740万人としても、世界人口の1%近くが死亡したことになる。感染者数は第1波が最大だったが、死者数は第2波が最も多かった。日本では、パンデミック期間中に約2380万人が感染(ただし複数回感染した人がいるので実数はこれ以下と思われる)、約39万人が亡くなったとされる(当時の内務省衛生局の統計による)。当時の日本の人口は5700万人程度なので、全国民の42%近くが感染し、6.8%が死亡したことになる。超過死亡数から試算すると死者数は45万人に達するという推計もある[1]。
日本ではスペインかぜと呼ばれるが、英語ではスパニッシュ・フルー、つまり「スペイン・インフルエンザ」である。ただしこの当時、インフルエンザがインフルエンザウイルスによる感染症であることはわかっていなかった。インフルエンザは、細菌の一種「インフルエンザ菌」によって引き起こされると考えられていたのだ。実際に、スペインかぜの患者からは高い比率でインフルエンザ菌が検出されたが、これは二次感染したものと考えられる。日本では、スペインかぜ流行時にインフルエンザ菌ワクチンが開発されたが、当然ながらスペインかぜに効果はなかった。
ウイルスは細菌よりも圧倒的に小さく、光学顕微鏡では確認できない(ただし近年になって細菌と同等かそれ以上の大きさで、光学顕微鏡でも観察可能なウイルス──メガウイルスやパンドラウイルスなど──が発見されている)。1898年に、タバコモザイク病になったタバコの葉の抽出液を細菌分離用のろ過器にかけたところ、ろ過器をすり抜けた液体のなかに正体はわからないがタバコモザイク病を引き起こす病原体が含まれていることがわかった。発見者のマルティヌス・ベイエリンクはこの病原体を、ギリシャ語で毒を意味する「ウイルス」と呼んだ。同じ年には、家畜の病気である口蹄疫のウイルスも分離された。インフルエンザの病原体がインフルエンザウイルスであると解明されたのは、1933年のことである。
表 過去のインフルエンザ流行による死者
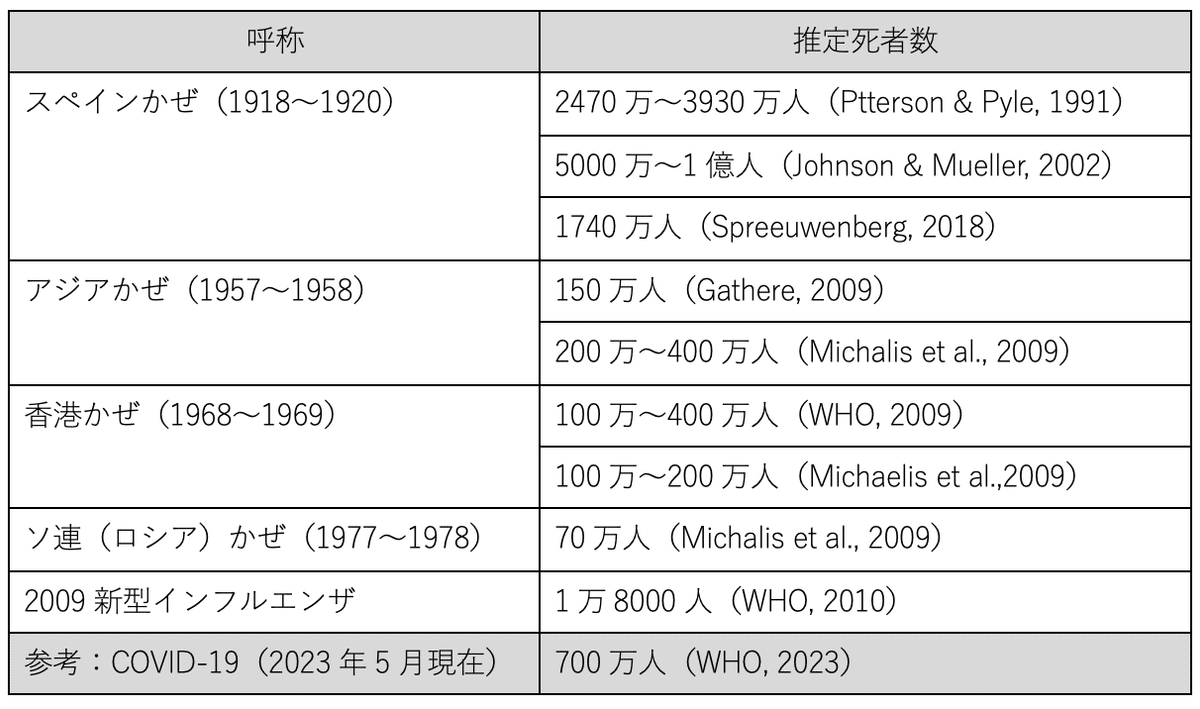
インフルエンザによるパンデミックは、その後3回繰り返されている。「アジアかぜ(アジアインフルエンザ)」(1957〜1958年、発生地は中国南西部)、「香港かぜ(香港インフルエンザ、発生地は香港)」(1968〜1969年)、そして2009年の新型インフルエンザである。2009新型インフルエンザは、メキシコで流行がはじまり、世界70か国以上に感染者が広がった。家畜のブタ由来だったことから「豚インフルエンザ(スワイン・フルー)」とも呼ばれた。
インフルエンザウイルスにはA型、B型、C型、D型の4つの型があり、このうちB型はヒトとアシカ亜目、C型はヒトとブタにしか感染しない。D型はウシやブタなど動物に感染症を引き起こすが、ヒトには感染してもほとんど発症しないと考えられている(ただし見逃されている可能性もある[3])。一方A型は、鳥にもほ乳類にもヒトにも感染する人獣共通感染症だ。
A型インフルエンザウイルスは、本来水鳥に感染するウイルスであることがわかっている。カモなどの水鳥の腸内には、多くの種類のインフルエンザウイルス(鳥インフルエンザウイルス)が感染している。これらのウイルスは糞とともに水中に落ち、その水を飲んだ他の水鳥が感染する。しかし、感染しても水鳥にはほとんど症状が出ない(「不顕性感染」)。鳥インフルエンザウイルスと水鳥類は長く共生してきたためだ。ところが、このウイルスがニワトリなど他のグループの鳥類に感染すると様相が一変する。鶏舎の近くを訪れた水鳥の糞に含まれるウイルスは、ホコリとともに舞い上がる。それをニワトリが吸い込み、呼吸器官に感染するとインフルエンザを発症する。このうち重い症状を呈して、高い比率でニワトリを死亡させてしまうものを高病原性鳥インフルエンザという。近年、冬季に世界各地で抗原性鳥インフルエンザが発生し、養鶏産業に大きな被害を与えている。2022−23シーズンの日本の事例件数は過去最大となり、飼料高騰と相まって鶏卵の価格が高騰した。
鳥インフルエンザウイルスは、家畜のブタやウマ、ペットのイヌなど動物に感染して発症させることもある。ニワトリ、家畜、ペットと濃厚に接触した人間にも感染リスクがある。
スペインかぜを引き起こしたのは、A型のうちのH1N1亜型(A/H1N1)だが、これも鳥起源だったことがわかっている。アジアかぜはH2N2亜型、香港かぜはH3N2亜型で、これらも、もともとは鳥インフルエンザだ。A型は何十年かおきに大規模な感染流行を繰り返すという特徴がある。その流行がおさまると、その亜型ウイルスは季節性インフルエンザとして秋〜冬に流行を繰り返すようになるとともに、それまでの季節性インフルエンザの亜型を駆逐してしまう「不連続抗原変異」という現象が見られる[4]。アジアかぜパンデミック後には、H2N2がそれまでのスペインかぜ由来季節性インフルエンザ・ウイルスH1N1にとって代わり、季節性インフルエンザ「Aアジア型」になった。H3N2は、香港かぜパンデミック収束後に「A香港型」となって「Aアジア型」を駆逐した。
奇妙なことに、香港かぜパンデミック後にいったん消滅したH1N1は1977年に「ソ連かぜ(ロシアかぜ)」として復活、その後季節性インフルエンザ「Aソ連型」になった。そのゲノムは、1950年代まで流行していたスペインかぜ由来の季節性H1N1とまったく同じものだったという[5]。真相は明らかになっていないが、保管されていたウイルスの人為的な漏出があったのだろうと推測されている。ただし、2009新型インフルエンザ(H1N1亜型)の流行で、このAソ連型も姿を消したと見られる。2023年現在流行しているA型季節性インフルエンザは、H3N2亜型とH1N1亜型(2009新型インフルエンザ由来)である。
このようにA型インフルエンザウイルスは季節性インフルエンザウイルスとして重要なだけでなく、いずれまたパンデミックを起こす可能性があるウイルス群として監視の対象になっている。鳥インフルエンザウイルスが、水鳥やニワトリ、ブタなどの家畜、そしてヒトのあいだを行き来するうちに、ヒトに対して高い感染性と強毒性(高病原性)を獲得した変異株が出現するおそれがあるからだ。
実際、近年になって鳥インフルエンザのヒトへの感染はたびたび起こっている。
1997年5月、香港で3歳の男児が亡くなった。診断はインフルエンザで、重いウイルス性肺炎を起こしていた。ところが患者から分離されたインフルエンザウイルスは、これまで人が罹ったことのあるどの亜型とも一致しなかった。ようやく突き止められたウイルスは、ニワトリに重い症状を引き起こし高い確率で死に至らせる、高病原性のH5N1亜型インフルエンザウイルスだった[6]。
当時香港では、複数の養鶏場でH5N1高病原性鳥インフルエンザが発生していた。その年の11月〜12月には同じ香港で、17人がH5N1亜型インフルエンザに罹患し、そのうち5人が死亡した。これをきっかけにして、H5N1亜型が新型インフルエンザパンデミックを引き起こしうるとして俄然注目を集めるようになった。このときはニワトリの大量殺処分によりそれ以上の感染拡大を防ぐことができたのだが、H5N1は変異を繰り返しながらアジア全体に広がり、2000年代以降たびたびニワトリへの感染流行を引き起こした。2005年にはインドネシアで、国家緊急事態宣言が発出されるほど大規模な流行があった。ニワトリ以外の鳥や家畜、ヒトへの感染も繰り返し起こった。さらに野生の水鳥の移動(渡り)によって世界中に運ばれた。
A/H5系統の高病原性鳥インフルエンザウイルスは、2022年の段階でH5N1、H5N2、H5N3、H5N4、H5N5、H5N6、H5N8の7つの亜型がアジア、ヨーロッパ、アフリカ、北アメリカから報告されており、そのうちH5N1、H5N6、H5N8のヒトへの感染例が報告されている[7]。H5N1型のヒトへの感染者数は、2003年〜2022年に、中東、アフリカ、アジア、ヨーロッパなど19か国で864人となっており、うち456人が死亡していて、死亡率が高い。
先述のように、2009年に新型インフルエンザパンデミックを引き起こしたのは、A/H5系統ではなく、スペインかぜと同じA/H1N1亜型だった。
ブタは、鳥とヒトの間をつなぐ役目をもつと考えられている。高病原性鳥インフルエンザウイルスとヒトの季節性インフルエンザウイルスがブタに同時感染し、ブタの体内で両者の遺伝子組み換えが起こって、高病原性とヒトに対する感染性をあわせもつ新たなウイルスが生まれる可能性があるのだ。
2009新型インフルエンザウイルスの誕生にも、ブタが大きくかかわっていた。ブタのあいだでは、H1N1、H1N2、H3N2の3亜型の変異株が循環していることがわかっている。ウイルス学者で東京大学医科学研究所の河岡義裕博士によると、もともとは、スペインかぜパンデミックを引き起こしたH1N1がブタに感染、そのまま「豚インフルエンザウイルス」(クラシカルスワイン)として感染がつづいていた。90年代後半に、クラシカルスワイン、鳥インフルエンザウイルス、A香港型(H3N2)インフルエンザウイルスがブタに同時感染、ブタの体内で3種類のウイルスの遺伝子が混じり合った「混合ウイルス」が生まれ、これが北米のブタに流行した。一方で、ヨーロッパでは70年代末からブタのあいだに鳥由来の別のインフルエンザウイルスが流行していた。このウイルスと3種混合型インフルエンザウイルスがブタに同時感染し、混じり合って、2009新型インフルエンザウイルスが生まれたのだという[8]。
こうした、同時感染によるウイルスの混合を「遺伝子再集合(リアソートメント)」と呼ぶ。実は1957年のアジアかぜウイルス、1968年の香港かぜウイルスも、ヒトインフルエンザウイルスと鳥インフルエンザウイルスの遺伝子再集合によって生まれたことがわかっている。3種類、4種類のウイルスの遺伝子再集合は珍しい現象だというが、今後も起こりうる。
2009新型インフルエンザ感染による死亡者の80%は65歳未満だったと推計されている。2009新型インフルエンザウイルスは1950年代まで流行していたH1N1の遺伝子をもっているため、その感染経験がある高齢者には、免疫をもつ人が多かったためと考えられる。
ブタはイスラム圏を除き世界中で飼育されており、大規模な養豚場もあれば、庭先で自給的に飼育されるブタもいる。後者の場合、同時にニワトリやアヒルなど家禽が一緒に飼われていることも多く、人間、ブタ、家禽が日常的に密に接している。
高病原性鳥インフルエンザウイルスに感染したニワトリやヒトの体内でウイルスが変異したり、ヒト季節性インフルエンザウイルスや豚インフルエンザウイルスと高病原性鳥インフルエンザウイルスに同時に感染したヒトの体内で遺伝子再集合が起こったりして、ヒト−ヒト感染を引き起こすようになることもありうる。こうして出現した新型インフルエンザウイルスに対する抗体を、人類はもっていないため、いったんヒト−ヒト感染するようになれば、爆発的な感染拡大が起きかねない。
鳥インフルエンザ・ウイルスを保有する水鳥の多くは渡り鳥で、夏にシベリアなど大陸北部・内陸部で繁殖、冬には越冬のために南下する。その経路はときに南北両半球にまたがる。これらの鳥は繁殖地でも、越冬地でも、あるいは経由地でも、集団で過ごすことが多く、東アジア、南アジア、ヨーロッパ、アフリカなど別々の越冬地から飛来した鳥たちが、狭い範囲に同時に滞在することも少なくない。そこで感染が広がり、ウイルスを持ったまま渡りをして、その先でまた感染を広げる。このようにして1羽の体内で生まれた新しいウイルスは、数シーズンのうちに世界中に広がってしまうおそれがある。<つづく>
[1] 奥積雅彦:統計報告書で見る我が国でのスペイン風邪の被害状況、統計図書館ミニトピックスNo.30
[2] Max Roser:“The Spanish Flu (1918-20): The Global Impact of the Largest Influenza Pandemic in History”, Our World in Data, March 04, 2020
[3] 村上晋, 堀本泰介:特集ウイルス研究の最前線3. 新しい―D型―インフルエンザウイルス, ウイルス, 67(2), 2017
[4] 国立感染症研究所:インフルエンザとはhttps://www.niid.go.jp/niid/ja/kansennohanashi/219-about-flu.html
[5] 河岡義裕:『新型インフルエンザ 本当の姿』、集英社新書、2009
[6] ロバート・ウェブスター(田代眞人・河岡義裕訳):『インフルエンザ・ハンター』、岩波書店
[7] 国立感染症研究所:鳥・ブタインフルエンザウイルスのヒト感染事例の状況について、https://www.niid.go.jp/niid/ja/diseases/a/flua-h7n9/2276-a-h7n9-niid/11103-avianswineflu-220422.html
[8] 河岡義裕:『新型インフルエンザ 本当の姿』、集英社新書、2009
この記事が気に入ったらサポートをしてみませんか?
