薬物ナノ粒子をT細胞に結合させて腫瘍組織へとデリバリーする技術
Twitterでは毎日論文紹介をパワーポイントで紹介中
https://twitter.com/kensho_2021pham
Twitter検索ワード
けむ論文紹介(スペース)61
タイトル
T cell-targeting nanoparticles focus delivery of immunotherapy to improve antitumor immunity
https://www.nature.com/articles/s41467-017-01830-8
【背景】
生体内T細胞を薬物送達キャリアとして用いることでリンパ組織へ薬物送達するシステムを以前紹介した。またT細胞などのリンパ球は血中を循環しており、静脈内投与するナノ粒子と出会う確率が高いのでキャリアとして適している。
実際に、こうしたキャリアを用いずにナノ粒子をガン細胞に対して直接的に狙うような試みも行われているようだが、あまり効率が良くガン細胞にデリバリーできていないという現状がある。
今回の論文では、CD8陽性T細胞に発現しているPD-1を標的として、T細胞に薬物ナノ粒子をくっつけて、腫瘍組織など広範に送達するテクノロジーを考案した。
【結果】
抗体―薬物複合体ナノ粒子の開発
著者らは、PLGAを粒子核としたマレイミド-PEGナノ粒子を用いた。PEGやPLGAは古くより生体適合性の高い高分子ポリマーとして用いられており、これまでにも何度が登場したナノ粒子成分である。マレイミドはSH基との結合リンカー化合物である。抗体のFc領域切断部(IdeZプロテアーゼ)のSH基とマレイミドを共有結合させた(図参照)。ちなみに、PLGAはFDAにより推奨されているポリマーらしい。
※FDA: Food and Drug Administrationは、アメリカ食品医薬品局のことで、薬の安全性を取り締まる機関であり、医薬品を販売する際に申請し承認が得られなければ販売することができない。
話はそれたが、抗体としてCD8aやPD-1抗体を使用することで特定細胞を標的としたナノ粒子が完成した。
PD-1抗体ナノ粒子
PD-1シグナル(免疫チェックポイントシグナル)はT細胞のガン細胞傷害性を弱めるため、PD-1抗体によりこれらの抑制シグナルも阻害されることが期待された。PD-1抗体結合ナノ粒子はPD-1発現T細胞との結合が確認された。
PD-1抗体―TGF-β阻害薬ナノ粒子による抗腫瘍効果
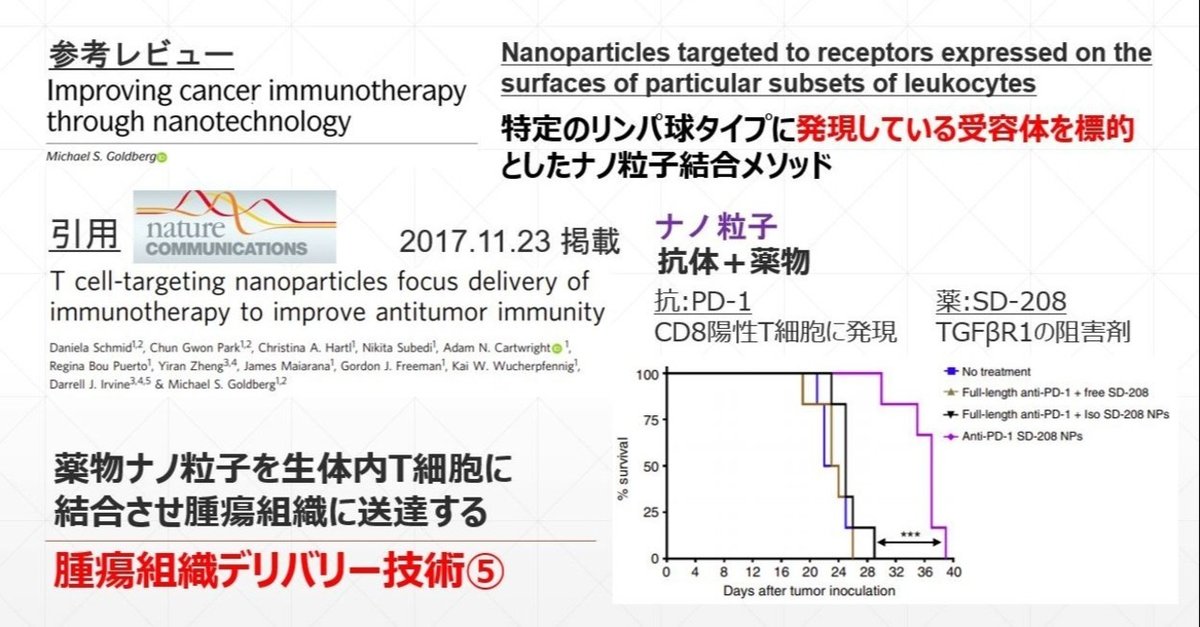
TGF-β受容体1の阻害薬物(SD-208)は疎水性であるため、脂溶性の高いナノ粒子に組み込むことは容易である。PD-1抗体SD-208ナノ粒子は、T細胞へのTGF-βシグナルを抑制した。そこで、以下の4群を用いてPD-1抗体SD-208ナノ粒子の効果を確かめた。
①無処置(コントロール)
②PD-1抗体とSD-208阻害剤
③PD-1抗体とアイソタイプ抗体SD-208ナノ粒子
④PD-1抗体SD-208ナノ粒子(今回の目玉)
マウスにガン細胞(MC38)を摂取した5日後に①~④を静脈内投与したところ、④でのみ腫瘍増殖の遅延とマウス生存率の改善が認められた。つまり、T細胞にナノ粒子を結合させSD-208を全身送達することが有用な手法であることを示した。
PD-1抗体―TLR7/8作動薬ナノ粒子による抗腫瘍効果
上記の結果を考えると、他の薬物もT細胞をキャリアとして送達できるのではないかと考えられる。TLR7/8作動薬(R848)を用いると、
CD8陽性T細胞の腫瘍組織への浸潤が高まった。さらにPD-1抗体―TLR7/8作動薬ナノ粒子の投与によって、腫瘍増殖の遅延とマウス生存率の改善が認められた。
【感想】
T細胞は全身巡っており、炎症部位や腫瘍組織にはケモカインなどで遊走される身体の仕組みがある。こうした生理的機能を利用したT細胞キャリアによる薬物の送達は理にかなっていると思う。
また、T細胞へのナノ粒子の結合に抗体分子、特にPD-1抗体を利用したことで、免疫チェックポイント阻害とナノ粒子結合の両方を叶えた点は画期的だと思う。
またナノ粒子に関しては、TLR7/8のアゴニストやTGF-β受容体阻害剤など幅広い薬剤との組み合わせの可能性が示されており、治療の幅が広いのは良いことだと思う。
ナノ粒子については徐放性医薬品基材であるPLGAを用いることで長期的な薬剤放出が可能となっているようで、ナノテクノロジーの技術には驚かされる。T細胞キャリアの研究にここ数日で魅力を感じている。
