
分子の形【改】
※期間限定無料。本記事は電子書籍出版後に有料記事になります。予めご承知おきください。2021/8月現在
分子のカタチには、直線形、折れ線形、三角錐形、正四面体形 などがあります。

「どの分子がどのようなカタチになるのか」を覚えてしまうのもアリです。しかし、ある考え方を1つだけ理解しておくと、ある程度予測を立てられるようになります。
それは、電子対反発則 です。分子内にある 電子対どうしは、電気的な反発によって互いにできるだけ離れようとします。電子対どうしは、-の電荷をもっているためだと捉えてください。
二重結合や三重結合のそれぞれの電子対は、まとめて1組の電子対とみなして考えてよいです。
メタン分子CH4 は 正四面体形 になります。
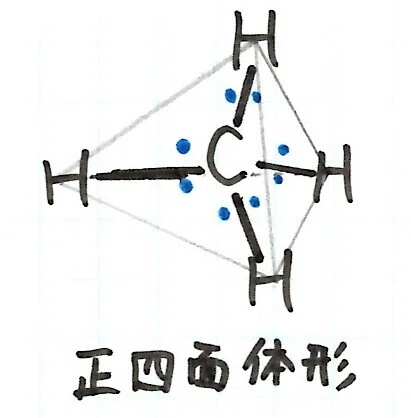
炭素原子Cのまわりに4組の共有電子対があります。電子はマイナスの電荷をもっているため、電子対どうしは反発します。メタンの場合は、4組の共有電子対が互いに反発するため、それぞれができるだけ遠い距離を取ろうとして 正四面体 になります。

アンモニア分子NH3 は 三角錐形 になります。

窒素原子Nのまわりに3組の共有電子対と1組の非共有電子対があります。1組の共有電子対と3組の非共有電子対が反発して、正四面体のカタチをとろうとします。しかし、Hは3つしかないため、結果的に三角錐形になります。

水分子H2Oは 折れ線形 になります。

酸素原子O のまわりに2組の共有電子対と2組の非共有電子対があります。これらの4組の電子対が反発して、正四面体のカタチをとろうとします。しかし、Hは2つしかないため、結果的に折れ線形になります。

二酸化炭素分子CO2は 直線形 になります。

炭素原子C は不対電子が4コ、酸素原子O 1コは不対電子を2コもっています。C原子から4コ、O原子2コからは合計4コの不対電子があることになります。これで、共有電子対2組が2つあることになります。共有電子対2組を大きな1組の電子対と見なすと、大きな1組の電子対どうしの反発によって、直線形 になります。
○まとめ
分子内にある電子対どうしは、電気的な反発によって互いにできるだけ離れようとします。分子のカタチには、直線形、折れ線形、三角錐形、正四面体形などがあります。
この記事が気に入ったらサポートをしてみませんか?
