
重症患者の栄養管理
勉強会で使用したスライドをほぼ流用した記事になります。スライドだけでは説明が不十分とか、わかりづらそうな部分に関しては解説しました。今後の診療の一助になれば幸いです。
はじめに

重症患者の治療は救命から長期予後を見据えた時代に突入しました。ICU-AWを含めたPICSを考慮したICU入室早期からの治療(栄養療法やリハビリテーション)が求められています。今までは救命すればいいって考えでしたけれども、その後の在宅を見据えた治療をちゃんとしましょうねってことなんです。
そんな中、2020年度より特定集中治療室における早期栄養介入管理加算が新設されました。この記事ではこの加算の条件にもある、日本版重症患者の栄養療法ガイドライン(J-CCNTG)を復習しつつ、最近のトピックについて触れたいと思います。
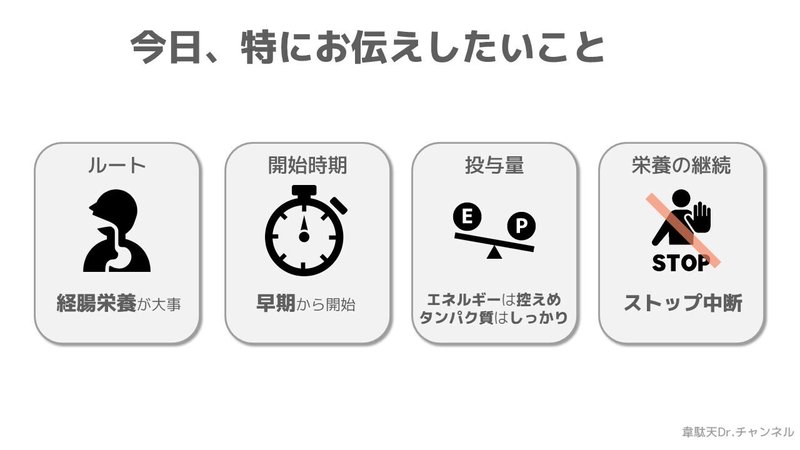
長文読むのが苦手な方は、こちらがこの記事でどうしてもお伝えしたい内容ですので、ぜひ覚えておいていただければと思います。
早期栄養介入管理加算

こちらは厚労省の資料[1]で早期栄養介入管理加算の内容になります。ビジーなので少し分解して解説していきます。

後ほど触れますが、在宅復帰を推進する観点っていうのが重要です。早期に栄養管理をすると色々といいことがあるんですが今回の加算のポイントの一つが在宅復帰だと思います。

1人当たり最大7日間×400点ですから、いわゆるNST加算の1週間で200点とはけた違いの加算です。それだけICUにおける栄養療法が重要と国も考えているのでしょう。


留意事項を見てみますと、
日本集中医学会のガイドラインに準拠しなさいよ!
とのことです。ですので、この後しっかり復習しましょう!

施設基準を満たすには特定集中治療室とNSTでの経験が3年以上ある管理栄養士が専任(専従より緩い基準でほかの業務もできる)で配置されていることです。
では、なぜこのような加算が新設されたのでしょうか?

こちらは、一般的な医薬品の経腸栄養剤、PPN・TPN製剤の薬価、熱量、タンパク質の量を表にしたものです[2–5]。栄養剤は安いのではという気がしますが少し比較が難しい表です。
そこで、コストをしっかり比較するために、一日に投与するよくある熱量1500kcal当たりの薬価を計算してみました。
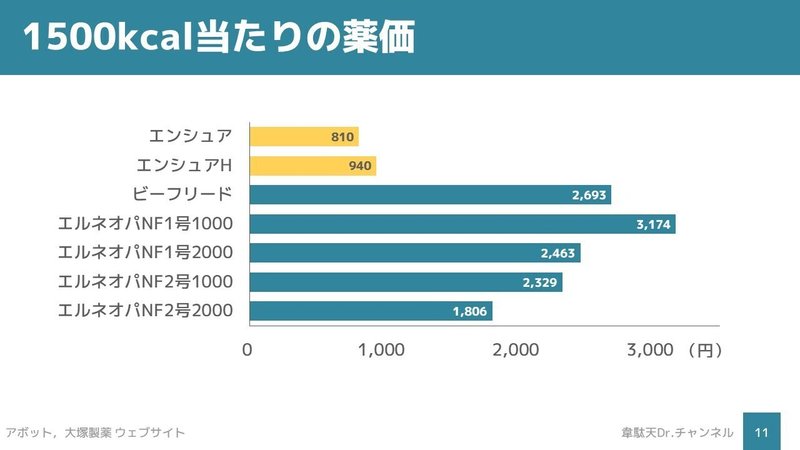
経腸栄養剤がPPN/TPN製剤に比べて50%以下のコストということがわかります。国が経腸栄養を進めたい理由の一つはこういった経済的な部分なのだと思います。
もう一つは、経腸栄養(EN)と静脈栄養(PN)でどちらが感染を抑制するかという点が、ENとPNを比較するうえで重要です。
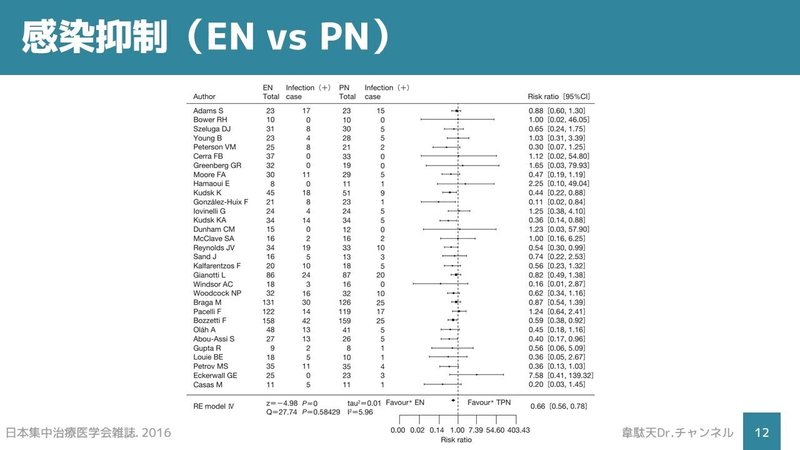
このメタ解析[6]によると、ENはPNに比べて感染抑制効果があるという結果でした。コスト面のメリットも大きいですね。
今回の加算では在宅復帰は目的の一つだったわけですけれども、ICUにおける栄養管理はその後の在宅につながります。今までは助ければよかった重症患者さんも、医学の進歩によりその先を見据えた時代になってきたのです。そのためには栄養管理がとても重要なのです。
ICU入室時の栄養障害および骨格筋の減少、ICUにおけるエネルギー負債などが重症患者の予後不良因子であり、ICU-AWを含めたPICSの発症と関連している可能性がある。高齢者のPICS対策として、タンパク投与を含む適切な栄養療法(と早期リハビリテーション)が有用である可能性がある[7]。
重症患者の栄養管理ガイドライン[6,8]

ここからは、ガイドラインの概要を紹介します。
ガイドラインはこちらから閲覧可能です。
(※直接リンク張るのはダメだそうでこのページで見つけてください)
Amazonでもダイジェスト版が購入できます。
このガイドラインは総論2016と病態別2017があります。総論2016のおもな内容はこちらになります。

量が多いので、なるべくポイントを抑えて解説していきたいと思います。

栄養療法の必要性に関しては、最初のCQとして、「重症患者の病態や病期に応じた栄養管理を行うことを強く推奨する。」と記載されています。
評価方法はこれといったものがないのでSGAやその他、入院前の状況などを鑑みて総合的に判断する必要があります。
栄養投与ルート、エネルギー消費量・投与量、タンパク質投与量はこの後別に解説します。

栄養投与ルートは、経腸栄養を優先することが強く推奨されています。というのも、死亡率はENとPNとの比較では差がありませんでしたが、感染症発生の抑制や在院期間の短縮、医療費削減効果などでEN群が良好な結果でした。

エネルギー消費量は間接熱量計での測定結果、もしくは推算式による算出に基づいて設定することを強く推奨するとあります。間接熱量計がある施設はそう多くはないように思います。Harris-Benedictの式は少し多めに出ることが多いので、現実的には簡易式で十分なのではないでしょうか。
急性期の栄養はエネルギー消費量よりも少なく投与することが望ましいと考えられる(いわゆるPermissive Underfeeding)。しかし、至適な投与量は未確定であるとあります。そうはいってもじゃあどうすれば?ってなりますので、10-20kcal/hrで開始し、消費量の70%(≒20 kcal/体重kg)程度を目標にします。
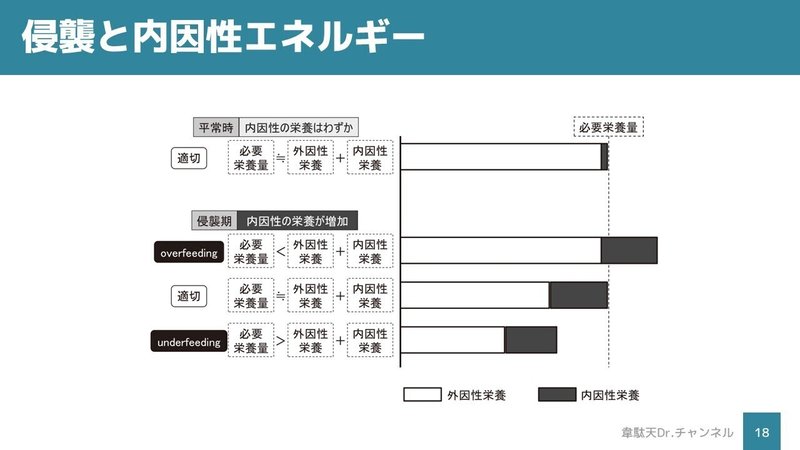
侵襲が加わると、内因性のエネルギー供給が起きます。蓄積されていた筋肉や脂肪が分解されてエネルギーとして供給されるのです。ですから外から点滴などで栄養を入れすぎるとoverfeedingとなり、高血糖などの栄養ストレスによって有害事象が引き起こされます。栄養療法自体が逆効果となり身体に悪影響を及ぼしてしまうのです。ですのであえて少なめに栄養を入れるのですね。

結論だけ言えば必要タンパク質量は1〜1.2 g/kg/day以上となります。

不安定な循環動態
※不安定な循環動態とは、高容量の昇圧薬投与・大量輸液・大量輸血が
必要な場合で、平均血圧 ≦ 60 mmHgが目安。
※投与する場合、栄養投与中のショックや非閉塞性腸管壊死(NOMI)などの発症に注意し、何かあればすぐ中断すること!
チューブの位置
※幽門後は肺炎が少ない幽門後にこだわるとENの開始が遅くなる。
※挿入方法は内視鏡ないし造影下に。
目標投与量
重症化以前に栄養障害がある症例では至適投与量は不明であるが、エネルギー負債が大きくなり過ぎない程度の投与量は必要。
静脈栄養は積極的には行わないのが原則です。
※ブドウ糖輸液単独では行わないことを弱く推奨する。
※ビタミン、微量元素、セレン:重症度の高い集中治療患者への総合ビタミン剤,微量元素製剤の通常量の投与を強く推奨するが、投与推奨量を決定する十分なデータはない。
※中心静脈ルートは浸透圧比3以上の輸液製剤を用いる場合に使用することを強く推奨する。

リフィーディング症候群は発症すると時に致命傷になるので、リスクの高い患者では十分に気を付ける必要があります。

腸蠕動音がなくてもENを開始するのはなかなか勇気がいりますが、開始することで腸も動くのです。
そして、なるべく継続させることが重要です。
経腸栄養に対する耐性(継続できるか?)のモニタリング
・患者の経腸栄養に対する耐性として、疼痛や腹部膨満感の訴え、理学所見、排ガス・排便、腹部X線写真などをモニタリングする。
・経腸栄養の不適切な中止を避ける。
・不耐性を示す他の徴候がない場合、随時確認した胃内残量<500 mlであれば経腸栄養を中断しない。
・不適切な栄養投与や麻痺性イレウスの長期化を防ぐために、診断や処置に伴う絶食期間を最小限にとどめる。
誤嚥や下痢対策も重要です。



特別な栄養素や補足的治療ではこれといったものないような印象です。
〇や×は以下の推奨度を表しています。
点線の〇:使用することを弱く推奨
薄い×:使用しないことを弱く推奨
濃い×:使用しないことを強く推奨(ショックや多臓器不全におけるグルタミンのみですね)

胃酸を抑える薬(PPIやH2RA)は肺炎の発生リスクを上昇させるので、消化管出血リスクを評価して適切に使用する必要があります。

血糖管理は重要です。あまり下げすぎると低血糖のリスクがあるので気を付けましょう。また簡易測定器での測定値は高く出ることがあるので、低血糖の発生をうっかり見逃してしまう可能性があります。なるべく血ガス分析機で測るようにしましょう!

こちらのスライドはご覧の通りです。
” I. 静脈栄養療法中の患者管理 ”
” 第3章 栄養管理の実際:小児 ”
に関しては解説を省略します。
さて、ここからは病態別2017の内容になります。
ARDS以外では高脂肪栄養剤は使わないのですね。
AKIではいわゆる腎不全用のタンパク質量が制限されたものではなく標準的な栄養剤を使用してください。なお透析中はタンパクを多めに入れる必要があります。
肝不全は慢性と急性で分けて考える必要がありますね。スライドの記載の通りです。
急性膵炎ではチューブを空腸に留置して経腸栄養をするのが重要です。
中枢神経障害に関してはこれといったものはありません。
高度肥満では理想体重で控えめのエネルギー投与と高タンパクですね。
以上、日本版重症患者の栄養管理ガイドラインをまとめますと、以下のようになります。

なるべく早期に経腸栄養を始めること。
あまり入れすぎず、安易な中断を避けること。
が特に重要です。
特別な栄養素というものはなく、主にエネルギー量とタンパク質が重要です。血糖コントロールも重要です。病態別にみても何か特別な栄養療法というのは多くありません。
最近のトピックス① タンパク質の投与
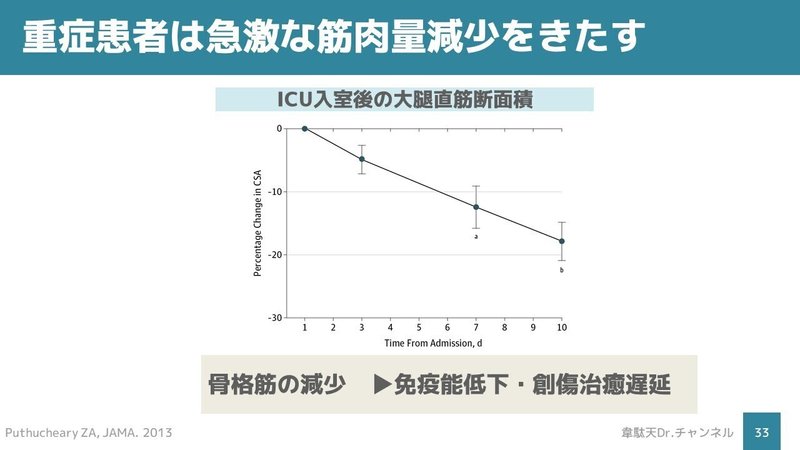
重症患者はICU入室後10日間で15-20%の筋肉量減少をきたします[9]。その結果、免疫能が低下したり、創傷治癒が遅延したりします。
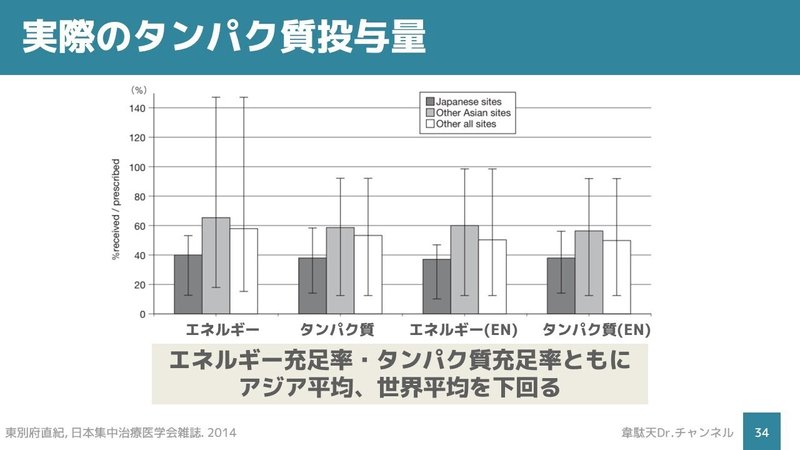
では、実際どのくらいのエネルギーやタンパク質が投与されているのでしょうか?
世界平均・アジア平均のエネルギー・タンパク質充足率はいずれも60%程度であるのに対し、我が国の充足率は40%程度で、かなり低いものとなっています[10]。
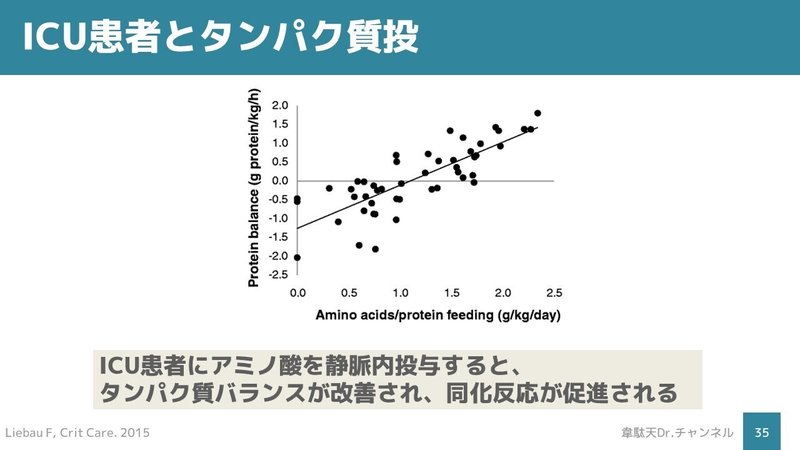
ICU患者にアミノ酸を静脈内投与するとタンパク質バランスが改善され、同化反応が促進されることが報告されています。
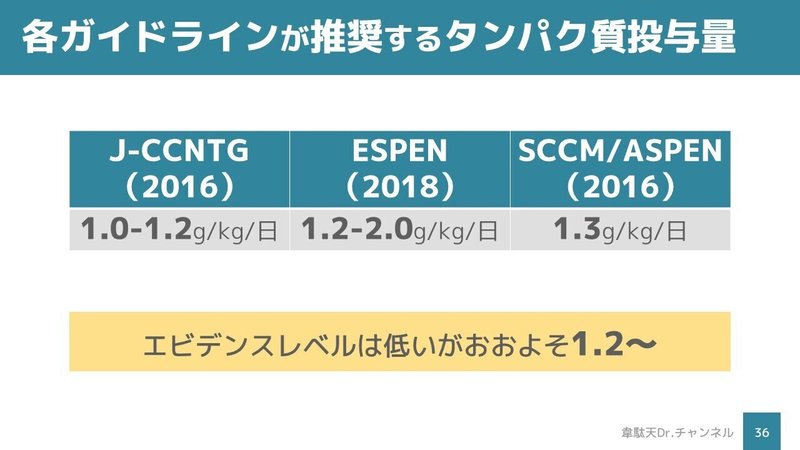
また、日本も含め各国のガイドラインもエビデンスレベルはあまり高くないもののおおよそ1.2g/kg/日のタンパク質投与を推奨しています。
エネルギーもタンパク質も足りてないから大事なのは実はエネルギーなんじゃないの?という方もおられるかもしれません。
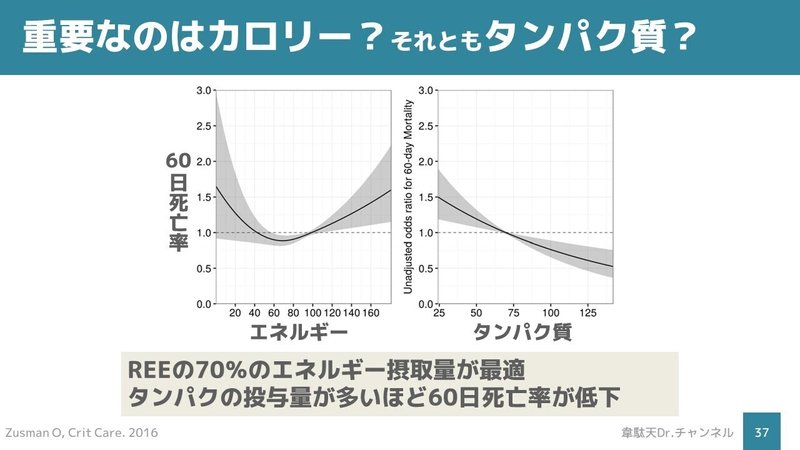
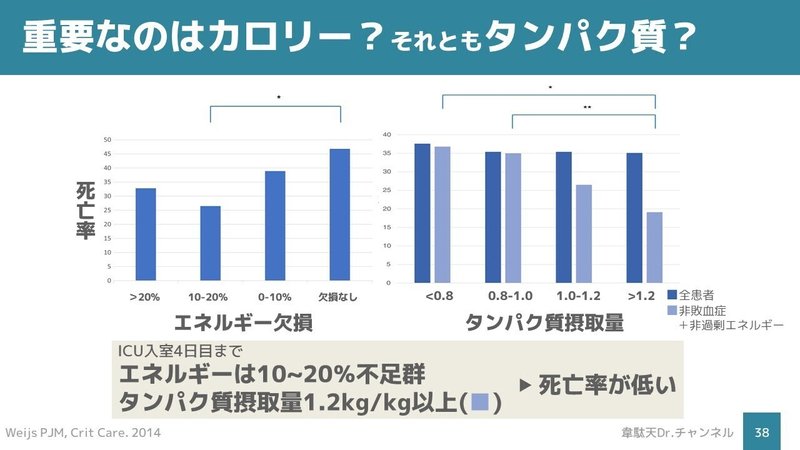
これらの文献によれば重要なのはエネルギーではなくタンパク質です。
エネルギーの過剰投与は死亡率を上昇させますが、タンパク質はより多く投与することで死亡率を低下させます。
ここで実際のエネルギーとタンパク質の投与方法の例を記したレビューがあったのでご紹介します。こちらのレビューではエネルギーとタンパク質の投与量を段階的に増やしていく必要性を述べています[16]。
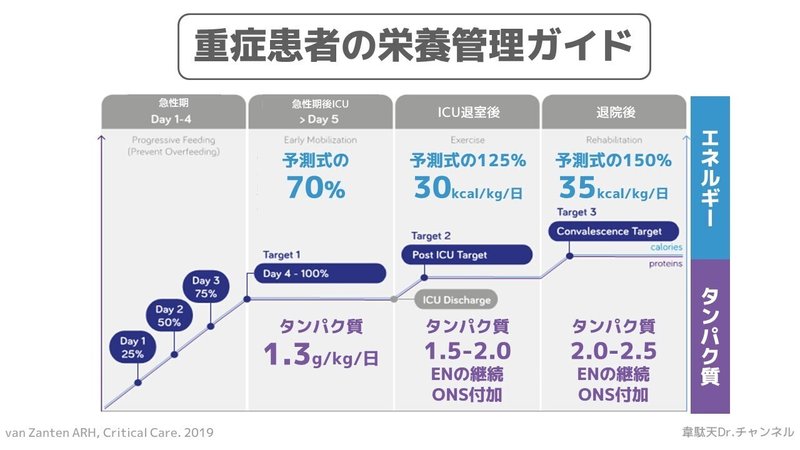
ICU滞在後に体力と筋肉量が著しく低下した患者では、回復のためにエネルギーとタンパク質の供給を大幅に増やすことがかなりの期間必要であり、数ヶ月から数年にわたって必要となる可能性が高い[17]。このような理解の欠如が、長期的な転帰やQOLの極端な低下につながっている可能性はないだろうか?
⼀般病棟でICU退出後経⿐胃管を抜去すると、摂取カロリーが⽬標値の22%、タンパク質摂取量が27%低下する(Van Zanten AR, personal communication)
ですので長期的な予後を考えると十分な栄養を摂取できない段階では経管栄養を併用ないしはONSを利用し、適切な量のエネルギーとタンパク質を投与する必要があります。
最近のトピックス② SPN
※SPN:supplemental parenteral nutrition=補充的静脈栄養
経腸栄養のみでは栄養が不足してしまい、なかなか実現できないこともあります。では、その不足する栄養(特にタンパク質)をPNで補ってみてはどうでしょうか?
まずみておきたいのはEPaNIC試験(2011)です。多施設共同無作為化試験において、ICUの成人患者を対象として早期(48時間以内)に経静脈栄養(PN)を開始したEarly PN群と晩期に(8日以降)にPNを開始したLate PN群を比較した試験です。

死亡率に差はありませんでしたが、感染症発生率、2日以上の人工呼吸器使用率、ICU滞在日数、腎代替療法施行日数、医療コストにおいて晩期PN併用群が有意に優れており、あまり早期からのPNはよろしくないという結果でした。
これだけだと追加PNする気にはなかなかなりませんよね。
J-CCNTG2016では、本論文のエビデンス評価は、術後ICU患者を中心とした研究であるため、クオリティA(RCTが相当)から1段階下げてクオリティBとした、とされています[6]。また、この研究ではBMI<17の栄養不良患者を除外してもいます。
これだけではSPNの評価は難しいので、いくつか気になるSPNに関する文献を紹介したいと思います。
次に紹介するのはTOP-UP試験(2017)です[18]。
こちらは4カ国11施設において実施された多施設無作為化比較パイロット試験です。対象は、72時間以上の人工呼吸器管理が必要と予想される急性呼吸不全のBMIが25未満(※つまり栄養不良患者も含めた試験)または35以上の成人ICU患者です。EN単独またはSPN+ENを投与する2群で比較しています。

SPN+EN群は、EN単独と比較して、ICU滞在の最初の1週間におけるエネルギーとタンパク質の摂取量を有意に増加させました。
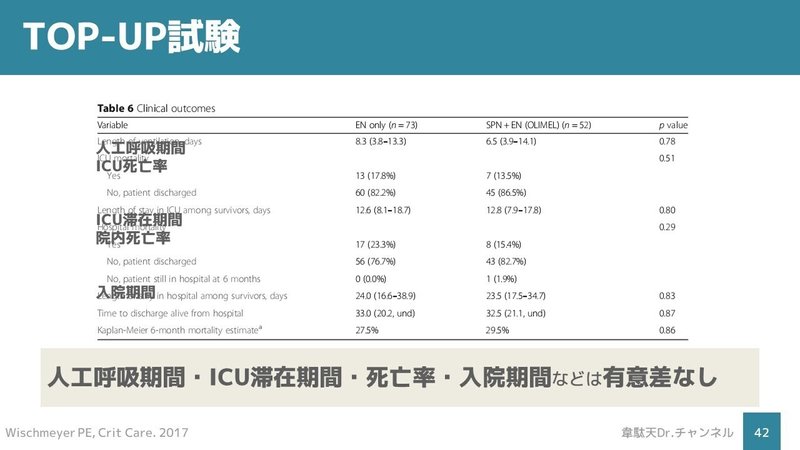
人工呼吸器期間やICU期間、死亡率、入院期間に差はありませんでした。
※有意差はないものの院内死亡率、退院時の機能的アウトカムおよびQoLアウトカムが改善傾向でした。

感染も優位に増加させませんでした。
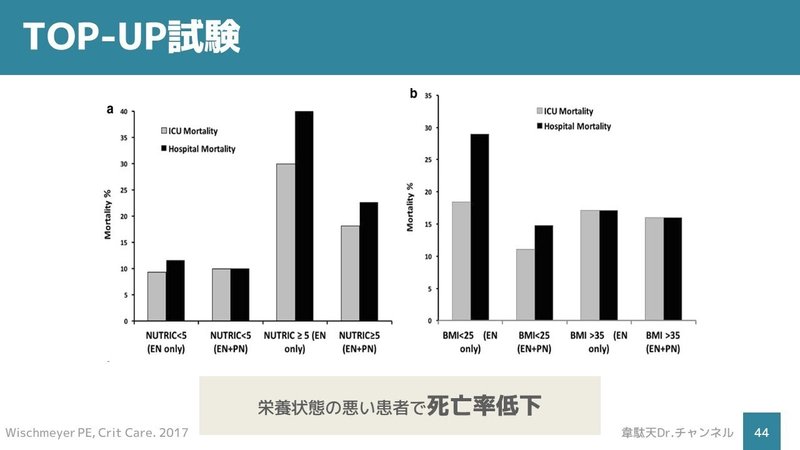
サブグループ解析でNUTRICscore≧5の栄養リスク⾼い患者群、BMI<25の群に関してSPN+EN群で院内死亡率が低い傾向にありました。栄養状態が悪い患者にはSPNは有効かもしれません。
次は2020年のメタ解析を紹介します。
SPNは、ENでは重症患者のエネルギー必要量を満たせない場合、
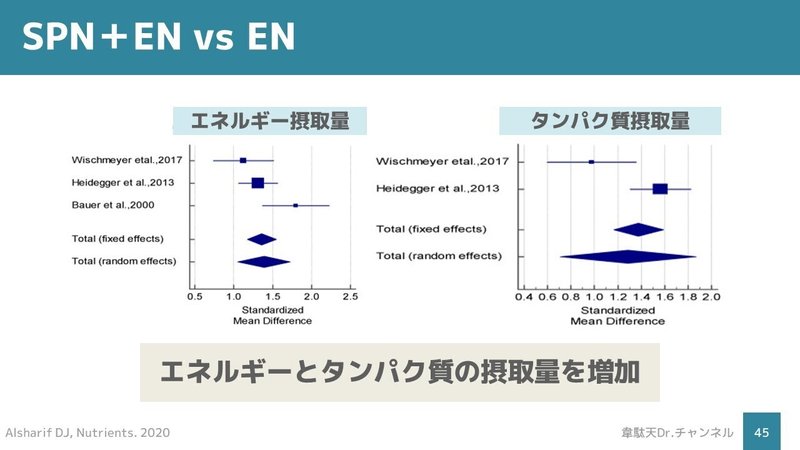
エネルギーとタンパク質の摂取量を増加させ、
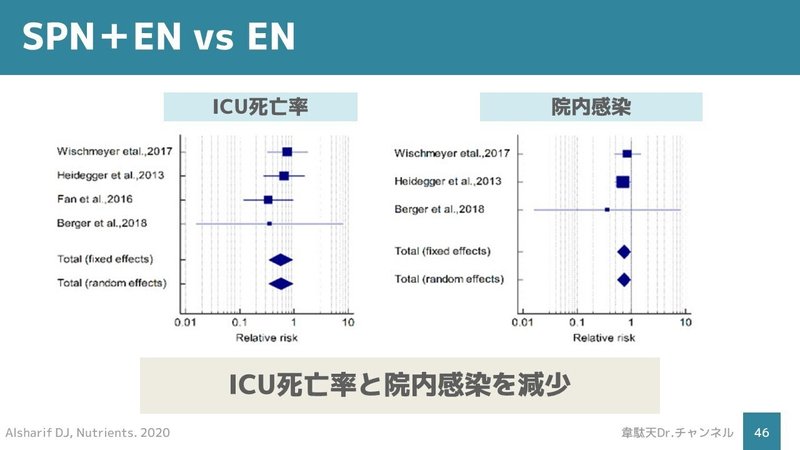
ICU死亡率と院内感染を減少させました。
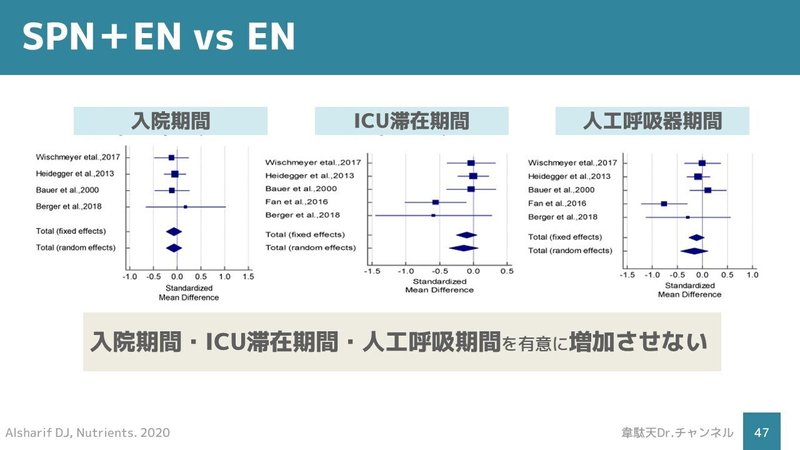
また、SPNは他の臨床転帰に悪影響を及ぼすことはありませんでした。
以上よりSPNはエネルギーおよびタンパク質摂取量を増加させることに加えて、院内感染およびICU死亡率を減少させるのに役立ち、有益であると考えられます。

当初はPNはよろしくないと考えられていました。
しかし、十分なエネルギー量・タンパク質量に達していない場合はエネルギーを考慮しつつ、SPNを検討するのは問題なさそうです。
特にもともとの栄養状態が悪い患者さんには効果がありそうです。
最近のトピックス③ 敗血症ガイドライン

最近、敗血症診療ガイドライン(J-SSCG)が改訂されました[20]。
ガイドラインはこちらから閲覧可能です。
(※直接リンク張るのはダメだそうでこのページで見つけてください)
Amazonでもダイジェスト版が購入できます。
この記事では栄養療法の部分をまとめたものを紹介します。
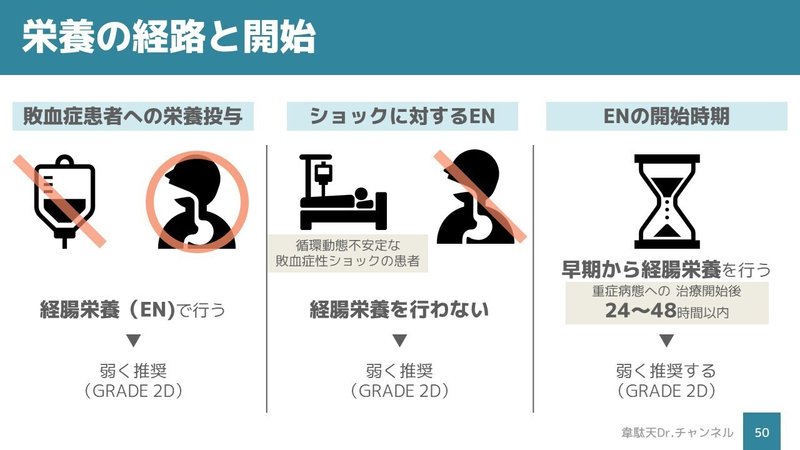
CQ12-1:敗血症患者への栄養投与は経腸栄養で行うことを弱く推奨する。
CQ12-2:循環動態不安定な敗血症性ショックの患者 において,経腸栄養を行わないことを弱く推奨する。
CQ12-3:敗血症患者において,早期(重症病態への 治療開始後24~48時間以内)から経腸栄養を行うことを弱く推奨する。
この辺は、J-CCNTGと一緒ですね。
次は栄養の投与量です。
CQ12-4:敗血症患者に対する治療開始初期は経腸栄養を消費エネルギーよりも少なく投与することを弱く推奨する。
CQ12-5:経腸栄養を行っているが投与エネルギー量 が不足している敗血症患者に補足的経静脈栄養を併用することを弱く推奨する。
CQ12-6:敗血症患者に対して急性期に1g / kg / day未満のタンパク質(ペプチド,アミノ酸)を投与することを弱く推奨する。
先日、ガイドラインを作成している先生の講演を聞いたところ、こう言ってました。
7日目までのタンパク投与量の多い少ないで筋肉量は増える傾向にあったが、入院期間が延びる傾向にあり、今回のガイドラインにおける重要度が、筋肉量重要度7点で、入院期間需要度8点だったため、1g未満を弱く推奨という表現になった。
今後、筋肉の重要性が増してくれば(そのようなエビデンスが積みあがれば)もう少し必要タンパク質量は多く推奨されると思います。
CQ12-7-1:敗血症患者に対して,ビタミンCの投与を 行うことを弱く推奨する。
CQ12-7-2:敗血症患者に対して,ビタミンD投与を行わないことを弱く推奨する。
CQ12-8:経腸栄養開始に腸蠕動音など腸管が働いている所見は必要でないとされる。一方,経腸栄養開始 後の不耐性を示す所見は,腸音欠如または異常腸音, 嘔吐,腸拡張,下痢,消化管出血,胃内残留物過多など,様々である。胃内残留物過多は不耐性を示唆するが,耐性の有無を判断するための胃内残留量の基準は不明である(BQに対する情報提示)。
CQ12-9:病態が急性期を乗り越えた場合,あるいは 1週間程度を超えた時期からは,必要エネルギー(タ ンパク質を含めて25~30kcal / kg / 日程度)を満たす投与量が必要と考えられている。同時期のタンパク質も 1g / kg / 日以上の投与量が望ましいとの考えがある。ただし,重症化前から栄養障害のある患者ではより早期 に投与量を増やすほうがよいとの意見もある(BQに対する情報提示)。
J-CCNTGではビタミンC、Dに関する記載はありませんでした。個人的にはビタミンにこだわるよりはエネルギー・タンパク質量であったり、開始時期や継続することの方が優先順位は高いと思います。
急性期以降では、エネルギー・タンパク質量ともにしっかりと投与しましょう。重症化前から栄養障害のある患者では、より早期に投与量を増やす方がよいとも記載されておりますので、入院初期からの評価も重要ですね。
まとめ
①投与経路は経腸栄養
If the gut works use it. (腸が使えるなら使え) という格言(と言っていいのか)の通りですね[21]。
②早期より開始
開始時期が遅くなればなるほど腸の機能が落ちてしまいます。
③エネルギーは控えめ、タンパク質はしっかり
Permissive Underfeeding と高たんぱくですね。
④ストップ中断!
安易な中断を避けましょう。
最後まで読んでくださいましてありがとうございました。皆様の日々の診療のお役に立てれば幸いです。
参考文献
[1] 令和2年度診療報酬改定の概要(入院医療) [Internet]. [cited 2021 May 17]. Available from: https://www.mhlw.go.jp/content/12400000/000691039.pdf.
[2] アボット | 製品情報 | エンシュア・リキッド® [Internet]. [cited 2021 May 17]. Available from: https://www.abbott.co.jp/our-products/ensure-liquid.html.
[3] ビーフリード輸液|【公式】大塚製薬工場 医療関係者向けページ Otsuka Pharmaceutical Factory, Inc. [Internet]. [cited 2021 May 17]. Available from: https://www.otsukakj.jp/med_nutrition/dikj/menu1/000271.php.
[4] エルネオパNF1号輸液|【公式】大塚製薬工場 医療関係者向けページ Otsuka Pharmaceutical Factory, Inc. [Internet]. [cited 2021 May 17]. Available from: https://www.otsukakj.jp/med_nutrition/dikj/menu1/000213.php.
[5] エルネオパNF2号輸液|【公式】大塚製薬工場 医療関係者向けページ Otsuka Pharmaceutical Factory, Inc. [Internet]. [cited 2021 May 17]. Available from: https://www.otsukakj.jp/med_nutrition/dikj/menu1/000214.php.
[6] 日本集中治療医学会重症患者の栄養管理ガイドライン作成委員会. 日本版重症患者の栄養療法ガイドライン. 日本集中治療医学会雑誌. 2016;23:185–281.
[7] 佐藤格夫, 安念優, 森山直紀. 栄養療法: ICU 患者の長期予後, PICS 予防との関連 (特集 PICS 集中治療後症候群)–(PICS は予防できるのか?). Intensivist= インテンシヴィスト. 2018;10:153–161.
[8] 日本集中治療医学会重症患者の栄養管理ガイドライン作成委員会. 日本版重症患者の栄養療法ガイドライン:病態別栄養療法. 日本集中治療医学会雑誌. 2017;24:569–591.
[9] Puthucheary ZA, Rawal J, McPhail M, et al. Acute skeletal muscle wasting in critical illness. JAMA. 2013;310:1591–1600.
[10] 東別府直紀, 讃井將満, 祖父江和哉, et al. 国際栄養調査から見える本邦 ICU における栄養療法の現状と問題点. 日本集中治療医学会雑誌. 2014;21:243–252.
[11] Liebau F, Sundström M, van Loon LJC, et al. Short-term amino acid infusion improves protein balance in critically ill patients. Crit Care. 2015;19:106.
[12] Singer P, Blaser AR, Berger MM, et al. ESPEN guideline on clinical nutrition in the intensive care unit. Clinical nutrition. 2019;38:48–79.
[13] McClave SA, Taylor BE, Martindale RG, et al. Guidelines for the Provision and Assessment of Nutrition Support Therapy in the Adult Critically Ill Patient: Society of Critical Care Medicine (SCCM) and American Society for Parenteral and Enteral Nutrition (A.S.P.E.N.). JPEN J Parenter Enteral Nutr. 2016;40:159–211.
[14] Zusman O, Theilla M, Cohen J, et al. Resting energy expenditure, calorie and protein consumption in critically ill patients: a retrospective cohort study. Crit Care. 2016;20:367.
[15] Weijs PJM, Looijaard WGPM, Beishuizen A, et al. Early high protein intake is associated with low mortality and energy overfeeding with high mortality in non-septic mechanically ventilated critically ill patients. Crit Care. 2014;18:701.
[16] van Zanten ARH, De Waele E, Wischmeyer PE. Nutrition therapy and critical illness: practical guidance for the ICU, post-ICU, and long-term convalescence phases. Critical Care. 2019;23:368.
[17] Puthucheary ZA, Wischmeyer P. Predicting critical illness mortality and personalizing therapy: moving to multi-dimensional data. Crit Care. 2017;21:20.
[18] Wischmeyer PE, Hasselmann M, Kummerlen C, et al. A randomized trial of supplemental parenteral nutrition in underweight and overweight critically ill patients: the TOP-UP pilot trial. Crit Care. 2017;21:142.
[19] Alsharif DJ, Alsharif FJ, Aljuraiban GS, et al. Effect of Supplemental Parenteral Nutrition Versus Enteral Nutrition Alone on Clinical Outcomes in Critically Ill Adult Patients: A Systematic Review and Meta-Analysis of Randomized Controlled Trials. Nutrients [Internet]. 2020 [cited 2021 Mar 13];12. Available from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7601814/.
[20] 江木盛時, 小倉裕司, 矢田部智昭, et al. 日本版敗血症診療ガイドライン2020. 日本集中治療医学会雑誌. 2020;28.
[21] Livingston A, Seamons C, Dalton T. If the gut works use it. Nurs Manage. 2000;31:39–42.
この記事が気に入ったらサポートをしてみませんか?
