
なぜコロナワクチンが大量のDNAで汚染されているのか?
コロナワクチンのDNA汚染を発見したKevin McKernan先生の実験の本来の目的はmRNAの品質チェックでした。コロナワクチンの主成分であるmRNAの品質管理に問題がある事は以前から知られており、欧州医薬品庁 (EMA) からリークされたEMAの高官によるメール (2020年11月23日付け) の中でも既に指摘されていました。
コロナワクチン内の大量の不良RNA
リークされた文書によると、ファイザー・バイオナンテック社のコビッド19ワクチンの初期商業ロットの一部は、インタクトなmRNAのレベルが予想より低かった。
https://www.bmj.com/content/372/bmj.n627
その電子メールによると、臨床バッチと商業用のバッチとの間に「完全長RNAの割合に有意な差があり」それらは約78%から55%であった。根本的な原因は不明であり、このRNAの完全性の喪失がワクチンの安全性と有効性に与える影響は「まだ定義されていない」と電子メールは述べている。
コロナワクチンはロット (バッチ) やバイアルによっては「不良RNA」が非常に多く、物によってはRNAの半分近くの量が不良品と言っても過言では無い状態です。では何故これほど大量の不良RNAがワクチンに含まれているのでしょうか?
https://anandamide.substack.com/p/curious-kittens
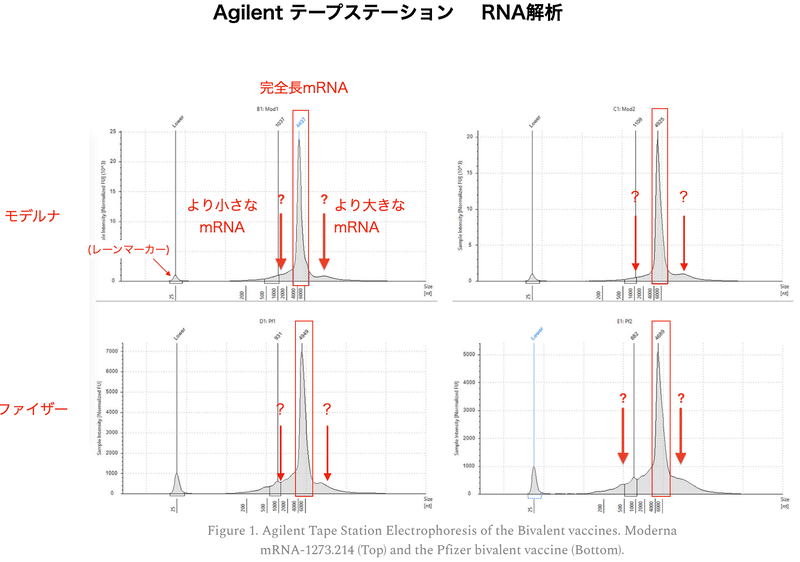
図1はMcKernan先生によるAgilentテープステーションの解析です。完全長mRNAの他に、より大きなmRNA、より小さなmRNAが存在しています。完全長mRNAの割合は約50〜80%程度でしょうか。割合はファイザーかモデルナでも違いがあり、またバイアルごとによっても違いがあります。(25 ntの小さなRNAのピークはレーンマーカーであり、これはテープステーションの仕様になります。)
DNA-RNAハイブリッド考察

O. L. Miller et al., Science 169:392, 1970.
本来、ゲノムからmRNAを転写してもゲノムが壊れるわけではありません。実際、同一DNA分子は何度も繰り返しmRNAの転写に使われます。図2は大腸菌でのmRNA転写とタンパクへの翻訳の電子顕微鏡画像です。ここでは大腸菌ゲノムDNAからmRNAが転写されています。転写開始点を決める制御領域がプロモーターであり、図2の転写開始点のDNAの左側に存在しています。大腸菌には核がないために、転写と翻訳が同じ場所で協調して同時に起こります。DNAからRNAの転写では、1つのDNA分子から複数のmRNAが次々に合成されていきます。そして、mRNAにリボソームが結合し、mRNAからタンパクへの翻訳が起こります。
ちなみに、ヒト細胞は核を持つため転写と翻訳の起こる場所は別であり、mRNAへの転写は核内で起こり、タンパクへの翻訳は細胞質で起こります。
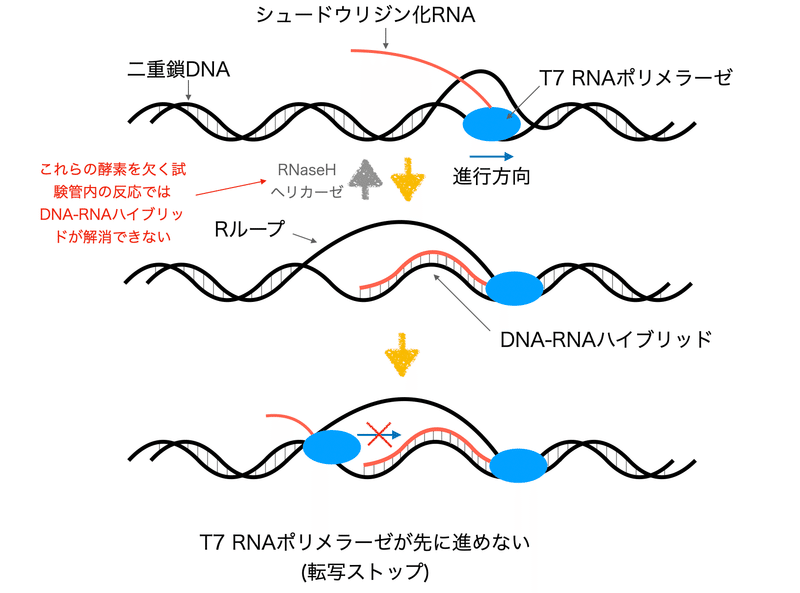
図3は説明のために私が描いたものです。T7 RNAポリメラーゼによる転写は効率が良く、本来1つの鋳型DNAから大量のmRNAを転写します。転写されたRNAは鋳型のDNAのコピーです。そのため、転写されたRNAがDNAに結合してしまうとDNA-RNAハイブリッドを生じます。「Rループ」はDNA-RNAハイブリッドと一本鎖DNAという3本の核酸鎖から構成される構造です。DNA-RNAハイブリッドは次の転写を止めるブレーキのような働きをし、新たな転写反応を阻害します。
シュードウリジン化RNAはDNAと強固に結合します。そして、GCリッチな配列がこの強固な結合にさらに拍車をかけます。このようにコロナワクチンのmRNAはDNA-RNAハイブリッドを生じさせやすいという特徴を持ちます。細胞内でRループを取り除く酵素はRNase H (DNA-RNAハイブリッド内のRNAを分解する) やRNA-DNAヘリカーゼ等です。DNA-RNAハイブリッドを除去する酵素を含まない試験管内の反応では、一旦生じたDNA-RNAハイブリッドは解消されません。
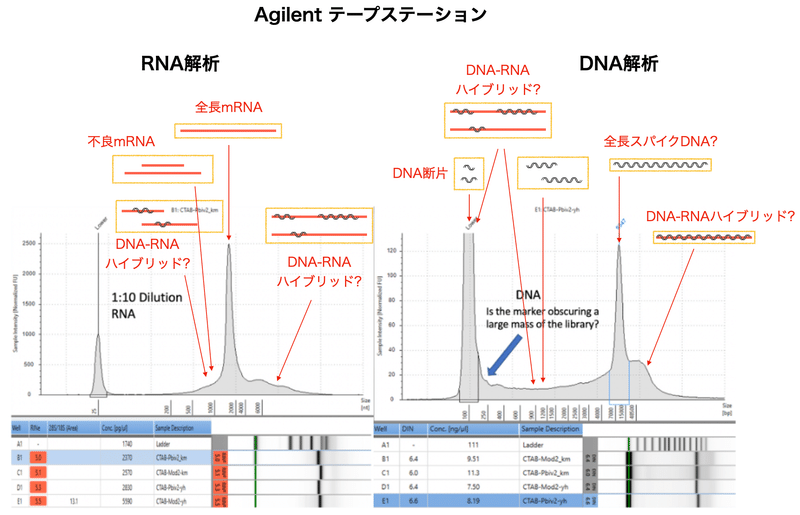
https://anandamide.substack.com/p/sequencing-of-bivalent-moderna-and?utm_source=post-email-title&publication_id=456768&post_id=113965391&isFreemail=true&utm_medium=email
DNA-RNAハイブリッドが転写の邪魔をするためにmRNAの合成量が少ないのであれば、mRNAに対する鋳型DNAの比率も元々高かったという事になります。また、途中で転写が止まった場合には「中途半端な」mRNAを生じます。このような不良RNAに加えてDNA汚染が生じる原因はDNA-RNAハイブリッドが考えられます。

https://en.wikipedia.org/wiki/R-loop
G4構造を含めた汚染DNAの複雑な高次構造
二本鎖DNAを検出するQubitのキットで検出されている事から、コロナワクチン汚染DNAには二本鎖DNAが大量に含まれていると判断できます。
RループはDNA-RNAハイブリッドとそれに関連する非鋳型一本鎖DNAからなる三本鎖核酸構造です。通常のRループ内のDNAは一本鎖DNAです。本来DNase Iは一本鎖DNAを分解します。では、どうして汚染DNAはDNase Iによる分解に耐性なのでしょうか?また、どうして汚染DNAには二本鎖DNAが含まれているのでしょうか?

https://ja.wikipedia.org/wiki/グアニン四重鎖
汚染DNAによって生じるRループ内の一本鎖DNAはおそらく単純な一本鎖DNAではありません。グアニン (G) は通常はシトシン (C) と水素結合で会合します。しかし、GCリッチな配列は分子内で会合し、複雑な二次構造、三次構造を生じます。その代表的なものがG-四重鎖構造です。
G-四重鎖二次構造 (G4) は、4つのGが水素結合によって会合し、正方形の平面構造を形成したものであり、2つ以上のG4互いの上に積み重なった構造をとる事ができます。また、G4はDNAだけではなくRNAでも形成されます。図は分子内で形成されたG4ですが、二分子、四分子でG4を形成する事もあります。そして、RNAのG4構造とプリオン病の関連も示唆されています。
RNAを構成する塩基はA、C、G、Tの4種類ですが、コロナワクチンはGとCの2種類のみが多い「単調な」配列です。そのため、部分的に同様な配列が多く生じます。そして、Rループ内の一本鎖DNAも部分的に似通った配列のRNAと複雑に絡み合っているはずです。
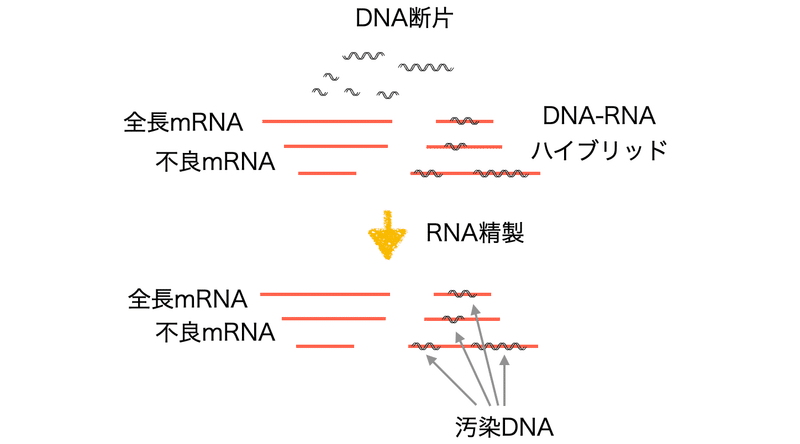
コロナワクチンはなぜ大量のDNAで汚染されているのか?
mRNAの鋳型に使われたDNAがDNase I分解耐性になるのは、シュードウリジン化RNAがDNAに強固に結合して、DNAを分解から保護するためです。この強固な結合の理由はシュードウリジン化RNA自体の性質に加えて、スパイク遺伝子の配列においてGとCの含有量が高いからであり、このRNAとDNAの強い結合はmRNAの精製にも影響するでしょう。たとえ小さなDNA断片だけを取り除こうとしても、mRNAにトラップされたDNAを除去する事は難しいからです。
汚染DNAにRNAが複雑にもつれた糸のように絡まっている状態をイメージして下さい。そのように複雑に絡まり合った状態では、内側のDNAの分解も除去も十分にできないのでないか、という事です。

DNA-RNAハイブリッド内のRNAは細胞質ではDNAをヌクレアーゼの分解から保護するでしょう。そして、細胞質には存在しないが核に存在するものがDNA修復です。核内ではRNase Hやヘリカーゼのような酵素の介助を受けてDNA-RNAハイブリッドからRNAを取り除く事ができますが、そうしたイベントが起こるのはまさに汚染DNAがゲノムに統合されるタイミングです。
整理すると、シュードウリジン化RNAとDNAの強固な結合は、1) mRNA合成を低下させ、2) mRNA品質を低下させ、3) DNaseIによるDNA分解を阻害し、4) RNA精製の際のDNA除去を阻害し、5) 細胞内 (細胞質) での汚染DNAの分解を阻害し得ます。言い換えると、シュードウリジン化RNAはDNAと強固に結びつき過ぎているために、mRNA合成もうまくいかず、DNA分解もうまくいかず、DNA除去もうまくいかず、細胞内に取り込まれても危険なままです。つまる所、DNA汚染はLNP/mRNA製剤における根本的な技術的欠陥を示しているという事です。
汚染DNAの本質的な問題は、その汚染DNAがゲノムに干渉し、ゲノムを改変するという懸念です。また、汚染DNAの配列に関わらず、汚染DNAのゲノムへの統合は遺伝子情報を破壊する原因となります。そして、その頻度は汚染DNA分子の数に比例するために、汚染DNAの分子数を知る事が重要になります。しかしながら、実際汚染DNAの質量を定量するだけでも簡単ではなく、汚染DNAの分子数の測定はそれよりもはるかに困難でしょう。現時点で手がかりとなる技術はナノポアによるディープシークエンシングとAgilentテープステーションやバイオアナライザーなどのデジタル電気泳動の技術です。ワクチン内の汚染DNAの質量や分子数の定量と並行して、ワクチン接種者の汚染DNAのゲノム統合を検出する技術が必要となります。
#コロナワクチン
#ワクチン
#コロナ
*記事は個人の見解であり、所属組織を代表するものではありません。
この記事が気に入ったらサポートをしてみませんか?
