
デジタルリハの論文紹介:2020年版
2020年のデジタルリハの海外の研究動向
2020年11月20日に@HiroakiKatoさんサロンにて行われた@h_kawag「2020年デジタルヘルス医学研究論文 総まとめ」という今年「npj Digital Medicine」に投稿された130本の論文を90分で紹介するという勉強会がありました.
大学院生として普段から自分の研究分野は読みますが,こういった分野の論文を読んでいなかったので,めちゃくちゃおもしろかったです!
デジタルヘルス分野にハマりつつありますが,メディアでつい目にする情報はビジネスサイドの情報が多かったりと,背景にある研究にあまり目を向けてなかったなーと気付かされました!
アカデミックな視点からもデジタルヘルスがどう生かされるか考えてみる機会になりました.
紹介された中で自分の身近なリハビリテーションに関する論文がいくつかあったので,
「デジタルリハ」の専門家を目指すべく「npj Digital Medicine」で投稿された「デジタルリハ」に該当する論文の全文を読み,学びをここにまとめました!

過去のデジタルリハの研究動向
国内でもVRを使った「仮想的に運動機能の拡張を体験させるアプローチ」¹や今年に新たにできた「運動量増加機器加算」で注目されたロボットを使った介入が広まってきています。こうしたVRやロボットを利用したリハビリテーションの研究は10年以上前より実施されており,医学論文のシステマティック・レビューを行なう国際的団であるコクランからも多くの論文が出ておりエビデンスが蓄積されつつあります。
そこで,今現在のデジタルリハの研究を調査することで10年後の普及されるテクノロジーを考案一助になると考え,2020年度に投稿さ世界中の医学研究者が注目したデジタルリハに関連する研究はどのような研究論文があったのか調査しました.
今回,デジタルヘルス分野での医学研究論⽂でおそらくトップジャーナルであり「npj Digital Medicine」に投稿された論文を対象とし,2020年から現在(11月時点)までに公開されているリハビリテーション関連の論文を調査しました.
デジタル・ヘルス・メトリックスの選択と検証のためデータ駆動型フレームワーク²
リンク:A data-driven framework for selecting and validating digital health metrics: use-case in neurological sensorimotor impairment
患者アウトカム・プロセスを評価する上で臨床的根拠の高いデジタル指標を選択・検証するためのデータ駆動型方法論(フレームワーク)が提案されている論文です。こちらの研究の出発点は大きく2つあります。①既存の評価尺度の問題点:今現在も機能障害を評価する尺度はありますが,天井効果やその解像度の低さ、行動の変動性などに関する知識が限定的であるために,軽微な障害を検知しずらい点,②既存のデジタル評価指標の問題点:既存の評価尺度の欠点を克服する指標として、センサーデータから抽出されるデジタル指標が提案されてきましたが、どれも数学的には最適化されている一方、半ばブラックボックス的に選択されているために直感的ではなく、臨床的根拠の低い評価指標にとどまっている点。そこで、この研究では「対象とする障害の病態生理学的解釈」「年齢や利き手といった参加者の人口統計学的影響」および「臨床的特性」を考慮されたデジタル指標を選択・評価可能なフレームワークを開発し、実際に「バーチャルペグ差しテスト(原文:Virtual Peg Insertion Test (VPIT)*」にフレームワークを適用することでその有効性を立証しました。
*バーチャルペグ差しテスト:どんな機械を知りたい方はこちらの動画をご覧ください。
ウェアラブルセンサーと機械学習を用いた精密なリハビリテーション介入が,運動機能回復の追跡を可能にする³
リンク:Enabling precision rehabilitation interventions using wearable sensors and machine learning to track motor recovery
機械学習を用いることで、動作課題実行中にウェアラブルセンサーから取得されたデータから既存の尺度を予測できると報告した論文です.この研究の背景としては脳卒中患者の上肢機能を評価する尺度としてFugl-Meyer Assessment (FMA)やFunctional Ability Scale (FAS)がゴールドスタンダードとなっているが,臨床現場では測定に30分以上が掛かることから,臨床業務のルーティーンとして計測することが困難であった現状がありました。この研究では患者は上腕,前腕には3次元,指には2次元の加速度計をつけ,いくつかの動作課題を実施したときに計測されたデータに対して機械学習を適用することでFMAとFASを予測可能であったことを示しました。将来的に、ウェアラブルセンサーを使用することで、在宅または臨床業務内における効率的な患者の身体機能測定ができるだけでなく、回復状態に基づいて進行中の介入の有効性を定期的に評価する「精密なリハビリテーション介入」の実現可能性についても言及していました.
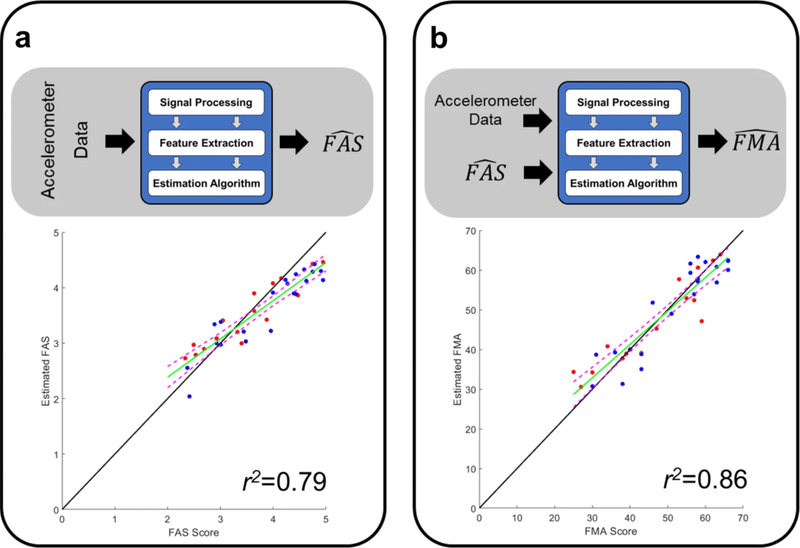
図³:aはFunctional Ability Scale (FAS)、bはFugl-Meyer Assessment (FMA)の予測結果(縦軸)と実際の結果の比較した図です。青は外傷性脳損傷後の患者、赤は脳卒中後の患者のデータです。
慢性閉塞性肺疾患が増悪した後のeヘルスアプリケーションによるサポートケアと通常のケアのランダム比較試験⁴
リンク:A randomised controlled feasibility trial of E-health application supported care vs usual care after exacerbation of COPD: the RESCUE trial
ランダム比較試験にて 慢性閉塞性肺疾患(Chronic Obstructive Pulmonary Disease, COPD)の在宅管理において通常行われる書面上での自己管理に比べて,デジタルヘルスAppの介入の方が90日以上にわたり再増悪と再入院率が低下することを示した研究です.この研究の背景には、英国ではCOPD関連のケアが充実しつつある一方でCOPDの再入院率が上昇しているという事実があり、患者の自己管理をより効果的に支援するために直接的なケアに留まらない新たなアプローチが必要とされていました。この研究で使われたのは, myCOPDというmyHealth社が開発したアプリです.COPD患者向けにリハビリテーションプログラム,吸入器の使い方,COPDについての教育プログラムなど自己管理を包括的にサポートし,また医療者も患者の在宅でのデータ習得を可能にしました.一方、興味深いデータとして当初研究への参加基準に適合すると判断された124人のうち66人が研究への参加を拒否したそうです。明確な理由は不明ですが、デジタルツールを使うことへの不安や抵抗感が参加への障壁となっている可能性もあると筆者は述べており、デジタルヘルスAppが今後直面していく課題なのかもしれません。
腰痛のアウトカム向上のための人工知能と臨床分類によるアプローチ方法:3つのシステマチックレビュー ⁵
リンク:Artificial intelligence to improve back pain outcomes and lessons learned from clinical classification approaches: three systematic reviews
こちらは腰痛の分類方法について,AI/機械学習を用いた腰痛の研究論文を体系的にまとめ,既存の腰痛分類方法(STarT Back tool*1とMcKenzie method)におけるAI/機械学習の利用法の違いを調査した研究です.現在、AI/機械学習を用いた腰痛の研究は黎明期でありますが、腰痛の分類を実施していた25本の研究は全て「腰痛発症の有無の検出」を目的とした研究でした。しかし、臨床場面ではすで腰痛を抱える人を診るため、腰痛発症の有無を検出するだけでは既存の2種類の分類方法には及ばず、AI/機械学習の有用性が臨床的に意味のある形で実現されていないことが浮き彫りになりました。そのため、今後は腰痛患者をさらに心理社会的要因の違いなどを考慮したサブグループに分類し,臨床的・社会的アウトカムを改善するためにより個別化された治療につながる研究を実施すべきであると指摘しています.特に既存の腰痛の分類方法であるSTarT Back toolはその簡易性と治療方法を判断する上で有効性が高いだけに,それを上回るAI/機械学習による分類方法を研究していく必要性があると著者は述べております.
*1) STarT Back toolとは、質問紙によるスクリーニングツールです。3つの層(low risk、medium risk, high risk)に分類し、 腰痛の予後に合わせた介入方法を考案するに使用されます⁶。
全体的な感想
まず、患者の機能改善を目的とした「介入方法」を比較する研究が多かったが,近年は身体機能の「評価方法」も見直されている傾向があると感じました.「個別化医療」を実現する上では,臨床上患者の「病名」以上の分類がより重要になると考え,今後も身体機能の評価方法についての研究が進むのでは無いでしょうか?
また、@h_kawagさんにこちらのまとめを事前に見てもらった後に、最近は「臨床での有用性」が重要になってきているように感じられたそうです。
ココ最近までは、AI/機械学習で分類・予測の精度の高さなどが議論されることが多かったのですが、それが実際に臨床・社会に実装された時、「どれくらい患者アウトカムを改善できるのか?」、「どんなワークフローを効率化できるか?」、「AI/機械学習が臨床上の課題の解決につながっているのか?」など、社会実装がどれくらい可能なのか重要視されてきているようです。
それだけAI/機械学習がより医療分野に浸透したことなのでしょう。正直、AI/機械学習が使用されるようになるのはリハビリテーション領域ではまだ先のことだと思っていましたが、一部のデータが蓄積されてきた、循環器や脳卒中の領域などでは臨床応用も近いのかもしれません。
また年間100を超える論文が出版されている雑誌の中で、リハビリテーション分野の論文は4つほどであったのは、リハビリテーション領域でのデジタル化の難しさも、浮き上がってきているのではないでしょうか。原因としては、デジタル化できていない情報がまだ多い(触覚情報、運動学習の成熟度etc)、デジタル化するのに時間や費用が掛かってしまっているなどを考えましたが、おそらく他も色々あるでしょう。
個人的にはこのデジタル化がどうやってまず定量化されたデータ量をリハビリテーション全体で蓄積できるか、なぜできていないのかを調べて行こうと思います。
参考文献
1. 文成金子 & 途行川上. 仮想的に運動機能の拡張を体験させるアプローチ. The Japanese Journal of Rehabilitation Medicine 57, 821–827 (2020)
2. Kanzler, C. M. et al. A data-driven framework for selecting and validating digital health metrics: use-case in neurological sensorimotor impairments. NPJ Digit Med 3, 80 (2020). CC BY
3. Adans-Dester, C. et al. Enabling precision rehabilitation interventions using wearable sensors and machine learning to track motor recovery. NPJ Digit Med 3, 121 (2020) . CC BY
4. North, M. et al. A randomised controlled feasibility trial of E-health application supported care vs usual care after exacerbation of COPD: the RESCUE trial. NPJ Digit Med 3, 145 (2020). CC BY
5. Tagliaferri, S. D. et al. Artificial intelligence to improve back pain outcomes and lessons learnt from clinical classification approaches: three systematic reviews. NPJ Digit Med 3, 93 (2020). CC BY
6. 浩松平 & 朋子藤井. 診療ガイドライン,エビデンスを踏まえた慢性腰痛に対する患者主導型治療へ向けて─ Stratified approach(層化アプローチ)の重要性. PAIN RESEARCH 32, 252–259 (2017).
この記事が気に入ったらサポートをしてみませんか?
