
公務員試験化学(物質の分類)
このnoteでは、ワンコインで公務員試験でよく出る知識を解説します。
ながら勉強とか、スキマ時間勉強で気軽に1点とりましょう!
お題
物質の構成に関する記述として、妥当なのはどれか。
1.1種類の元素からできている純物質を単体といい、水素、酸素及びアルミニウムがその例である。
2.2種類以上の元素がある一定の割合で結びついてできた純物質を混合物といい、水、塩化ナトリウム及びメタンがその例である。
3.2種類以上の物質が混じり合ったものを化合物といい、空気、海水及び牛乳がその例である。
4.同じ元素からできている単体で、性質の異なる物質を互いに同位体であるといい、ダイヤモンド、フラーレンは炭素の同位体である。
5.原子番号が等しく、質量数が異なる原子を互いに同素体であるといい、重水素及び三重水素は水素の同素体である。
今回にテーマは、よくよく紐解いてみると物質の分類と同位体&同素体の知識をピンポイントで押さえておけばすぐに得点化できます。実に美味しい分野なので、化学苦手な方も食わず嫌いせずに是非とも取り組んでみましょう。
化学のABC
化学の世界に入っていく下準備として最低限必要な知識を紹介します。
中学理科に毛が生えたような内容ですので、気軽に流していってください。
原子の構造
まずは懐かしの原子模型で原子の構造を思い出しましょう。
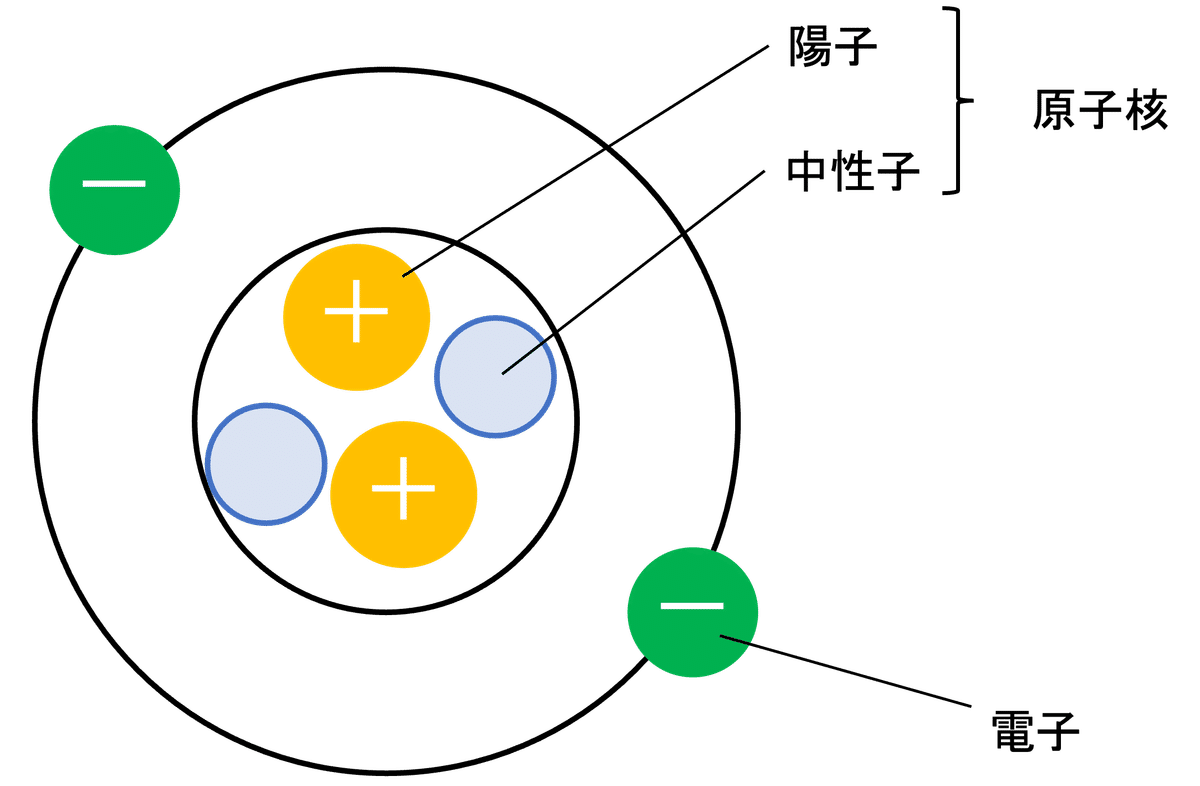
原子核は陽子と中性子から構成されていて、その周囲を電子が回っています。

重さの関係として、陽子の質量=中性子の質量>>電子の質量です。
電子は陽子・中性子の1/1840の質量です。
人間に例えるなら、電子はアクセサリーみたいなもので、重量としてはノーカウントです。
原子の重さは基本的は陽子数と中性子数で決まります。
そこで、陽子数と中性子の合計を質量数と定義します。
質量数=陽子数+中性子数
陽子の数=原子番号
原子の種類を決める要素は実は陽子の数です。
例えば、原子番号1番の水素Hは絶対に陽子数が1であり、陽子の数が2とか3の水素Hは絶対にありえないので注意しましょう。
原子番号と質量数の表現
原子番号2で質量数4であるヘリウムは以下のように書き表すことを覚えておおいてください。こう書くんだな、くらいで全然OKです。

この記事が気に入ったらサポートをしてみませんか?

