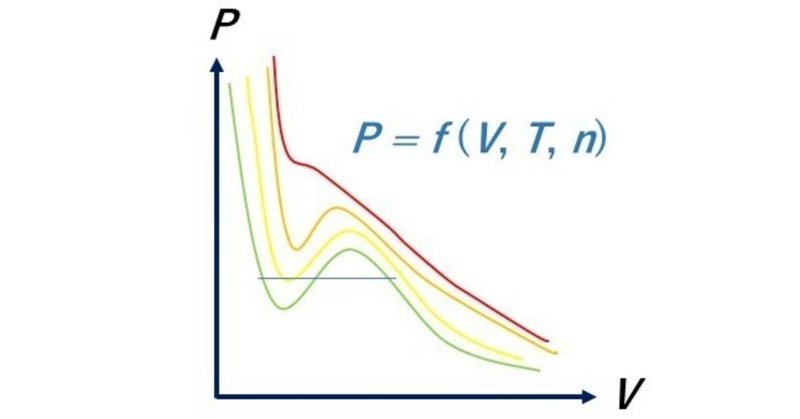
第5章【気体の性質】
●気体の性質として最も基本的で重要な概念は状態方程式です。いわゆるボイルの法則とシャルルの法則の組み合わせとして理解することも教育的ではありますが、分子運動論の観点から理解しておくと後々便利です。
●実在気体の状態方程式はかなり複雑な形をしており、いろいろなタイプのものが考案されています。とりわけ、ファンデルワールスの状態方程式の物理的意味は頻出の項目であり、高校生もよく研究する価値があります。
●蒸気圧はなかなか考えにくい概念ですが、要は気液平衡時に蒸気が器壁に及ぼす圧力のことで、明確な温度依存性があります。入試ではヘンリーの法則やラウールの法則、状態変化や相図との関連でかなり難しい問題が出題されることがあります。
それでは問題です。
【問題1】
次の問に答えよ。
①ボイルの法則とシャルルの法則から気体の状態方程式を導出せよ。
⓶気体の圧力と体積の積は内部エネルギーの2/3倍であることを分子運動論的に示せ。
③圧力P₁, 体積V₁の気体n₁モルと圧力P₂, 体積V₂の気体n₂モルが別々の容器に入っていて、それぞれの容器は連結コックでつながれている。コックを開いて気体を混合すると全圧Pと温度Tはいくらになるか。
④理想気体の断熱変化において圧力P, 体積をV, 比熱比をγとすると
PV^γ = 一定であることを示せ。
⑤ラウールの法則とヘンリーの法則について説明せよ。
【問題2】
(a) 重さw₀ g、体積Vの比重びんの中に適量の液体試料を入れた。これを水槽に浸して加熱し、その液体の沸点Tで全部の液体が揮発したのを確認したのち、室温に冷やすと液体が再び凝集して下にたまり、びんごと秤量すると重さがw₁ gとなった。この液体の分子量を求めよ。ただし、大気圧はP₀、室温はT₀とし、温度は絶対温度で測るものとする。
(b) 前問では試料の蒸気圧を無視しているが、実際は室温における試料の蒸気圧pはゼロではなく、計算結果に少なからぬ影響を及ぼす。この効果を補正した分子量を求めよ。ただし、空気の密度をρ₀とする。
【問題3】
n モルの実在気体に対するファンデルワールスの状態方程式は
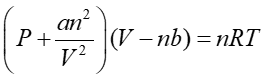
と表され、P, V, Tはそれぞれ圧力、体積、絶対温度で、a, bは定数である。以下、n = 1モルとしよう。
(a) PはVの関数であり、いわゆるP-V曲線を描くとある臨界点以下の低温では非現実なループが現れるので、その領域では圧力を定数とみなす。温度を上げていくとループは小さくなり、臨界温度TcではP-V曲線の変曲点となってループは消失する。そのときの圧力Pcと体積をそれぞれ臨界圧力、臨界体積Vcという。Tc, Pc, Vcを求め、臨界圧縮係数Zc = PcVc/(RTc)を計算せよ。
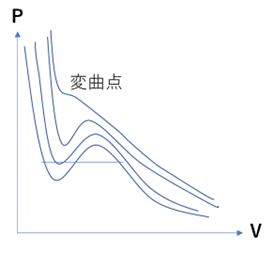
(b) π= P/Pc, φ = V/Vc, τ = T/Tcをそれぞれ換算圧力、換算体積、換算温度という。この3変数のあいだの関係式を求めよ。
【問題4】
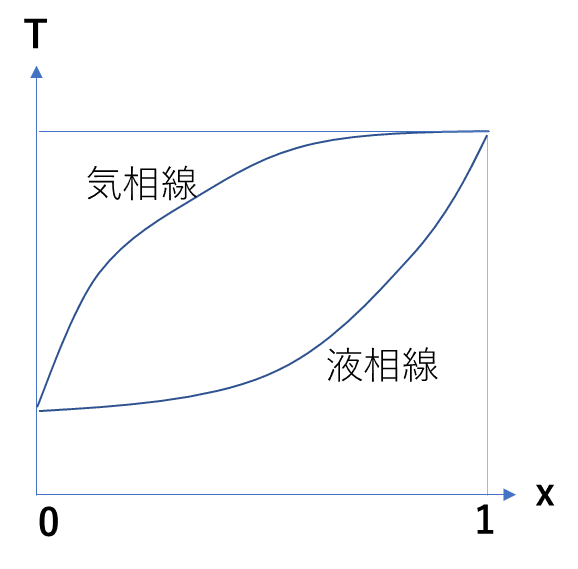
二種類の液体1と2の混合溶液がある。どちらかの成分の液相または気相中におけるモル分率に対して混合物の沸点をグラフ化したものを相図という。相図には液相線と気相線があり、ある沸点で平衡にある液相、気相中のモル分率を示す。いま、成分1と2の蒸気圧曲線がそれぞれP = p₁(T)、P = p₂(T)なる温度Tの関数で与えられているとする。常圧で混合溶液の沸点がTで、液相と気相が平衡にあるとき、液相における成分1のモル分率x₁、気相における成分1のモル分率y₁を求めよ。ただし、大気圧をP₀とする。
【問題5】
メタンとプロパンを空気比1.2で完全燃焼させると、水分を除いた乾き燃焼排ガス中の二酸化炭素濃度が10 体積%であった。はじめのメタンとプロパンのモル比を求めよ。ただし、空気の体積組成は酸素80%、窒素20%とし、それ以外の成分は考えなくてよい。ただし、空気比とは実際に使った空気の量を理論所要量で割ったものであり、気体については理想気体を仮定してよい。
【問題6】
(a) 水に不溶な液体化合物を水と混合して蒸留すると、その化合物のもとの沸点より低い温度で沸騰がはじまる。これを水蒸気蒸留というが、なぜ低い温度で沸騰がはじまるのか理由を付して説明せよ。また、このときの留分の質量比(化合物/水)はそれぞれの蒸気圧と分子量の積の比になることを示せ。
(b) 水蒸気蒸留において食塩など他成分に影響しない不揮発性の水溶性塩類を添加すると混合物の沸点はどのように変化するか、理由を付して述べよ。
解答・解説は有料にて公開しております。
この記事が気に入ったらサポートをしてみませんか?

