第3章【結合・分子構造】
●結合や分子構造を考えるにあたっては、まず、電子の数を数えることが大切です。とくに価電子と呼ばれる外殻の電子は結合を形成する重要な役割を担っており、結合にほとんどあずからない内殻の電子とは一線を画して扱います。
●分子構造を予測する経験則はいくつかありますが、いずれも厳密なものではなく、とくに対称性の問題を先験的に予測する方法はないと言ってよいでしょう。これはいわゆる対称性の破れの問題を含んでおり、最終的な答えを求めるには実験か分子構造の数値計算によるしかありません。高等学校の範囲では、非共有電子対の有無とその電子間反発、電子数、周期律などの情報を勘案して最も妥当な分子構造を考えることになります。
●結合長や結合角、極性、水素結合などは分子構造論の基礎研究として重要で、それに伴う物性も化学的になじみ深いものが多いため、入試でも頻出の分野です。
それでは問題を6問。
【問題1】
次の問に答えよ。
①水素原子、炭素原子、窒素原子、酸素原子における価電子の数はいくつか。また、価電子でない電子はそれぞれいくつか。
⓶アンモニウムイオン1個に含まれる価電子数はいくつか。また、価電子でない電子数はいくつか。
③有機分子における炭素間の一重結合、二重結合、三重結合を結合長が大きい順に並べよ。
④エチレン、ベンゼン、グラフェンの分子について、隣り合う炭素間の結合長が大きい順に並べよ。
⑤塩化水素分子のH-Cl結合は共有結合あるいはイオン結合のどちらに分類されるか。
【問題2】
①次の分子において非共有電子対の数はいくつか。
水、アンモニア、三フッ化ホウ素、二酸化窒素、ホルムアルデヒド
⓶次の分子またはイオンのうち、平面型でないものはどれか。
ベンゼン、三フッ化ホウ素、ホルムアルデヒド、オキソニウムイオン、エチレン
③次の分子またはイオンにおいて正四面体構造でないものはどれか。
メタン、アンモニウムイオン、シラン(SiH₄)、
テトラアンミン銅(Ⅱ)イオン、テトラアンミン亜鉛(II)イオン
④次の現象のうち、水素結合に直接由来しないものはどれか。
DNAの二重らせん構造、水分子の会合、酢酸分子の会合、
水分子の屈曲型構造、水の凍結における体積の膨張
⑤アルコール分子の会合度は極性溶媒または非極性溶媒中のどちらでより高いか。理由を付して述べよ。
【問題3】
(a) 次のそれぞれに示す2種類の元素のうち、より大きい原子半径をもつのはどちらか。
① NaとCs ⓶ BeとMg ③ NとSb ④ FとO ⑤ NaとMg
(b) 次のイオンをイオン半径が小さいものから大きいものへと順に並べよ。
N³⁻, Na⁺, F⁻, Mg²⁺, O²⁻, Al³⁺
【問題4】
二原子分子の双極子モーメントは(電荷×原子の位置ベクトル)の和で定義されるベクトルで、二原子分子の場合はその大きさが電荷×原子間距離となる。その大きさの単位はD(デバイ)で表し、1 D = 3.336 × 10⁻³⁰ C・m(クーロン×メートル)である。臭化水素分子の双極子モーメントは0.82 Dであり、水素原子と臭素原子の距離は1.414 Åである。臭化水素分子の共有結合性は何%か。ただし、電気素量は1.60×10⁻¹⁹ Cとする。
【問題5】
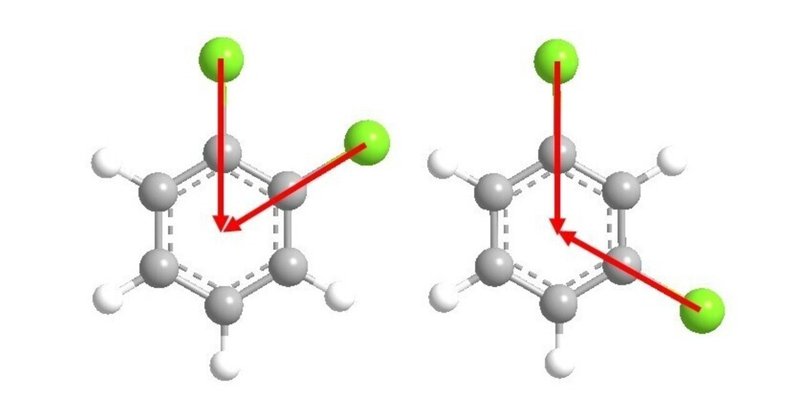
クロロベンゼンの双極子モーメントが1.57 D(デバイ)であるとき、オルトジクロロベンゼン、メタジクロロベンゼン、パラジクロロベンゼンの双極子モーメントを推算せよ。
【問題6】
下図は、ある化学種Aの中性状態A、陽イオンA⁺、陰イオンA⁻におけるエネルギー変化を示したものである。横軸は電子数N、縦軸はエネルギーEを表す。次の問いに答えよ。

(a) 中性状態Aにおける曲線の勾配(一次微分)の大きさが近似的に(1/2)(Ip+Ea)で表されることを示せ。ただし、Ip, EaはそれぞれAのイオン化エネルギーと電子親和力である。
(b) マリケンは電気陰性度を(1/2)(Ip+Ea)で定義した。なぜこの式が電気陰性度の定義として妥当であるか説明せよ。
(c) 中性状態Aにおける曲線の曲率(二次微分)の大きさが近似的に(Ip-Ea)で表されることを示せ。この量を2で割った(1/2)(Ip-Ea)は硬さ(hardness)として知られ、酸・塩基の反応性の尺度となる。
解答・解説は有料にて公開しております。
この記事が気に入ったらサポートをしてみませんか?

