
【有機化学のための物理化学】「熱力学的支配」と「速度論的支配」の具体例
(※2023/03/31 追記)
熱力学的支配を受ける反応とは、熱力学という理論をもとに説明される反応のことで、速度論的支配を受ける反応とは反応速度論に基づいて説明される反応のことです。
理論とは結果を説明するための手法であり、つまり結果に基づいて、それを説明するための理論が選ばれます。理論に基づいて予測を立てることは出来ますが、その予測が真実として正しいかどうかは結果が出るまで明らかに出来ません。
私が「熱力学的支配」と「速度論的支配」という概念についてピンと来ていなかったのは、理論というものの性質を理解していなかったためでした。何を言っているかわからない方のために、いずれ理論とは何か説明するための記事の作成を予定しています。
--
(以降本編)
この記事は、有機化学反応を理解していく上で、なぜ物理化学、特に熱力学と反応速度論の知識が必要になってくるのかという事を自分なりにまとめたノートです!
化学や物理のまともな教養なしに有機化学を専攻し、今に至ってしまったので、今更ながら有機化学をやっていくうえで必要そうな概念を勉強しなおしています。
化学の基本概念は「分子」と「反応」という2つからなりますが、分子については、単にエンジニアとして実験を行っていく上では、割とその場その場でその系に関わる分子特性を勉強して間に合うものがほとんどな気がしています。(もちろん、可能であれば体系的に学べるとよいですが、少し途方もない気がします!)
さて、反応ですが、よく「熱力学的支配」「速度論的支配」という点で議論されているのを見かけます。例えば酸塩基反応は熱力学的に進行し、求核反応は速度論的に進行すると説明されますよね。
ここで、分子の安定性について議論するのが熱力学的な支配で、いかに早く反応するかを議論するのが速度論的支配であるという事、なんとなくは理解でき、実際に化学反応を議論する、つまり問題を解くことはできるのですが、これについて、個人的に腑に落ちたと言えるレベルまで理解を深めるには至っていないので、この度この概念について追求し、ノートにまとめてみようと思いました。
ただし注意していただきたいのは、本記事は個人的な理解を深めるためにまとめるというのが目的であり、第三者にとってわかりやすいように説明する意図は無いということです(はっきり言って、分かりやすくはないと思います)。どうかそのつもりで読み進めていただけると幸いです。
しかしながら議論は大歓迎ですので、この記事の内容について何か不備や誤りがありましたら、ご指摘およびご教授の方いただけると大変うれしく思います。
--
まず、有機化学の反応を突き詰めると物理化学に帰着すると思うのですが、その中で特に有機化学に関連深い領域が「熱力学」と「反応速度論」というところになります。
まず初めに、速度論的支配と熱力学的支配のイメージを深めるためにいくつか具体例を紹介します。
こちらは速度論的支配と熱力学的支配の説明でよく引き合いに出されるブタジエンと臭化水素(HBr)の反応です。

まず、オレフィンが塩基としてプロトンを引き抜くわけですが、プロトンは1、2、どちらの炭素に付加するのでしょうか。カルボカチオンの安定性を考えて1番目の炭素につきます。
また、この二級カルボカチオン中間体は二重結合と共役しているため安定性が高いと言えます。仮に2番目の炭素に水素が付加したとしても、プロトン転移が起こるという事は十分考えられます。

ここで生じるカルボカチオン中間体のふたつの共鳴構造のうち、どちらに臭化物イオン(Br-)が付加するかという話ですが、共鳴構造の安定性を考えたとき、二級カルボカチオンの方が安定性が高いということは分かります。
しかしながら考えられる2つの生成物を見てみると、二置換アルケンと一置換アルケンとでは、二置換アルケンの方が安定であるため、二置換体のアルケンの方が多く得られそうです。

速度論的には1が生成しますが、熱を与えて無理やり化学平衡を起こすことで、活性化エネルギーの壁を越え、より安定な構造である2を得ることができるようになる、という話です。
熱を加えることで無理やり化学平衡を起こす、というのがポイントなんですね。
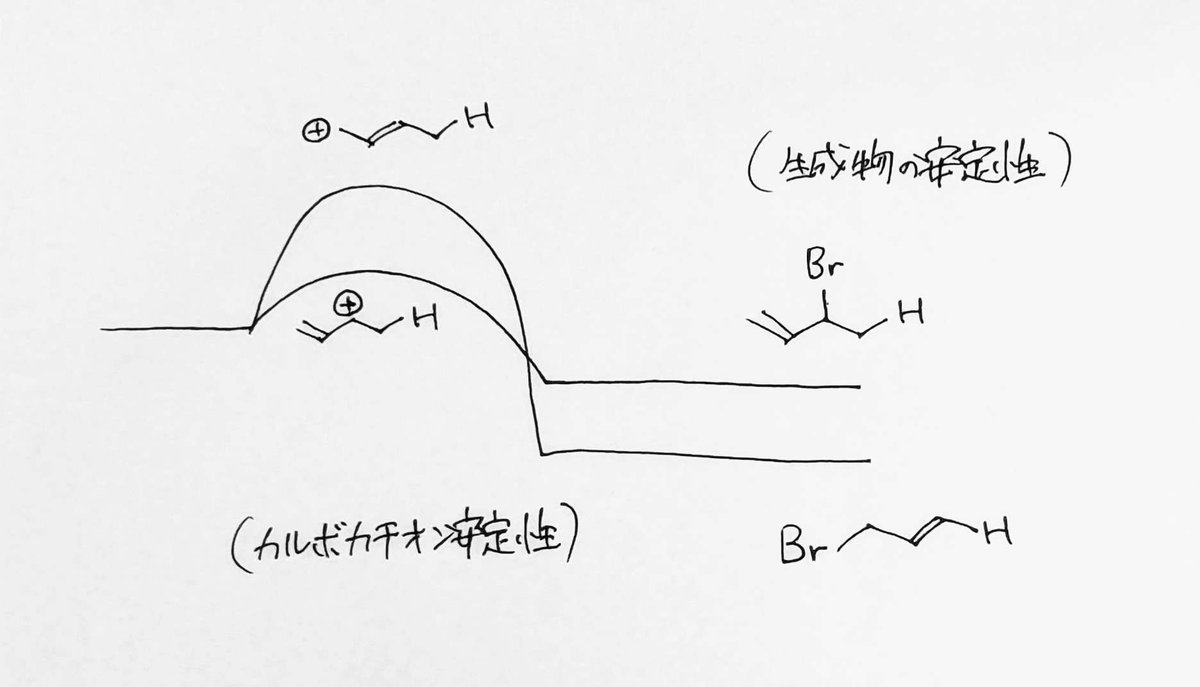
端的に言えば、高温で最終的にいきつく反応を考えるのが熱力学的な議論といえます。
(参考)YouTube:もろぴー有機化学・研究ちゃんねる
【大学有機化学】速度論的支配と熱力学的支配:活性化エネルギーが反応の生成物を変える!!
続いて実践的な例を見てみましょう。
こちらのアミンとカルボン酸を縮合させたいと考えます。

ここで熱を与えて化学平衡を起こすことを考えるとどうでしょうか。目的の反応とは別に、アミド結合が分解されてしまうことが考えられますよね。
そのため縮合反応のみを効率よく進行させるために、DCCをはじめとする縮合剤を用いたり、塩化チオニルを用いて酸クロライドを生じさせたりといった、速度論的な反応を行う必要があります。
同じく縮合の例で、こちらはポリイミドです。

通常、ポリイミドといえば環状イミド構造を持つポリマーを指し、芳⾹族テトラカルボン酸とジアミンを原料とした重縮合によって得られます。
ポリイミドの合成法はいろいろありますが、次は最も簡単な例です。
ジアミンに酸無水物を加えると、発熱を伴いポリアミド酸を得られます。これは中和反応で、平衡は大きく生成物側に傾きます。平衡を考えているわけですから、熱力学的な支配を受けますね。

続いて加熱することで脱水環化させ、イミド化します。こちらも平衡反応で、熱力学的支配を受ける反応です。平衡を生成物側に傾けるために、ディーンスターク装置を用いて水を除きながら合成を行うんだと思います。
またポリイミドは、一旦任意のアルコールで環化させ、生じたエステルを維持したままジアミンと縮合させポリアミド酸とし、最後に熱をかけイミドを得たい場合があります。
実は今僕が仕事で主に扱っている反応がこれなんですよね。任意のアルコールとエステルを形成したポリアミドを、ポリイミド前駆体として欲しい場合があるんですよ。
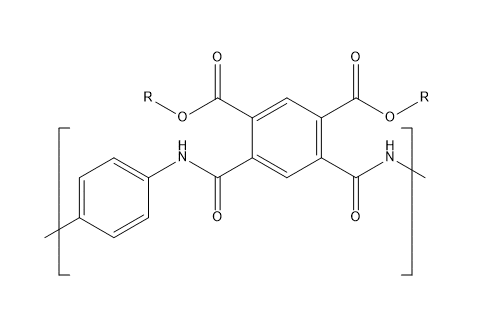
ここでポリアミド酸を合成するためには、先ほどのアミノアミドの例と同じように、縮合剤や塩化チオニル法を用いて速度論的支配をうける反応で縮合を行います。熱を与えることで熱力学的に反応を進行させようとすると、エステルが分解しイミド化まで進んでしまいます。
以上いくつか例を挙げてみましたが、熱力学的支配を受けるか、速度論的支配を受けるかという議論は、高温で反応させたときに最終的にいきつく反応というものを考えれば良よさそうだ、というところが見えてくると思います。
ひとまず今回の記事では、ここまででとどめておくことにしましょう。
次回以降から、有機化学反応に関わる反応速度論、熱力学の実践的な理論を掘り下げていこうと思います。
(とはいえ気分次第なので、以降の記事は出ないかもしれません…)
ここまで読んでいただきありがとうございます。
僕のほしいもののリストです。
何か買ってください。
この記事が気に入ったらサポートをしてみませんか?
