
中2理科の化学反応式を【理解】する(10) 硫化反応と組成式
中2理科の教科書を読んでいるところです。
前回のおはなしはこちら
最初から読みたい場合はこちらから。
3.硫黄と結びつく化学変化(硫化)
【実験】
鉄と硫黄の粉末を混ぜて加熱する。加熱前後の性質を調べて,以下のことを確認する。
できた物質は磁石につかなくなる。
できた物質にうすい塩酸をかけると,腐卵臭を持つ気体が発生する。
鉄 + 硫黄 → 硫化鉄
$${Fe + S → FeS}$$
【実験】銅線を硫黄と一緒に加熱する。加熱後の物質は青色になる。
銅 + 硫黄 → 硫化銅
$${Cu + S → CuS}$$
分子式と組成式
酸素との反応を酸化と呼ぶのと同様,硫黄との化学反応を硫化と呼びます。
【酸化】 物質 + 酸素 → 酸化物
【硫化】 物質 + 硫黄 → 硫化物
硫黄は周期表で酸素の下に位置するので,性質が似ています。考え方は酸化と同じなので,あえて何か新しいことを言う必要はないよね,と思っていました。しかし・・・ある時,気がついたのです。
$${Fe + S → FeS}$$
「あれっ,この化学式,これでいいんだろうか。硫黄は,たしか分子じゃなかったか?」
実は黄色い粉末状の硫黄は8個の硫黄原子が閉じた輪のようにつながって王冠の形になった$${S_8}$$という分子からなる結晶です。
ですから,化学反応式は以下のようになるはずではないだろうか・・・?
$${8Fe + S_8 → 8FeS}$$
ところが教科書には,物質名反応式と化学反応式の間に,以下のような粒子モデルが載っています。
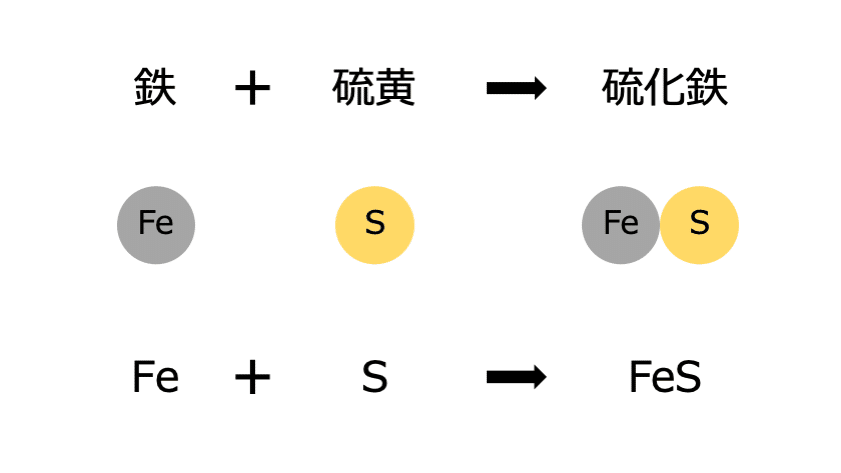
鉄も硫黄も硫化鉄も,なんだか1個の原子や分子のように描かれているのです。これは分子を作らない物質が持つ,多数の原子の「代表」であると,教科書の前のほうに書かれていました。

銀や食塩の構造は明確なのに,硫黄や硫化鉄の構造は教科書には載っていません。そういえば,これまで出てきた銅や酸化銀などの固体も同様に表現されていました。ここまで来て,「ああ,そういうことか」と思い当たりました。実は,結晶構造は高校化学の学習内容なので,中学校では教えることができないのです。

ですから結晶構造は示さずに,その代表だけを抜き出して粒子で表現し,それを化学式に置き換えるという作業をやっているのでしょう。固体を表す化学式は,どんな元素をどのような割合で含むのかだけを意味する「組成式」だったのですね。
一方,「分子式」は分子に含まれる元素の数を,元素記号の右下に小さな数字で示したものであって,これも,分子の立体構造に関する情報を持っているわけではありません。
化学式の意味
私は原子論的世界観だのイメージが大切だのと言ってきました。ですがその前に大切なことは,物質を元素に分解し,その元素が「どのような割合で含まれているか」という情報を真っ先に得ることだったのです。
もし硫黄の分子や硫化鉄の結晶構造を教科書に載せたらどうなるでしょうか。これまで分子として習ってきたものは,空気を構成するごく単純な構造を持った気体や水で,その後よく利用されます。ですが硫黄分子が$${S_8}$$であると覚えても,中学理科の範囲内では,その後その知識を利用する場面はありません。
また,硫化鉄は食塩とは全く異なった構造を持つ物質で,しかも,いくつか種類があります。情報を追加すればするほど化学は難しくなるだけで,中学生をただただ困惑させることにつながります。
したがって中学校では,分子を作るいくつかの重要な物質だけを分子式で表し,ある程度明確な分子のイメージを持たせる。一方,固体物質については分子を作らないことにした上で組成式で表現し,構造は脇に置いておき,考えない。
そうすることで,まずは単純な化学反応式を覚え,書くというスキルの向上に集中するという意図があるのかもしれません。
中学理科の学習指導要領を見ると,やはりこう書いてありました。
(内容の取り扱い)
イ アの(イ)のアの「化学式」及び「化学反応式」については,簡単なものを扱うこと。
ウ アの(イ)のイの「酸化や還元」については,簡単なものを扱うこと。
$${Fe + S → FeS}$$
結局,上式は原子が1つづつくっついて$${FeS}$$という分子をつくる,という意味ではありません。固体の鉄と硫黄が1:1の原子数比で結合して,固体である硫化鉄に変わることを意味しています。
この辺り,私も気が付かなかったのですが,中学生ならなおさらでしょう。今回の教科書の読解でわかったことは,化学式の意味のわかりにくさでした。明確なイメージ化ができる分子式よりも,イメージ化が難しく,やや抽象的な固体の組成式のほうが,明確に書かれていない分,混乱しそうだなという印象です。
次回のおはなし↓
まとめページ↓
この記事が気に入ったらサポートをしてみませんか?
