書記が物理やるだけ#274 水素分子の解法(原子価結合法と分子軌道法)
多電子系の解法として,原子価結合法と分子軌道法を紹介していく。
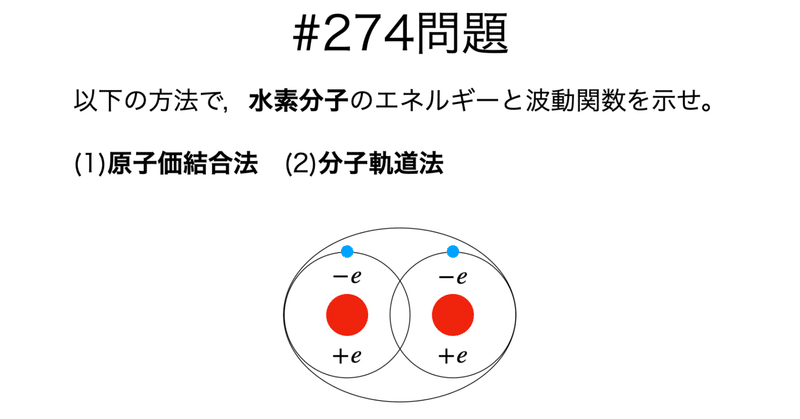
問題

説明
原子価結合法について:
1916年,G・N・ルイスは,化学結合が2つの共有された結合性電子の相互作用によって形成されると提唱し,ルイス構造として分子を描写した。1927年、量子力学的考察に基づいて水素分子H2の結合特性の計算を初めて可能にしたハイトラー–ロンドン理論が立てられた。。後に,ライナス・ポーリングは共鳴(1928年)と軌道混成(1930年)というVB法における2つの重要な概念を生み出すためにハイトラー-ロンドン理論とルイスの対結合の考えを使った。また,ジョン・スレーターとライナス・ポーリングによって多原子系に拡張された。そのため,ハイトラー・ロンドン・スレーター・ポーリング法、略してHLSP法と呼ばれることもある。

分子軌道法について:
1927年に原子価結合法が成立した後,フリードリッヒ・フント,ロバート・マリケン,ジョン・クラーク・スレイター,ジョン・レナード-ジョーンズらによって開発された。分子軌道理論はもともと「フント-マリケン理論」と呼ばれていた。「オービタル」という名前は1932年にマリケンによって導入された。1933年には分子軌道法は,有効な理論であると受け入れられるようになった。ドイツの化学者エーリヒ・ヒュッケルによると,分子軌道法の最初の定量的な利用は1929年のレナード-ジョーンズによって成された。分子軌道波動関数の正確な計算は,1938年にチャールズ・クールソンが水素分子について行った。1950年には,分子軌道は「自己無撞着場ハミルトニアンの固有関数(波動関数)」として厳密に定義され,分子軌道法は厳密でつじつまが合うものになった。この厳密なアプローチは分子におけるハートリー-フォック法として知られている。分子の計算において,分子軌道は原子軌道基底の観点で拡張され,ルーターン方程式が開発された。これは多くの非経験的分子軌道法の発展につながった。またそれとは別に,半経験的分子軌道法として知られる方法で導かれた経験的なパラメーターを用いる多くの近似法でも分子軌道法は適用される。

解答
まずは原子価結合法から。

ここで,粒子の同等性と反対称性を導入していく。

これにより,エネルギーがクーロン積分・変換積分・重なり積分により表される。

次に分子軌道法について,これは原子軌道でやったようにスレーター行列式から解いていく。


本記事のもくじはこちら:
学習に必要な本を買います。一覧→ https://www.amazon.co.jp/hz/wishlist/ls/1XI8RCAQIKR94?ref_=wl_share
