
難関大受験生は、過去問から知識の再構築をしよう【2019年化学[3]】
今回は、九州大、2019年化学第3問について書いてみます。
本稿のテーマは、知識の再構築です。
最初は、限界半径比についての理解です。
現役生を中心に「限界半径比って何?」となっている受験生も多いかもしれません。頻度はそこまで多くはないので、問題集での演習や模試ですり抜けてしまう可能性もあるテーマの一つといえそうです。
こちらのサイトで詳しい解説があります。
難関大受験生としては、しっかりと抑えておくべき知識といえます。九大の本問は塩化ナトリウム型結晶を扱っていますが、知らなかった受験生は、これを機に、塩化セシウム型、硫化亜鉛型(閃亜鉛鉱)の理解も深めておきましょう。
では、実際に出た九大の問題ですが、随分と簡略して出題しています。

面心立方格子型のNaClの正面からの結晶構造を図示すると
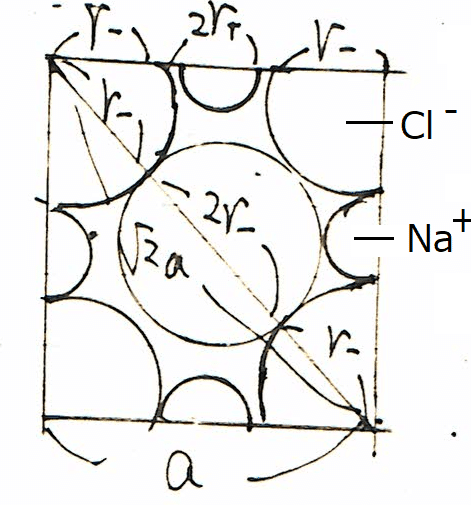
となります。1辺の長さを aとすると、

となり、aを消去すると、

と変形できます。あとは、本問では、r(-)を1と置いているので、変形していきます。

となります。
次にアルミニウムの溶融塩電解(融解塩電解)です。

これを踏まえての設問がこちらです。

アルミニウムの原子量を27として解いていきます。
さて、アルミニウムの溶融塩電解の陽極の式って覚えていますか?
[ウ]と[エ]には、知識として一酸化炭素、二酸化炭素が入ることを知っている受験生は多いかなと思いますが(本問はこの次の文章でウがCOと特定されます)、半反応式は知らないという受験生は多いのではと思います。

がそれになります。私も標準向けのプリントでは、ここは覚えなくても大丈夫と言っていますが、難関大受験生の場合はそうはいきません。
知らなかった人はここで知識を得ておきましょう。
本問は、陰極の式

から電子のモルを0.6(mol)と特定し、

からの関係性から二酸化炭素の体積を導出します。

となります。
難関大受験生は、このような過去問演習を通じて、知識の再構成をしていきましょう。
「当たり前」はこのような場で修正が必要です。
この記事が気に入ったらサポートをしてみませんか?
