
いつか役立つ!知って得するマイナー溶媒25選
1. 初めに
実験に欠かさせないものといえば溶媒です。ほとんどの有機合成反応は何らかの溶媒環境下で進行しますし、反応後の抽出、精製、分析にも溶媒が必要になってきます。一般的に溶媒というのはどの実験操作においても系内で最も大量に存在する物質となり、実験がうまく行くか行かないかを大きく左右するファクターの一つであるといえます。しかしながら、ちょっと構造が違う溶媒に変えるだけでも反応・精製・分析における挙動が大きく変わってしまうことが多く、実際その系にはどの溶媒が最適なのかはやってみなけりゃわかんないことの方が多かったりします。それでも、いやだからこそ、多くの溶媒に対する知識を深めて最適な溶媒を選択・提案できる力を身に着けることができれば、また一歩化学者として成長することができるのです。というわけで、本稿では溶媒として使われる物質をつらつら紹介していこうかなと思います。
2.本稿におけるメジャー溶媒とマイナー溶媒の定義
到達が容易な条件下で液体の物質なら原理上何でも溶媒として利用できるわけですが、実験溶媒としては沸点融点や反応性が扱いやすく溶解性が高く安定性も高く毒性は低くそれでいてなるべく安いものが求められます。そうなると適する物質は意外と限られます。実験室で溶媒として汎用されている物質は以下に示すものが主ではないでしょうか。

図1. 本稿における「メジャー溶媒」。
図1に示す物質はどれも融点融点が扱いやすく溶解性も優れているため、大体の実験における溶媒はこの中からいくつかチョイスすれば完遂できると思います。しかしながら、世の中で溶媒として使われる物質は他にもいろんな種類があり、系によっては図1に示す汎用溶媒を使うよりも反応選択性や光学純度、収率、反応速度などの点で優れた結果をもたらしてくれるものも多いです。そこで図1に示す物質をメジャー溶媒、それ以外の溶媒として用いられることがある物質をマイナー溶媒と定義し、本稿ではそんなマイナー溶媒についていくつか紹介していきたいと思います。ただ分野によっては図1の溶媒なんてむしろほぼ使わないなんて方もいらっしゃるかもしれませんし、は?それ全然マイナーじゃ無くね?と思う方もいらっしゃるかもしれませんが、まぁそこはどうか抑えていただきまして……。メジャー溶媒の皆さんはどれも非常に重要な物質なのでいつか各論で記事を書きたいですね。
3.マイナー溶媒の紹介
※1 なるべくアルファベット順で記載しています。
※2 出典や参考文献は膨大な量になってしまうことが予想されるのであえて記載していません。一部著者自身の感想に近いものや他の研究者から聞いただけの情報も入っているのでまぁ参考程度にということで。
※3 特に記載がなければ融点沸点等は1気圧下の値です。
※4 溶媒の日本語名は一般的(と個人的に判断した)なものを採用しています。
※5 各物質はあくまで「溶媒として」見た場合の性質の紹介にとどめます。
※6 値段は本稿執筆時のものです。あくまで参考までに。
※7「他にもこんな溶媒知ってるよ!」や「この溶媒は紹介されてること以外にもこんな時こんな使い方できてめっちゃ便利だったよ!」などの情報がありましたら是非コメントや著者のTwitterなどで教えていただけますと大変ありがたいです。
● 1,1,1,3,3,3-hexafluoro-2-phenyl-2-propanol [ 1,1,1,3,3,3-ヘキサフルオロ-2-フェニル-2-プロパノール, HFPP ]

沸点:160 ℃ / 融点:ー ℃ /密 度:1.45 (25℃) / 水と混和
LD50=ー / モル質量:244.14 g/mol
25g:23,000¥(TCI)
・好んで使われているのをほぼ見かけないプロトン性極性フルオラスアルコール溶媒です。
・有機合成でわざわざこの子を使わないとダメだという場面はほぼないと思いますが、ポリマー合成の場合は最後の切り札的存在たる子なので高分子を扱っている方は覚えておくといつか役に立つかもしれません。
・他の主要溶媒にはとけない剛直なポリマー、超高分子量ポリマーでもこの子なら溶かせる場合があります。特にポリスチレン系とポリアクリル系、ポリメタクリル系には強いです。
・HFIP等他のフッ素系アルコール溶媒と比較して沸点が高いので、加熱が必要な反応や重合、リビングラジカル重合の溶媒として使用可能です。
・弱酸性を示すため化合物中に酸に弱い部位がある場合は反応と分解を誘発する可能性があります。
・できた化合物やポリマーがこの子にしか溶けないとなるとその後の分析がやっかいですが、この子に溶けるやつはHFIPにも溶けることが多いので試してみましょう。HFIP-d2はまだ買える値段なのでNMR測定ができる希望があります。
・たっけえんですわ値段が。普段使いの溶媒ではないですね、ここぞというとき試してみる溶媒です。使ってみたいときは上司とよく相談しましょう。あと財布。
● 1,1,1,3,3,3-Hexafluoro-2-propanol [ ヘキサフルオロ-2-プロパノール, HFIP ]

沸点:58.2 ℃ / 融点:-3.3 ℃ /密 度:1.60 (20℃) / 水と混和
LD50=600 mg/kg(マウス経口) / モル質量:168.04 g/mol
500g:73,500¥(TCI)
・幅広い有機化合物とポリマーに対し高い溶解性をもつプロトン性極性フルオラスアルコール溶媒です。
・プロトン性高極性溶媒ながら高い揮発性を有しています。
・電離力と酸性度(pKa=9.3) が高いですが求核性は低いです。
・他の主要溶媒では溶けにくい多くの剛直性ポリマーや結晶性ポリマーに対する良い溶解性を有しています。特にポリエステルやポリアミド、ポリエーテル、ポリケトン等の水素結合性官能基を有するポリマーに対しては良好な溶解特性を示します。
・トリフルオロエタノールやトリフルオロ酢酸等と比較し反応性がマイルドでかつ溶解性も優れていることが多いです。
・HFIP-d2(HFIPの重溶媒) は購入できるので難溶解性ポリマーのNMRを取りたい時の最後の希望です。著者も助けられたことがあります。
・優れた水素結合ドナーであるこの子は強い水素結合で凝集している構造に割り込みそれをほぐすことができます。特にペプチドを扱う際に役立ち、溶媒としては勿論添加剤として用いてもよい効果を発揮してくれます。
・水とは混和しますが塩水溶液に対しては相分離させることができます。
・多くの有機溶媒と混和しますが飽和炭化水素に対しては相分離します。
・多くの酸化還元環境下で不活性であるため、電気化学反応や光酸化反応、高酸化試薬を用いる反応でも溶媒として使用できます。
・ラジカル重合用溶媒としても使用可能です。
・Morita-Baylis-Hillman反応の助触媒として用いると反応を加速させられることがあります。
・溶媒としても有能ですが試薬として使う機会も多い物質だと思います。例えば酸に弱い官能基存在下でN-bocだけを脱保護したい時とか超原子価ヨウ素試薬を用いる反応の促進剤として入れるとか。
・Pd触媒によるC-H活性化反応においてこの子を溶媒として使うと、他の溶媒にはない非常に特異な挙動(いい意味で) をするようです。
・というより反応系によってはこの子だけで達成できるC-H活性化もあるようです。
・Friedel-Crafts Acylationにおいてこの子を溶媒として使うと、溶媒兼基質活性化剤として作用し特にルイス酸などを添加せずともしかも室温で反応を進行させられるそうです。はえー便利。なお、電子豊富アリールじゃないとダメという制約はあるみたいです。
・私は見たことありませんがGPC溶離液としても使われてるみたいですね。ランニングコストえぐそう。
・この溶媒で立体特異的な反応系を見つけたという報告はありますが、一方でキラル触媒を用いた不斉合成反応の溶媒としては今のところ不向きとみられているようです(キラル触媒と基質とのイオン対形成がHFIPによって妨げられるためとかなんとか) 。ここら辺うまいことできればいいジャーナルに載せられるんじゃないでしょうかね。
・そこまで毒性が強いわけではありませんが、フッ素系溶媒にありがちな高い揮発性をもっておりその蒸気は強烈な臭気と腐食性がありますので安全装備をしっかりしましょう。多くの樹脂やグリースを容易に溶かすのでそれらが蒸気に触れないように注意しましょう。
・比重的にクロロホルムよりも重いので気を付けて扱ってください。いつもの軽い有機溶媒の感覚で容器をもったりすると思わぬ重さでつるっといったりします。
・弱酸性の溶媒なので塩基性水溶液で分液とかやらかさないように。
・くっさいくっさいだしたっかいたっかいなのです。ご利用は計画的に。
・そんなこんなで最近結構ホットな溶媒になってる気がしますね。IFが高めのジャーナルでHFIPでやったらこんなんできましたー!だけみたいな論文をちょいちょい見ますし。
● 1,2-Dimethoxyethane [ 1,2-ジメトキシエタン, DME ]

沸点:85.2 ℃ / 融点:-58 ℃ /密 度:0.87 (15℃) / 水と混和
LD50=2525~7000mg/kg(ラット経口) / モル質量:90.12 g/mol
500g:4,500¥(TCI)
・THFやジオキサンの代替で使える高沸点の非プロトン性極性エーテル溶媒です。著者のお気に入り溶媒の一つです。
・ジエチルエーテルやTHFでなんかうまくいかない反応は試しにこの子を使ってみるといいことがあるかもしれません。
・DMFの低沸点代替溶媒としても使用できます。
・二座配位性溶媒として振る舞いカチオンを溶媒和させます。その性質から有機金属反応の溶媒として優れており、Buchwald-Hartwigカップリングや鈴木-宮浦カップリング等のパラジウム触媒系反応やGrignard反応等で優れた結果をもたらしてくれることがあります。
・一部嵩高いエノラートのアルキル化でも優れた効果を発揮することがあります。
・ポリマーの溶解性も申し分ありません。また糖やアミノ酸などの超高極性化合物も場合によってはこれ単体で、もしくはDME-水系やDME-アルコール系で溶かせることが多いです。
・エーテル系溶媒の中では比較的過酸化物を作りにくいです。
・総じて優秀な溶媒ですがお値段がやや高めです。
・発癌性や生殖毒性が確認されているので注意しましょう。とはいえ常識的な安全設備のもと使えばさほど大きな問題ではありません。
・吸湿性が非常に強く無水状態にするのが大変です。ナトリウム-ベンゾフェノン系では不十分であることが多く(経験上)、きっちり無水状態にしたいならモレキュラーシーブ3A等での予備乾燥をマジできっちりするか金属カリウムを用いた蒸留精製をする必要があります。しかも放っておくとすぐ吸湿してしまうので保管しようと思わず面倒でも都度精製しましょう。無水のやつを購入するのが楽なのですがクッソ高いのですよ……。
・ジメトキシエタンはよくDMEと略されますが、ジメチルエーテルも普通DMEと略されるのでごっちゃにならないよう注意しましょう。
● 1,3-dimethyl-2-imidazolidinone [ 1,3-ジメチル-2-イミダゾリジオン, DMI, DMEU ]

沸点:225 ℃ / 融点:8.2 ℃ /密 度:1.05 (25℃) / 水と混和
LD50=300~2000mg/kg(ラット経口) / モル質量:114.15 g/mol
500ml:6,300¥(TCI)
・HMPAやDMFのより毒性が低く安定な代替溶媒として使用できる、環状ウレア構造を有する非プロトン性極性溶媒です。大体の反応系で反応だけなら問題なく代替できます(精製・分析も代替できるとは言っていない)。
・DMI自体の毒性は低く刺激性もほぼありませんが、溶解している物質の皮膚浸透性を高めるのでなるべく皮膚接触しないようにする対策は必要です。
・様々な有機化合物やポリマーを溶解でき、無機塩の溶解性も良好です。
・誘電率と双極子モーメントがDMF等と同等以上であり、その高い溶媒和効果により求核反応やカチオンの溶媒和を経る反応を促進できます。
・飽和炭化水素系溶媒を除く様々な溶媒と混和できます。
・同じくDMFやHMPAの代替溶媒として使用できるNMPに比べても酸塩基に対する耐性が高く高温条件でも安定しています。
・融点が高く除去がむずめですが、分液が可能ならジエチルエーテルかトルエンに溶かした後水で抽出除去するのが適当です。ただ・・・まぁ残る時はしつこく残ります。
・これ系の溶媒にありがちですが、吸湿性が強く脱水状態にするのがなかなか難しいですし手間です。
・長期間酸素に晒すと酸化される可能性があるため、特に蒸留精製などで安定剤を除去したものは不活性ガスパージして保存するのが賢明です(一番いいのは都度すぐに使い切ることです) 。
・強酸化剤および酸塩化物と混合するのは不適とされていますのでそういった反応に使うのは避けるべきです。
● 1,4-Dioxane [ 1,4-ジオキサン, ジオキサン ]

沸点:101 ℃ / 融点:11.8 ℃ /密 度:1.04 (20℃) / 水と混和
LD50=2000~6000mg/kg(ラット経口) / モル質量:88.11 g/mol
500g:2,300¥(TCI)
・THFと同程度の溶解能力を持つ高沸点の非プロトン性極性エーテル溶媒として使用できます。
・THFよりも沸点が高く高温反応用エーテル溶媒に適しています。
・溶媒としての性質はTHFに似ていますが、THFや他のエーテル溶媒にはとけないものもジオキサンなら溶けるという場合があるので試してみるのは手です。特にジオキサン-水混合系は一部の高極性難溶解性ポリマーの溶解能力に優れています。
・凍結乾燥溶媒として使用可能です。
・催奇毒性を有しておりTHFよりも毒性が強いです。
・吸水性が強く無水状態にするのがやや困難です。水素化カルシウムかモレキュラーシーブで一晩~一日程度予備乾燥させたのちナトリウム-ベンゾフェノン法で蒸留精製するのがオーソドックスな方法です。なお、THF同様乾固させるのは極めて危険なので蒸留の際は注意してください。
・ただ無水にするだけなら活性化モレキュラーシーブ3Aを使うのが簡単ですが、市販のジオキサンには抗酸化剤等の安定剤が入っていることがほとんどなのでそれがやりたい実験に影響しないか注意しましょう。
・THF同様過酸化物を作りやすいので、蒸留精製などで安定剤が除去されたジオキサンは保管しようとせずに速やかに使用するのが賢明です。どうしても保管したい場合は容器を不活性ガス置換して遮光下冷暗所に保管しましょう。その場合でも3日以内には使い切りましょう。
・金属ニッケル(特に粉体)との混合は爆発の可能性があり危険です。Raneyニッケルの反応などに溶媒として使うのは避けましょう。
・融点が比較的高いので単体では低温反応の溶媒に向いていません。
● 1-methoxy-2-propanol (Propylene glycol methyl ether) [ 1-メトキシ-2-プロパノール (プロピレングリコールメチルエーテル) ]

沸点:119 ℃ / 融点:-97 ℃ /密 度:0.92 (25℃) / 水と混和
LD50=4016 mg/kg(ラット経口) / モル質量:90.12 g/mol
500ml:3,000¥(TCI)
・高沸点のアルコール溶媒として、メタノール、エタノール、イソプロパノールの代わりに使用可能です。
・100℃以上の沸点を持ちながら水と混和する一価アルコールというのは限られており、しかも2級アルコールとなるとさらに対象は少なくなります。なので、例えば高沸点の2級アルコール(高級アルコール) 溶媒を使いたいが精製は水への再沈殿がしたいなんて時にこの子の名前をすっと出せるとドヤ顔できます。え?ピンポイントすぎる?……まぁ、うん、はい。
・2級アルコールは1級アルコールよりも求核性に劣るため、プロトン性溶媒を使いたいが加溶媒分解の可能性があるので1級アルコールは怖いというような反応を行う際の溶媒として有効であることがあります。
・高沸点の割には適度な揮発性をもつため、エバポレーターや減圧蒸留での除去が比較的容易です。
・似たような目的で用いられる2-メトキシエタノールが毒性を有するのに対し、この子は毒性が低く比較的安全なことからその代替溶媒として使用できます。
・高温が発生するマイクロ波合成の溶媒としても安定的に使用できます。
・この物質はアルコール溶媒であると同時にエーテル溶媒でもあるので、他のエーテル溶媒同様過酸化物の生成に注意を払う必要があります。
● 2,2,2-Trifluoroethanol [ トリフルオロエタノール, TFE ]

沸点:73.6 ℃ / 融点:-43.5 ℃ /密 度:1.38 (20℃) / 水と混和
LD50=336 mg/kg(ラット経口) / モル質量:100.04 g/mol
500g:19,700¥(TCI)
・エタノールと比較して強い酸性を持ち、トリフルオロメチル基の電子吸引による低い求核性を有するプロトン性極性フルオラスアルコール溶媒です。
・低温でも幅広い物質に対し優れた溶解性を示し、高極性溶媒の中では沸点融点が手ごろで扱いやすいです。
・水素結合性の強いポリマー、特にナイロンなどポリアミドの合成における優秀な重合溶媒&分析溶媒です。
・強力な水素結合供与体として作用し、一部の芳香族求核置換反応やアミンによるエポキシドの開環、エノンおよびアクリレートへのアミンの共役付加といった反応を劇的に促進させることが知られています。
・うまくいかない熱Diels-Alder反応を諦めたくない場合にこれを溶媒として試してみるとワンチャンあります。
・分子内水素結合相互作用を強化することにより、ペプチドおよびタンパク質のα-ヘリックス二次構造が安定化されたまま可溶化させることが知られています。
・値段がお高めなのでここぞってときの切り札にしましょう。
● 2-Methyltetrahydrofuran [2-メチルテトラヒドロフラン, 2-MeTHF]

沸点:80.2 ℃ / 融点:-136 ℃ /密 度:0.86 (20℃) / 水にやや不溶
LD50=300~2000 mg/kg(ラット経口) / モル質量:86.13 g/mol
500ml:10,900¥(TCI)
・水と混和しにくいTHF、簡単にいえばこれにつきます。
・THFの持つ幅広く良好な溶解性はほぼそのままに、酸素に隣接するメチル基の影響で水と混和しにくくなりました。そのため反応させたあと濃縮などを行わずに分液精製等を行うといったことができますしTHFよりも乾燥精製が容易です。
・水とは71℃(水11 wt%)の共沸混合物を形成するので系の大まかな乾燥に使えます。
・THFよりも乾燥が容易なためGrignard反応などの禁水反応の溶媒として使うといい成績が出せることがあります。
・THFよりも溶媒として使用可能な温度範囲が広く低温から高温反応までこなせます。
・キラル分子であるため対称性の良い分子に割って入りそれを攪乱することができることができます。その結果、特定の物質に対しては特異的な溶解特性を示すことがあります。
・総じてTHFの上位互換的溶媒ですが値段が高いです。
・メチル基がついた分THFよりも無機塩の溶解性は低下しています。
・人によってはTHFよりもかなり不快な臭いに感じます。
・THFよりも過酸化物を形成しやすいため注意が必要です。
・水とは混ざりにくいとはいえジエチルエーテルよりは混ざります。
・酸塩基に安定というのを見ますが、THFと比較したとき酸に対しては安定ながら塩基に対してはむしろ弱くなっているというデータがあります。
・他のエーテル同様配位子として振る舞うことがありますが、キラル分子であるために同じ分子相手に複雑な配位挙動をする可能性があります。
・オレフィンメタセシスの溶媒として一般的な塩素系溶媒の代わりに使用することもできますが、メタセシスの過程で二重結合の異性化を促進することがあるようです。
・再生可能資源から製造されるグリーン溶媒なので、昨今の風潮にのってあえてこの子を使ってみるのもいいんじゃないかと思います。SDGsが流行ってる今なら何かの反応溶媒を2-MeTHFにしてもうまくいきましたってだけみたいな論文でも通してくれるかもしれません(そんなに甘くはない) 。
・著者はこの子のことが嫌いなわけではないのですが、THFだって別に水層に塩を思いっきり溶かしてやれば普通に相分離しますし、世に知られ出した当初はまだしも今はもっと優れていてしかも安いエーテル系溶媒が多数市販されている中であえてこの子じゃないと駄目な場面ある?(ひろ〇き) という思いしかないのです、高いですし。勿論系によってはこの子が最適だというのもあるんでしょうから、反応設計時にあげる溶媒候補の一つに常に考えるようにはしていますが……。
● 4-Methyltetrahydropyran [ 4-メチルテトラヒドロピラン ,4-MeTHP ]

沸点:105 ℃ / 融点:-92.0 ℃ /密 度:0.86 (20℃) / 水に不溶
LD50=1000~2000 mg/kg(ラット経口) / モル質量: 100.16 g/mol
500ml:3,400¥(TCI)
・幅広い有機化合物やポリマー、そして無機塩に対して良好な溶解性をもつ比較的新しい環状エーテル系極性溶媒です。
・THFや1,4-ジオキサンのより毒性が低く安全でかつ水と混和しない代替溶媒として反応や抽出、精製に使用可能です。低分子有機化合物は勿論ポリマーについてもTHFとほぼ同等の溶解性を維持できているようです。
・酸塩基に強く幅広い反応で溶媒として使用できます。
・エーテル系溶媒の中では過酸化物を生成しにくく安全性も高いです。
・低温から高温まで幅広い温度領域で溶媒として利用可能です。
・疎水性が高く吸湿性が低いため乾燥精製が比較的容易です。脱水だけでいいなら十分に活性化したモレキュラーシーブ4Aを10wt%程度加えて24時間放置すれば20ppmレベルまでの脱水が達成できるようです。
・水とは85℃ (水19 wt%)の共沸混合物を形成します。そのためDean-Stark装置下で行う反応の溶媒としてトルエンなどの代替として使用できます。当然反応選択性や収率が(良くも悪くも)変化する可能性があるのは注意です。
・物理的な性質としては同じく比較的新しいエーテル溶媒であるCPMEとほぼ同等です(お値段もあまり変わらない) 。しかしながら周辺の立体障害の関係で酸素原子の配位性はCPMEよりも高いようなので、Grignard反応や薗頭カップリング等の有機金属反応、Wittig 反応、鈴木-宮浦カップリング等の遷移金属触媒反応の溶媒としてより優れているといえそうです。
・過酸化物を生成しにくいという特徴から、ジクロロメタンなどの塩素系溶媒の代替溶媒としてオレフィンメタセシスの溶媒に用いることができます。また、同じ用途で使用できる2-MeTHFよりもメタセシスプロセス中の二重結合異性化を抑えられるようです。
・不安定だったりTHFやジエチルエーテルでは調整困難なGrignard試薬(塩化アルキル原料のGrignard試薬等)もこの子なら作ることができたり副反応を抑制できたりすることがあります。
・多くの点で2-MeTHFの上位互換的な使い方ができます。値段もこっちの方がずっと安いです。
・酸化条件下では微量の分解が発生する可能性がありますが、目的の反応自体は問題なく進行することが多いようです。
・やや独特な臭いがしますがそこまで酷い臭いではないです(著者的には) 。
・総じて使い勝手のいい溶媒なのでTHFやジオキサンの疎水性代替溶媒が必要な時はCPMEと並んでファーストチョイス群ですね。ラボに一本常に置いときたいレベルです。
● Acetic anhydride [ 酢酸無水物 ]

沸点:140 ℃ / 融点:-73.1 ℃ /密 度:1.09 (15℃) / 水と反応
LD50=1780 mg/kg(ラット経口) / モル質量:102.09 g/mol
300ml:1,800¥(TCI)
・は?酢酸無水物ってアセチル化試薬やろ、溶媒ちゃうやんけ。と思ったそこのあなた。酢酸無水物は有機物や無機塩の溶解性がよくしかも水と反応して徐々に酢酸に変化するので意外と禁水反応の溶媒として悪くないんです。
・まぁとはいえ酸無水物の構造自体かなり反応性が高いですし、酸無水物構造に不活性でかつ酸(酢酸) が系内にいても問題ない反応というかなり限られた系のみ溶媒として使えますけどね。
・例えば硝酸を用いたニトロ化の溶媒として使われたりしますが、室温下において酢酸無水物と硝酸を混合すると発生する硝酸アセチルが爆発する可能性があるためかなり危険な反応です。他にも糖をアセチル化する反応の試薬兼溶媒としての使い方もあります。
・溶媒として使うにしろ試薬として使うにしろ酢酸無水物は眼への刺激性が非常に強いので必ず保護メガネを着用してください。酢酸無水物は加水分解が遅いため角膜を容易に透過し眼の奥深くへ入ってから暴れます。処置が遅れるとマジで失明するので気を付けてください。
● Acetonitrile [ アセトニトリル ]

沸点:81.6 ℃ / 融点:-43.9 ℃ /密 度:0.78 (25℃) / 水と混和
LD50=2450~3800 mg/kg(ラット経口) / モル質量:41.05 g/mol
500ml:2,200¥(TCI)
・正直著者自身も多用している溶媒なのでマイナー溶媒のカテゴリーかどうか迷いましたが、HPLC溶媒としてしか認識していない方に何人も出会ったことがあるのでマイナー溶媒のカテゴリーに含めました。
・有機物だけではなく無機塩や高極性ポリマーの溶解性にも優れています。とはいえ、一般的な傾向として他の非プロトン性高極性溶媒(DMF, DMSO等)と比較すれば溶解性は劣る傾向にあります。
・脱水の為には水素化カルシウム存在下加熱還流がオーソドックスですが、ただ脱水するだけなら10 vol%の活性化モレキュラーシーブ3Aで48時間乾燥させた方が最終的に到達できる無水レベルは高いようです。
・シリル化、アシル化、アルキル化などの反応で最適な溶媒です。
・ヘキサンやペンタン等の飽和炭化水素とは相分離するため、水が使えない物質や水には溶けないがアセトニトリルにはとけるような高極性化合物に対してアセトニトリル-飽和炭化水素系もしくは含水アセトニトリル-飽和炭化水素系での液液溶媒抽出が原理上可能です(経験上水-有機溶媒系よりエマルジョン化を起こしやすい気もしますが……)。
・水素化ナトリウムを用いる反応ではDMFよりもアセトニトリルを溶媒として使うべきです。(DMFは水素化ナトリウムで分解する危険性があるため。)
・低極性(高親油性)化合物の再結晶溶媒として優れた効果を発揮することがあります。
・酸触媒共存下ではRitter反応機構で進行する高い反応性を示すことがあるため注意が必要です。
・遷移金属イオンに対する配位能が高く、配位数が異なる種々の錯イオンを形成することがあり時折解析の妨げになります。また、一部希土類元素の過塩素酸塩は爆発性の錯体を作ることがあるので混合は避けるべきです。
・アセトニトリルの経口および経皮毒性は比較的軽度ですが、目に対しては激しく刺激し非常に危険です。反応溶媒として扱うときは勿論、機器分析用溶媒として扱う際も必ず保護メガネを着用してください。
● Benzene [ベンゼン]

沸点:80.1 ℃ / 融点:5.53 ℃ /密 度:0.88 (20℃) / 水に不溶
LD50=930~3400 mg/kg(マウス経口) / モル質量:78.11 g/mol
500ml:1,300¥(Wako)
・かつての超メジャー溶媒。いまや専らトルエンやキシレンに代替されていますが、今もなお分光測定や反応溶媒として需要があります。
・様々な有機化合物やポリマーの溶解性に優れ沸点が手ごろで揮発性もよく乾燥精製もしやすくて熱容量が比較的低いから加熱/冷却が簡単で物理的にも化学的にも安定であり供給も安定でしかも安いというまさに理想的な溶媒です。ちょっと前までは分析溶媒や工業用溶剤、ラボスケールは勿論工業レベルの反応溶媒として大量に使用されていました。……いやな、事件だったね。
・この子は凍結乾燥が可能です。溶媒を含んでねちっこくなりやすいポリマーをベンゼンに溶かして何度もエバポレートすることで系内の溶媒をベンゼンに置換させた後、再びポリマーをベンゼンに溶かして液体窒素で凍らせて凍結乾燥なんてのをよくやってました。これやるとからっからのポリマーが得られるので重宝してましたね。勿論「ベンゼンの凍結乾燥をする」ということを周りの人に必ず伝えたうえでです。
・ベンゼンは水と69℃(水8.8 vol%)という扱いやすい共沸混合物を形成するので、Dean Stark装置を用いた脱水系の合成反応溶媒としては相変わらず余人をもって替えがたいです。
・応用的な使い方としてDMFやDMSOなどの沸点が高くしかも脱水が難しいような溶媒に無水ベンゼン(モレキュラーシーブで乾燥させたやつで十分)を混ぜてやり、系内の水をベンゼン-水共沸混合物としてエバポレートで抜いてやるというのがあります。勿論この方法では完全な無水状態にはできませんが、そこまでシビアな禁水が求められない反応や本精製前の予備乾燥としては十分な威力を発揮してくれます。
・ベンゼンを良溶媒、シクロヘキサンを貧溶媒として用いる系は再沈殿再結晶用溶媒として非常に優れており、原料化合物やポリマーの精製に効果的です。ベンゼン-シクロヘキサン混合溶媒はほぼ一定の沸点を持ちかつ冷蔵庫程度の低温でも凍結せずとても扱いやすいです。
・ベンゼンは融点的に冷凍庫(装置によっては冷蔵庫) で凍るため、ベンゼン溶液で何か物質を保管するときは注意です。こればっかりは何とも言えなくて、ベンゼン溶液の状態で冷凍庫で凍らせると分解が抑えられて保存しやすくなるものもあるんですが、逆に分解や副反応が促進されるようなものもあるようです(凍結によって溶質の局所濃度が増加するのが要因?)
・ベンゼンは様々な物質と共結晶を形成しやすく、ベンゼン(もしくはベンゼンを成分として含む系) でしかまともに再結晶できないものもあります。
・トルエンやキシレンなどのいわゆるベンゼン代替溶媒でなんかうまくいかない反応や精製があったら、思い切ってベンゼンを試してみるというのは十分考慮に値する選択肢です。トルエンやキシレンはベンゼンを完全には代替できません。
・総じて優秀な溶媒なんですがほぼ唯一にして最大の欠点がその毒性です。ベンゼンはクラス1の発癌性物質であり、その他にも肝機能障害、造血器障害、自律神経障害等様々な障害の原因となることが明らかになっています。
・とはいえ、ベンゼンの毒性は確かに強いのですがそこまで恐れるようなものではないと私は思っています。工業スケールで何百リットルとじゃぶじゃぶ使うのはそりゃ憚られるべきですが、ラボスケールでの使用量なら常識的な安全設備(ドラフト、保護メガネ、手袋) で十分対応できます。というより使ったベンゼンで健康障害が出てしまうような環境で実験しているとかベンゼン関係なく危険です。この中で酒も煙草もやったことない人のみベンゼンに石を投げなさいとキリストも言ってます(言ってない) 。ただカラム溶離液としてはまぁ避けたほうがいいでしょうね、流石に量が多いですし。
・そういえば海鮮市場を豊洲移転する際土壌からベンゼンが出たとかでニュースになってましたねぇ。まぁそれは確かに問題なんですが、これまでずっとちやほやされてきたのに毒性が分かった瞬間手のひらを返して石を投げられ完全に悪の物質扱いされてしまうベンゼン君には同情を禁じえません。
・全然関係ないんですが、著者が高校生のころ有機化学の授業で化学の先生がクラスのみんなにベンゼンの臭いを嗅がせていたのを思い出しました。当時は当然今ほどの化学知識がないので「へー確かに芳香って割にはいい匂いじゃないんだな」くらいにしか思いませんでしたが、今思い返すとやべーことしてますよね先生(ちなみに著者はその先生が大好きで、その先生のおかげで化学が好きになり今があります。元気にしてらっしゃるかなぁ)。
● Benzotrifluoride [ ベンゾトリフルオリド, トリフルオロメチルベンゼン, トリフルオロトルエン ]

沸点:103 ℃ / 融点:-29.0 ℃ /密 度:1.19 (20℃) / 水に不溶
LD50=1500 mg/kg(ラット経口) / モル質量:146.11 g/mol
500g:8,400¥(TCI)
・ジクロロメタンと似た溶媒特性を示し、その高沸点代替溶媒として使用可能なフッ素系溶媒です。
・塩化アルミニウムとは反応するため、それを使うFriedel–Crafts反応の溶媒としてジクロロメタンの代わりには使えません。
・代替溶媒とはいえジクロロメタンよりも溶媒としての極性は低いようで、それもあってか溶解性という点ではジクロロメタンよりも劣るようです。
・私は直接使ったことが無いのですが、臭いはあまり気にならないらしいですね。
● Cyclohexane [ シクロヘキサン ]

沸点:80.7 ℃ / 融点:6.54 ℃ /密 度:0.78 (20℃) / 水に不溶
LD50=813 mg/kg(マウス経口) / モル質量:84.16 g/mol
500ml:2,500¥(TCI)
・水と混和しない飽和炭化水素系溶媒です。
・溶媒の性質としては他の飽和炭化水素系溶媒、特にヘキサンと共通点があります。ヘキサン同様アセトニトリルとは相分離します。
・通常市販されているヘキサンは純粋なものではなくn-ヘキサン・メチルペンタン・ジメチルブタン等の沸点が近いC6炭化水素の混合物であるのに対し、シクロヘキサンはほぼ純粋にシクロヘキサンで構成されています。まぁだから何だということはありませんが……。
・ヘキサンよりも溶解能に優れることが多く、抽出溶媒や再沈殿再結晶溶媒、またTLC展開溶媒やカラム溶離液の成分としてヘキサンを用いるよりも優れた結果をもたらしてくれることがあります。どこかで「シクロヘキサンの溶媒特性は環化したヘキサンというより水素化したベンゼン」というのを見ましたが確かにその通りだと思いました。
・高温と低温で物質に対する溶解能が大きく変化することがあるため、再沈殿や再結晶用の溶媒として優れています。
・特にベンゼンを良溶媒、シクロヘキサンを貧溶媒として用いる系は再沈殿再結晶用溶媒として非常に優れており、原料化合物やポリマーの精製に効果的です。ベンゼン-シクロヘキサン混合溶媒はほぼ一定の沸点を持ちかつ冷蔵庫程度の低温でも凍結せずとても扱いやすいです。
・w/o型マイクロエマルジョン反応の有機溶媒成分として優れた結果をもたらすことがあります。
・凍結乾燥ができる・・・らしいですが著者はあまりうまくいったことがありません(系が合わなかったのかもしれない)。
・NMRで線が一本しか出ないので不純物として入っていても脂肪族炭化水素溶媒と比較して目的物のスペクトルが見やすいです。
・n-ヘキサンよりも毒性は低いですが、それでも蒸気は目や粘膜を刺激し皮膚に触れると皮膚炎の原因になりやすく危険です。
・単体の場合融点が比較的高いので低温反応用溶媒には向いていません。
・基本的に多くの環境下で不活性な溶媒ですが、稀に脱水素を伴う反応を起こすことがあるため慢心してはいけません。
● Cyclopentyl Methyl Ether [ シクロペンチルメチルエーテル, CPME ]
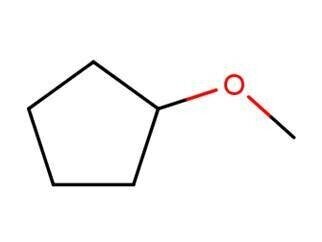
沸点:106 ℃ / 融点:-140 ℃ /密 度:0.86 (20℃) / 水に不溶
LD50=200~2000 mg/kg(ラット経口) / モル質量:100.16 g/mol
500ml:3,600¥(TCI)
・幅広い有機化合物やポリマー、有機金属試薬に対して良好な溶解性をもつ比較的新しい線状エーテル系極性溶媒です。
・THFや1,4-ジオキサンのより毒性が低く安全でかつ水と混和しない代替溶媒として反応や抽出、精製に使用可能です。溶解性についてもこれらエーテル溶媒と遜色ありません。ポリマーについても著者の経験の範囲ではポリスチレンやポリエステルに対する溶解性がTHFより悪いと感じたことはありませんでした。フルオレン系ポリマー等の共役系高分子もよく溶けてくれることが多いそうです。
・他の主要なエーテル溶媒の中では最も疎水的であり、水への溶解度は
1.1 g/100gwater (23℃)で溶媒への水の溶解度は0.3 g/100gsolv (23℃)です。
・その高い疎水性のためエーテル溶媒としては乾燥精製がしやすいです。単純な脱水なら活性化済みモレキュラーシーブ4Aを10 wt%加えて一晩~1日待てば数十ppmレベルまで脱水可能です。
・水と混ざらないため反応後の分液操作が容易です。また疎水性が高いためジエチルエーテルとかと比較して分液しやすい(分離が早かったりエマルジョン化しにくかったり分液回数が少なくても良かったり等)ことが多いです。
・水とは83℃ (水16 wt%)の共沸混合物を形成します。そのためDean-Stark装置下で行う反応の溶媒としてトルエンなどの代替に使用できます。当然反応選択性や収率が(良くも悪くも)変化する可能性があるのは注意です。
・主要エーテル溶媒の中では最も溶媒として使用可能な温度範囲が広く、低温反応から高温反応まで問題なくこなせます。THFが使いたいが反応温度的に厳しい!というときの代替溶媒にうってつけです。
・構造が安定しておりTHFやジオキサン等と比較して過酸化物を形成しにくく、酸塩基耐性も高いです。ただし塩化アルミニウムのような強いルイス酸に対する安定性は劣るようです。
・沸点は高いものの蒸発潜熱が他の主要エーテル溶媒と比較してかなり低いため、エバポレーター等による系内からの除去が容易です。
・TLCやシリカカラム精製等での溶媒として使うとクロロホルムに似た分離挙動を示します。多分極性(誘電率) 的に似ているからでしょうね。勿論目的物の構造によってはクロロホルムと互換性がない可能性もありますが、代替溶媒として使えるかもというのは頭に入れときたいですね。
・アルキルリチウム試薬等の求核試薬に対する安定性は他の主要エーテル溶媒よりも優れています。
・高い沸点とラジカル反応(水素引き抜き) に対する高い耐性からラジカル反応の溶媒としても機能します。AIBNを用いたアルキンのヒドロスタニル化、ヒドロシリル化やBarton-McCombie脱酸素化、リビングも含むラジカル重合等々の溶媒として使えます。
・Simmons-Smith反応の溶媒として優秀です。
・無機塩の溶解性は環状エーテル系溶媒と比べてかなり劣るようです。
・好き嫌いがわかれる臭いだと思いますが、ラボスケールで使う分には著者的に嫌いな臭いではありません。(何かが足りないハッカ、もしくは適当に買った安い歯磨き粉で歯を磨いた後みたいな臭いがします)
・総じて使い勝手のいい溶媒なのでTHFやジオキサンの疎水性代替溶媒が必要な時は4-MeTHPと並んでファーストチョイス群ですね。ラボに一本常に置いときたいレベルです。
● Decalin [デカリン, デカヒドロナフタレン ]

沸点:196(cis);187(trans) ℃ / 融点:-40.3(cis);-30.4(trans) ℃
密 度:0.90(cis);0.87(trans) (共に20℃) / 水に不溶
LD50=4170~9170 mg/kg(ラット経口) / モル質量:138.25 g/mol
500ml:3,300¥(TCI) ※cis and trans mixture
・高沸点ながら低融点であり幅広い温度領域で使用できる環式飽和炭化水素系溶媒です。
・ラボというよりかは工業用としての使用が主で、油脂や樹脂、塗料の溶剤として利用されています。因みに著者の経験上、この子を化学系の研究室で見たことはあまりなくむしろ電気系や機械工学系の研究室でよく見ました。
・低極性で高沸点かつ飽和炭化水素という安定な構造を有しているという性質から、アルキル鎖に富むポリマーの重合用溶媒や高温反応用溶媒として利用可能です。
・沸点は高いですが揮発性は悪くなく、減圧蒸留などを使えばそこまで苦労せず系内からの除去が可能です。
・毒性は0ではありませんが比較的低いです。
・精製は水素化カルシウムか金属ナトリウムで脱水処理したのち減圧蒸留で行うのがオーソドックスです。脱水するだけならモレキュラーシーブ4Aも使えます。
・酸素存在下では徐々に過酸化物が形成されることが知られています。特に高温下(110℃~)では数時間でかなりの量の過酸化物が生じるとされているので、高温反応用溶媒として使う際は不活性ガス置換を忘れずに行いましょう。そんなわけなので還流溶媒としては不向きかもしれませんね。
・デカリンから生成される過酸化物はそれ自体は蒸留可能なほど安定であり毒性もさほど高くなく、エーテル溶媒の過酸化物ほど危険ではありません。
・新品以外のデカリンは系内に過酸化物を含んでいる可能性が高く、精製を行わずに反応溶媒や重合溶媒として使ってしまうと反応の失敗や思わぬ事故を起こしかねません (特に熱ラジカル重合の溶媒として使うケースとかが危険)。必ず精製してから使用するようにしてください。(これがなかなか面倒だったりする)
● Dichlorobenzene [ ジクロロベンゼン, DCB ]

沸点:180 ℃(o) ,173℃(m) ,174℃(p) / 融点:-17.0 ℃(o) ,-24.8℃(m) ,53.0℃(p) /
密 度:1.31(o) ,1.29(m) (共に20℃), 1.24(p) (55℃) / 水に不溶/
LD50=4386(o) ,820(m) ,2950(p) mg/kg(全てマウス経口)
モル質量:147.01 g/mol / 500ml:2,900¥(o) ,500ml:7,300¥(m) ,
500g:2,300¥(p) (全てTCI)
・芳香族クロロ化合物であり、様々な有機化合物やポリマーに対する高い溶解性をもつ高沸点溶媒です。多くの場合において同じ芳香族系溶媒であるトルエンよりも高い溶解性を示します。
・特にアントラセン誘導体やフラーレン等の共役系化合物に対する溶解性に優れています。単体では勿論共溶媒にしても効果があります。
・ジクロロベンゼンにはo(1,2-) とm(1,3-) およびp(1,4-) という三つの異性体がありますが、値段や取り扱いのしやすさの点からo-ジクロロベンゼンが専ら使われます。m(1,3-) およびp(1,4-)はどちらかというと試薬としての側面の方が強いかもしれませんね。
・o-ジクロロベンゼンは高温でも比較的安定であるのとその溶解性の高さから溶液重合を行う際の溶媒として有用です。著者は100℃以上の高温条件で行う溶液リビングラジカル重合系の溶媒としてよく使ってました。
・特に140℃以上程度の高温に加熱した熱o-ジクロロベンゼンは、剛直性ポリマーや超高分子量ポリマー、π共役系ポリマー、ポリオレフィン等の一般的な有機溶媒には溶けないものを溶かすことができることがあります。そのため高温GPC測定における溶離液として重要です。多分ゴム系やエンジニアリングプラスチック系の研究開発を行うメーカーに就職したら、140℃のo-ジクロロベンゼンが流れているGPCを使うことになるでしょう。
・o-ジクロロベンゼンの持つ高沸点という特徴は長所でもあり短所でもあります。減圧蒸留か真空ポンプでガン引きにしたエバポレーターで抜くのがオーソドックスでしょうが大変そうなのは予想どうりです。溶液スケールによっては目的物の貧溶媒に落として再沈殿か再結晶させるのが一番手っ取り早いですかね。トルエンを入れてひたすら共沸させるというごり押し方法もできるっちゃあできます。まぁあまり大量には使いたくない溶媒ですよねぇ。
・蒸気を吸い続けると頭痛や倦怠感、肝障害といった症状をきたすことがあります。ジクロロベンゼンは殺虫剤としての用途もあるため、きちんと安全対策を取ったうえで使いましょう(全ての溶媒がそうですが) 。
・不思議なことに日本の一部界隈では化学系じゃない人にもこの物質の名前が認知されています。僕は何のために歌うんでしょうねぇ……。
● Dimethyl isosorbide [ ジメチルイソソルビド, DMI]

沸点:94 ℃ / 融点:-70 ℃ /密 度:1.16 (20℃) / 水と混和
LD50=5630 mg/kg(ラット経口) / モル質量:174.19 g/mol
25g:6,600¥(TCI)
・アミド系溶媒(DMF等) とエーテル系溶媒(THF等) の中間程度の特性を有する溶媒として使用できます。
・ペプチド固相合成の溶媒として優秀なようで、DMFやNMPの代替溶媒として提案されています。
・鈴木-宮浦反応、Mizoroki-Heck反応、薗頭反応といったPd触媒反応の溶媒としても使用できます。
・再生可能原料由来のいわゆるグリーン溶媒です。安全性も高いです。
・この溶媒自体の安全性は高めですが、この溶媒は皮膚浸透性が高いため毒性を持つ物質が溶解しているとそれの吸収性を高めてしまいます。DMSOの危険性と同じですね。
・値段がたっかいです。試しに買ってみるにしてはたっかいしかなりマイナーなので今んとこは知識として知っておくくらいで十分だとは思います。
・より知られている1,3-ジメチル-2-イミダゾリジノンもDMIと略称されるのでごっちゃにならないようにしましょう。
● Heptane[ ヘプタン ]
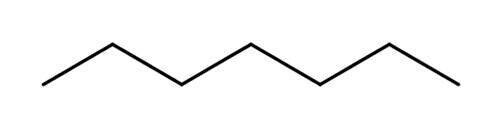
沸点:98.4 ℃ / 融点:-90.6 ℃ /密 度:0.68 (20℃) / 水に不溶
LD50=15000~ mg/kg(ラット経口) / モル質量:100.21 g/mol
500ml:3,000¥(TCI)
・溶媒としての性質はヘキサンのそれと大きく変わらず特筆するようなことはありません。
・低極性でアルキル鎖に富む化合物はよく溶かしますが、それ以外の化合物に対する溶解性はあまり高くありません。
・ヘキサンよりも低毒性で比較的安全な代替溶媒として使用できます。値段もヘキサンとあまり変わりません。
・アセトニトリルとは相分離します。
・ヘキサンのような神経毒性は有していないとされていますが、麻酔作用は相変わらず持っているため高濃度の蒸気に晒されることが無いように注意しましょう。
・余談ですが試薬として販売されているヘプタン、ヘキサン、ペンタン等の脂肪族炭化水素はそれぞれ沸点が似ているいくつかの成分が混在していることが多いため、表記を鵜呑みにして合成原料などにしてはいけません。
● Hexamethylphosphoric Triamide (ヘキサメチルリン酸トリアミド, HMPA)

沸点:233 ℃ / 融点:7.20 ℃ /密 度:1.02 (20℃) / 水に不溶
LD50=2000~ mg/kg(ラット経口) / モル質量:72.15 g/mol
500ml:21,800¥(TCI)
・20年前くらいまでは溶媒や試薬として幅広く使われていた物質です。
・炭化水素を除くほとんどの溶媒と自由に混和可能であり、メイン溶媒にHMPAを共溶媒として加えることで溶解性を大きく向上させられることがあります。
・低極性から高極性までの幅広い有機化合物と無機塩に対して非常に高い溶解性を示します。
・特にポリマーに対する溶解性の高さは特筆すべきものがあり、ポリビニルアルコールやナイロンのような極性ポリマーからポリ塩化ビニルのようなビニル系ポリマーに至るまで幅広く溶解できます。DMFやTHFに溶解しなくて困ってるポリマーもこの子なら溶かせられるかもしれません。
・金属イオンに対する配位性が高く、有機金属を使用する反応系に添加もしくは溶媒として用いると反応が促進されたり反応選択性が変化することがあります。特にリチウム塩とは相性がいいといわれています。
・特にGrignard反応においては、THFやジエチルエーテル溶媒では作りづらい構造のGrignard試薬でもHMPAなら作れる場合があります。
・いろいろと便利な物質ではありましたが、発癌性や胎児への悪影響といった無視できない毒性を持つことが指摘されてからはすっかり見る機会が減りました。今では専ら1-メチルピロリジン-2-オン(NMP) やテトラメチル尿素(TMU)、N,N-ジメチルプロピレン尿素(DMPU) といった物質がHMPAの代替溶媒として使われています。
・替えが効かないことも多いベンゼンと異なりHMPAは上記の代替溶媒で問題なく補完できることが多いので、古い文献でHMPAを使っていても躊躇なく代替溶媒を使ってしまうことをお勧めします。悲しきかなもう歴史上の化合物になってしまったといってもいいくらいですね。
・塩基性条件には比較的安定ですが、酸性条件では分解が起きる可能性があります。
・150℃を超える高温条件では徐々に分解する可能性があります。
・良くも悪くも沸点が高くしかも水を含みやすいので、精製や反応系からの除去が手間なことが多いです。水素の数が多くしかも系内に残りやすいため、特にH1 NMR測定では邪魔になります。
・余談ですがもともとは殺虫剤分野の研究を行っているときに作られた物質なんだそうです。殺虫剤としてはぱっとしなかったみたいですが、それゆえに当時は安定で比較的低毒性な物質と見られていたきらいがあるようです。
・あとはまぁ値段が高いですよね、うん。
● Methyl ethyl ketone [ メチルエチルケトン, ブタノン, MEK ]

沸点:79.6 ℃ / 融点:-86.7 ℃ /密 度:0.81 (20℃) / 水と部分的に混和
LD50=2500~4300 mg/kg(ラット経口) / モル質量:72.11 g/mol
500ml:1,200¥(Wako)
・アセトンの水素が1つメチル基になった構造のケトン系極性溶媒です。
・アセトンと同等の溶解特性を有していながら沸点と疎水性が向上しておりその代替溶媒として使用できます。
・特にアセトンに溶けがよくない基質のFinkelstein反応を行う際は溶媒候補になります。
・研究室ではあまり見かけないかもしれませんが、産業界では溶剤や払拭溶媒としてよく使われています。
・アセトンと違い水と完全には混和しないので抽出溶媒として使えないこともないですが、どうしてもケトン系溶媒で抽出しないとダメ!って場面は少ないので(著者は出会ったことがない) 頭の片隅に置いとくだけでいいと思います。
・アセトンと同様経口毒性は比較的低い有機化合物ですが、粘膜および皮膚刺激性はかなり強くなっているのでアセトンと同じ感覚で扱ってはいけません。(アセトンであっても不用意な皮膚接触はNGですが)
・一般的なケトン溶媒と同様過酸化物形成の可能性があるため、精製した(安定剤を抜いた) ものを酸素存在下で室温放置したり光に充てて放置したりしてはいけません。
・アセトン同様アルミナやシリカゲルのような弱酸に触れると縮合反応が誘発される可能性があるのでなるべく接触は避けるべきです。
・ハロゲン系溶媒との混合も避けましょう。アセトンとクロロホルムは混合すると誘導期間を置いたのち激しい発熱反応を起こす可能性があることは有名ですが、本質的にはケトン系溶媒とハロゲン系溶媒の組み合わせならどれでも起こりえます。
● N-methylpyrrolidone [ N-メチルピロリドン, NMP ]

沸点:204 ℃ / 融点:-24.4 ℃ /密 度:1.03 (20℃) / 水と混和
LD50=3600~4320 mg/kg(ラット経口) / モル質量:99.13 g/mol
500ml:3,600¥(TCI)
・幅広い有機化合物、ポリマー、無機塩に対する良好な溶解性をもつ非プロトン性極性溶媒です。その溶解性はDMFやDMSO、HMPAに匹敵します。
・その溶媒特性からHMPAやDMFの代替溶媒として使用されます。また、単体では融点が問題になりやすいDMSOの代替としても有能です。
・ポリマーに対する溶解性も非常に良好で、フッ素系ポリマーやポリオレフィンを除く多くのポリマーを室温下で十分溶解できます。
・熱的安定性も高く高温反応用溶媒として十分機能します。
・ほとんどの有機溶媒と水に対し混和します。
・多くの化学的・物理的条件下で比較的安定であり人体毒性も低いです。
・ただし最近は環境毒性が問題になり規制の動きがでていて、HMPAやDMFの代替溶媒であるNMPの代替溶媒として最近はジプロピレングリコールジメチルエーテルやジヒドロレボグルコセノン、3-メトキシ-N,N-ジメチルプロパンアミドなんかが候補として出てきています。まぁ、プロセス化学屋さんは気にしたほうがいいでしょうが、ラボスケールならまだ話半分でいいとは思います(NMPの代替溶媒はどれもくそ高い) 。
・その極性と高沸点ゆえに溶媒として使用後にエバポとかで抜こうとすると非常にだるいですが、分液が可能な系なら[酢酸エチルー1M LiCl水溶液]系で分液すれば大体サクッと水層に移ってくれます。それでも『抜け』がよくないときは酢酸エチルを酢酸イソプロピルのようなもっと低極性の溶媒にすると効果的なことがあります。
・著者の完全な感覚ですが、ポルフィリン誘導体はDMFよりもこの子の方が溶けがよかったように思えますね。あんまり関係ないかもしれませんが、カーボンナノチューブの分散性もTHFとかDMFよりいいみたいです。
・NMPは胎児に対して毒性(生殖毒性) を有している可能性があります。
・吸湿性が強いため乾燥精製が厄介です。水素化カルシウムを入れて減圧蒸留というのがオーソドックスなやり方ですが、揮発性が悪くとてもおっそいです。NMPは水と共沸しないので減圧蒸留による精製自体はあまり問題ではないんですがね……。
・NMPは酸素存在下で徐々に過酸化物を生成することが知られているため、開封後時間がたったNMPを精製せずに使うと特に遷移金属反応の溶媒として使った際に思わぬ悪影響を与える可能性があります。そうでなくてもこの子を反応溶媒として使うときはちゃんと精製しかつ念のためなるべく系内を不活性ガス置換させておきたいですね。
・NMP自体の人体毒性はそこまで高くありませんが、溶解した物質の皮膚浸透性を格段に高める効果があるため取り扱う際は皮膚に接触しないようにしましょう(DMSOの危険性と同じですね) 。樹脂溶解性が高いため普通のゴム手袋は余裕で透過してくるので注意です。
・pH2~10程度の範囲なら高温下でも耐えますが、その範囲外の強酸強塩基条件だと開環分解を起こす可能性があります。場合によってはそれが連鎖しNMPの開環重合による反応暴走の危険性があるため、この溶媒で強酸強塩基反応を行う際は必ず小スケールでの予備実験を行ってください。
・ちなみに著者は高分子屋なのでNMPと聞くとこの子よりもリビングラジカル重合系のNMP(ニトロキシド媒介ラジカル重合) の方が頭に浮かびます。
● N,N-Dimethylacetamide[ ジメチルアセトアミド, DMAc, DMA ]

沸点:166 ℃ / 融点:-20.0 ℃ /密 度:0.93 (20℃) / 水と混和
LD50=4900 mg/kg(ラット経口) / モル質量:87.12 g/mol
500ml:2,800¥(TCI)
・飽和炭化水素系を除く多くの有機化合物とポリマー、無機塩に対する高い溶解性を有する非プロトン性高極性溶媒です。DMFと同様の構造、沸点、双極子(μ=3.7D) を持ち溶媒としての性質も似ています。
・DMAcはDMFよりも安定性に優れる傾向にあります。例えばDMFは強塩基+還元剤系(ナトリウムナフタレニド等)や長時間の高温(100℃以上といわれています)等の条件では分解してしまいますが、DMAcはそのような条件でも耐えてくれることがあります。
・胎児への毒性を有していますが、総じてDMFよりも低毒性です(DMF自体そこまで毒性の強い物質ではありませんが) 。
・DMF溶媒でやってるけどなんかうまくいかない、もしくはDMFが使いたいけど反応系的に使えないといった場合の代替溶媒として役立ってくれます。
・ただ、DMFの代わりにDMAcを用いる利点はいくつか思いつけますが逆は思いつきません、値段以外に何かあるでしょうか。なのでラボスケールだったらもう最初っから全部DMAcでよくない?という思いはあります。
・とはいえDMFでできないことが何でもできるかというとそういうわけはありません。DMFの危険な分解を招く可能性がある水素化ナトリウムやNBSはDMAcでも同様の危険性をもっているため、それらを使う反応の溶媒として使ってはいけません。
・高沸点なため系内からの除去はDMFの時と同様に難儀します。目的物が非水溶性の場合ベンゼンかトルエンオンリー、もしくはエーテルか酢酸エチルにヘキサンを混ぜた有機層-水層系で分液すればさっくり水層に抜けてくれることが多いです。うまくいかない場合は水層にリチウム塩を混ぜてやると改善することがあります。有機層にクロロホルムやジクロロメタンを使うのはお勧めしません。有機層の方にずっと残ってしまいます。目的物も水溶性なんだよなぁという場合は高真空エバポレーターで頑張って抜きましょう。目的物が水溶性で低沸点なんだよなぁという場合は黙って減圧蒸留です。
・ポリハロゲン化アルカンやペルオキシドとは危険な反応を起こす可能性があるため、実験は慎重に行いできればこの組み合わせは避けましょう。
・ちなみに著者はDMFのことがあまり好きではなく、なるべくDMFを使わないように立ち回っているのでその代替であるDMAcもほとんど使ったことがありません。高極性ポリマーか糖類誘導体を扱ったときに仕方なく使ったくらいですかね。なぜDMFが好きではないかはいずれ語る時が来たら語ります。
● Pentane [ ペンタン ]

沸点:36.1 ℃ / 融点:-130 ℃ /密 度:0.62 (20℃) / 水と混和
LD50=2520~3360 mg/kg(ラット経口) / モル質量:179.2 g/mol
500ml:2,200¥(TCI)
・溶媒としての性質はヘキサンのそれと大きく変わらず特筆するようなことはありません。低極性でアルキル鎖に富む化合物はよく溶かしますが、それ以外の化合物に対する溶解性はあまり高くありません。
・アセトニトリルとは相分離します。
・ヘキサンよりも低毒性で比較的安全な代替溶媒として使用できます。
・沸点が低く、非常に揮発しやすいため系内からの除去が容易です。低沸点で高揮発性の溶媒を使いたいがジエチルエーテルやジクロロメタンが使えない!(溶解性や反応性などで)といったケースでの代打として考慮に値します。
● Tetramethylurea [ テトラメチル尿素, TMU ]
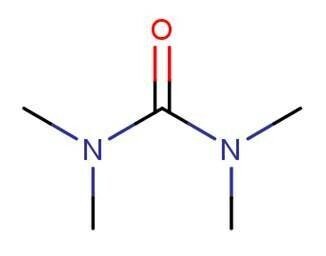
沸点:176 ℃ / 融点:-1.20 ℃ /密 度:0.97 (20℃) / 水と混和
LD50=2920 mg/kg(ラット経口) / モル質量:116.164 g/mol
500g:29,800¥(TCI)
・幅広い有機化合物やポリマーに対し良い溶解性をもつ非プロトン性高極性溶媒です。ただし無機塩に対してはアセトンと同等レベルの溶解性です。
・HMPAおよびDMFの代替溶媒として使用できます。
・高温領域でも比較的安定しています。
・テトラメチル尿素-酸塩化物混合物はアルコールやフェノール、アミンのアシル化反応に有用です。
・HATU試薬を用いたアミド合成反応をやったことがある方はこの子を溶媒に使うなんてありえないと思うかもしれませんね。HATUカップリングの際は副生成物としてこの子が出てくるのですが、反応系や目的物の構造によっては除去がとても難しく分液しようがカラムをかけようが真空引きしようがずーっと残ることがあります。そんなやつを溶媒に使うなんて……というわけもあり著者は一回も使ったことがありませんですはい。しかも高いし。
4. 最後に
うーん、自分で書いといてなんですが私が学生の頃にこういう記事見つけられてたらめちゃめちゃありがたかっただろうなぁなんて思います。今回執筆にあたっていろいろ調べてみて、世の中には様々な特徴を持つ溶媒がこんなにあるんだなぁと改めて感じました。今回は25個紹介していますが、結構絞った方です。ただまぁ、マイナー溶媒がマイナーなのは大体お値段か毒性のせいだなぁとも思いましたけどね。工業スケールでの使用量なら溶媒回収を繰り返せばある程度コストを下げられますが、ラボスケールの使用量だといちいち回収している方の方が珍しいでしょうし。そう考えるとやっぱメジャー溶媒群の方たちって優秀ですわ。
[補遺]
新しい溶媒を試してみるのは担当教員や上司先輩とよく相談してからにしましょう!
この記事が気に入ったらサポートをしてみませんか?
