
松廼屋|論点解説 薬剤師国家試験対策ノート問 108-107【化学】論点:アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用
第108回薬剤師国家試験|薬学理論問題 /
問107
一般問題(薬学理論問題)【物理・化学・生物】
化学|問 108-107
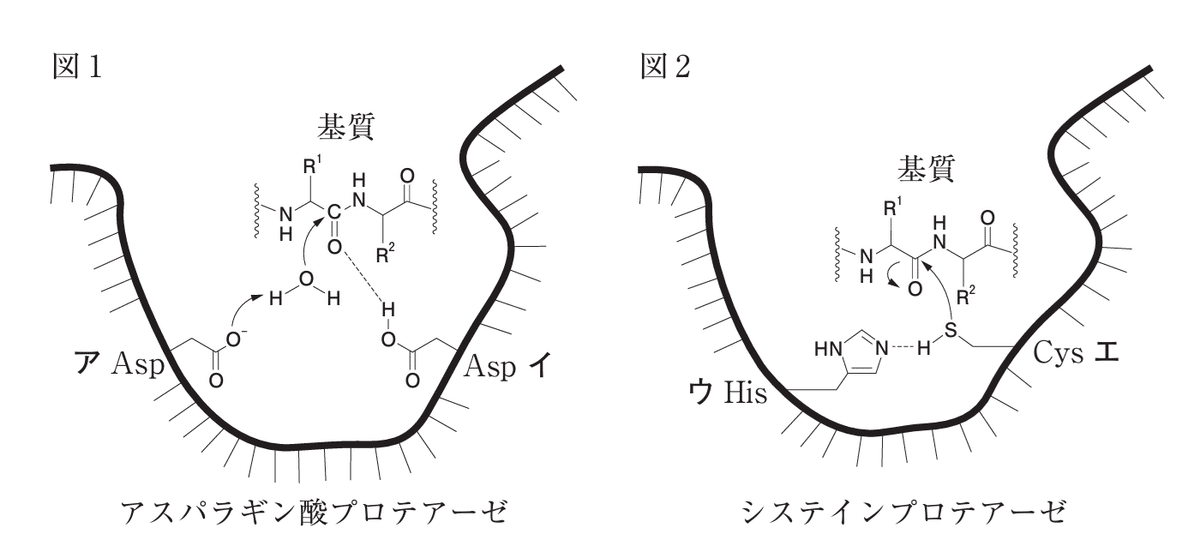
Q. 図1及び図2は、アスパラギン酸プロテアーゼ及びシステインプロテアーゼによる基質加水分解の初期反応過程の模式図である。以下の記述のうち、正しいのはどれか。2つ選べ。
■選択肢
1. アスパラギン酸残基アと水の相互作用は、水の酸素原子の求電子性を高めている。
2. アスパラギン酸残基イと基質カルボニル基の相互作用は、基質カルボニル基の求核性を高めている。
3. システイン残基エのスルファニル基は、塩基として働く。
4. ヒスチジン残基ウとシステイン残基エの相互作用は、エのスルファニル基の求核性を高めている。
5. アスパラギン酸残基アとヒスチジン残基ウは、塩基として働く。
松廼屋|論点解説 薬剤師国家試験対策ノート問 108-107【化学】論点:アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用|matsunoya
こんにちは!薬学生の皆さん。
Mats & BLNtです。
matsunoya_note から、薬剤師国家試験の論点解説をお届けします。
苦手意識がある人も、この機会に、薬学理論問題【化学】を一緒に完全攻略しよう!
今回は、第108回薬剤師国家試験|薬学理論問題 / 問107【化学】 、論点:アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用を徹底解説します。
薬剤師国家試験対策ノート NOTE ver.
matsunoya_note|note https://note.com/matsunoya_note
Here; https://note.com/matsunoya_note/n/nbdd2c114a26e
松廼屋|論点解説 薬剤師国家試験対策ノート問 108-107【化学】論点:アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用|matsunoya
薬剤師国家試験対策には、松廼屋の eラーニング
「薬剤師国家試験対策ノート」
マガジン|薬剤師国家試験対策ノート on note
👉マガジンをお気に入りに登録しよう!
このコンテンツの制作者|
滝沢 幸穂 Yukiho Takizawa, PhD
https://www.facebook.com/Yukiho.Takizawa
お友達や知り合いに、matsunota_note で学習したeラーニングを勧めてみたい方は、いいね!、口コミ、おススメなど、よろしくお願いします!
設問へのアプローチ|
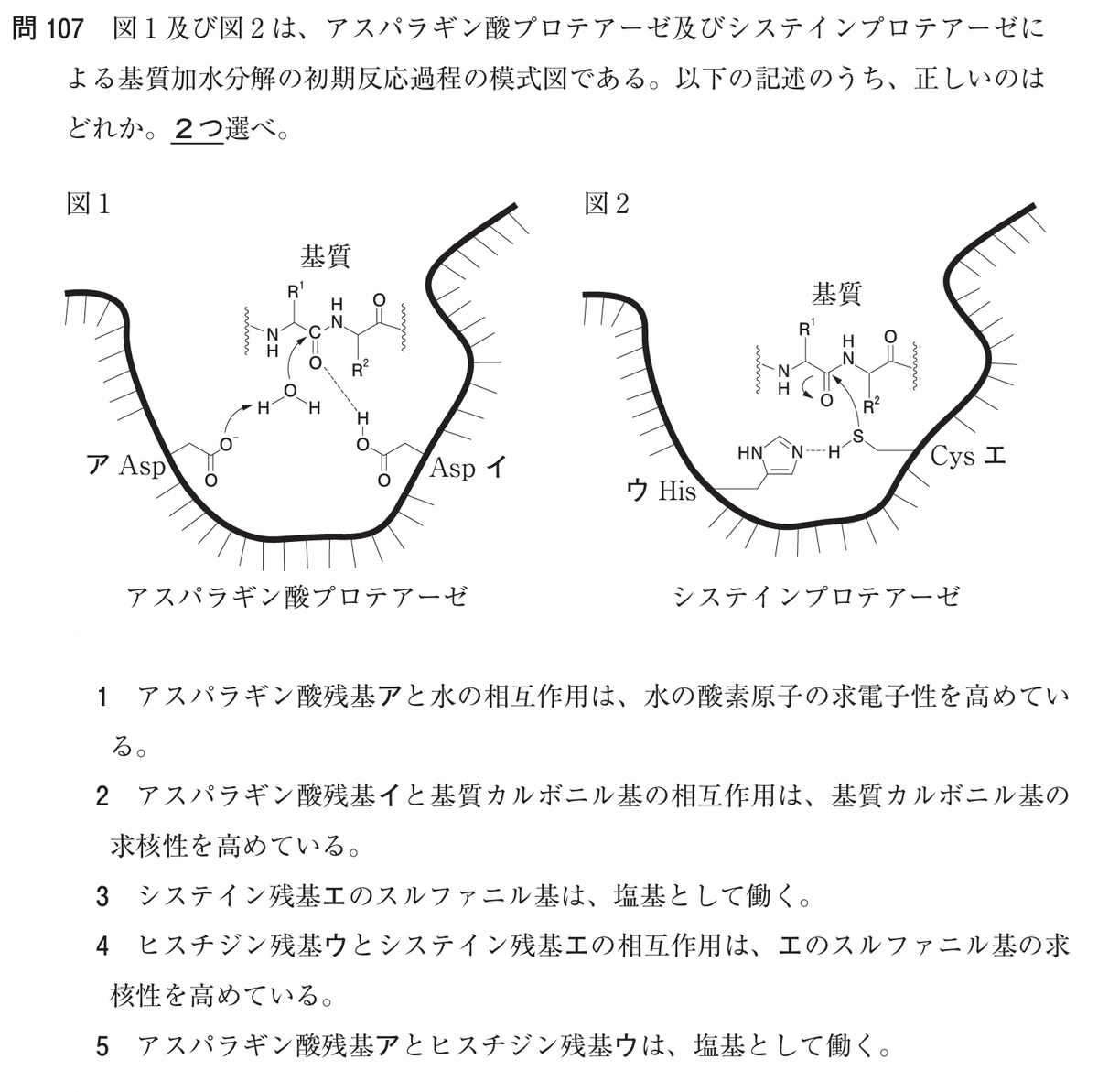
第108回薬剤師国家試験の問107【化学】(問108-107)では、化学構造からアスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用などが問われました。
今回の問題で、基本的に覚えておくべきことは下記の2点です。
電子の動きを表す⤴の先にある求電子性の原子に対して、⤴の根元の原子は、求核攻撃を行います。
例) アスパラギン酸残基 ア:
塩基として機能し、水分子からプロトンを引き抜く。
これによりH2Oから生成されるOH⁻は基質のカルボニル炭素への求核攻撃を担う。相手の官能基からプロトンを引き抜く官能基は、プロトン受容体です。
プロトン受容体は塩基です。
例) アスパラギン酸残基 ア:
塩基として機能し、水分子からプロトンを引き抜く。
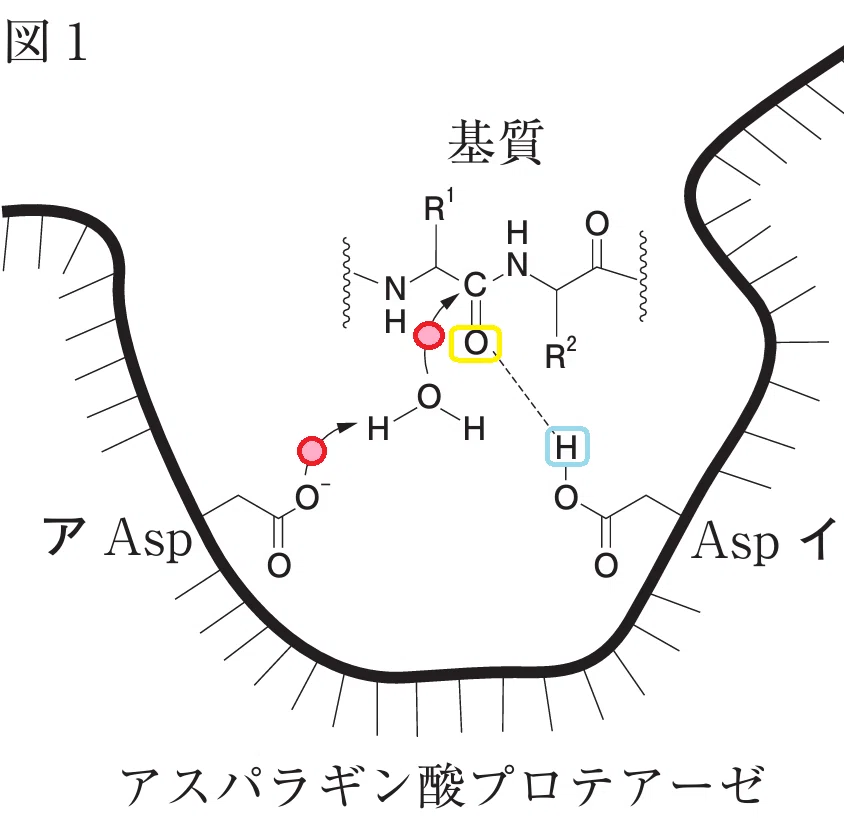
まず基本的な知識について復習しておきましょう。
アスパラギン酸プロテアーゼの基質加水分解における
残基の役割と反応機構

役割
アスパラギン酸残基 ア:
塩基として機能し、水分子からプロトンを引き抜く。
これによりH2Oから生成されるOH⁻は基質のカルボニル炭素への求核攻撃を担う。アスパラギン酸残基 イ:
基質のカルボニル基と相互作用し、その電子密度を調整して求核攻撃を受けやすくする。
反応機構
アスパラギン酸残基アが水分子からプロトンを引き抜き、求核剤である水酸化物イオン(OH⁻)を生成する。
生成されたOH⁻が基質のカルボニル炭素を攻撃し、カルボニル基の酸素に電子が移動する。
電子移動により生成された中間体が安定化され、酵素の活性部位でペプチド結合が切断される。
システインプロテアーゼの基質加水分解における
残基の役割と反応機構
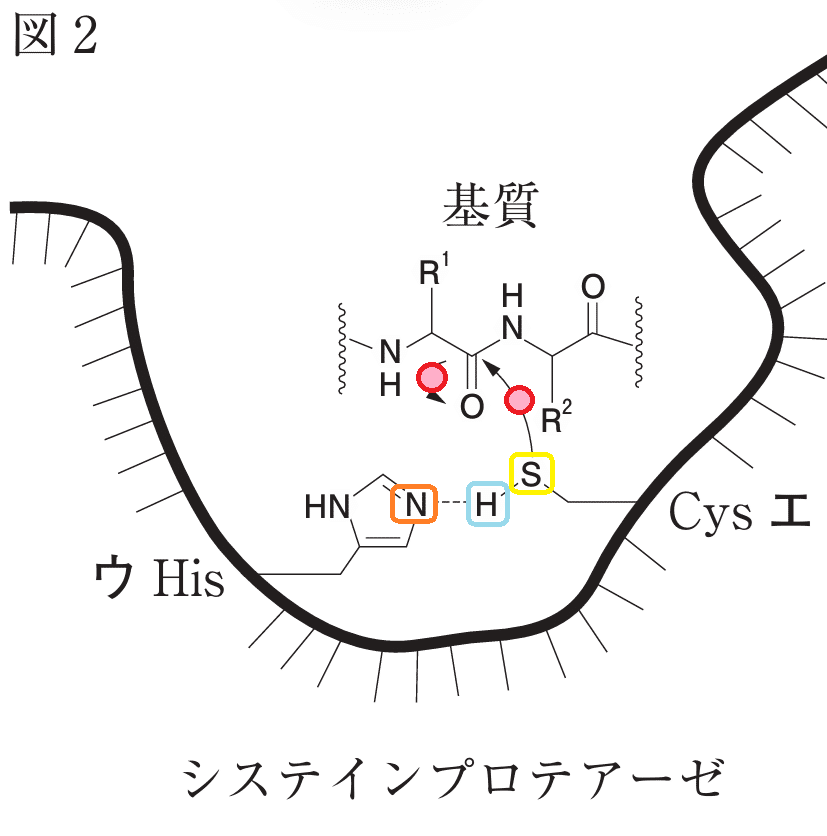
役割
ヒスチジン残基 ウ:
塩基として機能し、システイン残基エのスルファニル基(-SH)からプロトンを引き抜く。
これにより生成されるスルフィドアニオン(-S⁻)が求核攻撃を担う。システイン残基 エ:
プロトンを放出してスルフィドアニオン(-S⁻)を生成し、基質のカルボニル炭素を求核攻撃する。
反応機構
ヒスチジン残基ウがシステイン残基エのスルファニル基からプロトンを引き抜き、スルフィドアニオン(-S⁻)を生成する。
スルフィドアニオンが基質のカルボニル炭素を攻撃し、カルボニル基の酸素に電子が移動する。
基質内の電子の移動によりペプチド結合が切断され、反応が進行する。
比較ポイント
求核剤:
アスパラギン酸プロテアーゼでは、水分子が活性化されて求核剤(OH⁻)となる。
システインプロテアーゼでは、スルフィドアニオン(-S⁻)が求核剤となる。

塩基の役割:
アスパラギン酸プロテアーゼでは、アスパラギン酸残基が塩基として機能する。
システインプロテアーゼでは、ヒスチジン残基が塩基として機能する。
論点およびポイント
■■GPT4o
化学|問 108-107
論点|アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用
ポイント|

アスパラギン酸プロテアーゼでは、2つのアスパラギン酸残基が水分子の活性化を担い、基質のカルボニル炭素への攻撃を促進する。
アスパラギン酸残基の1つは塩基として機能し、水分子のプロトンを引き抜いて水酸化物イオン(OH⁻)を生成し、求核性を高める。

システインプロテアーゼでは、システイン残基のスルファニル基(-SH)が求核剤として働き、基質のカルボニル炭素を求核攻撃する。
ヒスチジン残基はシステイン残基のスルフヒドリル基からプロトンを引き抜き、スルフィドアニオン(-S⁻)を生成して求核性を高める。
アスパラギン酸プロテアーゼとシステインプロテアーゼのどちらも、基質のカルボニル基が求核試薬の標的となるように電子密度を調整している。
酵素活性部位における残基間の相互作用が、プロトン移動や電子移動を通じて反応を促進している。
薬剤師国家試験 出題基準
出典: 薬剤師国家試験のページ |厚生労働省 (mhlw.go.jp)
出題基準 000573951.pdf (mhlw.go.jp)
論点を整理します。
■■GPT4o
総合的な論点
本問のテーマは、アスパラギン酸プロテアーゼ(Asp protease)およびシステインプロテアーゼ(Cys protease)の初期反応過程における残基間の相互作用とその役割を科学的に理解することです。
具体的には、各酵素の活性部位に存在するアミノ酸残基がどのように基質の加水分解を促進するかについて、化学的メカニズムを解析することです。
反応メカニズムの背景
アスパラギン酸プロテアーゼ
アスパラギン酸プロテアーゼでは、2つのアスパラギン酸残基が活性部位で重要な役割を果たします。
一方のアスパラギン酸残基はプロトン供与体(酸)として、もう一方はプロトン受容体(塩基)として働きます。
この協調作用によって、活性部位での水分子の求核性が増強され、基質のカルボニル炭素への攻撃が促進されます。
システインプロテアーゼ
システインプロテアーゼでは、システイン残基のスルファニル基(-SH)が求核剤として機能します。
ヒスチジン残基との相互作用により、システインの求核性が高まります。
これにより、基質のカルボニル炭素への攻撃が効果的に行われ、酵素反応が進行します。
図1および図2からの情報
図1では、アスパラギン酸残基と水の相互作用を通じて水分子の活性化が示されています。

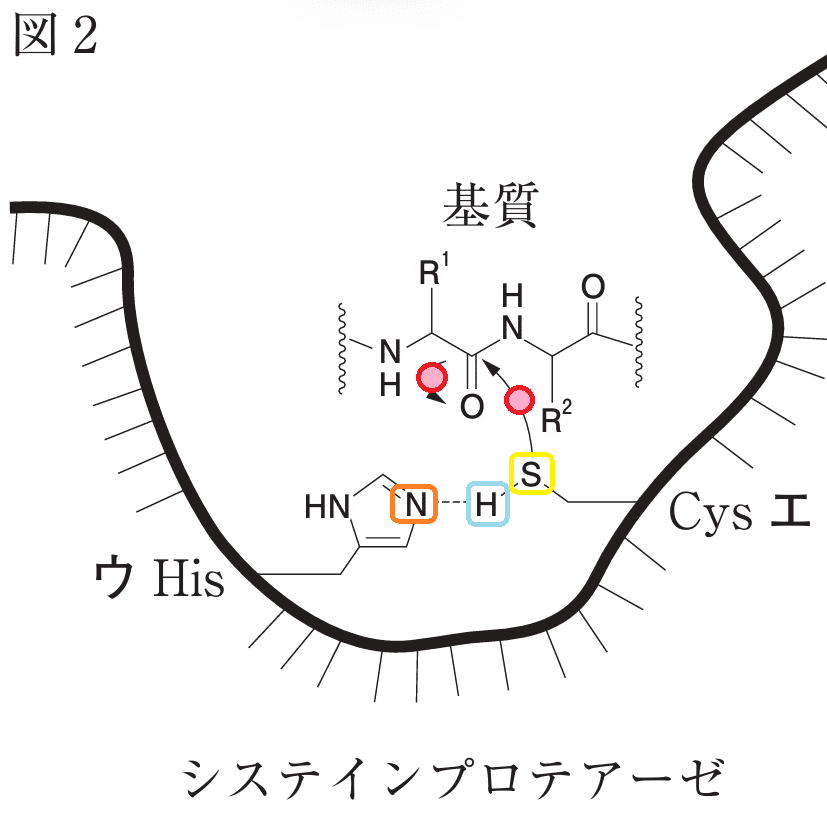
図2では、システイン残基の求核性向上にヒスチジン残基が寄与していることが示唆されています。これらの機構に基づき、選択肢の正誤を検討します。
各選択肢の論点および解法へのアプローチ方法
選択肢1
論点:
アスパラギン酸残基アと水の相互作用は、水の酸素原子の求電子性を高めている。

アプローチ方法:
図1では、アスパラギン酸残基アが水分子と相互作用しています。
アスパラギン酸のカルボキシ基(R-CH2-COO⁻)が水分子の酸素原子をプロトン化することにより、OH基の求核性を高めます。
この活性化されたOH基は、基質カルボニル炭素を求核攻撃し、反応を進行させます。「酸素原子の求電子性を高めている」という記述は誤りです。
酸素原子は求核性が高まるため、記述内容に矛盾があります。
結論: 誤り
選択肢2
論点:
アスパラギン酸残基イと基質カルボニル基の相互作用は、基質カルボニル基の求核性を高めている。

アプローチ方法:
アスパラギン酸残基イは基質カルボニル基と静電相互作用を形成しています。
この相互作用により、基質のカルボニル炭素(C=O)への電子密度が低下し、カルボニル基の炭素が求電子性を高めます。カルボニル炭素の求電子性が高まることで、水やOH⁻などの求核試薬による攻撃が促進されます。
選択肢の「求核性を高める」という記述は誤りです。正確には「カルボニル炭素の求電子性を高める」が正解です。
結論: 誤り
選択肢3
論点:
システイン残基エのスルファニル基は、塩基として働く。

アプローチ方法:
システイン残基エのスルファニル基(-SH)は、基質のカルボニル炭素を攻撃する求核剤として機能します。
スルファニル基は、塩基として働きません。
塩基としての役割を果たすのは、ヒスチジン残基 ウです。ヒスチジンはスルファニル基の水素を引き抜くことで、スルファニル基(-SH)をスルフィドアニオン(-S⁻)に変化させ、求核性を高めています。
結論: 誤り
選択肢4
論点:
ヒスチジン残基ウとシステイン残基エの相互作用は、エのスルファニル基の求核性を高めている。

アプローチ方法:
図2では、ヒスチジン残基 ウの窒素原子がシステイン残基エのスルファニル基(-SH)からプロトンを引き抜き、-S⁻を生成しています。
このスルフィドアニオンは求核性が高いため、基質のカルボニル炭素を攻撃する能力が向上します。
ヒスチジン残基とシステイン残基の協調的な役割が明確に示されており、この選択肢は正しいです。
結論: 正しい
選択肢5
論点:
アスパラギン酸残基アとヒスチジン残基ウは、塩基として働く。


アプローチ方法:
アスパラギン酸残基 ア:
図1では、アスパラギン酸残基アのカルボキシレート基(R-CH2-COO⁻)が水分子と相互作用し、プロトンを引き抜いて水酸化物イオン(OH⁻)を生成します。
この反応でアスパラギン酸残基は塩基として働いています。
その結果、活性化されたOH⁻は求核性が増し、基質のカルボニル炭素を攻撃できるようになります。ヒスチジン残基 ウ:
図2では、ヒスチジン残基ウの窒素がシステイン残基エのスルファニル基(-SH)からプロトンを引き抜き、スルフィドアニオン(-S⁻)を生成します。
この反応においてヒスチジン残基は塩基として機能し、システイン残基の求核性を高めています。
選択肢5では両方の残基が塩基として働くという記述がなされており、この点は図1および図2の反応メカニズムと一致しているため、この選択肢は正しいと言えます。
正解: 選択肢4、選択肢5
引用文献のリスト
以下は、アスパラギン酸プロテアーゼおよびシステインプロテアーゼのメカニズムに関する信頼性のある文献です。これらを基に議論を展開しました。
Brik, A., & Wong, C. H. (2003). "HIV-1 protease: mechanism and drug discovery". Organic & Biomolecular Chemistry, 1(1), 5-14.
アスパラギン酸プロテアーゼの反応メカニズムに関する解説が含まれています。
Otto, H. H., & Schirmeister, T. (1997). "Cysteine proteases and their inhibitors". Chemical Reviews, 97(1), 133-171.
システインプロテアーゼにおける求核攻撃のメカニズムが詳細に説明されています。
Baker, E. N., & Hubbard, R. E. (1984). "Hydrogen bonding in globular proteins". Progress in Biophysics and Molecular Biology, 44(2), 97-179.
水素結合と活性部位残基間の相互作用について。
Copeland, R. A. (2000). "Enzymes: A Practical Introduction to Structure, Mechanism, and Data Analysis". Wiley-VCH.
酵素活性部位の詳細な機能解析を含む、包括的な参考書。
Lehninger, A. L., Nelson, D. L., & Cox, M. M. (2017). "Lehninger Principles of Biochemistry". W.H. Freeman and Company.
生化学的反応と酵素機構の基礎的背景を提供。
まとめ
引用文献に基づき、問題の選択肢4と選択肢5が正しいことを確認しました。これらの資料を追加で参照することで、さらに理解を深めることができます。
以上で、論点整理を終わります。
理解できたでしょうか?
大丈夫です。
完全攻略を目指せ!
はじめましょう。
薬剤師国家試験の薬学理論問題【化学】からアスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用を論点とした問題です。
なお、以下の解説は、著者(Yukiho Takizawa, PhD)がプロンプトを作成して、その対話に応答する形でGPT4o & Copilot 、Gemini 1.5 Pro、またはGrok 2 (beta) が出力した文章であって、著者がすべての出力を校閲しています。
生成AIの製造元がはっきりと宣言しているように、生成AIは、その自然言語能力および取得している情報の現在の限界やプラットフォーム上のインターフェースのレイト制限などに起因して、間違った文章を作成してしまう場合があります。
疑問点に関しては、必要に応じて、ご自身でご確認をするようにしてください。
Here we go.
第108回薬剤師国家試験|薬学理論問題 /
問107
一般問題(薬学理論問題)【物理・化学・生物】
化学|問 108-107
Q. 図1及び図2は、アスパラギン酸プロテアーゼ及びシステインプロテアーゼによる基質加水分解の初期反応過程の模式図である。以下の記述のうち、正しいのはどれか。2つ選べ。

■選択肢
1. アスパラギン酸残基アと水の相互作用は、水の酸素原子の求電子性を高めている。
2. アスパラギン酸残基イと基質カルボニル基の相互作用は、基質カルボニル基の求核性を高めている。
3. システイン残基エのスルファニル基は、塩基として働く。
4. ヒスチジン残基ウとシステイン残基エの相互作用は、エのスルファニル基の求核性を高めている。
5. アスパラギン酸残基アとヒスチジン残基ウは、塩基として働く。
■■GPT4o
化学|問 108-107
■論点|アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用
この問題の論点は、アスパラギン酸プロテアーゼおよびシステインプロテアーゼの基質加水分解における残基の役割と反応機構を特定することです。
■解説1|
ヒスチジン残基ウとシステイン残基エの相互作用は、エのスルファニル基の求核性を高めている。(選択肢4)[正しい]

図2では、ヒスチジン残基ウの複素環の窒素が、システイン残基エのスルファニル基(-SH)からプロトンを引き抜く。このプロトン移動により、スルフィドアニオン(-S⁻)が生成される。
スルフィドアニオンは強い求核剤として基質のカルボニル炭素を攻撃し、加水分解反応を進行させる。この相互作用がシステインプロテアーゼの活性化に重要である。
アスパラギン酸残基アとヒスチジン残基ウは、塩基として働く。(選択肢5)[正しい]

図1では、アスパラギン酸残基アが水分子からプロトンを引き抜き、OH⁻を生成する。このOH⁻が基質のカルボニル炭素を攻撃し、加水分解反応を誘発する。
図2では、ヒスチジン残基ウがシステイン残基エのスルファニル基からプロトンを引き抜く。このプロトン移動により、スルファニル基が活性化され、求核攻撃が可能になる。
いずれの反応においても、アスパラギン酸残基アとヒスチジン残基ウは塩基としての役割を果たしている。
■解説2|
アスパラギン酸プロテアーゼの反応機構
アスパラギン酸残基の1つが水分子を活性化し、OH⁻を生成する。このOH⁻が基質のカルボニル炭素を攻撃する一連の反応が、加水分解を進行させる主要な駆動力となる。システインプロテアーゼの反応機構
ヒスチジン残基ウがシステイン残基エのスルファニル基を脱プロトン化し、求核性を持つスルフィドアニオン(-S⁻)を生成する。このアニオンが基質のカルボニル炭素を攻撃し、加水分解を引き起こす。選択肢4と5の共通点
どちらの選択肢も、酵素の活性部位における残基のプロトン移動が重要な役割を果たしており、それにより基質が攻撃されやすくなっている点がポイント。
■結論|
選択肢4と選択肢5が正しい。
■補足|
アスパラギン酸残基アと水の相互作用は、水の酸素原子の求電子性を高めている。(選択肢1)[誤り]

アスパラギン酸残基 アは水分子をプロトン化し、OH⁻を生成して、求核性を高める。
水の酸素原子の求電子性は高めない。
アスパラギン酸残基イと基質カルボニル基の相互作用は、基質カルボニル基の求核性を高めている。(選択肢2)[誤り]
基質のカルボニル基は求電子性を持つように調整され、求核性は増加しない。
システイン残基エのスルファニル基は、塩基として働く。(選択肢3)[誤り]

スルファニル基はプロトンを引き抜く塩基ではなく、プロトンを供与し、ヒスチジン残基 ウにより求核剤として活性化される。

必須問題の解説は、こちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 必須問題 第106回-第109回 一覧 powered by Gemini 1.5 Pro, Google AI Studio & GPT4, Copilot|matsunoya (note.com)
薬学理論問題の解説は、こちらからどうぞ。
薬剤師国家試験対策ノート|論点解説 薬学理論問題 第106回-第109回 一覧 powered by Gemini 1.5 Pro, GPT4o, Copilot, and Grok 2|matsunoya
お疲れ様でした。
🍰☕🍊
では、問題を解いてみましょう!
すっきり、はっきりわかったら、合格です。
第108回薬剤師国家試験|薬学理論問題 /
問107
一般問題(薬学理論問題)【物理・化学・生物】
化学|問 108-107
Q. 図1及び図2は、アスパラギン酸プロテアーゼ及びシステインプロテアーゼによる基質加水分解の初期反応過程の模式図である。以下の記述のうち、正しいのはどれか。2つ選べ。

■選択肢
1. アスパラギン酸残基アと水の相互作用は、水の酸素原子の求電子性を高めている。
2. アスパラギン酸残基イと基質カルボニル基の相互作用は、基質カルボニル基の求核性を高めている。
3. システイン残基エのスルファニル基は、塩基として働く。
4. ヒスチジン残基ウとシステイン残基エの相互作用は、エのスルファニル基の求核性を高めている。
5. アスパラギン酸残基アとヒスチジン残基ウは、塩基として働く。
楽しく!驚くほど効率的に。
https://note.com/matsunoya_note
お疲れ様でした。
🍰☕🍊
またのご利用をお待ちしております。
ご意見ご感想などお寄せくださると励みになりうれしいです。
note からのサポート、感謝します。
今日はこの辺で、
それではまた
お会いしましょう。
Your best friend
Mats & BLNt
このコンテンツ
松廼屋|論点解説 薬剤師国家試験対策ノート問 108-107【化学】論点:アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用|matsunoya
Here; https://note.com/matsunoya_note/n/nbdd2c114a26e
よろしければこちらもどうぞ
薬学理論問題の論点解説 一覧です。
走る!「基本骨格」Twitter Ver.|薬剤師国家試験対策ノート @YouTube
このコンテンツの制作者|
滝沢幸穂(Yukiho.Takizawa)phD
■Facebook プロフィール
https://www.facebook.com/Yukiho.Takizawa
■X (Former Twitter) プロフィール 🔒
https://twitter.com/YukihoTakizawa
CONTACT|
mail: info_01.matsunoya@vesta.ocn.ne.jp (Matsunoya Client Support)
tel: 029-872-9676
日々の更新情報など、Twitter @Mats_blnt_pharm 🔒から発信しています!
🔒🐤💕 https://twitter.com/Mats_blnt_pharm
https://note.com/matsunoya_note
note.com 右上の🔍で
( matsunoya_note 🔍 )
松廼屋 Mats.theBASE
https://matsunoya.thebase.in/
サポート感謝します👍
最後までお読みいただきましてありがとうございました。
Here; https://note.com/matsunoya_note/n/nbdd2c114a26e
松廼屋|論点解説 薬剤師国家試験対策ノート問 108-107【化学】論点:アスパラギン酸プロテアーゼ / システインプロテアーゼ / 酵素反応機構 / 基質加水分解 / 残基相互作用|matsunoya
ここから先は
¥ 1,000
医療、健康分野のリカレント教育における「最強コンテンツ」を note で誰でもいつでも学習できる、 https://note.com/matsunoya_note はそんな場にしたい。あなたのサポートがあれば、それは可能です。サポート感謝します!松廼屋 matsunoya
