
【前編】 新型コロナ人工ウイルス論: 新型コロナは本当に変異率が高いウイルスなのか?
武漢株を発端としたコロナウイルス騒動では、その後アルファ株に始まりオミクロン株に至るまで変異株が次々と現れ続けました。また、高病原性鳥インフルエンザやインフルエンザワクチンについても耳にする機会が増えています。では、そもそもこれらのウイルスはどこから来たのでしょうか? そして新型コロナ変異株はそれぞれ一体どこから来たのでしょうか? この疑問は古くて新しい課題なのです。
2021年12月27日のブログ記事で私は初めて新型コロナウイルスの不自然さに関して触れ、オミクロン株は人工ウイルスではないかと考察しました。
そしてその後、2022年6月5日の記事で改めて新型コロナウイルスの他の変異株も人工ウイルスなのではないかとより踏み込んで言及しました。当時のこのブログ記事は私のプレプリントを紹介したものですが、私の考えは現在でも変わりません。
研究生活を続けてきた中で私が体感したのは、物事の本質とは案外シンプルだという事です。そして、むしろシンプルすぎるために見落とされやすい事もあるのです。今回紹介させていただく論文における遺伝子解析の結果は、ある意味シンプルさを突き詰めた先に見えてくるものについてです。
約2年前に執筆した新型コロナ人工ウイルス説についての私のプレプリントは、諸事情から長らくペンディング状態になっていたのですが、そのプレプリントに新たな解析やデータを加えて大幅に改訂した論文がこのたび査読を通り正式に発表されました。実際、著作権が奪われたままであるといった問題等から場合によってはお蔵入りになる可能性も高かった論文なのですが、所属研究所の法務部の助けも借り、再投稿へと漕ぎ着ける事ができました。
SynBioはMDPI系列の2023年に創刊された合成生物学の専門誌です。今回発表した私の論文は合成生物学のむしろ悪い側面についてであり、そういった内容にも関わらずよく採用してもらえたものだと思いました。
この私自身の論文を参考資料として用いながら、新型コロナウイルス人工説についてさらに掘り下げて詳しく解説していこうと思います。全3回の記事になりますが、よろしければお付き合い下さい。

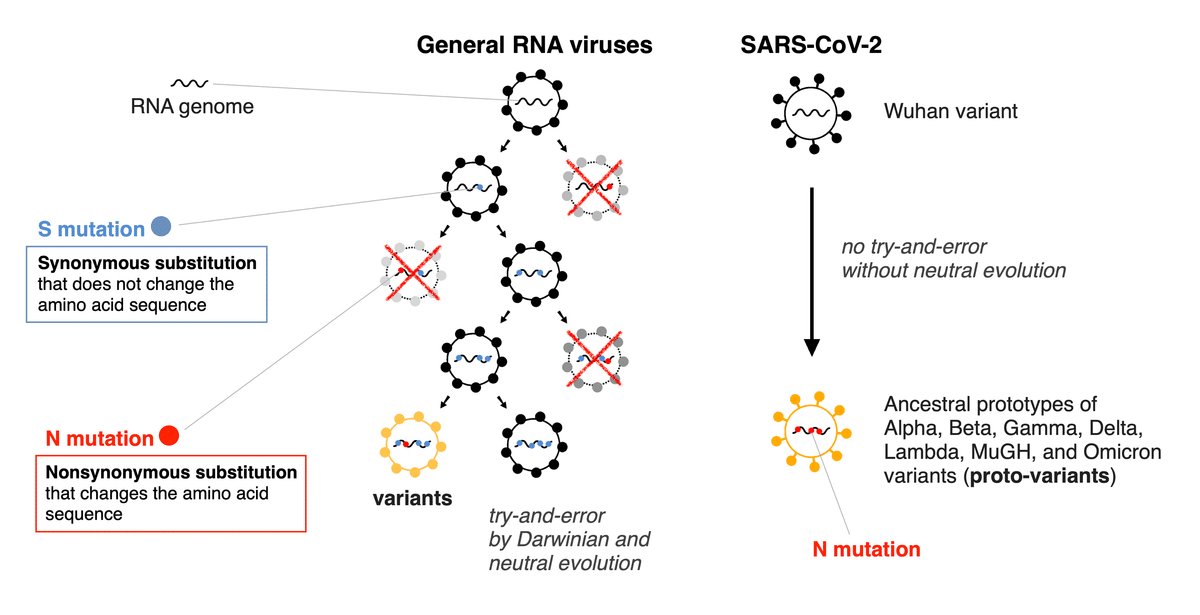
はじめに論文の要点をお話しさせていただきます。オミクロンだけではなく、そもそも新型コロナウイルス変異株のアルファ、ベータ、ガンマ、デルタ、ミュー、オミクロンのいずれもが進化の法則に従っていませんでした。基本的にウイルスはそれぞれの変異株が誕生した後も人や動物に感染を繰り返すうちに変異を重ねます。そのため、たとえどの変異株が人工ウイルスだったとしても、それぞれのウイルスの配列は「人工的な配列」+「自然な進化」の状態となります。私はこれらの「自然な進化」によるノイズを排除するために、まずそれぞれの変異株の祖先型を同定しました (図1)。そしてその祖先型が武漢型からどのように進化したのかを解析しました。その際に変異株の起源を「一般的なRNAウイルスの進化」と比較する事で、コロナウイルスの祖先型の変異株がいかに不自然で人工的であるのかが明らかになりました。
以下が論文のリンクです⬇︎
https://www.mdpi.com/2674-0583/2/3/17
The Natural Evolution of RNA Viruses Provides Important Clues about the Origin of SARS-CoV-2 Variants
Arakawa (2024) SynBio
RNAウイルスの自然進化は、SARS-CoV-2変異株の起源に関する重要な手がかりを与えてくれる。
荒川 央
最近のパンデミックにも関わらず、その原因であるSARS-CoV-2の起源については依然として論争が続いている。本研究では、武漢株の子孫であるいくつかのSARS-CoV-2の祖先型 (プロト変異株) を同定した。これらの祖先型変異株のゲノムの進化の歴史を徹底的に評価した結果、祖先型変異体の変異のほとんどがアミノ酸配列を変化させる変異に偏っている事が明らかになった。このような非同義置換 (N変異) はSARS-CoV-2祖先型変異体では一般的であったが、他のRNAウイルスでは同義置換 (S変異) と呼ばれるアミノ酸変化をもたらさないヌクレオチド変化が優勢であった。SARS-CoV2プロト変異体におけるN変異の偏りは、スパイク遺伝子と他のいくつかの遺伝子で見られた。一般的なRNAウイルスにおけるN変異とS変異の比率を解析した結果、RNAウイルスがプロト変異株を自然発生的に進化させる確率は、自然条件下では1.5 x 10⁻⁹から2.7 x10⁻²⁶の間である事が明らかになった。これらの結果は、SARS-CoV-2変異株が正規のルートで出現したものではない事を示唆している。
新型コロナウイルスの正式名称が「SARS-CoV-2」です。SARS-CoV-2オミクロン変異体 (B.1.1.529株) はボツワナで最初に同定され、2021年11月24日に南アフリカから世界保健機関 (WHO) に報告されました。オミクロンの新規変異の多くはスパイク遺伝子上に存在しています。その変異の多さと特異性から、当初からオミクロンはコロナワクチンによる免疫応答を効果的に回避する可能性が懸念されていました。
オミクロンの変異は段階を追って蓄積したというよりもむしろ「突然」多数の変異を獲得しています。そのため当時からオミクロン変異株の起源に関しては様々な仮説が立てられました。 1)COVID-19に慢性感染した免疫抑制患者で発生した、 2)ウイルス監視のインフラがほとんどない、あるいは全くない地域社会で数ヶ月かけてゆっくりと進化した、 3)マウスなどのヒト以外の宿主で進化した後、新たな変異のレパートリーとともに再びヒトに流入した、などです。
また、オリジナルの武漢型SARS-CoV-2起源の候補としてはコウモリやセンザンコウが挙げられています。他にもSARS-CoV-2変異株の進化にはネコが関わっている可能性までも推測されています。このようにオミクロンだけではなく、他のSARS-CoV-2変異株の起源についても依然謎に包まれており、意見が分かれているのが現状です。
生物は世代を経て変化しながら環境に適応しようとしていきますが、その背景には生物の設計図としての遺伝情報であるゲノムの変化があります。生物にとって有利な遺伝的形質を持つ突然変異は自然淘汰によって競争に勝ち残っていきます。これが「ダーウィン進化論」です。しかしながら、タンパク質のアミノ酸配列を変化させる遺伝的変化 (N変異) のうち有益な変化などというものは本来まれであり、遺伝子の突然変異のうちほとんどはタンパクの機能を損なうものです。一方、アミノ酸配列を変化させない変異 (S変異) はタンパク質の機能性向上とは関係無くランダムにゲノムに固定されます。これが木村資生が提唱した「中立進化」です。この2つの概念が進化論の大前提であり、ウイルスや哺乳類など多くの種の進化では、変異の多くはS変異に偏る傾向がある事が知られています。

GISAIDデータベースにはすでに数百万のSARS-CoV-2の遺伝子配列が登録されており、大規模な遺伝子配列の研究によってそれぞれの変異株がどのように進化してきたかが報告されてきました。そうした論文報告の中にはSARS-CoV-2の進化的変異体の特徴と適性、およびワクチンの影響などが解析されています。そしてここで留意すべき点は、変異株の進化には変異株が誕生するまでの進化と市中感染を繰り返す中での進化が混在しているという事です。そのため私は、市中感染における「自然な」進化のノイズを取り除く事により、変異株がどのように誕生したかに焦点を当てました (図2)。
SARS-CoV-2変異株の祖先型配列の推定
では新型コロナ変異株はどのように進化してきたのでしょうか。すでに膨大な数の各変異株の塩基配列がデータベースに登録されており、それらは変異、欠失、挿入によって多様性を蓄積しているのが確認できます。さらにディープシークエンシングのエラーも各配列に影響します。実際、シークエンシングの「電子的なエラー」と実際に「遺伝子上に起きた変異」を区別するのは困難です。
今回のこの研究で私は各SARS-CoV-2変異株がどのように誕生したのかについて焦点を当てました。また、変異株が誕生した後に蓄積した変異などの影響を最小限にするために、利用する配列をそれぞれの変異株で最も早期に収集された配列に限定しました。それぞれの変異株の祖先型の配列は、データベース由来の配列をお互いに比較し、共通する配列として同定されました。ここでは変異株の祖先型配列をプロトタイプ型、つまりプロト-変異株と呼んでいます。

20年以上前となる2002年11月から2003年7月にかけて、中華人民共和国南部を中心に重症急性呼吸器症候群 (Severe acute respiratory syndrome; SARS) のアウトブレイクが発生したのを覚えている方も多いかと思います。SARS-CoV-1はこの「SARS」を引き起こしたコロナウイルスです。そして、コウモリコロナウイルスRaTG13はSARS-CoV-2の近縁起源の一つです。図3はプロト-変異株とこれらのウイルスの関係を分子系統樹として表したものです。横軸の長さが進化的距離であり、変異などによる遺伝子配列の違いの大きさを意味します。図3のようにプロト-変異株同士を比較すると一見遺伝子の変異が多いように見えます。

しかしながら、大切な事は単に変異株同士だけを比べるのではなく、進化について俯瞰するためのより大きな視点を持つ事です。実際、図4のようにプロト-変異株とSARS-CoV-1、RaTG13の遺伝子配列を比較すると、プロト-変異株の間の変異は、プロト-変異株やRaTG13との間の変異よりもはるかに少ないのです。

そして図5はこれらのウイルス間の遺伝子配列の相違をパーセンテージで示した物です。プロト-変異株間の違いはオレンジ色で強調表示しています。これを見ると、プロト-変異株の間の変異のほとんどは0.5%以下に過ぎず、プロト-変異株とRaTG13 (約4%)、プロト-変異株とSARS-CoV-1の間の変異 (約21%) と比べるとはるかに少ない事が分かります。
さて、それではSARS-CoV-2は本当に「変異率が高く、たくさんの変異を蓄積してきた」ウイルスと呼べるのでしょうか?
#コロナワクチン
#ワクチン
#コロナ
*記事は個人の見解であり、所属組織を代表するものではありません。
この記事が気に入ったらサポートをしてみませんか?
