
肥満治療薬をめぐる攻防 LLYとNVOと新たなライバル
本記事では肥満治療薬、減量薬として人気のGLP-1アゴニストとその販売元であるEli Lilly、Novo Nordiskについて解説した上で、これら2社に対抗しようとしている新たな製薬企業について最新の動向をまとめます。
本記事は分量も多く、今後新たなトライアル結果も随時発表されるため、適宜加筆、修正を行い、記事購入者には通知していく予定です。
以下に修正履歴を記載していく予定です。
2024/8/21 初版執筆
また本記事は医学的な内容はエビデンスに基づき、正確を期しているつもりですが、齟齬がありましたら御指摘願います。
GLP-1アゴニスト
GLP-1(glucagon-like peptide-1)は小腸で作られるホルモンで、インスリンの分泌を刺激し、グルカゴンの分泌を抑えることで、血糖を下げる働きがあります。
GLP-1と似た構造を持ち、同様の作用を身体に及ぼす薬剤を総称してGLP-1受容体作動薬(GLP-1 agonist)と呼びます。
これらの薬は当初糖尿病(Diabetes Mellitus, DM)の治療薬として承認されましたが、投与された患者の体重が減少する報告を受け、メーカーは新たに体重減少を適応症としてFDAに申請しました。

上の表の通り、2017年にNovo Nordiskが開発したセマグルチド(Semaglutide)が成人の糖尿病治療薬としてFDAの承認を受け、商品名オゼンピック(Ozempic)として販売が開始されました。
後に同様のSemaglutide注射剤が減量薬としてFDAに承認され、ウェゴビー(Wegovy)という商品名で販売が開始されました。
Ozempic、Wegovyともに有効成分はSemaglutideですが、WegovyはOzempicと比較して高用量バージョンになっているという違いがあります。
GLP-1 + GIP
Novo Nordiskから遅れること数年、Eli LillyがGIPとGLP-1の2つの受容体に作用するGIP/GLP-1受容体作動薬を開発しました。
GIPはGastric inhibitory polypeptideの略で、GLP-1と同様に小腸で分泌され、インスリン分泌を促進する作用がある一方で、グルカゴンの分泌を増やし、中性脂肪を増加させるなどといった、一見肥満を誘発するのではないかと考えられる作用も持っています。

このような作用があるGIPですが、マウスを使った研究で、生理的な濃度では肥満を誘導する一方で、薬理的な濃度まで上昇させると肥満を抑制する方向に働くことが示唆されました。(Kim SJ, et al. PLoS One. 2012;7:e40156.)
またGIP受容体作動薬、GLP-1受容体作動薬の2剤同時投与により、GLP-1受容体作動薬単独に比べ、体重減少効果が大幅に増強されることが示唆されました。(Killion EA, et al. Nat Commun. 2020;11:4981.)。
これらの研究を受け、Eli LillyがGIP/GLP-1受容体作動薬を開発し、2022年に糖尿病治療薬としてチルゼパチド(Tirzepatide)がFDAの承認を得て、商品名マンジャロ(Mounjaro)として発売されました。2023年には肥満症に対してもFDAの承認が得られ、商品名ゼプバウンド(Zepbound)として発売が開始されています。
LLY、NVOの決算
ともに糖尿病治療薬、肥満治療薬を販売しているLLYとNVOですが、2024年の年初来のパフォーマンスは30%程度差が出ています。以下では2社の直近の決算を見ていきます。

<LLY 2024 2Q決算>
EPSは予想$2.73に対し結果$3.92でした。
売上高は予想99.6億ドルに対し結果113億ドルでした。
売上高成長率は前年同期比+36.0%でした。
2024年のEPSは予想$13.68に対し、新ガイダンス$16.1〜16.60が提示されました。
2024年の売上高は予想429.3億ドルに対し、新ガイダンス454〜466億ドルが提示されました。
売上高の成長は主にMounjaro、Zepboundからもたらされました。
世界のMounjaro売上高は30.9億ドルでした。前年同期は9.8億ドルでした。米国Mounjaro売上高は24.1億ドルでした。

Zepboundは肥満治療薬として2023年11月から販売を開始しており、米国Zepbound売上高は12.4億ドルでした。

<NVO 2024 2Q決算>
米国預託証券(ADR)1枚当たり利益は予想$0.71に対して、結果$0.65でした。
売上高は予想99.1億ドルに対して、結果98.2億ドルでした。
通期の売上高成長率は従来の19%-27%から22%-28%に引き上げる一方で、営業利益の成長率予想は従来の22%-30%から20%-28%に引き下げました。
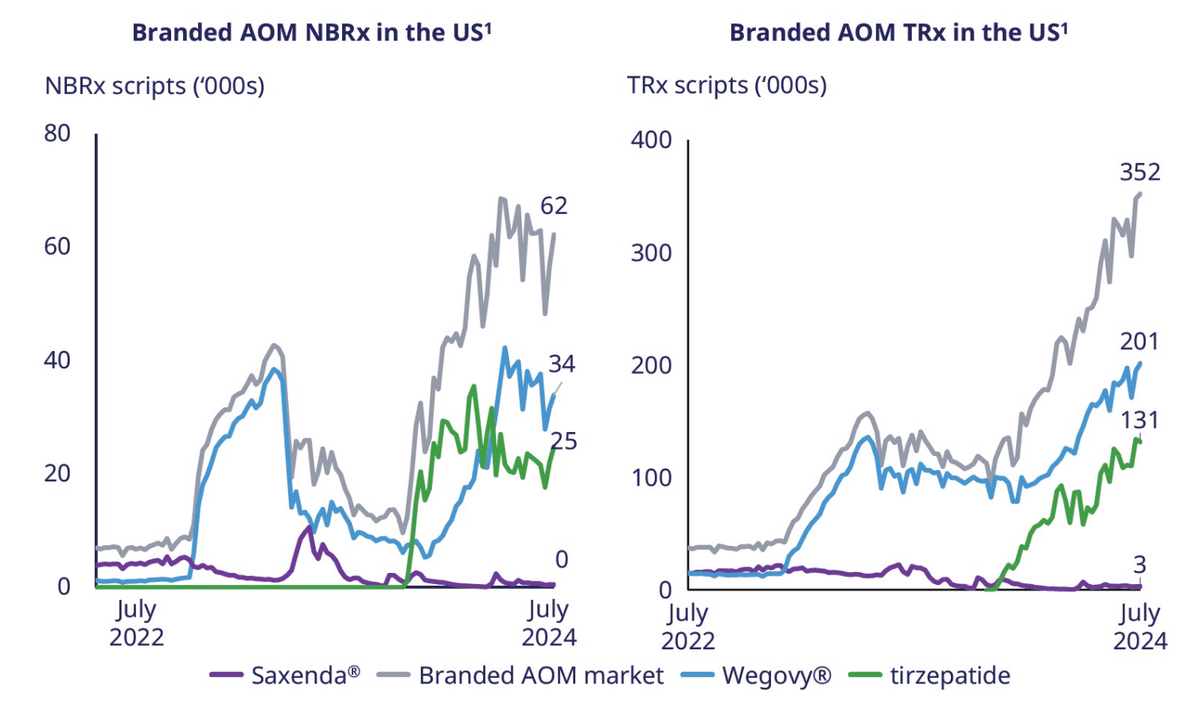
Ozempicの売上高は前年比30%増の42.6億ドルでしたが、アナリスト予想の43.8億ドルを下回りました。
Wegovyの売上高は前年比69%増の18.8億ドルでしたが、アナリスト予想の19.6億ドル下回りました。
以下ではLLY、NVOに対抗すべく、新たな肥満治療薬を開発している会社を紹介します。
Zealand Pharma(ZEAL)
デンマークに本社を置くバイオ医薬品企業で、1998年に設立されて以来、糖尿病、肥満、消化器疾患などの治療薬を中心に研究開発を進めてきた会社です。
現在ドイツのBoehringer Ingelheim社と共同開発しているSurvodutide (BI 456906; long-acting, glucagon/GLP-1 receptor dual agonist)の第3相試験が進行中です。
第2相試験は3つ行われ、1つ目の研究では安定したメトホルミン療法を受けている2型糖尿病患者に対して、16週間後に血糖値やHbA1cの用量依存的な減少が見られました。
2つ目の研究では過体重または肥満を抱える患者に、46週間後に用量依存的な体重減少が確認されました。
3つ目の研究では、代謝機能異常関連脂肪性肝炎(MASH)を抱える人々に対して、48週間後にMASHおよび肝線維症の改善が見られました。


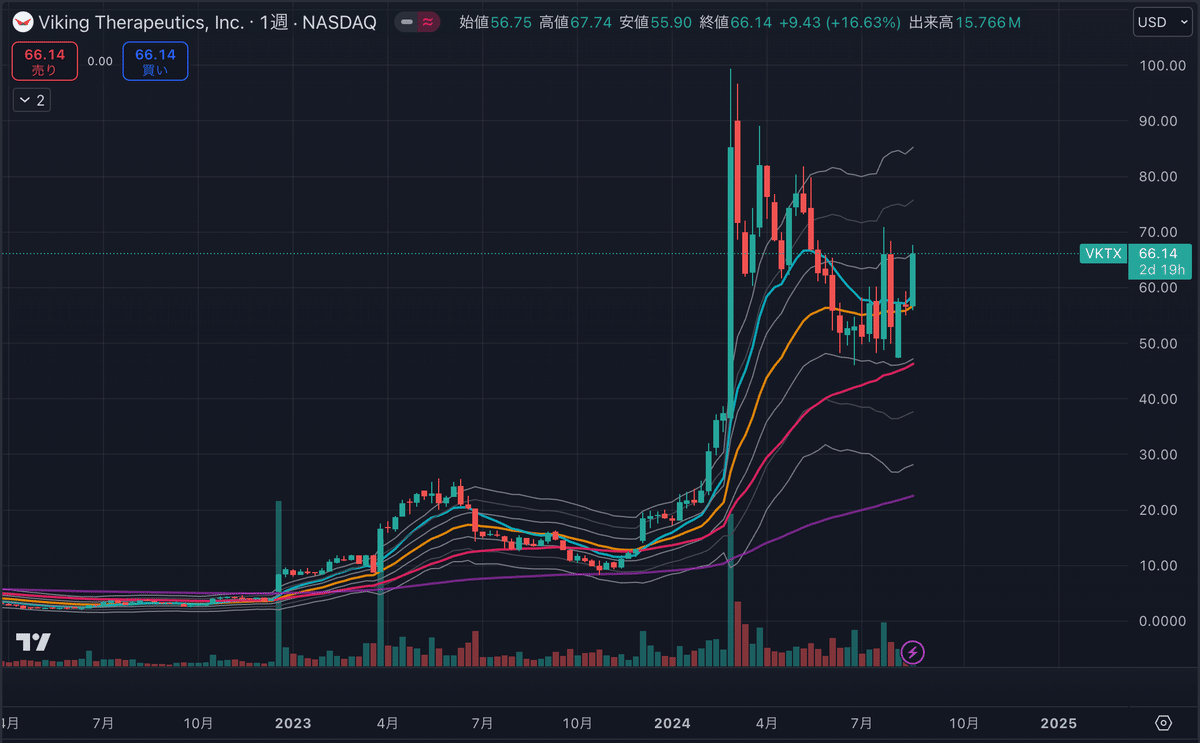
Viking Therapeutics(VKTX)
Viking Therapeuticsは2012年に設立され、特定の受容体をターゲットにした新しい薬剤の開発を行っており、非アルコール性脂肪肝炎(NASH)の治療薬の開発歴があります。
2024年2月にVK2735(Dual GLP-1/GIP Receptor Agonist)を投与された患者がプラセボと比較して統計的に有意な体重減少を示し、第2相VENTURE試験が主要評価項目およびすべての副次的評価項目を達成したと発表しました。この結果を踏まえ、VK2735の開発の次のステップについてFDAと協議する予定です。
また2023年第1四半期にVK2735の経口製剤を評価する第1相試験を開始し、2024年3月にVK2735の経口錠剤製剤に関する良好な結果を発表しました。
この第1相の結果に基づき、2024年後半に肥満症を対象としたVK2735の経口製剤による第2相試験を開始する計画です。

Terns Pharmaceuticals(TERN)
Terns Pharmaは2018年に設立された医薬品開発企業です。現在GLP-1ホルモンを標的とした経口減量薬(TERN-601)を開発しており、2024年後半に28日間の減量データを発表する予定です。


Structure Therapeutics(GPCR)
Structure Therapeuticsは2016年に設立された医薬品開発企業で、GSBR-1290と呼ばれる経口1日1回投与のGLP-1製剤の開発に取り組んでいます。この製剤は6月に行われた第2相試験でプラセボ投与と比較して6%以上の体重減少が確認されました。


Altimmune(ALT)
Altimmuneは2005年に創業された米国の臨床ステージバイオ医薬品企業で、2023年11月にGLP-1とグルカゴンのdual receptor agonist(pemvidutide、ALT-801)について、肥満症を対象とする第2相試験(MOMENTUM試験)で主要評価項目を達成したと発表しました。
2022年から実施していた研究で48週間のデータ解析を完了し、最大用量群で体重が平均15.6%減少したことを報告しています。
除脂肪体重を維持しながら、体重減少を誘導する(ほとんど脂肪による体重減少が得られる)ことが評価されるだろうとCEOがコメントをしています。

その他大手製薬会社の動向(Pfizer, Amgen, Roche, AstraZeneca)
<Pfizer>
肝臓酵素の上昇を理由に1日1回投与のロティグリプロン、強い副作用を理由に1日2回投与のダヌグリプロンという2つの薬剤の試験を中止しています。
<Amgen>
GIP受容体の阻害とGLP-1受容体の活性化を同時に行うことができる注射薬MariTideのトライアルが進行中です。
2024年2月に第1相試験のデータを発表し、糖尿病のない肥満者を対象にした研究で、85日後に体重を14.5%減少させることができたと発表しました。
また第2相試験も良好な結果が得られているとして、第3相試験を実施する計画であると発表しています。
<Roche>
減量薬開発企業カーモット・セラピューティクスを27億ドルで買収し、同社の週1回投与の注射薬CT-388のトライアルが進行中です。
CT-388の週1回皮下注射により、平均体重減少率18.8%が達成されました。
24週目にはCT-388投与群の100%が5%以上の体重減少を達成し、70%が15%以上、45%が20%以上の体重減少を達成しました。
<AstraZeneca>
中国のEccogene社と経口1日1回投与のGLP-1受容体作動薬であるECC5004 の独占的ライセンス契約を締結しました。
第1相試験の速報結果ではプラセボと比較して忍容性が良好で、試験された用量レベル全体においてグルコースおよび体重の減少が認められました。
投資見解
ここから先は
¥ 500
この記事が気に入ったらサポートをしてみませんか?
