
GOG-218の解析データについてのSupplementary Materialの解説
GOG-218試験の概要について
Mutations in Homologous Recombination Genes and Outcomes in Ovarian Carcinoma Patients in GOG218: An NRG Oncology/Gynecologic Oncology Group Study この論文のサプリメントについての解説記事です。
論文の要旨は以下。
GOG-0218試験の卵巣がん患者1,195人を対象に、ホモロガス組換え修復(HRR)関連遺伝子の変異解析を行った。
307人(25.7%)にHRR遺伝子の病的変異が認められた。
BRCA1変異が148人(12.4%)
BRCA2変異が78人(6.5%)
その他のHRR遺伝子変異が81人(6.8%)
HRR変異陽性例では、変異陰性例に比べて無増悪生存期間と全生存期間が有意に延長していた。
BRCA1、BRCA2、その他のHRR遺伝子変異のいずれも、予後改善と関連していた。
ベバシズマブ併用の有無とHRR変異状態に交互作用は認められなかった。
低異型漿液性癌では、HRR変異率が有意に低かった(10.9% vs 27.0%、P=0.02)。
体細胞変異のみの32例でも、HRR変異例と同様に予後が良好であった。
したがって、HRR経路の欠損は卵巣がんの予後予測因子となり得ることが示唆された。
サプリメントの内容


要旨
要旨の解説
このSupplementary Materialは、卵巣がんの治療における新しいバイオマーカーKELIMスコアの有用性を評価した臨床試験GOG-0218の追加データを提示しています。
主な内容
KELIMスコアは、CA-125値の動態から算出される指標で、がん細胞の増殖能力と薬剤感受性を反映する。
多変量解析により、KELIMスコア不良群では良好群に比べて無増悪生存期間が有意に短かった(ハザード比0.51)。
ベバシズマブ併用化学療法において、KELIM不良群ではベバシズマブによる全生存期間の延長効果が認められた(ハザード比0.78)。
一方、KELIM良好群ではベバシズマブの追加効果は限定的だった。
別の第III相試験ICON-7でも同様の結果が得られ、KELIMスコアの予後予測能と治療選択のバイオマーカーとしての有用性が示された。
したがって、KELIMスコアは卵巣がんの予後予測と個別化治療の決定に役立つ新しいツールになり得ることが示唆されています
Suppl Fig 1: 研究の対象患者の選択フロー

このフローチャートは、GOG-0218試験に登録された1,873人の患者から、KELIMスコアが評価可能な患者を選別するプロセスを示している。
初めに211人の患者が、治療開始後100日以内にCA-125値が3回未満しか測定されていないため除外された。
残りの1,662人についてKELIMスコアが算出され、最終的に1,644人が無増悪生存期間(PFS)解析対象、1,657人が全生存期間(OS)解析対象となった。
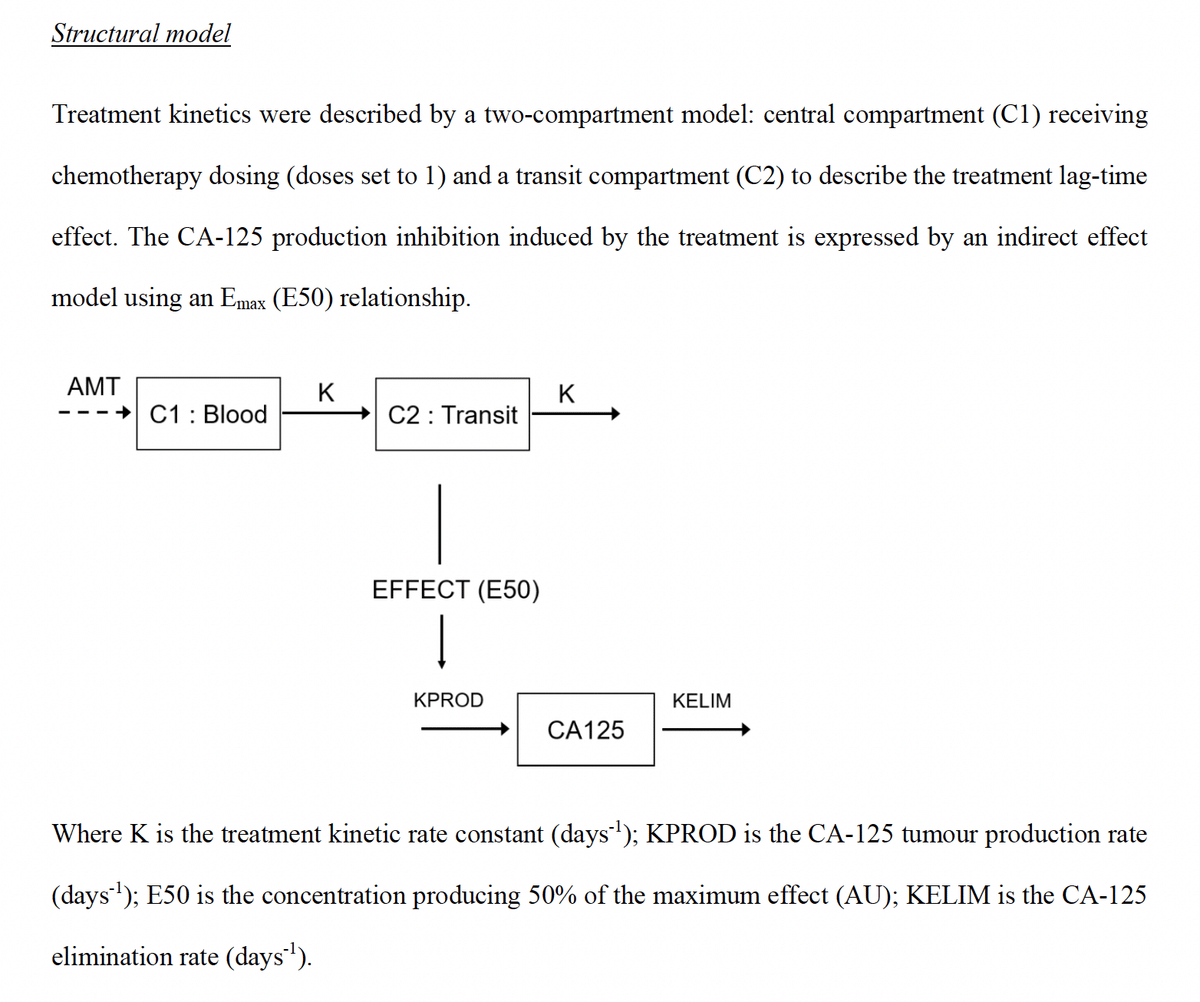
Suppl Fig 2: モデル適合度の評価

この図は、CA-125値の動態を記述するモデルの適合度を示している。
観測値と予測値のプロットでは、両者がよく一致していることがわかる。
正規化予測誤差分布のヒストグラムも正規分布に従っており、モデルの当てはまりが良好であることを示唆する。
Suppl Fig 3: 治療群別のKELIMスコア分布

この図は、プラセボ対照群(Arm 1)とベバシズマブ併用群(Arm 3)におけるKELIMスコアの標準化値の分布を比較している。
両群間でKELIMスコア分布に有意な違いはなく(p>0.05)、治療による選択バイアスはないことが示された。
Suppl Fig 4: KELIMスコアと無増悪生存期間

このfigureは、KELIMスコアが良好群(≥1.0)と不良群(<1.0)で無増悪生存期間(PFS)に有意な差があることを示すKaplan-Meier曲線。
KELIM不良群はKELIM良好群に比べて、PFSが有意に短かった(中央値7.4か月 vs 15.1か月)。
ハザード比は0.50(95%CI: 0.45-0.55)と算出され、KELIM不良群のリスクが約2倍高いことがわかる。
したがって、KELIMスコアは卵巣がんの無増悪生存期間を予測するバイオマーカーとして有用であることが示唆されています。
Suppl Fig 5: KELIMスコアと全生存期間

の図は、KELIMスコアが全生存期間(OS)の予測にも有用であることを示すKaplan-Meier曲線である。
KELIM不良群はKELIM良好群に比べて、OSが有意に短かった(中央値32.9か月 vs 55.7か月)。
ハザード比は0.53(95%CI: 0.47-0.59)。
つまり、KELIMスコアが不良な患者では良好な患者に比べて死亡リスクが約2倍高い。これらの結果から、KELIMスコアは卵巣がんの予後予測において重要なバイオマーカーとなり得ることが示唆されている。
Suppl Fig 6: 低リスク群における治療とKELIMスコアの相互作用(全生存期間)

この図は、ステージIII期で最適デバルキング術後の低リスク卵巣がん患者において、ベバシズマブ併用の有無とKELIMスコア(良好vs不良)による全生存期間への影響を示している。
KELIM良好群では、ベバシズマブ併用による全生存期間の延長効果はわずかで。
KELIM不良群においても、ベバシズマブ追加の明確な利益は認められず。
したがって、低リスク卵巣がん患者では、KELIMスコアがベバシズマブ併用療法の適応を予測するバイオマーカーとしての役割は限定的であることがわかる。
Suppl Fig 7: 高リスク群における治療とKELIMスコアの相互作用(全生存期間)

A) ICON-7試験の高リスク群
この図は、ステージIII期の亜最適デバルキング術後またはIV期の高リスク卵巣がん患者において、KELIMスコアとベバシズマブ併用による全生存期間への影響を示している。
・ KELIM不良群では、ベバシズマブ併用によりOSが延長する傾向がみられた(中央値29.7か月vs 20.6か月、ハザード比0.78)。
・ 一方、KELIM良好群ではベバシズマブの追加効果は限定的。
B) GOG-0218試験の高リスク群
GOG-0218試験の高リスク群においても、ICON-7試験と同様の結果が得られた。
・ KELIM不良群では、ベバシズマブ併用によりOSが有意に延長。
・ KELIM良好群ではベバシズマブの追加効果はわずか。
これらの結果から、KELIMスコアは高リスク卵巣がん患者において、ベバシズマブ併用療法の有効性を予測するバイオマーカーとして有用である可能性が示唆された。
Suppl Fig 8A: ICON-7試験の低リスク群におけるKELIMスコアと全生存期間

Suppl Fig 8A:CON-7第III相試験における初期研究(Colomban et al JNCI CS 2020)
左図は、ステージIII期で最適デバルキング術後の低リスク卵巣がん患者において、KELIMスコアの良好/不良とベバシズマブ併用の有無による全生存期間への影響を示している。
・KELIM良好群でも不良群でも、ベバシズマブ併用による全生存期間の延長効果は認められなかった。
・つまり、低リスク患者ではKELIMスコアがベバシズマブ併用療法の適応を予測するバイオマーカーとしての役割は限定的であることがわかる。
Suppl Fig 8B: GOG-0218第III相試験における外部検証研究
GOG-0218試験の低リスク群においても、ICON-7試験と同様に、KELIMスコアとベバシズマブ併用効果に明確な関連は認められなかった。
KELIM良好群、不良群ともにベバシズマブ追加による全生存期間の延長はわずかであった。
したがって、これらの結果から、KELIMスコアは高リスク卵巣がん患者においてはベバシズマブ併用療法の適応を判断する有用なバイオマーカーとなる可能性が高いものの、低リスク患者ではその予測能は乏しいと考えられる。
この記事が気に入ったらサポートをしてみませんか?
