
101章 痛風の症状と治療
kelley101章は Clinical Features and Treatment of Gout
キーポイント
・痛風は尿酸ナトリウム(MSU)結晶沈着の慢性疾患である。
・高尿酸血症は痛風発症の中心的な危険因子であり、この危険性は血中の尿酸値に依存する。
・MSU結晶は、強い痛みを伴う断続的で再燃性の急性炎症性関節炎を引き起こし、MTP関節、中足部、足首に好発する。
・関節炎は関節可動域の制限、感染の合併、関節損傷、変形を引き起こし、身体障害や健康関連QOLの低下と関連している。
・MSU結晶の同定は痛風診断のゴールドスタンダードであるが、臨床診断ルール(後述)の精度も高い。
・超音波やDual-Energy CT などの画像診断法は、診断が不確かな場合に役立つ。
・痛風発作は、プレドニゾロン、非ステロイド性抗炎症薬(NSAIDs)、コルヒチン、抗IL-1β療法(使用可能な場合のみ)などの抗炎症薬で管理される。
・痛風の慢性管理の戦略は、尿酸降下薬(ULT)で血清尿酸値の目標値を6mg/dL未満、重症患者ではさらに低い値(5mg/dL)にしてMSU結晶を溶解することである。
・ULTを徐々に増量し、低用量コルヒチン(または他の抗炎症薬)で抗炎症予防を行うことにより、ULT開始時の痛風再燃リスクを軽減することができる。
・ほとんどの患者にとって第一選択のULTであるアロプリノールは、低用量から開始し、血清尿酸値の目標値を達成するまで漸増する。
・アロプリノールが忍容できない場合、または尿酸値の目標値を達成できない場合には、フェブキソスタットが選択肢となる。フェブキソスタットは、アロプリノールと比較して心血管系死亡率および全死因死亡率が高い可能性がある。
・内服薬で目標値を達成できない重症患者では、ペグロチアーゼを2週間ごとに静注することも選択肢になる。
・痛風患者には併存疾患の有病率が高いため、心代謝疾患や腎疾患などの積極的なヘルスメンテナンスの管理が必要である。
・肥満の患者への減量、甘い飲み物の回避、危険な飲酒に対するアルコール摂取量の削減に関する食事アドバイスは、痛風患者を含むすべての人々にとって重要である。
・通常のプライマリ・ケアと比較して、リウマチ学会のガイドラインに従った看護師主導のケアは、ULTの遵守率が高く、尿酸値が低下し、痛風の再燃、痛風結節、医療関連QOLなどの臨床転帰が大きく改善する。そして、費用対効果も高い。
100章の病態生理についてうちのエースが神がかったまとめをしてくれているので、ぜひそちらを参照してください。複雑系の免疫学が本当におもしろいことを痛感できると思います。
Pearl: 2015年米国リウマチ学会(ACR)/欧州リウマチ学会(EULAR)の痛風分類基準は、臨床試験の組入基準を整えるものであり、診断のために使用されるべきではない
Comment: The 2015 American College of Rheumatology (ACR)/European League Against Rheumatism (EULAR) gout classification criteria are intended for identifying subjects who may be eligible for entry into a clinical study and should not be used for diagnosis.
・いつものように、分類基準は診断基準ではない、という話し。大事なことは怒涛の反復。
・2015分類基準の原著(下図)、ウェブでもアプリっぽくチェックできます

※診断に使ってはだめとなっていますが、ACR/EULAR2015 (Sn68%, Sp98%, PMID: 28431109)の特異度は非常に高いです。臨床的にはだいたい分かるので使いませんが、高得点をつないでいくと、典型的な痛風になるのでみてみましょう。
例えば、以下Table2(下の表)の高得点を辿っていくと、
・母趾(第1MTP)関節炎(2)
・発赤・押すと痛い・痛くて歩けない(3)
・24時間以内にピークが来る急性発症
・14日以内に寛解・非発作時は症状がない(3)
・痛風結節がある(4)
・尿酸値が6以上(6-8: 2, 8-10: 3, 10以上: 4点)
・関節液に尿酸結晶あり
・画像で結晶あり(4)・びらんあり(4)
これが、典型的な痛風発作です。これがTable2.

https://acrjournals.onlinelibrary.wiley.com/doi/epdf/10.1002/art.39254
下の表は用語の定義です。Chronic gouty arthritis、Podagraあたりは押さえておきましょう。ポダグラ・ポダグラ・ポダグラ...
Gout, Hyperuricemia and Crystal-Associated Disease Network Consensus Labels and Definitions for Disease Elements in Gout

Myth: 慢性的に関節炎があるような痛風をChronic goutと呼ぶ
Reality: The use of the word ‘chronic’ in this context was felt to be redundant and potentially confusing when gout, by its very nature, is characterised by chronic crystal deposition. Consensus for the recommendation that “the label ‘chronic gout’ should be avoided” was achieved with 28 out of 29 (97%) voting in favour of this recommendation.
・上の表の8にG-CANとは: Gout, Hyperuricemia and Crystal-Associated Disease Network。G-CANのコンセンサスステートメントから。 https://acrjournals.onlinelibrary.wiley.com/doi/epdf/10.1002/acr.23607
・chronic goutを避けるべき理由は、痛風はそもそも慢性的な結晶沈着を特徴とするわけなので、慢性痛風という言葉は分かりにくく、通常の痛風と慢性的に炎症が起きているというものを分けるために、chornic gouty arthritisというべきである、ということのよう- 29人中28人(97%)がこれに同意。
はじめに
・痛風は尿酸ナトリウム(MSU結晶沈着の慢性疾患である。MSU結晶は、組織の尿酸値が高い状態で形成され、急性炎症性関節炎の間欠的な再燃の引き金となる。
・高尿酸血症の一部の患者では、痛風結節が形成されることがある。これらの病変は、関節の損傷や変形につながることがある。
・痛風発作は、非ステロイド性抗炎症薬(NSAIDs)、コルヒチン、プレドニゾン、抗IL-1β療法などの抗炎症薬で管理される。
・長期痛風管理の戦略は、尿酸降下療法(ULT)によるMSU結晶の溶解である。
Pearl: 高尿酸血症の人のほとんどは痛風ではないが、尿酸値10mg/dL以上を15年追跡すると49%は痛風を発症する。
Comment: Hyperuricemia is nearly universal among patients with gout, yet the majority of individuals with hyperuricemia do not develop gout. However, a 15-year longitudinal study shows that 49% of individuals with urate levels exceeding 10mg/dL eventually develop gout.
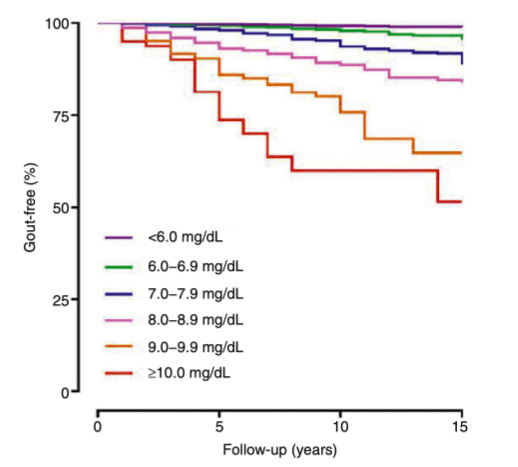
・ほとんどの高尿酸血症は痛風ではないが、痛風発症率は尿酸値が高いほど高くなる。
・ベースライン時に痛風でなかった18,889人の解析では、15年間の累積発症率は尿酸値が6mg/dL未満の1.1%、そして10mg/dL以上では49%となった(上図)。これをみるとやはり尿酸値10超える人は下げたくなる気持ちは分かりますね。CKDの痛風発作の治療はステロイド中心になるので苦戦しますね、慣れていないと。DMあるとさらにインスリン調整しながらになりますし。
Pearl: 高尿酸血症のカットオフ6.8mg/dLは、実験室において37℃、pH7.0で痛風結晶が形成される濃度である。
Comment: One commonly used, and physiologically based, definition of hyperuricemia is 6.8 mg/dL; this is the concentration at which MSU crystals form in the laboratory at 37°C and pH 7.0.
Arthritis Rheum 15(2):189–192, 1972.
・高尿酸血症の定義として一般的に用いられているのは、生理学的根拠に基づく6.8mg/dLである。これは、実験室において37℃、pH7.0でMSU結晶が形成される濃度である。遠位関節の温度は通常、中心部の推定温度より低く、外反母趾の推定温度である35℃では、MSU結晶は6mg/dLの濃度で形成される 。さらに、血清尿酸値6mg/dLは、痛風の発症リスクが上昇し始める濃度である。

https://onlinelibrary.wiley.com/doi/epdf/10.1002/art.1780150209
・足趾など37℃未満だと6.8未満でも結晶が形成されうることが分かる。
Pearl: 女性の痛風は閉経前はほとんど認めず、閉経後でも0.1-0.3%程度と男性の10%に満たない

・痛風のほとんどが男性である。
・男女比20:1。男性の有病率は30-40代でおよそ1%、ピークが60-70代で3.5%である。女性の痛風は閉経前はほとんど認めず、閉経後でも0.1-0.3%程度と男性の10%に満たない。
kelleyによると、「欧米諸国では、痛風の有病率は男性で3~6%、女性で1~2%である」。
・つまり日本は欧米と比べて痛風は少ない。欧米よりさらに多いのは...
Pearl: 台湾人、アボリジニ、ニュージーランドのマオリ族、ポリネシアの太平洋諸島民など、一部の集団では有病率がかなり高く、これらの集団の有病率は他の民族の少なくとも2倍である。
・There is a substantially higher prevalence in some populations, including Taiwanese Aborigines, Māori in Aotearoa/New Zealand, and Polynesian Pacific Islanders; these populations have a prevalence that is at least twofold greater than other ethnicities.

・この文献は読んでおきたい。
・台湾多いなー。日本だと高齢男性3%程度だが、台湾は10%<。遺伝的要素は大事。
Pearl: 利尿薬、ACE阻害薬、β遮断薬、アスピリン、カルシニューリン阻害薬などは痛風のリスクである
・Medications frequently used to treat these conditions including diuretics, ACE inhibitors, beta blockers, low-dose aspirin, and calcineurin inhibitors are also associated with hyperuricemia and incident gout. BMJ 344:d8190, 2012.
痛風のリスク/トリガー

Lancet. 2016 Oct 22;388(10055):2039-2052.の表を日本語にしました
・高齢、男性、女性の閉経後、遺伝的要因、乾癬や骨髄増殖性疾患のような慢性的に細胞のターンオーバーが亢進する疾患
・薬剤だと、利尿薬、ACE阻害薬、β遮断薬、低用量アスピリン、カルシニューリン阻害薬
・関連疾患に、肥満、慢性腎臓病、閉塞性睡眠時無呼吸症候群、高血圧、心不全、その他の心血管系疾患がある。
・入院で痛風発作のリスクは10倍になる (J Rheumatol. 2018 Aug;45(8):1188-1191。
※100章のshotaroに聞いたパール:低用量アスピリンは尿酸値があがるけど、高用量ではそうはならない。100章kelleyは秀逸です。
Pearl: 全体として、特定の食事成分が血清尿酸塩濃度に及ぼす影響は、一般集団では極めて小さい。
Comment: Overall, the effects of specific dietary components on serum urate concentrations are quite small in the general population.
meta-analysis of popula- tion based cohorts, BMJ 363:k3951, 2018
・赤身肉、魚介類、ビールなどの高プリン体食品、砂糖入り飲料などの食事因子は高尿酸血症と痛風に関連している。
・低脂肪乳製品、コーヒー、ビタミンCの摂取は、血清尿酸値の低下および痛風発症リスクの低下と関連している。
・高血圧食で有名なDietary Approaches to Stop Hypertension(DASH)食も痛風リスクを低下させる。DASH食:果果物、野菜、低脂肪乳製品を重視し、脂肪・コレステロールの摂取を減らす
・がしかし、全体として、特定の食事成分が血清尿酸塩濃度に及ぼす影響は、一般集団では極めて小さい。
食事と尿酸値のグラフ
紫 尿酸値上げる
黄 尿酸値下げる
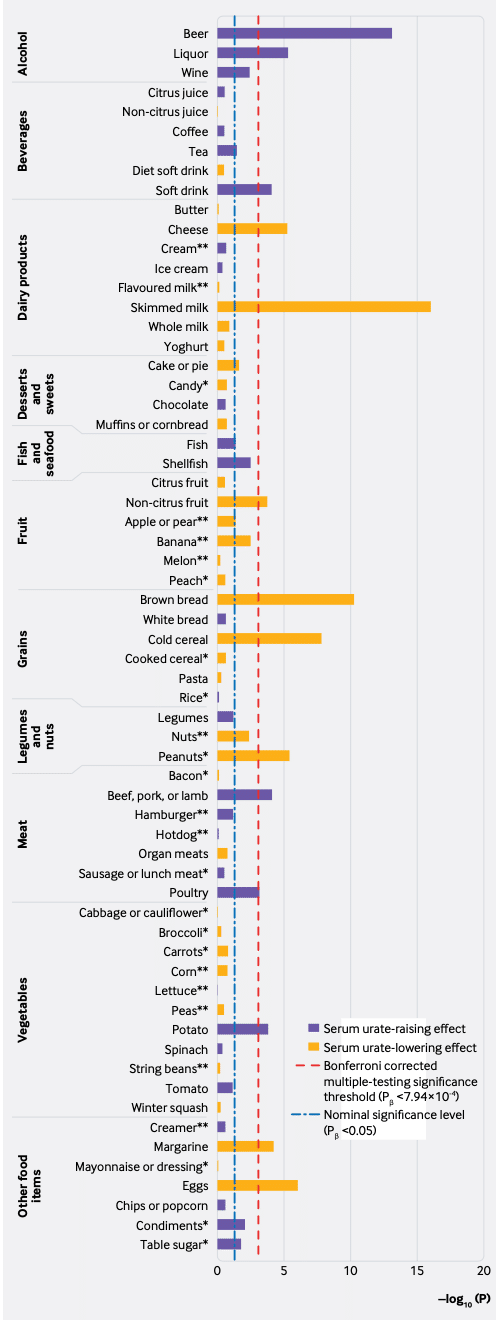
BMJ2018の表
だめ:ビール、酒、ワイン、ジャガイモ、鶏肉、ソフトドリンク、肉(牛肉、豚肉、羊肉)
良い:卵、ピーナッツ、冷シリアル、スキムミルク、チーズ、ブラウンブレッド、マーガリン、柑橘類以外の果物
・果物はいいと思っていたが、まさかの柑橘系を除く。
ぷちパール:果物はいいと思っていたが、まさかの柑橘系を除く。さくらんぼは痛風を減らす?
・サクランボはいいらしい、ってそんなに食べないでしょ!山形にふるさと納税いきますか?
Cherry consumption and decreased risk of recurrent gout attacks, Arthritis Rheum 64(12):4004–4011, 2012.
・なぜ柑橘系を除くのは、本来は掘り下げていかなければならないのだが、調べてみても良く分からなかったので皆さん教えて下さい。プリーズ。
Pearl: 尿酸降下薬の開始時に痛風の再燃は非常に起きやすい
Comment: During the initiation period of ULT, gout flares occur more frequently, particularly if the serum urate is rapidly reduced or if anti-inflammatory prophylaxis is not co-administered. Nevertheless, in the long-term, ULT prevents recurrent gout flares. Some other factors have been associated with reduced risk of recurrent gout flares, including lower serum urate levels and cherry intake.
・これは基本としておさえておかなければならない。尿酸値の変動は痛風発作のリスクになる。
痛風患者における再燃の臨床的危険因子
・痛風発作後、約3分の1の人がその後4年間で少なくとも1回は再燃する。
・再発のリスク因子:血清尿酸値の上昇、急性疾患、外科的疾患、利尿薬の使用、プリン体を多く含む食品やアルコールの摂取、脱水、関節の損傷や酷使、低用量アスピリンの使用、罹病期間の長期化、併存疾患の存在など
・気温が高い時や湿度が極端に高いときもおきやすい。
・それに加えて、尿酸降下薬の開始期に、コルヒチンなどの予防投与がない場合、特に尿酸値が急速に低下すると、痛風の再燃は頻発する。尿酸値の上昇に加えて、急激に下るときも痛風が起きやすい。
Pearl: 痛風をみたらヘルスメンテナンスと心得る!腎臓病、糖尿病、心血管疾患の危険因子を管理すべし。
Comment: In clinical practice, it is important to recognize that people presenting with gout are at high risk for cardio-metabolic conditions and also mortality and to systematically screen and manage risk factors for kidney disease, diabetes, and cardiovascular disease.
Pearl: 大規模痛風患者コホートでは併存疾患別に痛風は5つのクラスターに分類でき、異なる病態生理であることが推測される。
Comment: Cluster analysis of comorbidities in gout allowed us to identify five different clinical phenotypes, which may reflect different pathophysiological processes in gout.
C1(12%):痛風のみ、合併症なし。
C2(17%):肥満。高血圧・脂質異常症も多い。肥満それ自体が痛風と関係している可能性あり。
C3(24%):2型糖尿病。
C4(28%):脂質異常症(コレステロールとTG)。心血管障害、肝障害、腎障害なし、2%しか肥満がない。
C5(18%):心血管疾患、腎不全、利尿薬。多くは二次性痛風の症例、女性が多い。
Revisiting comorbidities in gout: a cluster analysis, Ann Rheum Dis 74(1):142–147, 2015
・5つのクラスターは痛風の異なる病態生理学的過程を反映していると、ってなんのこっちゃ。C5は薬剤性またはCKD合併なのでよく分かります。

・痛風の合併症の割合をまとめました。高血圧と慢性腎臓病が多い。日本語訳の表はchatgptですぐ作れるのでおすすめですが、ズレがないか注意しています。

chatgptといえば、今日筆者愛用の本要約サイトflierも、chatgptを使ってこんな感じで要約作成に使ってみました、みたいなことを言っていて時代だなーって思いました。Netflixよりflier。Netflixは私解約しました。今の御時世、時間泥棒に注意せよ。
Pearl: 痛風の治癒期は皮膚は落屑する
Comment: The overlying skin may desquamate during the resolution phase.
典型的な症状の復習
・母趾(第1MTP)関節炎(2)
・発赤・押すと痛い・痛くて歩けない(3)
・24時間以内にピークが来る急性発症・14日以内に寛解・非発作時は症状がない(3)
・痛風結節がある(4)
・尿酸値が6以上(6-8: 2, 8-10: 3, 10以上: 4点)
・関節液に尿酸結晶あり
・画像で結晶あり(4)・びらんあり(4)
Kelleyの症状のところで書かれているものを改めてまとめてみます。
・痛風は通常、急性の単関節炎として現れるが、小関節炎や多関節炎が起こることもある。
・第1中足趾節関節(podagra)は痛風の初発部位として多く、その他中足部、足関節、膝関節も多い
・発症後24時間以内に最大の痛みが急速に出現し、1~2週間かけて徐々に消失する
・これらのエピソードは夜間に始まることが多い
・炎症の典型的な特徴として、関節の腫脹、熱感、紅斑、運動制限を伴う激しい関節痛がある
・関節は非常に圧痛があり、歩行などの活動は制限される。治癒期には皮膚は落屑する。
Podagraの病態について古い文献を見つけたので貼り付けておきます。
ポダグラはしばしば足の酷使の後に起こり、典型的には夜中に起こる。このような特徴から、結晶は滑液貯留の解消時に形成される可能性がある。水分は尿酸塩の2倍の速さで関節腔から出るため、このような滲出液では尿酸塩濃度が一過性に上昇するはずである。局所濃度が尿酸塩の溶解度を超えると、結晶が形成され、急性関節ポダグラを誘発する。

・2倍の速さってどうやって測ったのだろう。

・高尿酸血症が持続すると、痛風結節(Tophus)や慢性痛風性関節炎が発症する。痛風結節、「透明な皮膚の下に、しばしば血管を伴う、排膿性またはチョーク状の皮下結節として現れ、典型的な部位:関節、耳、肘頭滑液包、指掌、腱(アキレス腱など)に存在する。
・チョーク状、というより豆腐です。触ると柔らかい。
Pearl: 尿酸降下薬がない時代は、豆腐、いや、痛風結節は最初の痛風発作から10年後に発症した。
Comment: Chronic gouty arthritis manifests as nonresolving synovitis, often in patients with tophi. In the pre-ULT era, tophaceous gout typically occurred approximately a decade after presentation of the first gout flare.
・いまは治療薬があるので、何度も痛風があっても痛風結節がない患者も多くいます。
痛風の症状
・80-90%が下肢の急性単関節炎で、「痛くて歩けない」と訴えて来院する。もっとも多いのがMTP関節(50%)、ついでMTP以外の下肢の関節であるリスフラン関節・足首・膝関節(40%)に頻発する。MTP関節炎は90%程度の患者が一度は経験している。 ・手指、手関節、肘などの上肢や、少-多関節炎でもきうるが、この場合は何度も発作を経験している患者がほとんどである。関節周囲の滑液包炎、腱鞘滑膜炎も認めることがある。
・稀に椎体、仙腸関節でも痛風発作はおこる。
・ピークは12時間以内にきて、症状は通常5-14日以内に自然寛解する(J Am Med Assoc 116(6):453–455, 1941.)が、3週間以上続くこともある。
・疼痛、発赤、熱感、腫脹は強く、蜂窩織炎や化膿性関節炎と区別がつかないほどである。
・未治療のケースでは2年以内にほとんどが再発する。
・再発率は62%が1年以内、78%が2年以内、10年以内は93% (Gutman AB. Gout and gouty arthritis. In: Textbook of Medicine, Beeson PB, McDermott W (Eds), Saunders, Philadelphia 1958. p.595.)
Myth: 痛風発作時に尿酸値が6未満であれば痛風ではない
・尿酸値が上がってなくても痛風は除外してはならない。
・なぜなら尿酸値は、痛風の再燃時に最大40%で急性に正常範囲に低下することがあるから。もちろん下がらないこともある。
・関節炎があるときの尿酸値は参考程度にして、むしろ過去のデータや発作後の痛風値を参考にする。
Pearl: 非発作時、症状がないときの関節にも痛風結晶は検出されることがある。
Comment: MSU crystals may also be present in asymptomatic joints of hyperuricemic patients with gout, particularly in joints that have presented with a gout flare.]
Ann Intern Med. 1999 Nov 16;131(10):756-9.
・検出感度は下がるけれども、痛風結晶は検出される。
Pearl: 腎尿酸排泄量の評価は日常的には行われていないが、若年発症や尿酸排泄促進薬の治療検討する場合には行ってもよい。
Comment: Assessment of renal uric acid excretion is not routinely undertaken in clinical practice but may be of value for patients who present with gout at a young age or when uricosuric agents are being considered.
・尿酸分画排泄量(FEUA)はスポット尿から推定できる。
・尿酸クリアランス/クレアチニンクリアランス比([ 尿酸U× クレアチニンP]÷[ クレアチニンU× 尿酸P])
・FEUAが5.5%未満であれば、尿酸の腎排泄不足の可能性が高い

Myth: 超音波のdouble contur sign(DCS)の感度は高い
Reality: In the multicenter SUGAR study, the affected joints were scanned by ultrasound in 824 people presenting with joint swelling. This study showed high specificity for gout for double contour and tophus on ultrasound, compared with MSU crystal identification as the gold standard. 58 In those with early disease (defined as onset of first episode within 2 years), the specificity for double contour sign was 92.3%, but the sensitivity was only 50.9%. High specificity was also observed in those with early disease for ultrasound tophus (95.4%), but the sensitivity was only 33.6%. These findings indicate that, when present, a positive ultrasound feature can provide valuable supportive evidence of gout, including in those with recent onset of disease. Many patients with early disease, however, do not have the characteristic ultrasound findings.
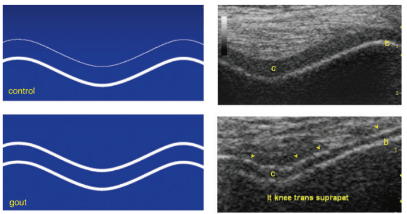
・SUGAR trialの824人データ、ゴールドスタンダードである痛風結晶の同定と比較して、超音波検査でのDCSと痛風結節を評価した
・早期痛風(初回発作2年以内)では、DCSの感度50.9%、特異度は92.3%、痛風結節の感度33.6%、特異度95.4%。
・感度はそこまでだが、特異度は高い。
Pearl: 無症候性高尿酸血症患者の4分の1以上でdouble contur signや痛風結節を認める
Comment: Although more frequent in those with symptomatic disease, some ultrasound features of MSU crystal deposition (including double contour and tophus) are also present in those with asymptomatic hyperuricemia who have no history of gout. These findings can be observed in more than one quarter of people with hyperuricemia
Arthritis Care Res (Hoboken) 63(10):1456–1462, 2011.
・痛風発作のリスクになるかはまだ不明だが、理論的にはリスクになると考えるのが自然。
Myth: Dual Energy CT(DECT)ではほぼ100%痛風結晶は同定できる
Reality: DECTは「濃い」尿酸塩沈着(少なくとも15vol%~20vol%の尿酸塩を含む)を同定できるが、尿酸塩量が少ない沈着は検出できない。

Meta-analysis of DECT studies has shown high sensitivity (87%) and specificity (84%) compared with the gold standard of microscopic MSU crystal confirmation. Sensitivity of DECT in this situation is probably lower, with estimates as low as 50%.
・メタ解析では感度87%、特異度84%だが、おそらく発症早期では感度50%程度と推測されている。
・とはいえ魅力的なツールです。被爆が多く値段が高いが、とにかくすごい自信だ(キン肉マン〜)。
Pearl: MRIで骨びらん、痛風結晶、滑膜炎の評価ができる。痛風結節はT1w画像で中程度の信号強度を示す腫瘤、T2wではより多様である
Pearl: 痛風発作の鑑別のなかでmust rule outは感染症と骨折である
Comment: The differential diagnosis of the gout flare presentation includes other causes of acute monoarthritis, the most important of which is septic arthritis. Other important differential diagnoses are fracture, other acute crystal induced diseases such as “pseudogout” due to calcium pyrophosphate deposition (CPPD) or basic calcium phosphate arthritis or tendinitis, reactive arthritis, and psoriatic arthritis .
・痛風だと思っていたら実は折れていた、ということは実際にある話。病歴を聞けば分かるのだが、一度決めつけてしまったら診断エラーにつながる。system2は無意識にはでてこない、これは先日なく亡くなったダニエル・カーネマン。

・通常はMRIは不要だが、腱断裂、骨髄病変、感染症の合併の評価のときには撮影することもある。骨髄炎の評価にMRIはよい。
AJR Am J Roentgenol 168(2):523–527, 1997.

Myth: リウマトイド結節と慢性多関節炎をみたら、RF陰性、抗CCP抗体陰性でもリウマチである
Reality: In chronic rheumatoid arthritis, seronegative RA is less common than you think, what you think is a rheumatoid nodule may be a gouty nodule, and the seronegative RA you are seeing may be chronic gouty arthritis.
Comment: The differential diagnosis for tophi include other causes of subcutaneous nodules, including rheumatoid nodules, tumoral calcinosis, lipid deposits, or osteophytes
・あなたが見ているのはリウマトイド結節ではないかもしれない。
・痛風結節の重要な鑑別は、リウマトイド結節である。迷ったら結節を穿刺してみるとよい。我々も騙された経験がなきにしもあらず。オーマイゴッド。
関節穿刺
・関節穿刺液による針状の痛風塩結晶がみえたら確定診断となる。ただMTPやリスフラン関節など関節穿刺が難しいことがあり、結晶が証明される痛風はよくて50%程度である(PMID: 25777045)
・関節液の結晶の感度85%以上、特異度100(PMID: 16462524 )
・関節液は細胞数20,000~100,000/mm3で好中球優位である
Pearl: 関節穿刺なしに痛風を診断しよう、というDiagnostic Ruleなるものがある
Comment: A Diagnostic Rule for Acute Gouty Arthritis in Primary Care Without Joint Fluid Analysis
The 2010 Gout Diagnostic Decision Rule、なるものがあります。

7項目評価して
・スコア≦4:痛風の可能性は非常に低い
・スコア>4かつ<8:痛風の診断が不確定(関節穿刺を考慮)
・スコア8以上:痛風の可能性が高い
・痛風は穿刺できないことが多く、多くの場合は臨床診断で治療するのが現実ですからね。参考程度に。
痛風の治療
①患者教育、行動変容
②挙上、冷却(30分冷却を1日4回, 朝昼晩寝る前)
③薬物療法:NSAIDs、コルヒチン、ステロイド注射、プレドニン0.5mg/day。
痛風のマネージメントに関しての推奨比較、Best Pract Res Clin Rheumatolから。このジャーナルはClinical keyで読めるのでおすすめです。以下はそのジャーナルの表から一部抜粋されたkelleyのまとめ。

・治療だけ抜粋するとこんな感じ。

・腎機能が悪いとNSAIDsやコルヒチンは使えないので、ステロイド中心になりますね。
・いずれ予防投与はするので、最初からコルヒチンは少なくとも予防量でいれることがほとんどです。腎機能が許せば。
以下は筆者のまとめ
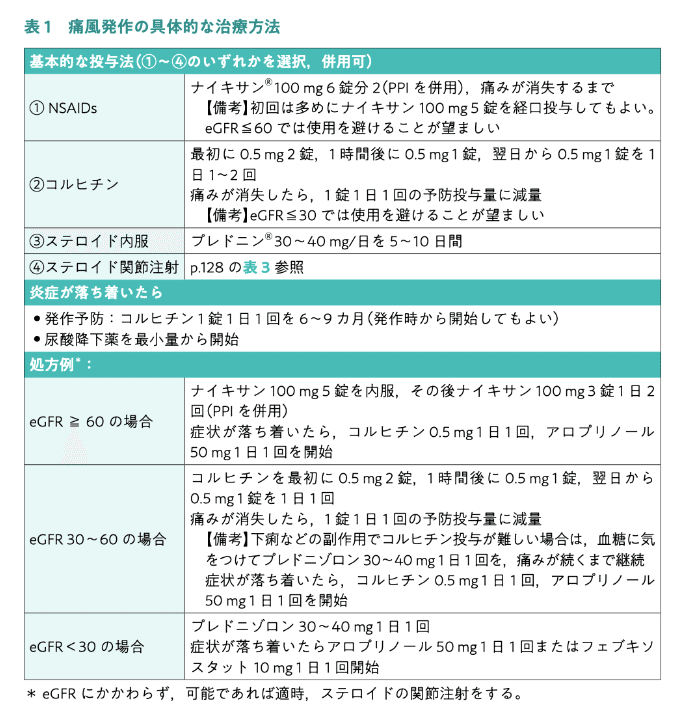

・コルヒチンの容量は多すぎないように注意。
・プレドニンは30mg/日(おおよそハーフ)を炎症おさまるまで、NSAIDsはナプロキセン600mg分2、コルヒチンのみで治療することは私はあまりありませんが、使うなら少量、上の表の通りです。下痢になるコルヒチンが有効なのは治療的診断ができること、だと思います。穿刺はできていないが感染症は心配、という地点では経口ステロイドは使えませんからね。RICEと効果のない?アセトアミノフェンで粘っても患者さんかわいそうですし。
・MTP関節にステロイド注射は打てますが、痛いので必ず患者さんは動きます。臥位にして、効果は高いですが痛いですよと事前に伝え、27Gなどの細い針で、しっかり誰かが足首を固定して注射します。
Pearl: ACTHは効果は高いが、現場ではなかなか使えないこととコスト面であまり使わない
Comment: Adrenocorticotropic hormone (ACTH) acts via melanocortin type 3 receptor to produce anti-inflammatory effects in gout. In hospitalized patients with multiple comorbidities where NSAIDs, colchicine, and corticosteroids are contraindicated, a single dose may be effective. Nevertheless, availability and cost of ACTH can be barriers to the use of this agent in current clinical practice.
・コートロシン注射用0.25mgは1瓶1363円。効くらしいです。
・ACTHを第一選択で治療をしたギリシャの病院での181の後方研究, ACTH as first line treatment for acute gout in 181 hospitalized
・patients, Joint Bone Spine 80(3):291–294, 2013.
ACTH量は:Patients were treated with 1mg (100IU) of synthetic ACTH intramuscularly、つまりコートロシン4瓶、5000円オーバー、たしかに高すぎる。ここでは、ACTHは痛風に効くという事実をそっと胸に刻んでおきましょう。
ぷちパール:非選択的およびシクロオキシゲナーゼ-2(COX-2)選択的なNSAIDsは、痛風フレアの治療に有効であることが証明されている。特定のNSAIDが他のNSAIDよりも痛風のフレア管理に有効であるという明確な証拠はない
Comment: NSAIDs, both nonselective and cyclo-oxygenase-2 (COX-2)-selective, have proven efficacy for treatment of gout flares. There is no clear evidence that any specific NSAID has greater efficacy for gout flare management than the others.
Pearl: 世界のほとんどの国では、高尿酸血症で痛風のない患者には尿酸降下薬は推奨されていない
Comment: In most countries throughout the world, ULT is not recommended for people with hyperuricemia but without gout.
・そのmost countriesに入っていない、実は良くできている日本の2019年改定 高尿酸血症・痛風の治療ガイドライン第3版はこんな感じ。

Myth: 痛風であっても年1回程度であればアロプリノールを開始する必要はない
Rreality: The 2016 EULAR update recommends that “urate-lowering therapy should be considered and discussed with every patient with a definite diagnosis of gout from the first presentation,” and that earlier ULT initiation should be considered in those who present with gout at a young age (<40 years), have very high serum urate levels (above 8 mg/dL, 0.48 mmol/L), or have major comorbid conditions, such as heart failure, coronary artery disease, or kidney disease.
・そんなことはない。2016年EULAR update「痛風と確定診断されたすべての患者に対して、初診時から尿酸降下療法を考慮し、話し合うべきである」となっている。
・EULARの続きとしては、40歳未満の痛風発作、尿酸値8以上、心不全・冠動脈疾患・腎疾患などがある場合は、早期から治療をすべき、となっている。厳密な病歴と診察の後、これをかいくぐって治療を開始しない、となるケースは稀である、といってよい。
・例えば、
P: 尿酸値7以上 & 過去痛風発作1-2回
I: フェブキソスタット
C: Placebo
O: 痛風発作

横軸:全体、0-6ヶ月、6-12ヶ月、12-18ヶ月、18-24ヶ月
Arthritis Rheumatol 69(12):2386–2395, 2017.
・フェブキソスタットにより2年間の痛風発作は優位に減っており、プラセボ群の再発は41%もあった。治療するしないの根拠データのイメージとしてはとても役に立つ。治療をすれば長期的にはかなり発作は抑えられる。
・尿酸値の治療目標は6未満、痛風結節があれば5未満。
・は2nd lineは尿酸排泄促進薬(ベンズブロマロン、プロベネシド、ブコローム、ドチヌラド)。1stのアドオンとして使用する。腎結石と高度腎機能障害で禁忌。ドチヌラド(ユリス)は2020年5月に承認された新規の尿酸排泄促進薬。
Myth: 尿酸降下薬は一生飲み続ける必要がある
Reality: For patients who have achieved complete dissolution of MSU crystals and have had a prolonged asymptomatic period, dose reduction or stopping ULT may be considered.
・痛風結晶が完全に溶解し、無症状期間が長くなった患者では尿酸降下薬の減量または中止を検討できる。
・ 痛風患者211人の前向きコホートにおいて、ベースライン時に痛風結晶がなかった場合は5年後、または痛風結晶が消失した場合は5年後に尿酸降下療法を中止してみた研究がある。
two-stage approach to the treatment of hyperuricemia in gout: the “dirty dish” hypothesis, Arthritis Rheum 63(12):4002–4006, 2011.

・この場合は、尿酸値7未満であれば痛風発作は起きていなかったが、7を超えると再発しているという結果であった。
・痛風結節が消失した、というのを正しく見るのはかなり大変そうだが、それが出来たとしたら尿酸結節がないと判断した地点で5年治療して、その後尿酸値7未満という目標値を少し甘くしても良い、という感じになるのだろうか。
Myth: 痛風発作がおきているときに尿酸降下薬を開始してはいけない
Reality: Traditionally, it has been recommended that ULT be initiated after the gout flares have completed resolved (typically 2 weeks after flare resolution) because of concerns that ULT initiation may worsen or prolong the gout flare. Two small trials have reported that initiation of allopurinol at the time of flare did not prolong the flare duration or worsen pain scores, and the 2012 ACR guidelines recommended that ULT could be started during a gout flare, provided effective anti-inflammatory prophylaxis was also prescribed. The EULAR taskforce did not provide guidance on this issue.
・Traditionally、尿酸降下薬の開始は痛風発作を悪化させる懸念があったため、再燃が治まってから2週間後に開始することが推奨されてきた。
・ただ、2つの小規模試験、再発時にアロプリノールを開始しても問題なかったという報告がされて
Am J Med 125(11):1126–11234 e7, 2012., J Clin Rheumatol 21(3):120–125, 2015
2012年のACRガイドラインでは炎症を抑える治療をしているのであれば痛風発作中に尿酸降下薬を開始してもよいと、としている。ちなみに。EULARではこれらの問題に関しての言及はない。
さて、いよいよ、アロプリノールとフェブキソスタット問題
Myth: フェブキソスタットはアロプリノールと比べて心血管系イベントを増やすので、控えるべきである
・議論のあるところだが現地では心血管系の死亡リスクがあるという根拠はない可能性が高い、といってよい。
ことの経過を短くまとめると
①2018年CARES trialで、フェブキソスタットを投与された患者では、アロプリノールと比較して、全死因死亡率および心血管系死亡率のリスクが高かったことが報告された
②FAST trialでは両者の安全性は非劣性と2020年lancetにでてきた。
③2021年にCARES trialに登録されている患者の追跡調査で、心血管死亡率の優位差はなくなった、ということが判明し、改めてフェブキソスタットの安全性が主張された。
Comment: Febuxostat use is not associated with increased risks of all-cause mortality, death from CVD, or CVD events. Accordingly, it is a safe drug for the treatment of gout. J Rheumatol. 2021 Jul;48(7):1082-1089.
Myth: 慢性腎臓病の患者にはアロプリノールは使用できない
Reality: Once allopurinol has been tolerated at low dose, however, the dose can be safely increased until the serum urate target is achieved. This approach is effective in achieving serum urate target in the majority of patients and is well tolerated.
・腎機能が悪い患者へのアロプリノールは Allopurinol Hypersensitivity Syndrome(AHS)と関連しているという観察研究から、腎機能に応じてアロプリノールの容量を制限すべきという推奨がなされた。Am J Med 76:47–56, 1984.
・これにより当然だが、尿酸値のコントロールは不十分になった。
・その後の研究でアロプリノールの開始用量がAHSと関連していることががわかり、アロプリノールが低用量で問題なければその後増量していけることができることが判明した。最初がもんだいなければ忍容性は良好である。Ann Rheum Dis 76(9):1522–1528, 2017.
アロプリノールの処方例:
eGFR 60以上: アロプリノール100mgから開始、毎月100mgずつ増量
eGFR 60未満: アロプリノール50mgから開始、毎月50mgずつ増量
※皮疹がでたらすぐにやめるように伝えること。これはバクタやアザチオプリンなど薬疹が多い薬を処方するときと同様。
以上です、お付き合い感謝します!
この記事が気に入ったらサポートをしてみませんか?
