COPD急性増悪:血液好酸球数による全身性グルココルチコイド使用 vs 非選別ステロイド使用
COPDの急性増悪時の血液好酸球指向プレドニゾロン療法は、標準治療に非劣性であり、臨床実践において全身性グルココルチコイドの使用を安全に減らすことができる
無作為化の時点で、ポイントオブケアの血液好酸球数が高い(≥2%)場合、BET群の参加者はオランダのオウド=ベイエルランドにあるTiofarma BV製の経口プレドニゾロン30mgを1日1回服用しました。一方、血液好酸球数が低い(<2%)場合は、代わりにマッチしたプラセボを服用しました。ST群の参加者は、ポイントオブケアの血液好酸球数に関係なく、経口プレドニゾロン30mgを1日1回服用しました。すべての参加者は、プロトコル開発時の国の指針に従い、調査薬(プレドニゾロンまたはマッチしたプラセボ)を14日間毎日1回服用しました。
2週間・30mg/dと、比較的長く高用量のステロイド投薬
Ramakrishnan, Sanjay, Helen Jeffers, Beverly Langford-Wiley, Joanne Davies, Samantha J Thulborn, Mahdi Mahdi, Christine A’Court, ほか. 「Blood eosinophil-guided oral prednisolone for COPD exacerbations in primary care in the UK (STARR2): a non-inferiority, multicentre, double- blind, placebo-controlled, randomised controlled trial」. The Lancet. Respiratory medicine, 2023年11月1日, S2213-2600(23)00298-9. https://doi.org/10.1016/S2213-2600(23)00298-9 .
背景
慢性閉塞性肺疾患(COPD)の急性増悪において、全身性グルココルチコイドの使用が推奨されていますが、その使用には増加したリスクが伴います。我々は、COPDの急性増悪時に好酸球バイオマーカー指向の経口プレドニゾロン療法を使用することが、プレドニゾロンの使用を減らしつつ有害な結果に影響を与えないことを仮説としました。
方法
急性増悪と反応研究(STARR2)は、英国の14の一次ケア施設で行われた多施設、無作為化、二重盲検、プラセボ対照試験でした。我々は、成人(40歳以上)で、現在または過去の喫煙者(少なくとも10パック年の喫煙歴がある)で、一次ケア医師によって以前に記録された気管支拡張薬後のFEV1/強制肺活量比が0.7未満のCOPD診断を受け、過去12ヶ月間に少なくとも1回の全身性コルチコステロイド(抗生物質の使用の有無にかかわらず)を必要とする増悪の歴史がある患者を対象としました。すべての研究スタッフと参加者は、研究グループの割り当てと治療の割り当てについて盲検されていました。参加者は無作為に割り当てられ(1:1)、好酸球数が高い場合(≥2%)は経口プレドニゾロン30mgを1日1回、好酸球数が低い場合(<2%)はプラセボを受ける血液好酸球指向治療(BET)または、好酸球の結果に関係なくプレドニゾロン30mgを1日1回受ける標準治療(ST)に割り当てられました。治療は14日間処方され、すべての患者は抗生物質も受けました。主要なアウトカムは、増悪後30日での治療失敗率で、これは抗生物質またはステロイドの再治療、いかなる原因による入院、または死亡の必要性として定義され、修正された意図を持つ治療集団で評価されました。参加者はさらなる増悪時に再無作為化の対象となり、参加者1人あたり最大4回の増悪が可能でした。安全性分析は、無作為に割り当てられたすべての参加者に対して行われました。優越性試験として設計されたものの、データロック前に無作為化コードの誤りが特定された後、試験は非劣性を示すものに変更されました。95%CIの上限値1.105が非劣性の限界として定義されました。この研究はEudraCTに登録されており、2017-001586-24で完了しています。
結果
2017年11月6日から2020年4月30日の間に、14の一般診療所から308人の参加者が募集されました。93人の参加者(平均年齢70歳[範囲46-84]、平均予測FEV1 60.9%[SD 19.4]、52人[56%]が男性、41人[44%]が女性、民族データは収集されませんでした)から144回の増悪(BET群73回、ST群71回)が修正された意図を持つ治療集団分析に含まれました。
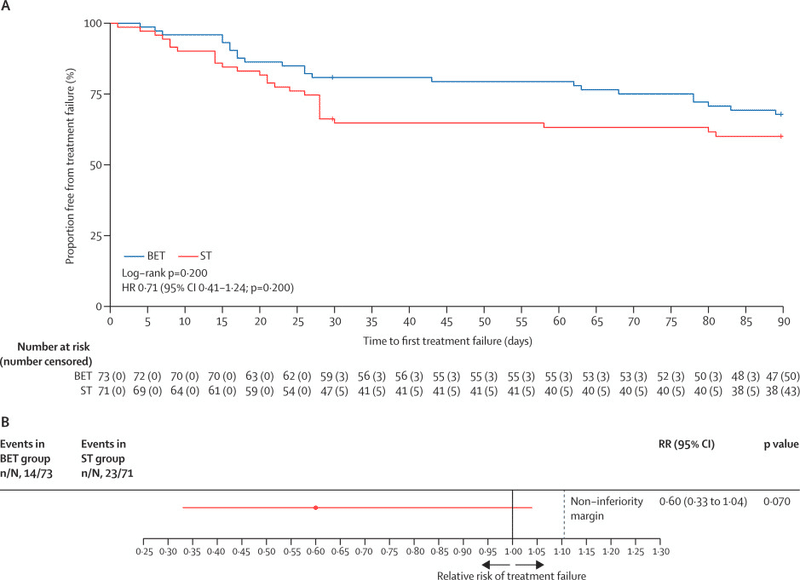
BET群では14件(19%)、ST群では23件(32%)の治療失敗が増悪後30日で発生しました。
COPD増悪後の治療失敗を減らすためのBETとST間の大きな非有意な推定効果が見られました(RR 0.60 [95%CI 0.33-1.04]; p=0.070)。
非劣性分析は、BETがSTに非劣性であることを支持しました。
両研究群間で有害事象の頻度は同様で、糖尿(BET群2/102 [2%]、ST群1/101 [1%])とCOPD増悪による入院(BET群2/102 [2%]、ST群1/101 [1%])が両群で最も一般的な有害事象でした。研究中に死亡は発生しませんでした。
解釈
COPDの急性増悪時の血液好酸球指向プレドニゾロン療法は、標準治療に非劣性であり、臨床実践において全身性グルココルチコイドの使用を安全に減らすことができます。
資金提供
国立健康およびケア研究所。National Institute for Health and Care Research.

COPD Exacerbations: BET With Prednisolone Noninferior to ST (medscape.com)
日本語訳:written with ChatGPT4
トップライン:
血液好酸球指向治療(BET)と標準治療(ST)は、慢性閉塞性肺疾患(COPD)の急性増悪後の治療失敗を同様に減少させました。
方法論:
研究者たちは、平均年齢70歳の152人の成人を、好酸球数が2%未満の場合はBETまたはプラセボ、または基準好酸球数に関係なく標準治療に無作為に割り当てました。最終的に分析可能な集団には、血液好酸球群の47人と一次ケア群の46人が含まれ、それぞれ73回と71回の増悪がありました。
参加者は増悪後の基準時点、14日目、30日目、90日目に評価されました。主要なアウトカムは、増悪後30日の治療失敗率で、これは抗生物質またはステロイドの再治療、入院、または死亡のいずれかの必要性として定義されました。副次的アウトカムには、健康関連の生活の質、1秒間の強制呼気量、視覚アナログスコア呼吸症状が含まれます。
参加者は2017年11月6日から2020年4月30日の間に14の一般診療所から募集されました。この研究は、COVID-19パンデミックのため、2023年4月30日に終了しました。
結論:
BETは非劣性解析においてSTに非劣性でした。
増悪後30日時点で、BET群で14件、ST群で23件の治療失敗が発生しました。相対リスクは0.60(P = .070)でした。
両群間で有害事象の頻度は同様でした。最も一般的な有害事象は糖尿とCOPD増悪による入院で、両イベントタイプともBET群で2%、ST群で1%でした。研究期間中に死亡は発生しませんでした。
サブグループ分析では、プレドニゾロンを受けた高好酸球数の患者に両群で最大の利益があることが示されました。
実践において:
「プラセボまたはプレドニゾロンが処方されたかに関わらず、好酸球数が低い増悪において、肺機能、生活の質、症状の改善が見られた」と著者は議論で述べています。
この記事が気に入ったらサポートをしてみませんか?
