「治験が終わっていない」は誤り
[2023/9/24更新]
「治験が終わっていない」は誤り。治験とは承認の為の臨床試験なので承認時点で終了。国内第Ⅰ/Ⅱ相と国際共同第Ⅰ/Ⅱ/Ⅲ相で特例承認の審査完了し、現在は第Ⅳ相(製造販売後試験)中。米国はEUA後も第Ⅲ相を継続中だったが、2021/8/23に正式承認された。
【解説】
Pfizer製ワクチン「コミナティ筋注」は薬機法第14条3により特例承認されている。本承認の治験には以下の2つがある。
①海外C4591001(第Ⅰ/Ⅱ/Ⅲ相)
②国内C4591005(第Ⅰ/Ⅱ相)
治験とは「治療承認のための臨床試験」の略で、法的には特例承認が下りた時点で治験も終了している(因みに承認後の臨床試験提出は特例承認であっても認められない)。特例承認審議結果報告書によれば、②は「承認後に製造販売後試験に切替えて長期の安全性を検討する」と記され、①は「海外の情報を収集し安全性を継続的に評価する」と記されているように、第Ⅳ相臨床試験(製造販売後試験)を残すのみである。
◾️BBC: Pfizer製ワクチンFDA正式承認
https://www.bbc.com/japanese/58314498
◾️FDA: Pfizer製ワクチン正式承認
https://www.fda.gov/news-events/press-announcements/fda-approves-first-covid-19-vaccine
◾️Pfizer: FDA正式承認のプレスリリース
https://www.pfizer.com/news/press-release/press-release-detail/pfizer-biontech-covid-19-vaccine-comirnatyr-receives-full
◾️FDA: モデルナ製ワクチン正式承認
https://www.fda.gov/news-events/press-announcements/coronavirus-covid-19-update-fda-takes-key-action-approving-second-covid-19-vaccine
◾️Moderna: FDA正式承認のプレスリリース
https://investors.modernatx.com/news/news-details/2022/Moderna-Receives-Full-U.S.-FDA-Approval-for-COVID-19-Vaccine-Spikevax/default.aspx
◾️日本: 特例承認に係る審議結果報告書
https://www.mhlw.go.jp/content/10601000/000739089.pdf
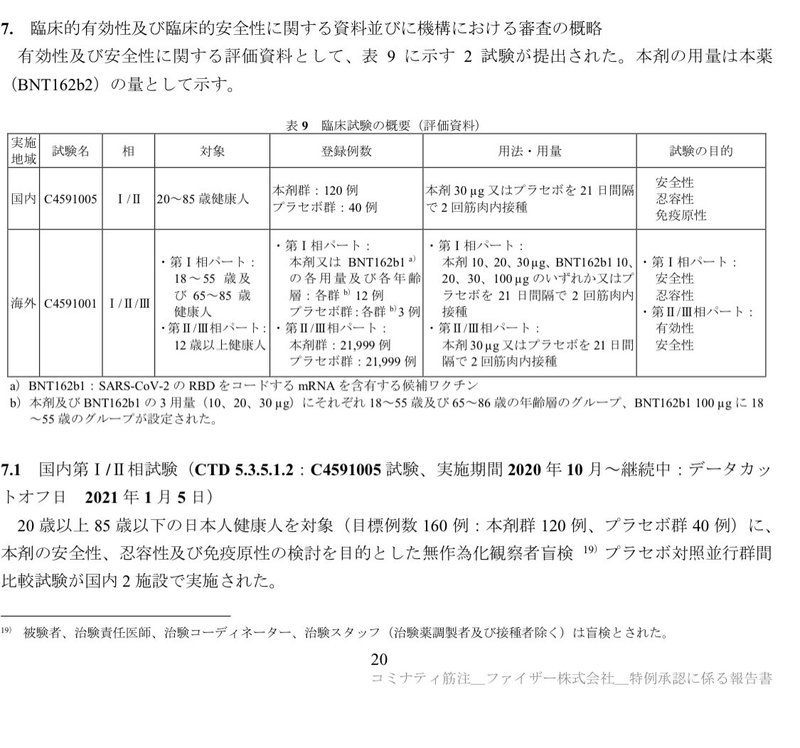

①が2023年まで継続中とあるので「実質的には治験は終わっていないのでは」と懸念する声もあるが、現在継続中の内容は、②では、JRCTに製造販売後臨床試験として登録された「最終接種12ヵ月後のSAE」のみ、①では、長期安全性モニタリングのみ。「治験」とは日本だけの呼称で、米国では第Ⅲ相も第Ⅳ相も同じ”Clinical Trials(臨床試験)”と呼称する。日本の第Ⅳ相試験(製造販売後試験)に相当するものが2023年まで続くということで、これは治験ではない。
◾️JRCT C4591005
https://jrct.niph.go.jp/latest-detail/jRCT2071200045
◾️臨床研究情報ポータル C4591005
https://rctportal.niph.go.jp/detail/jr?trial_id=jRCT2071200045
◾️国際共同試験 C4591001
https://www.nejm.org/doi/full/10.1056/NEJMoa2034577
◾️海外C4591001試験 NCT04368728
https://clinicaltrials.gov/ct2/show/NCT04368728
◾️Pfizer第Ⅲ相試験の解析結果発表
https://www.pfizer.co.jp/pfizer/company/press/2021/2021_04_05_02.html

第Ⅳ相臨床試験(製造販売後試験)で今後注視すべきことは、適正使用ガイド「リスク管理計画における重要な特定されたリスク」に記されている。
◾️コミナティ筋注 適正使用ガイド
https://www.med.or.jp/dl-med/kansen/novel_corona/sokuho/comirnaty_guide.pdf

FDA承認はBLA(生物製剤申請)の承認だから、まだ今もEUA(緊急使用許可)のままで、製剤(製造)が承認されただけだとする意見があるが、これは和訳の意味を取り違えた間違い。
◾️BLA(生物製剤承認申請)
FDA承認は種別に以下3つの何れかで承認される。
・BLA
・NDA
・ANDA
ワクチンはBLAで承認される。
BLA (Biologic License Application)の和訳は「生物製剤承認申請」だが、これは「製剤(製造)」を許可したという意味ではない。「Biologic(生物製剤)」という薬を承認したという意味である。
以下は用語解説。
◾️治験
薬機法第2条17項に基づき、医薬品もしくは医療機器の製造販売に関して、医薬品医療機器等法上の承認を得るために行われる臨床試験のこと。誰Ⅰ〜Ⅲ相までを治験と言い、第Ⅳ相は治験ではなく製造販売後試験と言います。

◾️特例承認
薬機法第14条の3第1項に基づき、1. 疾病のまん延防止等のために緊急の使用が必要、2. 当該医薬品の使用以外に適切な方法がない、3. 海外で販売等が認められている、という要件を満たす医薬品について、承認申請資料のうち臨床試験以外のものを承認後の提出としても良い等として、特例的な承認をする制度。
◾️薬機法
https://elaws.e-gov.go.jp/document?lawid=335AC0000000145
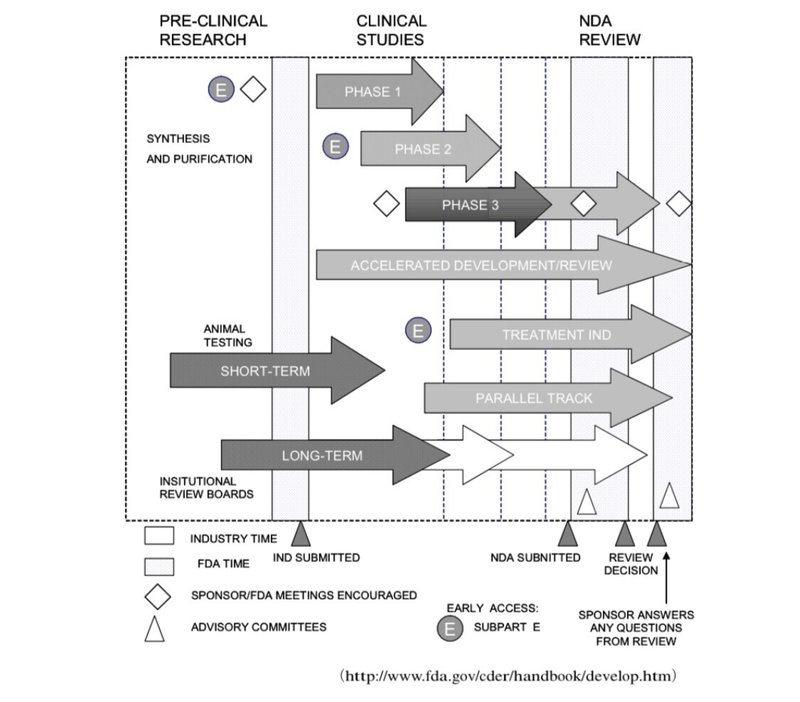
◾️海外ClinicalTrial(臨床試験)プロセス
海外では治験も臨床試験も同じClinical Trialsと称します。フォローまで入れたら第Ⅲ相臨床試験が完全に終了するのは数年後になり、その前に承認されるのが一般的である。
◾️製造販売後試験の実施基準
http://www.it-asso.com/gxp/regulations/gpsp-syourei.htm

◾️薬事承認
https://japanknowledge.com/contents/nipponica/sample_koumoku.html?entryid=1690
以下の記事でも詳しく解説されています。
◾️ほえのブログ
「ワクチンは治験が終わってないから危険」の嘘
https://www.hoe2021.com/?p=151https://www.hoe2021.com/?p=151
【追記】
ワクチンの有効性・安全性については自己でご判断ください。当方は、皆さんが正しい情報を基に判断できるよう、デマの指摘に努めます。
