ストークスシフト〜なぜ吸収波長と発光波長は異なるのか?〜
お久しぶりです、のうむです。
半年以上ぶりの更新になってしまいました•••。
プライベートで多忙なこともあり、更新できていませんでしたが、今後も不定期で何かしらの記事が書けたらと思っています。
さて、今回はストークスシフトについてお話しします。
内容としては少し高度な内容ですので、光化学をある程度知っている方、これから大学等で光化学の研究を行う人向けになると思います。
そもそも光の吸収と発光とは?
化学(とりわけ光化学)に触れている人間からすれば説明不要だと思いますが、光の吸収と発光とは何でしょう?
光の波長とエネルギーの関係
今回のお話では光の波長とエネルギーの関係についてを知っている前提でお話しします。
よくわからない人は下記の記事にて解説しておりますので、こちらをご参照ください。
光の吸収
物質は特有の波長の光を吸収します。
物体に色がついて見えるのはこの光の吸収が関係しています。
基本的には吸収されなかった色の光が反射されることで、人間の目にはその色が見えます。
(構造色など例外はありますが、、、)

発光
スマートフォンやテレビ、照明など身の回りには光を発するものがたくさんあります。
これらの光は物質の発光現象を利用しています。
吸収同様、物質により特有の光は発します。
発光する光が可視光の場合、人間の目で識別できます。
また、光は物質によって特有の色のみを出すため、光の三原色を組み合わせることで、さまざまな色を作ることができます。
ここ数年でよく耳にする有機ELは有機材料でできた発光物質です。
また、近年は有機ELの次世代発光材料として量子ドットなどもあります。
有機化合物の吸収・発光
既に述べていますが、有機化合物は特有の波長の光を吸収、発光します。
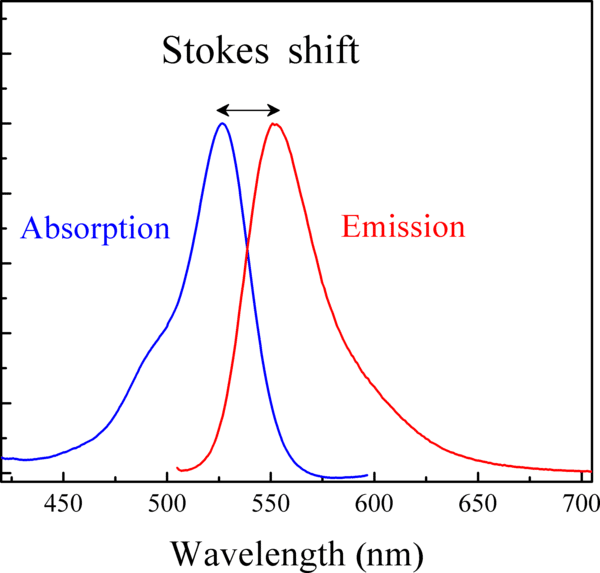
どの有機化合物も例外なく吸収波長より発光波長の方が長波長化(低エネルギー化)します。
この差のことをストークスシフトと言います。
吸収波長は何で決まるのか?
では、有機化合物の吸収波長は何によって決まるのでしょうか?
その答えはHOMOとLUMOのエネルギーギャップです。
有機化合物に光を照射すると、HOMOとLUMOのエネルギー差に相当する波長の光を照射することで、HOMOの電子がLUMOへ励起します。
ずれた波長でも励起はできますが、ドンピシャのエネルギー差を持つ波長だと励起しやすいので、その波長の光が最も吸収されます。
これは吸収波長です。

発光波長は何で決まるのか?
では発光はどのように決まるのでしょうか?
実はこちらもHOMOとLUMOのエネルギーギャップです。
光吸収などで励起した後、電子がLUMOからHOMOに戻る際、エネルギーを放出します。
このエネルギー放出を光で行われると発光となります。

ここで生まれる疑問
さて、吸収波長と発光波長の決まり方を説明しましたが、どちらもHOMO–LUMO gapであることをお話ししました。
でもこれだと2つの波長は同じになるのではないか?
ストークスシフトなんて生じないのでは?
となると思います。
実はこれにはカラクリがあります。
それはスピン多重度です。
スピン多重度を考える
スピン多重度とは?
スピン多重度については過去に解説していますのでこちらの記事をご参考ください。
吸収過程のスピン多重度
光を吸収する前のスピン多重度について考えてみましょう。
これはすなわち基底状態ですので、HOMO以下のエネルギー準位に2電子ずつ入っています。
そのため、スピン多重度はS0になります。

つまり光の吸収は、S0のHOMOから始まります。
発光過程のスピン多重度
一方で、発光過程は起こる前の状態を見てみましょう。
発光は、光を吸収して励起状態でないと起こりません。
ここでは一番単純な励起状態を考えると、スピン多重度はS1になります。

従って、発光過程はS1のLUMOから始まります。
電子遷移は垂直遷移で起こる
S0とS1のエネルギー準位はどうなっているのか?
吸収と発光のスタートする状態がS0とS1が異なるため、エネルギー状態を考えてみましょう。

このように、S1に励起することで、エネルギー準位が高くなるだけでなく、座標もずれます。
エネルギー準位が高くなるのは光の吸収などでエネルギーを吸収しているのでその分増加します。
座標がずれる理由ですが、エネルギーを吸収した状態では分子(化合物)の安定な状態が変わるためです。
例えるなら、荷物を持っている時と持っていない時で安定する姿勢がわかるようなイメージです。

吸収と発光を考える
このエネルギー準位で吸収と発光を考えてみましょう。
光の励起や発光は一瞬にして生じます。
光はどんな物質よりも速く移動しますからです。
そのため、光の吸収や発光が生じる際、座標は変化しないので、垂直方向に遷移が生じます。
光の吸収を書き込むと次のようになります。
基底状態(S0)の中でも通常は最もエネルギーが安定な状態(エネルギー準位が低い状態)にいるため、この位置から光の吸収を図示できます。

一方、発光過程はこの吸収後にすぐに起こるのではなく、S1の最もエネルギー準位の低い位置まで変化してから起こります。
この過程を振動緩和といい、熱によってエネルギーを若干放出します。

その後、S1の安定状態から発光が起こります。
こちらも吸収同様に垂直遷移が起こります。

この矢印の大きさが吸収する光と発光する光のエネルギー、即ち波長に相当します。
つまり、矢印の大きさ=エネルギーは吸収>発光となるため、波長は吸収<発光となり、異なる波長となることからストークスシフトが生じることになります。
ストークスシフトは予想できる
このような理由からストークスシフトが生じます。
この理屈さえわかっていれば、なぜ化合物によってストークスシフトが違うのかも説明できます。
単純に基底状態S0と励起状態S1の安定構造に起因するので、計算科学的手法を使えば、吸収波長と発光波長を予測できます。
(吸収はS0、発光はS1の構造を計算すれば予測できます)
まとめ
大雑把ではありますがこれがストークスシフトのメカニズムです。
各部分の詳細な解説を入れてしまうと記事が長くなってしまうので割愛していますが、ご了承ください。
(コメントいただければ答えられる範囲でお答えします。。。)
次回更新がいつになるかわかりませんが、今後もよろしくお願いします。
それでは、また。
この記事が気に入ったらサポートをしてみませんか?
