
食物アレルギーと腸内細菌叢
本文へスキップ記事へスキップ
エルゼビアロゴ
食品科学技術の動向
140巻 10月 2023, 104141
食物アレルギーと腸内細菌叢
著者リンク オーバーレイパネルを開くJiachen Liang a b, Baodong Zheng a b c, Yi Zhang a b c, Hongliang Zeng a b c
もっと見る
共有
引用
https://doi.org/10.1016/j.tifs.2023.104141
権利と内容の取得
概要
背景
食物アレルギー(FA)は、食物アレルゲンによって引き起こされる過敏状態を反映している。世界の小児の約10%、成人の約4%が食物アレルギーを経験していることから、この病態は腸内細菌叢が明確な役割を担っており、非常に一般的である。さまざまな腸内細菌叢の発酵産物に由来する可能性があるFAsは、腸内細菌叢やポストバイオティクスを介した食事によって調節される。
範囲とアプローチ
本稿では、FAsにおける免疫グロブリンEのメカニズム、腸内微生物の構造、FAsを緩和する微生物叢のメカニズム、およびFAsを緩和する食事成分の推定メカニズムについて系統的に概説した。
主な所見と結論
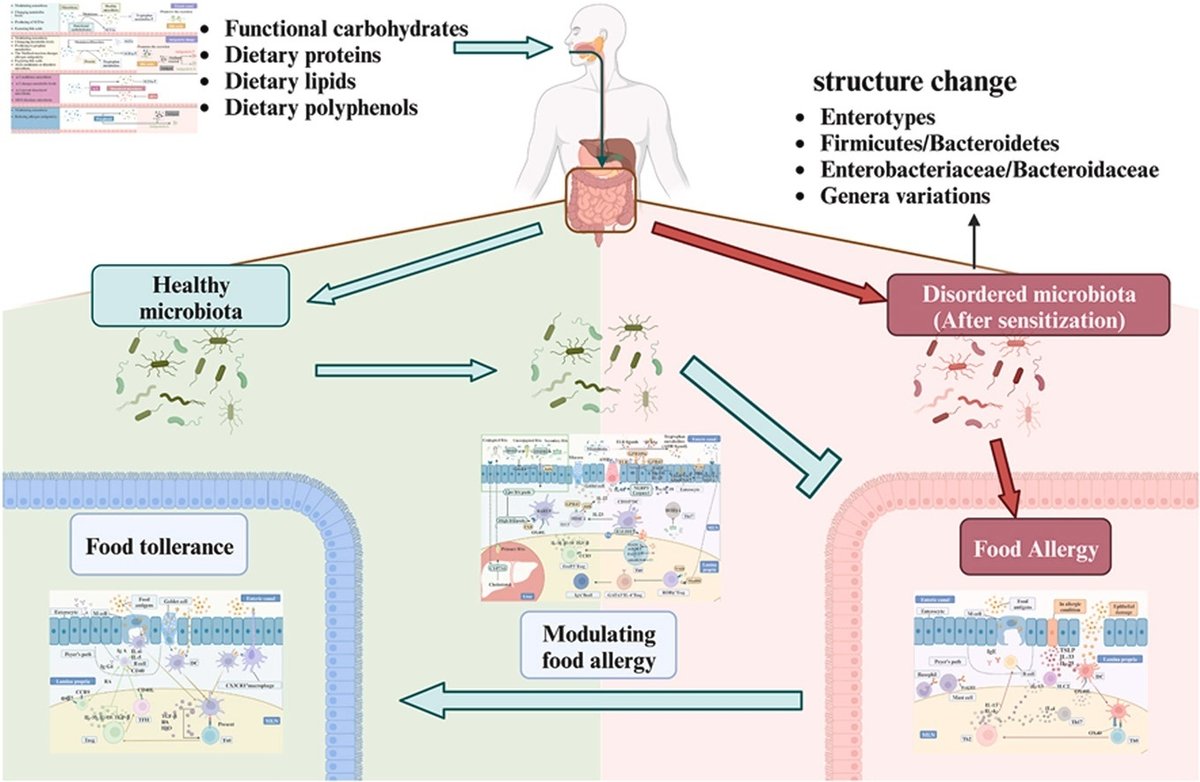
ヘルパーT細胞(Th)1/Th2および制御性T細胞/Th17のアンバランスがFAを引き起こし、腸型、ファーミキューテス/バクテロイデーテス、腸内細菌科/バクテロイデーテス科の比率、およびその他の属はFA後に変化する。さらに、微生物叢は、直接アクセス、胆汁酸(BA)プール維持、ポストバイオティクス生成の3つの方法でFAsを緩和する。(1)短鎖脂肪酸(SCFA)として代謝される機能性炭水化物によってFAsは緩和され、微生物叢と代謝産物を調節し、toll様受容体4(TLR4)と相互作用し、BAの排泄を促進する。(2)FAsは、トリプトファン代謝産物を生成し、微生物叢と代謝産物を調節し、BA排泄を促進する抗タンパク質を生成する食事タンパク質によって緩和され、FAsは、アレルゲン感作と微生物叢の変化を介してメイラード反応後のタンパク質によって二重に変化する。(3)FAは高脂肪食(HFD)によって誘導され、omega3/6比によって緩和される。(4)FAsは、微生物叢の調整、腸管バリアの強化、アレルゲン感作の減少、免疫細胞の制御から、食事ポリフェノールによって緩和される。本総説では、FAsの予防と緩和において、個人に合わせた正確な食事設計のための科学的根拠を提供する。
図解抄録
画像1
ダウンロード 高解像度画像ダウンロード(311KB)
ダウンロード フルサイズ画像のダウンロード
はじめに
近年、衛生環境の改善や食習慣の変化に伴い、食物アレルギー(FA)は大幅に増加しており、世界の小児人口および成人人口のそれぞれ約10%および約4%が罹患している(Sicherer & Sampson, 2018)。FAの有病率は発展途上国でも徐々に増加しており、遺伝では説明できない。現代のライフスタイルの変化により、共生腸内微生物も同様に変化している。Strachan(1989)による衛生仮説では、FAにおける微生物の重要な役割が仮定され、集団におけるFAと腸内細菌叢の異常との関連が確認され、無菌、広域抗生物質投与、FA関連マウスモデルにおける微生物叢とFAとの因果関係が決定された(Wangら、2021)。
効率的なFA治療法がないため、アレルギーの可能性のある食品を避け、適切な治療法をとるしかない(Sicherer & Sampson, 2018)。しかし、腸内細菌叢とFAの因果関係から、FAが腸内細菌叢によってどのように制御されているかが示されている。食事組成も腸内細菌叢に影響を与える重要な因子である。プレバイオティクスの食事からの摂取は、特定の細菌の存在量を増加させ、腸内微生物を有意に制御し、それによって群集組成を変化させるだけでなく、短鎖脂肪酸(SCFAs)、トリプトファン代謝産物、胆汁酸(BAs)代謝産物、その他のポストバイオティクスなど、さまざまな代謝産物を介してFAsに影響を与える発酵基質としても作用する。このように、FAsは食事によって腸内細菌叢を調節することによって改善される可能性がある。この目的のため、我々は、FAs、微生物叢、食事調節、FAメカニズム、さまざまなFA動物モデルにおける腸内細菌叢構造の関係、および微生物叢がFAsに直接的または間接的にどのように影響するかに焦点を当てた。免疫学的な「食事調節-腸内細菌叢-FA」軸を構築し、食事成分が微生物叢を調節することによってFAをどのように緩和するかを検討した。我々の知見は、FAsを予防し、個別化された正確な食事設計を改善するための科学的根拠を提供する。
セクションの抜粋
FAsについて
FAsは、免疫グロブリン(Ig)E介在性、非IgE介在性、またはIgE-および非IgE共介在性のメカニズムに関与するが、その中でもIgE介在性メカニズムが主要なタイプである。IgE介在性アレルギー反応は、アレルゲン摂取後に急速に反応し、強い不快感を引き起こし、数分から数時間以内に皮膚(蕁麻疹)、呼吸器(喘鳴、咳)、消化管(吐き気、嘔吐、下痢)の症状を誘発する(Tordesillas et al.)
FA後の腸内細菌叢
FAのリスク因子は数多く存在し、性別、人種、遺伝、アトピー性疾患、衛生状態、ビタミンDの欠乏、食事脂肪量、抗酸化物質の摂取減少、制酸剤の使用増加、肥満、食物曝露期間、食物曝露経路、腸内細菌叢などが挙げられる(Sicherer & Sampson, 2018)。近年、さまざまな集団におけるFAsと腸内細菌叢の関係が報告されており、FAsと腸内細菌叢の因果関係が動物モデルで検証されている(
腸内細菌叢とFAs
ポストバイオティクスとは、「宿主に健康上の利益をもたらす無生物微生物および/またはその成分の製剤」のことである(Salminenら、2021年)。腸内細菌叢を介したFA制御に関するかなりの研究が、ポストバイオティクスが重要な役割を果たすことを示している。FAsは腸内細菌叢によって、腸管バリアとの直接的な接触を通じてだけでなく、SCFAs、トリプトファン代謝産物、二次および一次BAsを含むポストバイオジェニック代謝を通じて間接的に制御されている。以下はその一例である。
機能性炭水化物
機能性炭水化物には主に食物繊維、機能性単糖、機能性オリゴ糖、活性多糖が含まれ、これらはヒトの健康と密接に関連し、主に腸内細菌叢を介してFAsに対抗する。食事成分がFAsにどのような影響を与えるかを図4に示す。
さまざまな多糖類やオリゴ糖は、アレルゲン特異的IgE抗体産生を低下させたり、エフェクター細胞(例えばマスト細胞)の活性化やTh2サイトカインをダウンレギュレートすることにより、アレルギー症状を抑制する。
結論
Th2/Th1比およびTh17/Th1比の不均衡がFAを引き起こす。腸内細菌型、F/B比、E/B比、および特定の属はすべて、感作後に変化する。腸内細菌叢はIECと相互作用し、腸管バリアを維持するためにIL-22産生を誘導する。FA食餌成分の緩和作用は以下の通りである: (1) FAは、SCFAとして代謝され、微生物叢と代謝産物を調節し、TLR4の発現を誘導し、BAの排泄を促進する機能性炭水化物によって緩和される。(2)FAsの緩和
CRediT著者貢献声明
Jiachen Liang:調査、形式分析、原稿執筆、ソフトウェア。Baodong Zheng: 調査、資金獲得。Yi Zhang: ビジュアライゼーション、執筆、レビュー、編集。Hongliang Zeng:プロジェクト管理、監督、執筆・査読・編集、資金提供、資金獲得。
利益申告
著者らは、本論文で報告された研究に影響を及ぼすと思われる競合する金銭的利益や個人的関係がないことを宣言する。
著者らは、潜在的な競合利益と考えられる以下の金銭的利益/個人的関係を宣言する。
利益相反宣言
著者らは利益相反がないことを宣言する。
謝辞
本研究は、福建省大学先導人材育成プログラム(助成金番号660160190)および福建省「ヤングイーグルプラン」第3期青少年トップ人材育成プログラム(助成金番号118362308)の助成を受けた。
参考文献 (102)
B. Cassani et al.
インテグリンα4β7およびCCR9を発現する腸管向性T細胞は、マウスにおける経口免疫寛容の誘導に必要である。
消化器病学
(2011)
R.S. Chinthrajahら.
食物アレルギーおよび食物耐性の分子および細胞機構
アレルギーと臨床免疫学ジャーナル
(2016)
M. コロンナ
自然リンパ球: 多様性、可塑性、免疫におけるユニークな機能
免疫学
(2018)
J.J.ドレンスほか
気道曝露はマウスのIL-1経路とT濾胞ヘルパー細胞の関与によってピーナッツアレルギーを開始する
アレルギーと臨床免疫学ジャーナル
(2018)
P. Dong et al.
早期の腸内細菌叢と牛乳アレルギー-前向き症例-対照6ヶ月追跡研究
サウジアラビア生物科学ジャーナル
(2018)
L.L.フーほか
ヨーグルト由来のプロバイオティクス細菌はエビトロポミオシン誘発アレルギー性粘膜障害を緩和し、微生物叢と代謝の改変を介する可能性がある
アレルゴロジー・インターナショナル
(2019)
X. Guo et al.
肥満における脂肪組織の炎症性免疫学的作用と食物アレルギーのリスク: 免疫学的メカニズムに焦点を当てる
アレルギー学と免疫病理学
(2020)
T.Y.F. Halim et al.
2群自然リンパ球は適応Tヘルパー2細胞を介するアレルギー性肺炎の開始に重要である
免疫学
(2014)
C.H. Huang et al.
ラクトバチルス・ロイテリはマウスにおいて食物アレルギーに対する腸管免疫寛容を誘導する
機能性食品ジャーナル
(2017)
M. Hussain et al.
高食餌性脂肪摂取は食物アレルギーを促進する微生物叢シグネチャーを誘導する
アレルギーと臨床免疫学ジャーナル
(2019)
他の文献を見る
引用文献 (0)
推薦論文 (0)
全文を見る
© 2023 Elsevier Ltd. 無断複写・転載を禁じます。
エルゼビアのロゴとワードマーク
サイエンスダイレクトについて
リモートアクセス
ショッピングカート
広告掲載
お問い合わせとサポート
利用規約
プライバシーポリシー
当社は、サービスの提供・向上、コンテンツや広告のカスタマイズのためにクッキーを使用しています。続行することで、クッキーの使用に同意したことになります。
このサイトのすべてのコンテンツ: 著作権 © 2023 Elsevier B.V.、そのライセンサー、および寄稿者。テキストマイニング、データマイニング、AIトレーニング、および同様の技術に関するものも含め、すべての権利はエルゼビアに帰属します。すべてのオープンアクセスコンテンツには、クリエイティブ・コモンズのライセンス条件が適用されます。
RELXグループホームページ
フィードバック
この記事が気に入ったらサポートをしてみませんか?
