
期待の新薬アデュカヌマブはどのくらい「効く」か? <3/終> risk/benefit バランスとコスト問題
地域医療ジャーナル 2022年3月号 vol.8(3)
記者:kei_e-cats
医師
今回も前回の記事に引き続き,
認知症新薬のアデュカヌマブの効果は,どの程度期待できるのか?
について考えていきたいと思います。
*この記事の記載内容に関し,筆者が開示すべき COI はありません。
前回の復習
毎度のことながら,前回までに取り扱った内容を簡単に復習します。
アデュカヌマブの第 III 相試験は2本あり(EMERGE・ENGAGE)
いずれも早期アルツハイマー型認知症・MCI を対象とした国際共同試験
中間解析で無益性の判定となり,両試験とも途中中断された(EMERGE 803例,ENGAGE 945 例が解析対象)
中断後の後付け解析で,EMERGE では主要評価項目(認知機能スケール CDR-SB)の有意差を示したが,ENGAGE 試験ではプラセボよりも成績が悪かった(EMERGE 1638 例,ENGAGE 1647 例が解析対象)
アミロイドPETの画像所見は,いずれの試験でも有意に改善させていた
「画像改善」という〈代用アウトカム〉をもとに〈迅速承認〉された
今後 10 年以内の 市販後検証的試験(第 IV 相試験)で認知機能スケールでの有効性を示すことができなければ,承認取消となる
また,投与に伴う主なリスクとして,9人ごとに1人 脳内微小出血(NNH 9)を起こし,4人ごとに 1人 脳内浮腫を起こす(NNH 4)
─── データ出典 ───
● NCT: EMERGE試験 (NCT02484547), ENGAGE試験 (NCT02477800)
● FDA: 諮問委審議ページ,提出されたプレゼンテーション
──────────────
治験データに関しては,連載第1回 の無料公開部分で非常に詳細に取り扱っていますので,そちらをご覧いただければ幸甚です。
とはいえもう一度,公開されている治験結果のデータの要点のみ復習しておきましょう。
PICO-T

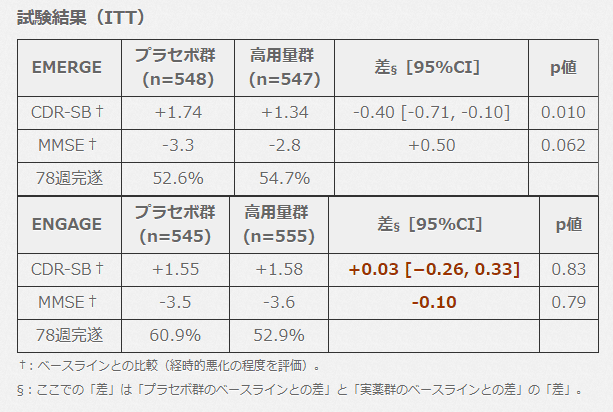
試験結果(ITT)
▶︎ 総括)
ENGAGE はプラセボより実薬の方が成績が悪かった(有意差以前の問題)。
EMERGE のみ,主要評価項目(CDR-SB)で有意差あり。
ただし CDR-SB は 0.5 点刻み 18 点満点のスケール。プラセボとの 0.40 [0.71, 0.10] の差が臨床的に有意かは要検討。
有害事象
ARIA:アミロイド関連画像異常
ARIA-E(edema):脳内血管性浮腫;早期中断すれば多くは可逆性
ARIA-H (hemorrhages) :頭蓋内微小出血や脳表ヘモジデリン沈着

▶︎ 総括)
脳浮腫の NNH 4,脳内微小出血の NNH 9
4人ごとに1人余分に脳浮腫を起こし,9人ごとに1人余分に脳内微小出血を起こす。
以上から考えたい数々の問題
上記のデータや迅速承認の経緯からは様々な問題点が見えてきますが,医療統計・医薬品リテラシーの教材として考えた場合,特にポイントとなるのは以下の5点だと思います。
そもそも本当に「有意」なのか?(多重検定の問題)
「代用アウトカムで迅速承認」の問題
外的妥当性(一般化可能性)の問題(日本でも使えるデータか?)
risk/benefit バランス(ARIAと認知機能)
cost/benefit バランス(値段が高い問題)
連載第1回の記事では〈多重検定の問題〉という観点から,後付けでひねり出された p=0.010 という数値の妥当性,「本当に有意と言えるのか」といった問題について考えました。
また連載第2回の記事では,「代用アウトカムで迅速承認(accelerated approval pathway)」というプロセスが抱える問題について取り扱いました。
最終回となる今回は,のこる以下の問題について取り扱いと思います(▼)。
外的妥当性(一般化可能性)の問題(日本でも使えるデータか?)
risk/benefit バランス(ARIAと認知機能)
cost/benefit バランス(値段が高い問題)
最初に結論を述べてしまうと,本稿の要旨は以下の3つです。
アデュカヌマブの治験データは,本邦では原理的に再現できない
効果の期待値が頭蓋内出血のリスクに釣り合うか要検討
コストの高さに見合うかは要検討
以下は購読者の方限定となりますが,お付き合いいただければ幸いです。
※この記事の記載内容に関し開示すべき COI は特にありません。
ここから先は
¥ 100
いただいたサポートは記事充実のために活用させていただきます。
