ロイコトリエン受容体拮抗薬モンテルカストとChurg-Strauss症候群のリスク:ケースクロスオーバースタディ
PMID: 18276721
https://pubmed.ncbi.nlm.nih.gov/18276721/
概要
背景ロイコトリエン受容体拮抗薬が Churg-Strauss 症候群(CSS)の発症を促進する可能性があることが懸念されている。そこで,ロイコトリエン受容体拮抗薬であるモンテルカストとCSS発症の関係を調査した.
方法
フランスとドイツのCSS患者78名の薬歴を、患者、主治医、調剤薬剤師への問診とカルテから追跡した。ケース・クロスオーバー研究デザインにより、CSS発症直前の3カ月間の「指標」期間におけるモンテルカストおよびその他の喘息薬の曝露量を、過去4回の3カ月間の「対照」期間の曝露量と比較した。オッズ比(OR)は条件付きロジスティック回帰により算出された。
結果
CSS発症のORは,モンテルカストで4.5(95%CI 1.5~13.9), 吸入長時間作用型β2アゴニストで3.0(95%CI 0.8~10.5), 吸入コルチコステロイドで 1.7(95% CI 0.5~5.4), 経口コルチコステロイドで 4.0(95% CI 1.3~12.5 )であった.モンテルカストの対照期間中の曝露量は、1999年から2003年のCSS発症の連続する3暦年間において時間的に増加していた(ptrend <0.0001)。
結論
モンテルカストの使用は、3ヶ月以内のCSS発症リスクを4.5倍高くすることと関連していた。
しかし、他の長期喘息コントロール薬で得られた正の推定値は、この関連性がCSS発症前の一般的な喘息治療のエスカレーションによって混乱させられる可能性を示唆するものであった。
本研究で観察されたモンテルカストとCSSの関連は、おそらくこの薬剤の使用量が時間とともに増加したことによっても説明される。
チャーグ・ストラウス症候群(CSS)は、喘息と好酸球増多を背景に発症する小血管炎である。
この希少で生命を脅かす可能性のある疾患の病因は不明です。
この10年間に、ロイコトリエン受容体拮抗薬(LTRA:モンテルカスト、ザフィルルカスト、プランルカスト)による喘息治療を受けている患者において、100例以上のCSSが公表または市販後調査システムに登録されました。
これらの報告は、CSSの誘発または薬剤による発症の可能性が以前から疑われていただけに、LTRAによってCSSが誘発されるかもしれないとの公衆衛生の懸念を引き起こしました。
臨床観察に基づき、LTRA と CSS の関係を説明するためにこれまで提唱された仮説の中で最も広く支持されているのは、LTRA の投与により喘息の治療に必要な副腎皮質ホルモンの漸減が可能になり、それによって偶然に CSS の潜在的な病態が明らかになったというものであった。
しかし、この理論は、コルチコステロイドの減量を併用しない場合にLTRAに関連するCSSが発生するという報告、LTRAの全体的に控えめなコルチコステロイド節約効果、吸入コルチコステロイドなどコルチコステロイド内服量の削減効果がより高い薬剤に見られる少数の同様の観察と矛盾しています。
最も重要なのは、LTRAとCSSに本当に関連があるかどうかを判断しようとした観察研究のみが稀であることです。
我々は、症例が自らの対照となる研究デザインであるケースクロスオーバースタディを実施し、調査地域で入手可能な唯一のLTRAであるモンテルカストへの曝露とCSS発症の関係の可能性を探りました。
Box 1 Churg-Strauss症候群の分類基準
米国リウマチ学会の基準27(6項目のうち4項目が必要とされる。)
気管支喘息
好酸球増加率10%以上(白血球の微分値において)
単発性または多発性神経障害
非固定性肺浸潤
副鼻腔の異常
生検での血管外の好酸球
Lanhamら28の基準(3項目すべて必須)
喘息
末梢血好酸球数ピーク値>1500/mm3
肺外2臓器を侵す全身性血管炎
方法
研究対象者
フランス血管炎研究グループ(FVSG)とドイツBad Bramstedtの血管炎学際センターからレトロスペクティブに研究参加者を募集した。
フランスからの研究参加候補者は、1995年から2005年にかけてFVSGが実施した前向き臨床試験に登録された患者から特定された。
この試験は、新たにCSSと診断された患者の治療戦略を評価するもので、フランスののセンターと他のいくつかのヨーロッパの医療センターから140人の患者が参加した。
法的な理由から、フランスのセンターがこの試験に登録した患者のみをこの試験の対象とした。
三次紹介施設のInterdisciplinary Vasculitis Center Bad Bramstedtは、1991年以降に同施設で追跡調査された全血管炎患者の前向き登録から、本試験の参加候補者を特定した。
モンテルカストは、1998年3月から4月にかけて両国において初めて承認されました。
本研究では、CSS(下記参照)発症前の15ヶ月間の曝露を評価するため、1999年7月から2004年4月の本研究開始時点までにCSSと診断されたすべての個人に関するデータベースを検索したところ、CSS発症前の15ヶ月間の曝露が確認されました。
調査の結果、CSSの発症が1999年7月より前であることが判明した人は、その後、解析から除外された。
また、最終的な解析では、American College of Rheumatology(ACR)の分類基準またはLanhamらが提案した分類基準(ボックス1)を満たす被験者のみを対象とした。
不完全なデータの可能性を避けるため、ACR基準の「好酸球10%以上」は、末梢好酸球絶対数1500/mm3以上でも満たされていると考えた。
データ収集
本研究に関連するCSSの発症時期および喘息治療歴は、3つの情報源から調査された。
(1) 参加者、(2) 地域の主治医と病院のカルテ、(3) 薬剤師の3つの情報源を用いて、本研究に関連する喘息治療歴の有無を調べた。
喘息の長期管理薬として以下の4つのクラス(それぞれの活性原理のもの)の曝露を記録した。
LTRA(モンテルカスト)、吸入長時間作用型β2アゴニスト(ホルモテロール、サルメテロール)、吸入コルチコステロイド(ベクロメタゾン、ブデノシド、フルチカゾン)、経口コルチコステロイド(ベータメタゾン、デキサメタゾン、メチルプレドニゾロン、プレドニゾロン、プレドニゾン)である。
さらに、アレルギーや予防接種のために処方された免疫療法に関する情報も収集し、これらのCSSの誘因と考えられるものの交絡効果を確認した。
調査期間中、参加者とその医師、薬剤師には、モンテルカストに関する特定の焦点を明らかにせずにCSSのリスク決定要因を検討することがこの研究の目的であることを伝えた。
研究参加者へのインタビュー
すべての研究参加者は、標準化された詳細な質問票を用いた40〜60分の電話インタビューを受けた。
参加者は事前に質問票を受け取り、面接に備えた。
過去に使用した薬剤を思い出しやすくするため、8ページと10ページの質問票には、フランスとドイツでそれぞれ喘息治療によく使用されている36種類と62種類の薬剤(薬剤クラスでグループ化し、アルファベット順に分類)がブランド名で列挙されている。
また、アンケート用紙には、記載されたすべての薬剤の原包と製剤および機器を示すラベル付きのカラー写真も含まれています。
フランスとドイツでは、医薬品はメーカーから提供された特徴的なオリジナルパッケージで配送されます。
さらに、患者さんには、医師の処方箋の複製を探すように勧めました。
インタビューでは、喘息、副鼻腔炎、アレルギーの病歴と、CSSの初期症状、発症日、その後の診断までのすべての症状について詳細に記録しました。
問診票に記入された薬のリストに基づいて、CSS発症前の2年間に服用したすべての抗喘息薬の名前を挙げてもらった。
曝露期間は、開始と中止の月数と年数で記録された。
最後に、地域の医師(主に開業医、呼吸器科医、アレルギー科医、耳鼻咽喉科医)および調剤薬局薬剤師の身元と連絡先を尋ねた。
また、問診時に口頭で伝えた情報に加えて、記入済みの問診票を郵送で返送してもらった。
主治医へのアンケートとカルテの確認
各参加者の一般開業医、および該当する場合は、喘息治療の使用に関して信頼できる情報を提供できる地元の治療専門医の少なくとも1人と連絡を取るようにした。
医師には、郵便で回答を求めるか(ドイツ)、電話で質問した(フランス)。
後者の場合、電話をかけた研究者は、患者の面接で収集した情報を知らなかった。
医師は、CSS発症の2年前から診断までの間に処方されたすべての抗喘息薬の詳細な情報と、患者が電話インタビューで最初に提供した日付に基づいて、CSSの最初の症状について尋ねられた。
病院の医療記録(治験報告書や退院通知書など)に、CSSの発症日や徴候、薬歴について目を通した。
調剤薬局薬剤師へのアンケート
被験者が指定したすべての薬剤師に、上記の調査期間中に被験者に調剤した薬剤の電子記録のプリントアウトを郵送で提供するよう依頼した。
フランスとドイツでは、医薬品の配達は最大30日分までと決められているため、長期間の投薬を受けている患者は毎月薬局に足を運ばなければならない。
CSS発症と過去の被曝の定義
CSSの発症日は、CSSに起因する症状が最初に発生した日と定義されます。
喘息、副鼻腔炎、アレルギーに起因する症状や薬物への暴露は、CSS発症の判断材料には含まれません。
発症した正確な日や週が特定できない限り、各月の15日を発症日とした。
この日付をもとに、CSS発症前の15ヶ月間の個人曝露履歴を作成した。
長時間作用型β2作動薬と副腎皮質ステロイドの吸入併用療法では、同じ薬理学的分類の薬物への曝露時間を累積して、曝露を両分類に割り当てた。
曝露の正確な開始と終了は、主に担当医および/または薬剤師から得た情報を用いて決定した。
入手できない場合は、曝露期間は患者および/または病院の記録から得た日付を用いて定義した。
ケースクロスオーバー解析
この伝統的な症例対照研究の変種は、事象(例えば、疾患の発症)の直前の「指標」期間における潜在的危険因子への曝露を、それ以前のいくつかの「対照」期間における曝露と比較するものである。
発症メカニズムに基づき、我々は一次解析において、CSSの発症はモンテルカストまたは他の医薬品への最初の曝露から3ヶ月以内に起こると考えた。
したがって、各患者について、3ヶ月の指標期間の直前の連続した4つの3ヶ月の期間を対照期間とした。
指標期間または対照効果期間は、その期間中に少なくとも1日、その薬効分類に属する薬物が使用された時点で、その薬効分類に曝露されたと定義された。
ある薬物群の使用期間が正確に決定できない場合、該当する効果期間は欠損データとして扱われた。
さらに、感度分析(2ヶ月(指標1つ、対照6つ)および4ヶ月(指標1つ、対照2つ))およびサブグループ分析を行い、一次分析の結果の頑健性を検証した。
CSS発症前の4つの対照期間中の曝露レベルを比較し、次にCSS発症年別に分析した4つの対照期間中の曝露レベルをプールして比較することによって、検討した各薬効群の曝露確率に経時的に線形傾向がないという仮定を検証した。
統計解析
カテゴリー変数はχ2検定、必要に応じてFisher exact検定で比較し、連続変数はStudent t検定またはKruskal-Wallis検定で比較した。すべての統計解析において、両側p値<0.05を有意とみなした。
結果
患者の選択と調査への回答
合計110件のファイルから、すべての選択基準を満たし、研究への参加に同意した78人(71%)の患者が特定された(図1)。

図1
研究対象者のフローチャート(括弧内の数字は、それぞれフランスの血管炎研究グループおよびバート・ブラムステットの学際的血管炎センターで確認されたチャーグ・ストラウス症候群(CSS)の患者を指す)。
ACR、American College of Rheumatology(米国リウマチ学会)。
71名(91%)の参加者について、少なくとも1名の地域医師から情報を入手した。
薬剤師が調剤した薬のプリントアウトは、調査した15か月間の全期間について40人(51%)、この期間の一部について11人(14%)が入手した。
3名(4%)は主治医、調剤薬局のどちらからも情報を得られなかった。
臨床データ
78名の被験者の主な特徴を表1に示す。
ほとんどの患者(96%)がCSSのACR分類基準を満たし、Lanhamの基準のみに基づくものは3名(4%)だけであった。
また、1名を除くすべての被験者が以下の項目のうち少なくとも1つを満たしていた。(1) 血管炎、肉芽腫症および/または血管外好酸球の組織学的証明 (2) 抗好中球細胞質抗体(ANCA)検査陽性 (3) 1500/mm3以上の末梢好酸球および/または白血球数の10%以上の好酸球。
表1
78名の被験者のChurg-Strauss症候群(CSS)診断時の特徴

CSS発症から診断までの平均(SD)期間は3.8(4.0)ヶ月(中央値2.4)であった。喘息の既往がある76人(97%)では、喘息発症からCSS発症までの平均(SD)間隔は92.8(120.3)カ月(中央値42.8)であった。17人(22%)は、CSS発症の15カ月未満前に喘息を発症していた。
薬物曝露量
表2は、CSS発症前の15ヵ月間におけるモンテルカストおよびその他の調査対象クラスの喘息薬の曝露率を、全体として、あるいは3ヵ月の指標期間と対照期間で層別して示したものである。
全体として、これらの抗喘息薬の平均(SD)使用数は2.2(1.3)であった(中央値2.5)。
4種類の喘息薬の使用率は、統計的に有意ではなかったが、最も早い対照期間から最も遅い対照期間にかけて増加した(表2)。
表2
Churg-Strauss症候群(CSS)発症前15カ月間のモンテルカストおよび他の抗喘息薬の曝露率:合計および個々の3カ月効果期間、CSS発症年による層別化
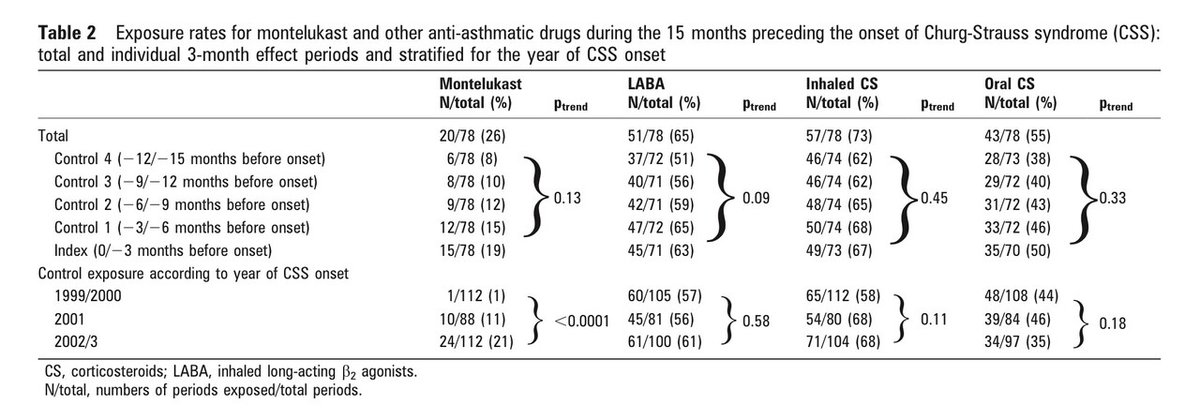
薬剤摂取に経年的な傾向があるかどうかを調べるために、CSS発症の時間3分位で層別した対照期間(1999年7月から2000年12月、2001年1月から12月、2002年1月から2003年12月)に、プールした曝露頻度を比較した。
この解析では、モンテルカストへの曝露が時間とともに統計的に有意に増加することが示された(p<0.0001、表2)。
20人(26%)がCSS発症前の15ヶ月間にモンテルカストに曝露されていた。
そのうち16人(80%)については、モンテルカストの摂取に関する情報が少なくとも2つの情報源から得られていた。
モンテルカスト服用開始からCSS発症までの平均(SD)間隔は11.3(13.8)カ月(中央値8.4)であった。
CSS発症時期に対するモンテルカストの個々の服用期間を図2に示す。
重要なことは、これら20人のうち7人はモンテルカスト投与開始の3ヶ月間、経口コルチコステロイドを服用していなかったということである。
さらに、他の7人(9%)は、モンテルカストを研究対象期間の15ヶ月前(n = 3)またはCSSの発症後(n = 4)にのみ摂取していたことが確認された。
図2
Churg-Strauss症候群(CSS)発症前の15ヵ月間に20/78人の被験者がモンテルカストを使用した時期。横棒は、CSS発症日(0ヶ月目)、3ヶ月の「指標」期間(濃い灰色)、3ヶ月の「対照」期間(薄い灰色)に対してプロットされた曝露期間を示す。

CSSの臓器症状やANCA陽性などのベースライン特性を比較した結果、CSS発症前の15カ月間にモンテルカストに曝露した患者と曝露しなかった患者の間に、統計的に有意な差は認められませんでした(表1)。
3ヶ月の指標期間中に、2人の患者がアレルギーに対する免疫療法を、他の3人の患者がインフルエンザワクチン接種を受けたことが確認されたが、これら5人の患者はいずれもモンテルカストに曝露されたことはなかった。
免疫療法は、CSS発症の2年以上前に開始されていた。
ケースクロスオーバー解析
ケース・クロスオーバー解析の結果を表3に報告する。
一次解析では、モンテルカストへの曝露と3ヶ月以内のCSS発症により、4.5(95%信頼区間(CI)1.5~13.9)のORが得られた。
また、感度分析では、他の抗喘息薬のクラスや、2ヶ月または4ヶ月の指標期間と対照期間についても、正のORが得られた(表3)。
4つの喘息治療薬クラスすべてを共変量として含む多変量モデルでは、3ヵ月間のORはモンテルカストで6.7(95%CI 1.3~34.1), 吸入長時間作用型β2作動薬で 2.9(95% CI 0.6~13.3), 吸入コルチコステロイドで 1.0(95% CI 0.2~4.8), 経口コルチコステロイドで 4.2(95% CI 1.2~14.6 )であった。
表3
血管炎発症前3カ月間(主要解析)および2カ月間または4カ月間のリスク期間(感度解析)におけるモンテルカストまたは他の抗喘息薬への曝露(ケースクロスオーバー解析による)とChurg-Strauss症候群の関連性リスク
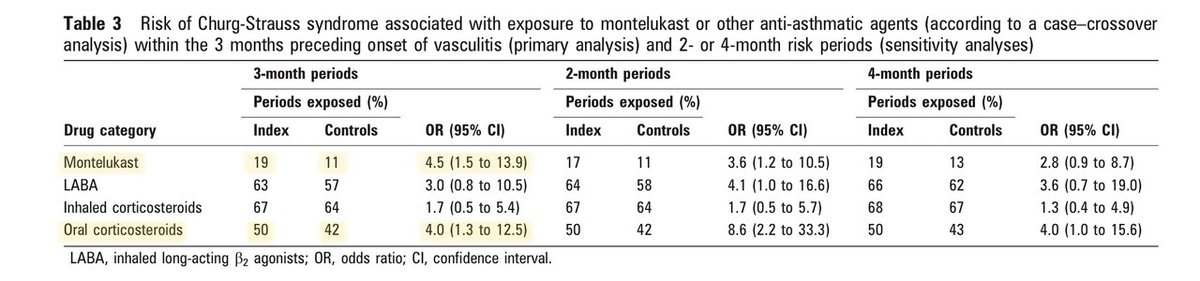
モンテルカストの長期的な曝露量増加の暦年による影響を評価するため、上記で定義したCSS発症の3つの期間についてモンテルカストのORを計算した。
このサブグループ解析により、最も早い期間(1999年7月~2000年12月)のORは無限大となり、続く2つの期間(2001年1月~12月、2002年1月~2003年12月)ではそれぞれ2.2(95%CI 0.5~10.9)および2.3(同0.3~16.7)のORが算出された。喘息の病歴が15ヵ月以上ある59人(76%)に限定したさらなるサブグループ解析では、3ヵ月リスク期間のORは、モンテルカスト 4.5(95% CI 1.5~13.7) 、長時間作用型β2作動薬 3.7(95% CI 0.7~19.5) 、吸入コルチコステロイド 0.3(95% CI 0.05~1.8) および 経口コルチコステロイド 5.0(95% CI 1.4~17.4 )であった。
考察
CSS患者79名を対象としたケース・クロスオーバー解析の結果、モンテルカストによる治療は、3ヵ月以内にCSSを発症するリスクを4.5倍に高めることが統計的に有意であることが示されました。
しかし、吸入長時間作用型β2アゴニストと経口コルチコステロイドの使用も、CSS発症のリスク比を同程度に増加させたが、後者のみが統計的に有意であった。
効果期間の長さを変えた感度分析、およびCSS発症の少なくとも15カ月前に喘息と診断された患者のサブグループについても、一貫した効果の大きさが推定された。
これらの知見を総合すると、CSSの発症との関連はモンテルカストに特有のものではなく、重症喘息の長期コントロールのために処方される薬剤群に関連した現象である可能性が示唆されるかもしれません。
この手法は、当初は急性事象に対する一過性の曝露の影響を分析するために考案されたが、長期間の曝露やより微妙な発症の事象の設定においても有用であることが証明されている34 35。
この手法はセルフマッチングを用いるため、症例と対照の間に存在しうる未測定または未知の要因の差異による個人間交絡のリスクが排除される。
しかし、ケースクロスオーバーデザインは、研究対象の危険因子への曝露が対照期間を通じて一定であることを暗黙の前提としているため、曝露に時間的傾向がある場合には、バイアスが生じる可能性がある36。
ケースクロスオーバーデザインは、従来のケースコントロール研究よりも、特に有効な対照群を選択するという困難な課題を回避できたため、LTRAと関連したCSS発症リスクの可能性をより適切に評価することができたと我々は考えている。
CSS発症前の15ヵ月間に吸入長時間作用型β2アゴニスト(65%)、経口(56%)および吸入コルチコステロイド(73%)に多く曝露されていることが示すように、CSSに関連する喘息は通常重症で、モンテルカストが26%の被験者に投与されていたという事実は、この重症度を強調しているのかもしれません。
したがって、従来の症例-対照計画では、CSSを発症した喘息患者と喘息患者対照との間で異なる可能性のある喘息の表現型またはその他の測定されない因子について対照を不完全にまたは一致させないためにバイアスがかかる危険性がある。
このような対照群の不適切な選択の可能性は、LTRAがCSSに及ぼす潜在的影響を検討した以前に実施されたケースコントロール研究の解釈を難しくしている。
その研究でもCSSとLTRAおよび他の抗喘息薬の使用との間に関連が認められたが、その結果は、一般の喘息集団から選ばれた対照群の喘息が軽い可能性に起因している可能性がある。
今回の結果は、LTRAとCSSの関連性について、これまで提唱されてきたものとは異なるメカニズムを示唆している。
CSS発症前に喘息治療が持続的かつ全般的にエスカレートしていることを考慮すると(表1)、モンテルカストとCSSを関連づける最も妥当な説明は、喘息が徐々に悪化したことによる適応症の交絡であると思われる。
しかし、このシナリオは、CSSの特徴である血管炎が出現する前に、喘息発作の頻度と重症度が増加するという前駆期の概念に合致するものである。
この長い間隔は、好酸球の化学吸引やコルチコステロイドの漸減がCSSの「仮面を剥ぐ」あるいはモンテルカストに対する過敏性といった薬物付随効果の理論とは整合しがたい。
なぜなら、こうした有害事象は初回曝露時の初期に予想されるからである。
モンテルカストの処方パターンの分析からも、この薬剤とCSSとの間に観察された関連について洞察することができる。
この結果は、1998年にモンテルカストが承認されて以来、臨床でモンテルカストが使用されるようになったことを反映している。
曝露の確率が時間依存的である状況におけるケースクロスオーバーデザインの脆弱性を考慮すると、この長期的な傾向は、モンテルカストとCSS発症の観察された関連にさらに寄与している可能性がある。
実際、CSS発症年数で層別化したORは、直近の2つの期間についてより保守的な2倍のリスクを示し、モンテルカスト市販承認後の最も初期の段階における低い処方率によって全体の推定値4.5が膨れ上がったという示唆を裏付けている。
他の新薬と同様に、モンテルカスト使用量の顕著な経年的増加は、モンテルカストに関連するリスクに対する一般的な認識を歪めた可能性もある。
本研究には長所と短所がある。CSSは年間100万人に3人という非常に稀な疾患であるが、本研究の長所は、十分に特徴付けられ、かつ先験的に選択されていない多数の個人により、解析結果の一般化可能性と相応の統計的検出力が得られていることである。
また、様々な抗喘息薬の薬歴を複数の独立した情報源から丹念にたどることで、想起バイアスの可能性を最小限に抑えることができた。
CSSの発症日を正確に定義し、決定することが困難であったという制限もあるが、モンテルカストと他の薬剤群の推定値には、非差異的誤分類が同様の影響を及ぼすはずであった。
また、我々の研究の前提は、CSSが薬理学的危険因子に曝露された後の明確な期間内に発生することであることを念頭に置かなければならない。
もう一つの欠点は、フランスとドイツで承認されている唯一のLTRAであるモンテルカストのみに焦点を当てたことである。私たちは、ZafirlukastやPranlukastの曝露後や、他の喘息薬やアレルギー薬の治療後にCSSが発生した場合にも、このデータの解釈が成り立つと考えています。
結論として、本研究の結果は、モンテルカストの摂取と急性期CSSの発症との間に密接な関係があることを実証しています。
モンテルカストの使用は、個人レベルで徐々に悪化する喘息の代理指標であり、一般的にモンテルカスト曝露の重要な増加であると仮定される。
この記事が気に入ったらサポートをしてみませんか?
