XBB.1.5 ブースター接種の効果について
主張:2023年秋の追加接種には、必要な人に対してXBB.1.5 変異株対応の組み換え蛋白ワクチンを使用することが望ましかったです。
mRNAワクチンには複数のメカニズムによる使用に対する疑義が発生しています。もう随分前からですが。。。
速やかに市場における使用停止が妥当です
また、ワクチン接種事業を先導する識者を信頼しておられる皆様、特に医師の皆様、はるかに安全性の高いXBB.1.5 変異株対応の組み換え蛋白ワクチンが日本に導入されていない現実を、その理由をどうか考えてください
CDCのワクチン推奨を話し合う諮問委員会 ACIPによるワクチンの有効性をもとに考える
ワクチンの有効性について
ワクチン有効性は集団レベルの推定値で、ワクチンの有効性が 80% の場合は、ワクチン接種を受けた集団では、ウイルスに接触したときに病気にかかる人が 80% 少ないことを意味します。

米国 18歳以上の成人の COVID-19発症に対する2023~2024年のワクチンの有効性
年齢層別、投与後の時間別
期間:2023年9月 – 2024年2月
XBB.1.5対応ブースター接種により、XBB.1.5対応ブースター接種をしていない人よりもどのくらい発症が減少したかをもとに計算した結果、49才までのグループはブースター接種から2か月後まで50%以上発症が減少した。
50才以上は接種後に高い効果は出なかったが、4か月後くらいまで発症が最低でも24%減少した。高齢になるほどどんなに接種を重ねても有効性の出ないポピュレーションが増えます。

資料1. p10
上のテーブルの右端が各年齢グループにおけるXBB.1.5 ブースター接種した人がしてない人よりも発症する頻度が減少したワクチン効果です。
見づらいので、抜き出してグラフにします。
50才未満は、効果が接種60日後まで緩やかに上昇した。
50才以上は最大でも40%台ですが、接種120日後まで緩やかに上昇した。

資料1. p10 より作成
上記のワクチン効果を測定した2023年9月 – 2024年2月に米国で流行していた変異株の変遷を見てみましょう。EG.5やXBB群の流行していた9月末からスタートして、60日後の11月末にはJN.1 が10%以上に、そして120日後の1月末には90%以上はJN.1 が循環していました。上のグラフと合わせてアバウトに表現すると、50才以上ではJN.1 が流行するようになってもXBB.1.5 ブースター接種による発症予防効果が40%以上あった。(比較はこのブースター接種をしてない人)。

予測資料1. p11
もう一つ重要なグラフが公開されています。XBB.1.5 ブースター接種をした人は、新型コロナウイルス感染症で入院した患者の2%から5%でした。

資料2. p11
ベースとなるブースター接種を受けた人口の割合は、約21%です。下のグラフの最下段の濃紺の範囲になります
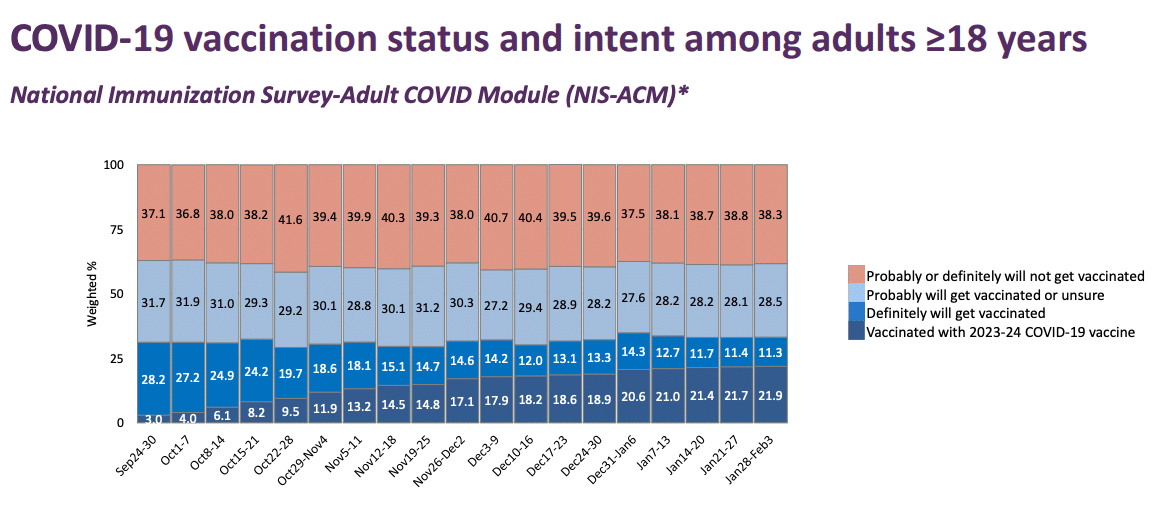
結論:昨年の秋にXBB.1.5 対応mRNAワクチンを接種した人は現在日本で流行しているJN.1 変異株に発症や入院以上の重症化からある程度の利益を得ました。春からのキャンペーンは、まだ最終接種から1年経っていないのでもう一度同じXBB.1.5 対応ワクチンを接種する意味がわかりません。
また、XBB.1.5 対応ワクチンはより安全なノババックスの組み換え蛋白ワクチンがあります。EUでは2023年10月末より12才以上を対象に接種可能になっています。
しかし、日本ではこのタイプを接種することができません。
日本で昨年秋からXBB.1.5 対応ワクチン (組み換え蛋白型) を接種できない状況は、ワクチン接種を推奨しておきながら手落ちであったと主張します。
また、春に流行する予定の変異株の推測はされていますか?もはやXBB.1.5 対応ワクチンによる免疫を逃避する変異株になっている可能性がありませんか?
現行のmRNA型ワクチンに指摘されている不具合は別の記事でご説明いたします。この記事を書いているパイロン先生は現行のmRNA型ワクチンの接種はしてほしくないと考えています。どうぞ次の記事をお待ちください。
追伸:春になる前の寒波が来ていますし、マグニチュード5〜6程度の地震予報も出ています。どうぞお健やかにお過ごしください。
資料1. COVID-19 vaccine effectiveness 訳前半 訳後半
資料2. COVID-19-associated hospitalizations among adults – COVID-NET 訳
資料3. COVID-19 vaccination coverage update
XBB.1.5、JN.1 のスパイク蛋白を持つシュードウイルスを用いた実験結果をもとに考える
JN.1 とは?
JN.1 は Omicron BA.2 とは独立して出現したBA.2.86 のわずかな変異体です (ref 7)。
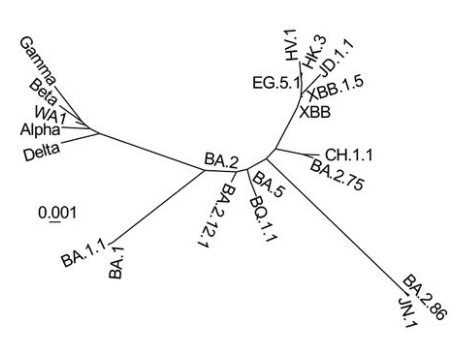


JN.1 に有効な中和抗体製剤はない
組換えモノクローナル抗体 (mAb) は COVID-19 治療に使用されて成功していますが、現在の SARS-CoV-2 系統はそれらのほとんどまたはすべてに対する耐性を獲得しました ( ref4 )。以前に COVID-19 治療用に承認された、または現在開発中の 12 種類の mAb のパネルを使用して中和活性を調べた実験があります。ソトロビマブのみが XBB.1.5 シュードウイルス中和に対して有効であり、JN.1 シュードウイルスを中和する mAbs はありませんでした (ref5)。

有効用量 50 (EC50) 値を示します。ref 5の図2Bより
XBB.1.5 対応ブースター接種者は感染の既往がないと、JN.1 の中和活性の出ない人がいる
参加者の免疫状況は次の通りです
すべての参加者は非XBB.1.5に適応したCOVID-19ワクチンによる少なくとも4回のワクチン接種を受けており、最後の感染またはワクチン接種後3か月以内に血漿サンプルが収集されました。
コホート 1 のメンバーには SARS-CoV-2 感染歴がありませんでしたが、コホート 2 のメンバーは 2022 年 1 月から 2023 年 3 月の間に SARS-CoV-2 感染を記録していました。
コホート3および4には、XBB.1.5ブースターワクチン接種を受けていない参加者が含まれており、1回(コホート3)または2回(コホート4)のSARS-CoV-2感染を経験し、直近の感染はJN.1波中に発生しました。
シュードウイルスを血清で中和する実験です。
全員が4回、XBB.1.5 非対応の COVID-19 ワクチンを接種しています。XBB.1.5 ブースター接種をしてもオミクロン感染の既往がない場合は (図①)JN.1 を中和する活性が出ない人がいます。また、オミクロン以降の感染既往があってもXBB.1.5 ブースター接種をしていない場合はJN.1 の中和活性の低い人がいます (図③④)。
結論:4回XBB.1.5 非対応の COVID-19 ワクチンを接種した人にJN.1 シュードウイルスの中和活性を誘導するためには、オミクロン以降の感染の既往とXBB.1.5 対応ブースター接種が有効のようです。

示された S タンパク質を含むシュードタイプ粒子を、Vero 細胞に接種する前に、さまざまな希釈度の血漿とともにインキュベートし、細胞溶解物中のホタルルシフェラーゼ活性存在下での侵入に対してさらに正規化し(阻害0%として設定)、中和力価50値を非線形回帰モデルに基づいて計算した。
統計的有意性は、Wilcoxon 対応ペア符号付き順位検定によって評価されました。ref5の図2Cより
未感染者に最新の一価mRNAワクチン(XBB.1.5 MV)を投与したところ、XBB.1.5(27.0倍)に対して血清中和抗体が有意に上昇した
未感染者に最新の一価mRNAワクチン(XBB.1.5 MV)を投与したところ、XBB.1.5(27.0倍)および現在主流となっているEG.5.1(27.6倍)だけでなく、HV.1、HK.3、JD.1.1、JN.1などの主要な新興ウイルスに対しても血清中和抗体が有意に上昇した(13.3〜27.4倍)。
*ここでの未感染者は、野生型一価 mRNA ワクチンを 3 ~ 4 回接種し、その後 BA.5 二価 mRNA ワクチンを 1 回接種している。(ref 6)

以前にオミクロン亜変異体に感染した人では、検査したすべてのウイルス変異体に対して血清中和力価が最高レベル(1,504対22,978)まで上昇した。最新のワクチンでも免疫学的インプリンティングは依然として明らかだが、以前に認可された二価 BA.5 ワクチンほど深刻ではない。(ref6)
ref 4. SARS-CoV-2 BA.2.86 enters lung cells and evades neutralizing antibodies with high efficiency. Cell. 2024 Feb 1;187(3):596–608 e17.
ref 5. Virological traits of the SARS-CoV-2 BA.2.87.1 lineage. doi: https://doi.org/10.1101/2024.02.27.582254
ref 6. XBB.1.5 monovalent mRNA vaccine booster elicits robust neutralizing antibodies against emerging SARS-CoV-2 variants.
doi: https://doi.org/10.1101/2023.11.26.568730
ref 7. Antigenicity and receptor affinity of SARS-CoV-2 BA.2.86 spike. DOI: 10.1038/s41586-023-06750-w
この記事が気に入ったらサポートをしてみませんか?
