
mRNA ワクチンのロット間分析
(タイトル)
Analysis of mRNA Injections Lot-to-Lot
Republishing vax lot analyses from VAERS data on Substack
mRNA 注射のロット間分析
VAERSデータからVAXロット解析をSubstackに再掲載。

【解説】
この記事は、mRNAワクチンのロットの品質のばらつきをVAERSからデータを得て解析したものです。
ロット番号とは、製造プロセスで一定期間にまとめて製造した製品に付けられる番号です。そのため、通常は同じロット番号のワクチンは同じ品質とならなければなりません。
ところが、FDAは長期間に渡って製造されるワクチンに同じロット番号を付け続けることを許可しているということです。
これでは、ロット番号による品質管理やトレーサビリティの機能を果たせません。
VAERSの有害事象データベースからインフルエンザ・ワクチンと新型コロナワクチンのロット単位の有害事象発生頻度を調査したところ、インフルはバラツキが小さいのに対して、コロナはバラツキが過大であった。
この事実より、
「コビッド19ワクチンの製造工程が現行の適正製造基準(cGMP)法に準拠していない」
と結論づけています。つまり、違法な品質の製品ということです。
ロット間の有害事象発生率のバラツキは非常に大きいにも関わらず、当局はこの問題をスルーしている。
インフルワクチンと比較して、コロナワクチンは有害事象の発生率が高い、また、ロット毎の品質のバラツキはインフルワクチンの最大12倍とみられる。
『結論として、Covid-19 ワクチンは、製造ロット間の一貫性を示していない』
ファイザー製はモデルナ製よりも品質のバラツキが大きく、有害・無害の差が大きいです。
以下、記事の翻訳。
注:これは、ワクチンのバッチに関する私の歴史的分析の要約である。医薬品のバッチまたはロットは、すべての中間工程と原材料を特定の製造ラインと供給者にまで遡ってトレーサビリティを持つ単一の生産工程であるべきである。
最近、FDAは連続生産(非バッチ)のmRNA製品を「認可」(対策を規制しないので偽認可)しました。例えば、ロットFL0007は6ヶ月以上かけて製造され、いくつかの有効期限があり、1,200万回以上投与されています。これはバッチではなく、数カ月にわたって生産され、すべてに同じ番号が付けられているものです。したがって、今後、製造不正を発見するためのバッチ分析法はもうないでしょう。FDAは消費者保護を破壊しました。私たちが彼らの行動に責任を持てるようになるまで、誰も二度と彼らの製品を信用してはいけません。
私はもうCDCのVAERSデータベースには注目していませんが、2021年と2022年に多くのデータ分析を行い、mRNA/DNA注射の展開直後に観察された製造上の不整合や現行の適正製造規範(cGMP)の遵守の欠如を明らかにしました。
私はVAERSデータベースを使用して、ロット番号に基づく重篤な有害事象(生命を脅かすもの、障害、流産、入院、ER訪問、医師の診察)および死亡の変動性を調査しました。ロット番号またはバッチ番号は、1回の製造(バッチ)で製造・充填されたバイアルを表し、バイアルに印刷されており、vaxカードやvax損傷報告書に記録されることになっている。
VAERSレポートを記入する際に、人々が常にヴァックスカードを持っているとは限らないので、しばしば欠落していることがあります。多くの場合、誤入力と思われます。私が「思われる」と言ったのは、私を含む多くの調査員がVAERSデータのアルゴリズム操作を検出したからで、CDCは安全性シグナルの検出をさらに困難にするためにロット番号を変更していると思われます。
その頃、イギリスから来た薬学生のクレイグ・パールデコパーと出会いましたが、彼はVax義務化のために大学を去らなければなりませんでした。私たちは、「チーム・エニグマ」という名前で、他の数人のデータベースやソフトウェア、データアナリストと協力し合いました。私たちの仕事は、有害事象のデータと世界中で展開されている注射剤の製造ロットとの関係を理解しようとすることに重点を置いていました。
今でこそ、小瓶に入った兵器化された技術であることが分かっていますが、2021年当時はまだ甘く、これは医薬品であるはずだと考えていたのです。クレイグは、データを一般に公開するためにウェブサイトHow Bad Is Your Batch(www.howbad.info)を立ち上げました。その後、2023年1月には1300万回の訪問を記録し、開設以来1億1000万回を超える訪問を記録するなど、教育・データリソースとして大成功を収めています。このウェブサイトは、世界中で展開されているジェノサイドに関する膨大な量の集合的な研究と記録を紹介しています。
BACKGROUND
CPG Sec. 420.100 法第501条(b)および501条(c)に基づく医薬品の不純物混入。セクション501(b)に基づく不純物混入医薬品の直接参照押収権限。
食品医薬品化粧品法(FDA)第501条(b)は、品質、強度、純度に関する公式基準に適合しない場合、公式医薬品(すなわち、公式コンペンディウムで名前が認識されている医薬品と称される、または医薬品として表される医薬品)を粗悪品とみなしています。501(b)に基づきこのような適合性を判断する場合、一般的な試験または測定方法が使用される。この基準は、個々のモノグラフ、およびUSP/NFの一般通知のセクションの一部に記載されている。力価、無菌性、溶解性、重量変化、含量均一性などの特性について、規格と試験方法が確立されている。
公式医薬品が強度、品質、純度に関する1つまたは複数の一般的な基準に適合していないが、ラベルにその基準との違いを明確に記載している場合、その医薬品は501条(b)の下で粗悪品とみなされない。
同法第501条(c)は、公式大要で認められていない医薬品が、その医薬品が有すると主張又は表示される強度、純度又は品質を満たさない場合、粗悪品とみなす。公式コンペンディウムで認められていない医薬品に適用される品質基準は、医薬品(または医薬品製品)のラベル、製造者の仕様書、新薬申請書などの情報源から判断することができます。(試験方法は通常、仕様書や新薬承認申請書に記載されています)*。
方針
方針:品質、強度、純度について、コンデンディアルな方法で検査してもコンデンディアルな基準に適合しない公的医薬品は、その基準との違いが医薬品のラベルに明確に記載されていない限り、不純物である。
公式大要で認められていない医薬品は、その強度が、科学的に健全な方法で試験した場合に、その医薬品が有すると主張または表示されているものと異なるか、その純度または品質がそれを下回る場合、粗悪品である*。
関連する事例
関連事例:バッチ変動/適正製造規範からの逸脱に対するFDA警告状 - 不純物混入医薬品
当該企業は、バッチが既に配布されているか否かにかかわらず、説明のつかない不一致やバッチまたはその構成要素が仕様のいずれかを満たさないことを徹底的に調査しなかった(21 CFR 211.192)。
混入した原薬によるFDAを欺くための共謀の容疑:
グラクソ・スミスクライン社から、cGMPに関連する問題から混入した医薬品による6億ドルの民事和解金と1億5000万ドルの刑事罰の和解金:
https://www.fbi.gov/stats-services/publications/financial-crimes-report-2010-2011
Covid-19ワクチンのロット間分析:
データセットは、米国からのみ提出された報告に限定して、VAERSウェブサイトからダウンロードした(2021年12月10日現在)。調査結果の概要
12カ月未満の期間にCOVID-19ワクチンのロットで報告された有害事象、重篤な有害事象、死亡の総数は、入手可能な全期間(約30年間)に季節性インフルエンザワクチンのロットで報告されたこれらの事象の総数よりはるかに多い。すべての評価項目において、非常に大きな差が存在します:合計、ロットあたりの最大および平均の有害事象、重篤な有害事象、および死亡。
COVID-19ワクチンのロット間で有害事象、重篤な有害事象、死亡に過度のばらつきがあることは、30年間に報告された季節性インフルエンザワクチンのロットに関連する有害事象のばらつきが非常に小さいことと対照的であるように思われます。この所見は、コビッド19ワクチンの製造工程が現行の適正製造基準(cGMP)法に準拠していないことを示しています。
これらの結果は、特定のロット番号に関連するコビッドワクチンからの有害事象および死亡報告の異常で憂慮すべきデータパターンを示しています。 これらの所見は容易に発見でき、明らかであるにもかかわらず、規制当局や公衆衛生機関は今日までこれらのシグナルを「検出」していません。 この故意の不作為は、私の数字以上に大きな声で語っています。
結果
データセットは、VAERSからダウンロードしたデータです。

*有効でないロット-すなわちVAERSデータベースに存在するロットで、明らかに誤記されたロットを多く含む生出力。これは、同じシグナル/ノイズの問題、つまり明らかに大きな割合の「mistyped」ロット番号を持つインフルエンザワクチンのデータセットと比較する際には問題ではない。この問題は、多数の有害事象と死亡に関連するロット番号には影響しない。
**各カテゴリーでVAERSに報告された事象の数。不明」、「なし」、データ欠落のある報告、およびいくつかの明らかなタイプミスを削除しています。
2021年12月3日現在、COVID-19ワクチンロットと30年以上前の季節性インフルエンザワクチンロットを比較したデータでは、以下のようになりました。このデータは、2021年12月にFDAとCDCの関係者に送られたジョンソン上院議員の監視書簡に含まれています(その後、彼は40通以上の手紙を送りましたが、ほとんどが無視されるか、不誠実でガス抜き的な返答がなされました):
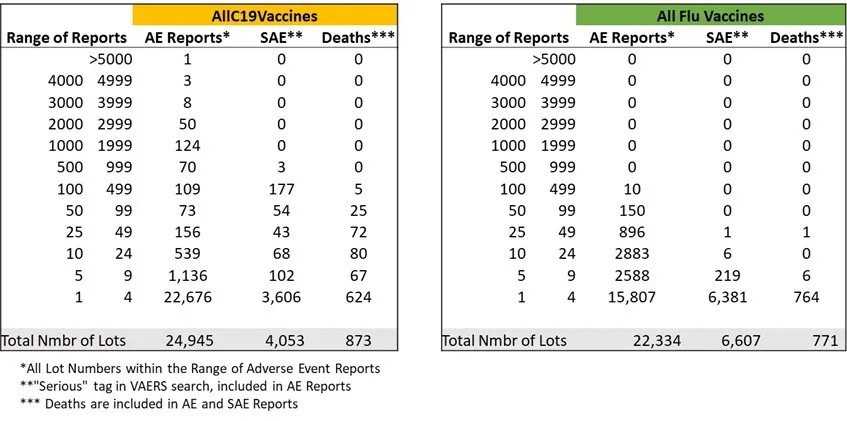
調べてみると、30年以上にわたって、季節性インフルエンザワクチンは、1つのロットで合計137件以上の(重篤でないものを含む)有害事象が報告されたことはないそうです。 しかし、VAERSのデータによると、1年足らずの間に、COVID-19ワクチン(Moderna 039K20A)の1ロットに対して5,297件の有害事象が発生しました。 さらに、COVID-19ワクチンのVAERSで報告された米国内のみの有害事象の約80%は、ワクチンのロット番号の約1%にしか関連しておらず、重篤な有害事象(救急外来受診、入院、死亡を伴うもの)の約80%は、ワクチンのロット番号の約5%にしか関連していないという分析結果が出ています。
COVID19注射液と季節性インフルエンザワクチンとのロット間変動性
この分析では、製造品質、安定性、再現性、および製造された製品のロット間の一貫性に関連するその他の要因に主に関心を持ちました。
ワクチン製造は規制された産業である。 それにもかかわらず、製品が高品質の製造環境で製造され、製品のロット間の整合性があることが期待されています。
医薬品は、製造ロット間で管理されたパラメータが一定の狭い範囲に収まることが期待されています。製造業者や規制当局からは、異なる製造ロットから採取された製品が本質的に同じであることが期待され保証されています。 さらに、製造業者や公衆衛生当局からは、Covid-19ワクチンが異なる製造業者のものを互換的に使用できることが保証されています。しかし、これを実証する臨床研究はなく、一般市民はメーカーや保健当局の言葉を信じることが期待されています。
季節性インフルエンザワクチンと比較して、Covid-19ワクチンのロット間変動を調査するために、まず季節性インフルエンザデータセットの全製造ロット番号の重大有害事象をアルファベット順に並べてプロットしました:
季節性インフルエンザワクチン、重大な有害事象がゼロでない全ロット

次に、Covid-19 ワクチンデータセットについて、Serious Adverse Events/製造ロットを見て、アルファベット順に並べ、同じプロットを作成しました。
Covid-19注射剤データセットのロット間:

これらのデータセット間の製造ロット間変動の違いをまとめるために、各データセットの変動係数を比較した。変動係数(CV)とは、平均値に対する標準偏差の大きさを示す変動性の相対的な尺度である。標準化された単位を持たない尺度であり、異質なグループや特性間のばらつきを比較することができる。パーセンテージで表されることが多い。 この結果から、Covid-19データセットのCVは、季節性インフルエンザワクチンデータセットのCVの最大12倍であることがわかります。

結論として、Covid-19 ワクチンは、製造ロット間の一貫性を示していない。 この結果は、若い健康な成人、子供、妊婦を含む何百万人もの人々に注射されるこれらの製品の製造が、医薬品に期待される製造品質基準に準拠しているか、一貫しているかどうかを疑問視するものです。 一般の人々は、これらのワクチンが安全で効果的であり、最高水準の品質で製造されていると思い込んでいます。 私の分析は、実世界の結果データに基づき、これが事実でないことを実証しています。 これらの知見は非常に憂慮すべきものであり、調査が必要です。
翻訳、ここまで。
参考情報
ワクチンのロットに関する記事。
ワクチンのロットに関する様々なデータが提供されています。
以上
