グリカンゲートがSARS-CoV-2スパイクタンパク質の開口を制御(2021年8月)
A glycan gate controls opening of the SARS-CoV-2 spike protein
グリカンゲートがSARS-CoV-2スパイクタンパク質の開口を制御する
元→A glycan gate controls opening of the SARS-CoV-2 spike protein | Nature Chemistry

Abstract
SARS-CoV-2 感染は、スパイクタンパク質受容体結合ドメイン (RBD) の開口によって制御されます。RBD は、グリカンで保護された「ダウン」状態から露出した「アップ」状態に移行し、ヒトアンジオテンシン変換酵素 2 受容体に結合して細胞に感染します。
「アップ」状態と「ダウン」状態のスナップショットはクライオ電子顕微鏡法とクライオ電子トマグラフィーによって取得されていますが、RBD 開口遷移の詳細は実験的特徴付けを回避しています。
ここでは、完全にグリコシル化されたスパイク外部ドメインの 130 µs を超える加重アンサンブルシミュレーションにより、300 を超える連続的で速度論的に偏りのない RBD 開口経路を特徴付けることができます。
クライオ電子顕微鏡データの ManifoldEM 分析とバイオレイヤー干渉測定実験と合わせて、RBD 開口を促進する N343 位の N グリカンのゲーティング役割を明らかにします。残基 D405、R408、および D427 も関与しています。
ここで提供されるグリコシル化スパイク活性化メカニズムの原子レベルの特性評価は、アンサンブル経路シミュレーションの画期的な研究であり、SARS-CoV-2 ウイルスの侵入と感染の基本的なメカニズムを理解するための基礎を提供します。
Main
重症急性呼吸器症候群コロナウイルス 2 (SARS-CoV-2) はエンベロープ RNA ウイルスであり、世界中でかなりの罹患率と死亡率を引き起こしているコロナウイルス疾患 2019 (COVID-19) の原因物質です。
ウイルスの主な感染機構である、ウイルスの外側にあるスパイクタンパク質は、ビリオンが宿主細胞と接触する最初のポイントであり、主要なウイルス抗原です。
スパイクタンパク質のクライオ電子顕微鏡 (クライオ EM) 構造が最近かなり多く報告されており、スパイクタンパク質の構造状態に関する情報が総合的に得られています。
解明された構造の大部分は、細胞侵入のためのアンジオテンシン変換酵素 2 (ACE2) 受容体との相互作用を調節する受容体結合ドメイン (RBD) の位置によって定義される「ダウン」または「アップ」状態のいずれかに分類されます。
受容体結合モチーフ (RBM) が ACE2 結合に利用可能になるためには、RBD が「ダウン」状態から「アップ」状態に移行する必要があり (図 1)、したがって、活性化メカニズムは細胞への侵入に不可欠です。
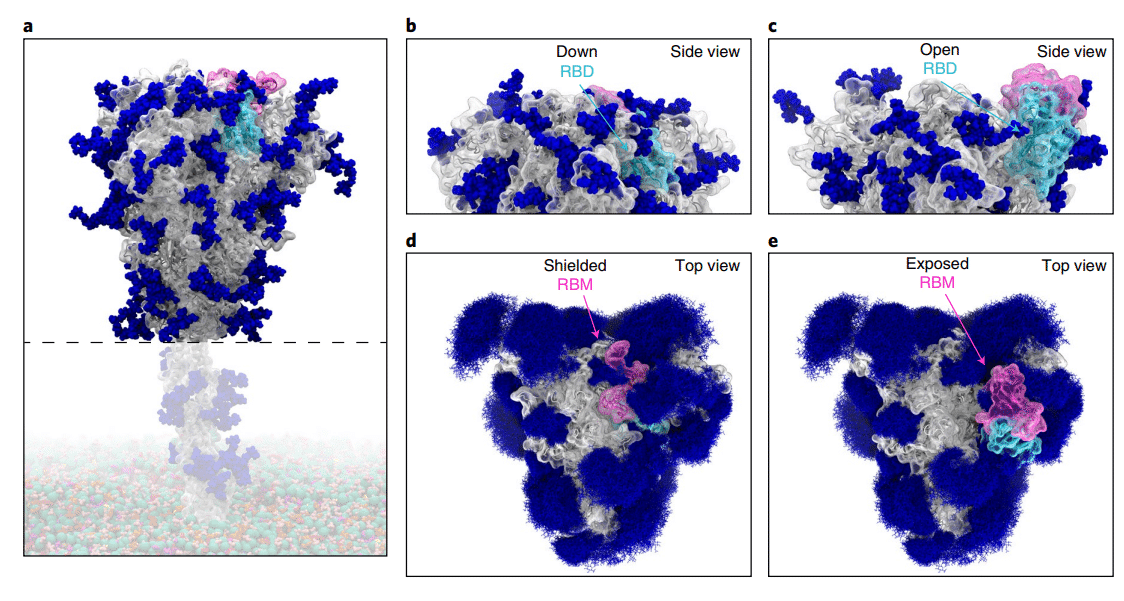
Lu らは、単一分子蛍光 (Förster) 共鳴エネルギー移動 (smFRET) イメージングを使用して、スパイクの動態をリアルタイムで特徴付けました。
彼らの研究により、スパイクは 4 つの異なる立体構造状態を動的に訪れ、その集団はヒト ACE2 受容体と抗体の存在によって調整されることが示されました。
しかし、smFRET や従来の構造生物学技術では、このような動的移行の基盤となる原子レベルのメカニズムに関する情報を得ることができません。
最近、スパイクタンパク質の全原子分子動力学 (MD) シミュレーションでは、実験的に正確なグリコシル化と裏付け実験により、スパイクグリカンによる広範な遮蔽と、位置 N165 と N234 のグリカンが RBD を「開いた」構造で支える機械的役割を担っていることが示されました。
Casalino らが行った従来の MD シミュレーションでも、スパイクのダイナミクスをより適切に特徴付けるマイクロ秒単位のダイナミクスが明らかになりましたが、クライオ電子顕微鏡構造とエネルギー的に類似したサンプリング構成に限定されていました。
この経路を研究するために、強化サンプリング MD シミュレーションがいくつか実行されましたが、これらのシミュレーションでは、スパイクタンパク質のグリコシル化が欠如していたか、外力の追加が含まれ、メカニズムの詳細が提供されませんでした。
・・・中略・・・
私たちの研究は、スパイクの開口の一連の遷移経路を特徴付け、ManifoldEM によってクライオ EM データセットで検出された立体配座と一致し、開口メカニズムに関与する N343 の位置にあるグリカンなどの重要な残基を特定します。
私たちのシミュレーション結果は、バイオレイヤー干渉法 (BLI) 実験によって裏付けられており、これらの重要な残基の変異後にスパイクが ACE2 と相互作用する能力が低下することを示しています。
Results and discussion
WE simulations of spike opening
スパイク開口のWEシミュレーション
※省略します。
Comparison with spike conformations detected by ManifoldEM
ManifoldEMで検出されたスパイク構造との比較
※省略します。
The N343 glycan gates RBD opening
N343グリカンがRBDの開口を制御する
「ダウン」状態では、SARS-CoV-2 スパイクの RBD は N165・N234・N343 の位置にあるグリカンによって保護されています。
RBDdown 状態と RBDup 状態ではグリカンの保護が調査されていましたが、WE シミュレーションにより、開口プロセス中の保護の特性評価が可能になり、RBD が「ダウン」状態から「アップ」状態に遷移するとグリカンの保護が急激に減少することが明らかになりました。
N165 位置と N234 位置にあるグリカンは一貫して RBM を保護しますが、N343 グリカンによる保護は RBD の開口とともに減少します (補足図 6)。
保護以外にも、N165 位置と N234 位置にあるグリカンの構造的役割が最近報告され、「ロード アンド ロック」メカニズムによって RBD を「アップ」構造で安定化しています。
私たちの WE シミュレーションは、スパイクの開口メカニズムにおけるグリカンのさらに具体的で重要な役割を明らかにしました。N343 グリカンは、ACE2 結合モチーフの残基 F490、Y489、F456、および R457 の間に「ハンドジャイブ」動作で挿入することにより、RBD を「下」から「上」のコンフォメーションに押し上げる「グリカン ゲート」として機能します (図 2a ~ e、3、および補足ビデオ 4)。

したがって、N343 グリカンは、グリカン N165 および N234 の安定化の役割とは異なり、遷移を開始する積極的な役割を果たします。
このゲーティング機構は、最初にスパイク開口のいくつかの成功した経路で視覚化され、その後、すべての成功した経路で N343 グリカンが前述の各残基と接触 (3.5 Å 以内) していることが判明した 310 の成功した経路すべてを分析して確認されました (補足図 7)。
N343 グリカンの同じメカニズムの動作は、2 つの完全に独立した WE シミュレーションで観察されました。これは、WE やその他の強化されたサンプリング シミュレーション方法に問題となる可能性のある不完全なサンプリングにもかかわらず、結果が堅牢であることを示唆しています。
N343 グリカンがキーゲーティング残基として果たす役割をテストするために、BLI 実験を実施しました。
BLI 実験では、スパイク RBM (残基 438 ~ 508) の ACE2 への結合レベルを評価し、各スパイク変異体の「上」の位置にある RBD の相対的な割合の代理として機能します。
結合に直接関与する残基は変異させず (つまり、RBM-ACE2 インターフェース)、変異に応答した RBD の開口の影響を制御された方法で検出できるようにしました。
以前の結果では、SARS-CoV-2 S-2P タンパク質の N165A および N234A 変異体の結合レベルが低下したことが示されていますが、N343A 変異体では ACE2 結合がさらに低下し、スパイク結合レベルが約 56% 低下しました (図 4 および補足表 1)。

ネガティブコントロールとして、ジスルフィドによって 3 つの RBD ダウン構造に固定されると予想される S383C/D985C バリアントは、ACE2 受容体との関連性を示さなかった。
これらの結果は、RBDup 構造が N343 の位置でのグリコシル化によって大幅に影響を受けるという仮説を裏付けている。
Atomic details of the opening mechanism
開口機構の原子レベルでの詳細
RBDdown 状態は、RBD-A の T415 と鎖 C の K986 の間の水素結合、RBD-A の R457 と RBD-B の D364 の間の塩橋、RBD-A の K462 と N 末端ドメイン C (NTD-C) の D198 の間の塩橋を特徴としています (図 5a~c、e および補足図 8)。
水素結合 T415A-K986C は、K986C が RBDA-D427 と短命 (平均持続時間は 2%) の塩橋を形成する前に、「up」状態への成功経路の平均 12% を費やします (図 5b、e および補足図 8)。次に、RBDA が開き続けると、K986C は E990C および E748C と塩橋を形成します。これらの接触は、310 の成功した経路すべてで形成されます (補足図 8)。

K986 のプロリンへの変異は、ワクチン開発などにおいて、融合前スパイクを安定化するために使用されており、これらのシミュレーションは、RBD の開口におけるこの残基の追加の役割に分子的背景を提供します。
その後、成功した経路の平均 16% で、「アップ」状態への経路の途中で、R457A-D364B 塩橋が壊れ、RBDA が RBDB から RBDC に向かって上向きにねじれ、RBDA の R408 と RBDC の D405 の間に塩橋が形成されます (図 5c、e および補足図 8)。この塩橋は、「アップ」状態への成功した経路の 20% にわたって持続し、310 の成功した経路すべてに存在します。
RBDA の R466 と NTDB の E132 の間の塩橋は、「アップ」状態への 204 の成功した経路のうち 189 に存在し、「オープン」状態への 106 の経路すべてに存在します。この接触は、「アップ」状態と「オープン」状態間の遷移中に最も多く発生します。
最後に、RBDA の D428 と RBDC の R454 の間の塩橋は、「アップ」状態から「オープン」状態への 106 の経路すべてにのみ存在し、S1 サブユニットが剥離し始める前の「オープン」状態の RBD とスパイク間の最後の塩橋です (図 5d、e および補足図 8)。この時点で、RBDA への最後の接触は、NTBB の位置 N165 のグリカンです。
特定された主要なスパイク残基 R408A、D405A、および D427A の追加の BLI 実験は、シミュレーションで観察された経路を裏付けています。
これらはそれぞれ、スパイクと ACE2 の結合相互作用を約 13%、約 27%、約 52% 減少させます (図 4 および補足表 1)。

また、特定された残基 D198、N343、D364、D405、R408、T415、D427、D428、R454、R457、R466、E748、K986、および E990 は、SARS-CoV スパイクと SARS-CoV-2 スパイク間で保存されており、RBD 開口の主要なスパイク機能を調整する上での重要性を裏付けています。
出現した変異体 SARS-CoV-2 株、B.1 (D614G)、B.1.1.7 (H69–V70 欠失/Y144–Y145 欠失、N501Y・A570D・D614G・P681H・T716I・S982A・D1118H) 、B.1.351 (L18F・D80A・D215G・R246I・K417N・E484K・N501Y・D614G・A701V)、P.1 (L18F・T20N・P26S・D138Y・R190S・K417T・E484K・N501Y・D614G・H655Y・T1027I)、CAL.20 C (L452R・D614G)、には、RBD の開口を促進するためにここで特定した残基の変異体は含まれていません。
※ただしBA.2:D405N・R408S変異あり。
開口経路に沿った出現株で変異したものに隣接する残基とグリカンの分析は補足表 2 に詳しく示され、各残基とグリカンと RBDA との距離は補足ビデオ 5 にまとめられています。
Conclusions
我々は、糖鎖付加された SARS-CoV-2 スパイクヘッドの広範囲な WE MD シミュレーションを報告し、RBD の「ダウン」コンフォメーションから「アップ」コンフォメーションへの遷移を特徴づけています。
130 µs を超えるシミュレーションでは、300 を超える独立した RBD 開口遷移経路が提供されます。
シミュレーションされた開口経路は、ManifoldEM 法を使用してクライオ EM から検出されたコンフォメーションと非常によく一致しています。
独立した WE シミュレーションからのこれらの経路の分析では、開口遷移全体を通じて RBD を持ち上げて安定化させる N343 のグリカンに明確なゲーティングの役割があることが示されています。
また、スパイク RBD の「開いた」状態も特徴付けました。この状態では、鎖 B の N165 グリカンが、S1 のさらなる開放に向かう途中で RBD と最後に接触することになります。
N343、D405、R408、D427など、開放遷移の鍵となる残基のBLI実験は、私たちの計算結果を広く裏付けました。
特に、N343A変異体のACE2結合が56%減少したことは、以前に報告されたN234A変異体の40%減少とN165A変異体の10%減少と比較して、RBD開放プロセスのゲーティングと支援におけるN343の重要な役割を証明しており、メカニズムの詳細を完全に理解するには機能遷移をサンプリングすることの重要性を強調しています。
個々の変異のいずれも ACE2 結合を完全に無効にしなかったため、ウイルスはスパイクの開放を調整するために複数の残基を含むメカニズムを進化させたことが示されています。
私たちの研究は、スパイク開口における N343 グリカンの重要なゲーティング役割を示しており、この重要な病原体のウイルス感染のメカニズムに関する新たな知見を提供しています。
以下省略。
この記事が気に入ったらサポートをしてみませんか?
