免疫不全症の人が新型コロナウイルスに感染すると?
こんにちは。皆さまは雨の被害がありましたか? 今回 ご紹介する論文は先天性免疫不全症の人が対象です。扱い方を間違えると差別につながりかねないテーマなのでこれまで取り上げませんでした。少し専門的になってしまいましたがフォローしてくださっている皆様のために全文無料です。
抗体反応のない人がSARS-CoV-2に感染すると?
これまでの経験から明らかなことは、抗体による感染防御ができない疾患の人たちの新型コロナウイルス SARS-CoV-2 に感染には3つの特徴があります。1) 感染早期に症状は軽い人が多いが、2) 長期感染し、3) 症例致死率が高い。
ひとつめは2020年11月4日にCellに掲載された論文です。

SARS-CoV-2 は、感染した人の体内でウイルス遺伝子の変異が起こります。これをウイルス遺伝子の宿主内変異と言います。SARS-CoV-2の宿主内変異は比較的限定されていて、感染の過程を通じて主要な SARS-CoV-2 集団は同一のままです。つまり、一般人が感染した場合に体内で新型コロナウイルスの遺伝子変異が起こる。しかし変異の幅は限定的である。
これに対して、免疫不全症患者の体内で予測不能な変異株のできる可能性がある。
European Centre for Disease Prevention and Control. Rapid increase of a SARS-CoV-2 variant with multiple spike protein mutations observed in the United Kingdom. December 20, 2020. リンク

2020年2月12日、10年来の慢性リンパ性白血病(CLL)、後天性低ガンマグロブリン血症、貧血、慢性白血球増加症を患う71歳の女性が、腰と下肢の痛みを訴えて救急外来を受診した。 2日後にがんに関連する脊椎骨折と狭窄の手術を受け、リハビリ施設に移動した。2020年3月2日にPCR検査でSARS-CoV-2陽性が判明したため陰圧個室の隔離病棟に入院した。 対応する医療スタッフは、電動空気清浄呼吸器 (PAPR) または N95 マスクとゴーグル、ガウン、手袋で構成される完全な個人用保護具を使用した。
当時の様子を思い出してみましょう↓ 武漢の病院で新型肺炎の入院患者を診察する医師です。N95マスク、ゴーグル、防護服、手袋は最初に病人を診療した中国に教えてもらいました。写真の動画へのリンク


このかたの臨床症状の記載は特にありません。
最初の診断後、感染性 SARS-CoV-2 の排出は最長 70 日間、ゲノムおよびサブゲノム RNA の排出は最長 105 日間観察された。
もともとある低ガンマグロブリン血症に対して免疫グロブリン製剤を定期的に投与し、さらにSARS-CoV-2 感染に対して回復期血漿が2回投与された。
最初の回復期血漿投与後も感染し続け、2回目の回復期血漿投与から数週間後にようやくSARS-CoV-2 のRNAは検出されなくなった。

定期的に投与された免疫グロブリン製剤にはほとんど新型コロナウイルス中和能がなく、2回投与された回復期血漿の中和能は初回が60、2回目が160でした。


治療前後の患者血中の抗スパイク蛋白抗体価 IgG を測定しました。初回の回復期血漿投与後には効果がほとんど見られませんでしたが、2回目の回復期血漿投与で抗体価の上昇が確認されました (図2C)。

図2(C) 全長組換え SARS-CoV-2 スパイク外部ドメインに対する IgG 力価は、71 日目 (薄灰色) および 82 日目の回復期血漿輸血の直前および直後を含むいくつかの時点で収集された患者血清中の ELISA によって測定されました ( 暗灰色)

回復期血漿を投与する前の、49 日目と 70 日目に採取された鼻咽頭ぬぐい液から培養された SARS-CoV-2 の走査型(図3Bの白い球)および透過型電子顕微鏡検査(図3CDの黒丸)により、コロナウイルスの形態と一致するウイルス粒子が示されました。この実験結果は、49 日と70 日に、この人から感染性ウイルスが排出されていたことを示唆します。

Bは走査型電子顕微鏡写真、CDは透過型電子顕微鏡
70日以降の患者の鼻咽頭スワブからウイルスの培養はできませんでした。

しかし2度目の回復期血漿投与から23日後まで鼻咽頭スワブのPCR検査は陽性であり続けました (図1)。

もしPCR検査陽性を隔離期間と指定するならば、ここではウイルスゲノムRNAではなくウイルスサブゲノムRNAのqRT-PCRが推奨されています。

49、70、85、および 105 日目に収集された鼻咽頭スワブから決定したSARS-CoV-2 の全ゲノム配列 (表 S4)から、感染したのは患者のいるワシントン 州で流行中の系統 A.1 に属し、その後患者体内でウイルスに変異が起こったが、検出されたウイルスはすべてが同じ系統 A.1 に属していた。

2 つの分離株ゲノムにスパイク糖タンパク質コード領域に 2 つのインフレーム欠失が観察されました。 1つは、S1 の N 末端ドメイン (NTD) で 21 nt のフレーム内欠失 (残基 21,975 ~ 21,995) で7 アミノ酸の欠失 (アミノ酸 [aa] 139 ~ 145) が発生しました。1つは 70 日目の分離株のゲノムに見つかったもので、S1のN末端ドメイン(NTD) に 12 nt 欠失 (残基 21,982 ~ 21,993) によりNTD の 4-aa 欠失 (aa 141 ~ 144) が生じました。
参考論文:Case study: prolonged infectious SARS-CoV-2 shedding from an asymptomatic immunocompromised individual with Cancer.
Cell. 2020; 183: 1901-1912.e9. https://doi.org/10.1016/j.cell.2020.10.049
2つ目の論文
2つめの論文は、大阪市立総合医療センター感染症科の森田諒先生、白野 倫徳先生、大阪大学免疫学フロンティア研究センター分子免疫学研究室の山崎 晶教授、大阪大学微生物病研究所感染機構研究部門 ウイルス感染制御分野塩田 達雄教授、中山 英美准教授、佐々木 正大助教先生たちの業績です。
皆さま、論文掲載おめでとうございます。

論文:COVID-19 relapse associated with SARS-CoV-2 evasion from CD4+ T-cell recognition in an agammaglobulinemia patient.
iScience. 2023 May 19;26(5):106685. doi: 10.1016/j.isci.2023.106685.
下のスクショは5月28日の阪大宮坂先生のこの論文に対するFacebookコメントです。全文はこちらの リンク からどうぞ。

この論文の対象が先天性免疫不全症の人なので、先に説明します。
先天性免疫不全症という病気
生まれつき免疫機能にデフェクトがある、先天性免疫不全症の人たちがいます。先天性免疫不全症には非常に多くの疾患が含まれますが、この中に新生児期に細菌感染症を発症し抗体価のあがらない人がいて、さらにそのうちの85%はブルートン型細胞質チロシンキナーゼ Btk に遺伝子異常によって発症するX連鎖無ガンマグロブリン血症です。
X連鎖無ガンマグロブリン血症では血中のすべての免疫グロブリンのレベルが低いか全くない。また血中の成熟B細胞が2%以下にとどまります。その理由はブルートン型細胞質チロシンキナーゼがPro-B細胞からPre-B細胞へ分化するのに必要だからです(下図)。

コラム:X 連鎖無ガンマグロブリン血症 (XLA) を少し詳しく
原因:X 連鎖無ガンマグロブリン血症 (XLA) はブルートン型チロシンキナーゼ (BTK) をコードする遺伝子変異によります。
ブルートン型チロシンキナーゼ (BTK)遺伝子はX染色体に存在し、B 細胞の発生と成熟 B 細胞の機能の両方に不可欠です。B細胞の前駆細胞であるプロB細胞からプレB細胞への分化障害が生じ、成熟B細胞がごく少数になり、抗体がほとんど、または全く産生されない。
症状:血清免疫グロブリンIgG、IgA、IgM、すべてのクラスの値の低下が著しく、末梢血B細胞比率が2%以下で、細菌感染症をしばしば反復する。
疫学:発症頻度は出生男子10万に1人と推測されている。
治療:免疫グロブリン製剤の定期補充療法。200~600mg/kgを3~4週間隔で静脈投与し、血清IgGトラフ値 (血中最低濃度値) を少なくとも500mg /dL以上に保つ。
最初の入院で無症状
25 才の男性は、2020 年 7 月末に発熱し、8月上旬の新型コロナウイルスの qRT-PCR 検査で陽性となり入院しました。入院後も全身状態が安定していたため、入院9日めに退院しました。入院初日から退院後も持続的にアセトアミノフェン1800mg/日が投与されています。レムデシビルの特例承認は2020年5月7日でしたが使用しなかった。

この人は生後 11 か月の新生児の時に、免疫不全症のX 連鎖無ガンマグロブリン血症と遺伝子診断されています。BTK遺伝子のエクソン 6 スキップ変異(スプライシング部位変異、c.392-2A>G)です。この変異は単球の BTK 発現レベルを顕著に低下させることが報告されています(14)。治療は、自分の体で免疫グロブリン産生ができないので定期的に免疫グロブリン製剤を静脈注射しています。
免疫能は、好中球殺菌機能とナチュラルキラー細胞活性は正常範囲内でしたが、好中球の貪食機能が低下していました。 B細胞として、CD19 リンパ球サブセットは検出されませんでした (表 S1)。
経過期間中に軽度の症状があった。PCR検査で高いCt値だった
アセトアミノフェン1200mg/日、定期的に免疫グロブリン製剤を静脈注射し外来にて経過を見ていた。経過中、血液検査で炎症のマーカーであるCRPが3〜5 (mg/dL) と上昇している。また、SARS-CoV-2のRNA 量も0となることはあまりなかった。

コラム:この論文で行われたqRT-PCR検査
サンプルを 10,000 rpm で 30 秒間遠心分離して、不溶性物質を除去する。
キアゲン社の説明書に従って、QIAamp Viral RNA Mini Kit (QIAGEN) を使用して、140 μL の上清からウイルス RNA を抽出する。
qRT-PCR のアッセイは、OneStep PrimeScript™ RT-PCR Kit (Takara Bio) を使用し、N2 セットのプライマーと、国立感染症研究所によって公開された方法に従って設計されたプローブを使用して実行した。
qRT-PCR の条件はQuantStudio™ 3 リアルタイム PCR システムを使用して、52 °C で 5 分間、95 °C で 10 秒、その後 95 °C で 5 秒、60 °C で 30 秒を 40 サイクルです。
難易度:下図のピペットマンで少量の液体を分注することができる。初めてでもすぐできるようになります。そしてマニュアルに従って実験する。使用する機械は遠心機、ボルテックス、リアルタイムPCRマシン。PCRマシンの取り扱いはヘルシオで料理を作るくらいの難易度です。

退院後
患者は時折、倦怠感や発熱を経験した。 血液検査では、CRP レベルのわずかながら持続的な上昇が示されました(範囲、2.51 ~ 7.49 mg/dL、中央値、4.85 mg/dL)(図 1A)。
99、163、195、216、および 232 日目に実施された CT では、移動性すりガラス陰影を伴う肺炎が示されました(図1B)。
2020年9月27日には抗体製剤のソトロビマブが特例承認されていたので使用可能でしたが、論文に唾液サンプル中のqRT-PCRでSARS-CoV-2のCt値が中央値35.3(範囲33.82~36.5)と高値のため使用しなかったと記載してあります。

器質化肺炎の可能性を考慮し、218日目に気管支肺胞洗浄を伴う気管支鏡検査を行ったところ、肺炎罹患領域の生検組織に非特異的炎症が確認された。 63、77、175、176、181日目に採取された喀痰および唾液サンプル中のSARS-CoV-2のqRT-PCR検査では、高いサイクル閾値(Ct)値(33.82~36.5、中央値35.3)のSARS-CoV-2 RNAが検出された。
[18F]-2-フルオロ-2-デオキシ-D-グルコース (FDG)-陽電子放射断層撮影 232 日目の PET/CT では、肺炎部位にのみ FDG の蓄積が示されました (最大標準化取り込み値、5.6) (図 1B、下図)。

約 235 日目に、患者の全身状態が著しく悪化した。 悪寒、震え、倦怠感、および制御不能な高熱(40 ℃)。 血液検査では CRP とIL-6 のレベルの上昇が示され、CT では肺炎の増悪が示された (下図)。アセトアミノフェンを1 日あたり 1,800 mg に増量した。

239日目のSARS-CoV-2のqRT-PCR検査では、Ct値の低下が示されウイルス量が増えた。 同日に行われた 19 件の気道感染症に対する喀痰サンプルの多重 PCR 検査 (BioFire FilmArray Respiratory Pannel 2.1) では気道感染症を引き起こす他のウイルスや細菌は検出されまなかった (表 S2)。
大阪市立総合病院に再入院し、239日目からレムデシビルを、1日目は200mg/日、2日目以降は100mg/日を合計10日間投与した。
おおよそ224、238、247、276目に合計4回、血漿投与した(図1A)。レムデシビル投与 2 日目 (240 日目) には、熱は下がり、悪寒、震え、倦怠感が消失しました。 血液検査では CRP および IL-6 のレベルの急速な低下が示された (図 1A、表 S3)。

画像検査では肺炎の解消が確認された (図 1B下図)。

SARS-CoV-2 の喀痰サンプルの qRT-PCR 検査では Ct 値の上昇が示され、患者は 243 日目にウイルス検査で陰性でした (図 1A、表 S4)。 レムデシビル投与後の喀痰サンプルからはSARS-CoV-2は分離されなかった。 患者は、症状がすべて解消され、血液検査と画像検査の結果が改善した後、248日目に退院した。 退院後 9 か月間再発は発生しておらず、治療が成功したことが示されています。 患者には毎月免疫グロブリン(IVIG)の静脈内注射が施され(図1A、表S5)、この研究の全過程を通じてSARS-CoV-2に対するワクチン接種はしなかった。


PCR陽性になってからレムデシビル投与まで患者に感染していたウイルスの研究
ウイルスゲノムと増殖能の解析
感染性ウイルスは、次の凍結保存検体から分離された(表S4)
1日目の鼻咽頭スワブ(NPS)
218日目の気管支肺胞洗浄液(BALF)および肺組織、
224日目の喀痰
239日目の新鮮喀痰
全ゲノム配列は、5 つの分離株と 1 日目の NPS 検体から得らた。 系統解析の結果、ウイルスはすべてB.1.1.284クレードに属した。患者が感染していた期間に日本で流行していたクレードである。
単離された 1 日目ウイルスは 1 日目 NPS 検体と同じコンセンサス配列を示し、他のウイルスは 1 日目ウイルスと異なるクラスターを形成した (図 2A、表 S6)。
218日から239日に日本で検出されたウイルスはほとんどB.1.1.7に属していた。 症状の増悪した患者から分離されたウイルスは B.1.1.284 に属していたので、患者体内で持続感染し変異したことが示唆された。

ウイルス変異のほぼ 3 分の 2 は非同義であった (表 S7)。
塩基が変化した結果、アミノ酸が変るときは非同義置換とよぶ
1 日目のウイルスと比較して、他のすべての分離株では 11 個のアミノ酸の変化と 2 個の同義のヌクレオチド置換が共通して観察された (図 2B)。

218日目のBALFおよび肺組織からの分離株と、224日目および239日目の分離株で、さらに2個、1個、3個、および5個のアミノ酸変化が見出された。 ORF1ab の K3353R 変異は CoV-GLUE データベースにあった。他は新しく発見した変異である (18) (表 S7)。
1,000 ヌクレオチド当たりの平均変異数は E (6.67)、M (3.00)、ORF7a (6.89) の領域で 1 を超えていたのに対し、ORF1a (0.454) の変異は 、ORF1b (0.278)、S (0.720)、および ORF3a (0.303) は 1 未満だった。
ORF6、ORF8、および N 領域には変異はない。
この患者における SARS-CoV-2 の進化速度(9.37 × 10^4 / 部位 / 年)は、一般集団で報告されている速度(3.95 ~ 6.67 × 10^4 / 部位 / 年)よりも高かった(表 1)。
他の免疫不全患者からの公開された配列データに基づいて SARS-CoV-2 の進化速度を計算し、SARS-CoV-2 がより速く進化することを確認した。 一般集団よりも免疫力が低下している宿主のSARS-CoV-2 ゲノムの進化速度は速いことが多かった(表 1)。

分離されたウイルスの増殖能力
焦点形成アッセイとしてウイルスを、24ウェルプレートにまいた細胞にウイルスを感染多重度0.01で感染させた。そして感染から 1 日後にウイルスの焦点サイズを比較した (図 2C)。焦点サイズがウイルスの増殖能力と相関すると考え、1日目のNPS検体から分離されたウイルスは小さな病巣、239日目に喀痰から分離されたウイルスは大きな病巣、218日目に肺組織から分離されたウイルスは小さな病巣、218日目にBALFから分離されたウイルスは大きな病巣と小さな病巣、224 日目に喀痰から分離されたウイルスは中程度の大きさだった。218日目にBALFから分離されたウイルスは複数のクローンの混合物と示唆された。

次に、患者から分離された複数の変異ウイルスが免疫逃避能をもつか?を免疫学者が調べた
T 細胞認識を回避する変異の獲得
ORF3a の T32I 変異は T 細胞認識を回避する変異の獲得します
方法:324 日目に患者の血液から末梢血単核球 (PBMC)を収集した。この PBMC を培養し、12日間にわたりSARS-CoV-2 Wuhan-Hu-1 株 (Wu) のペプチドで刺激した後で細胞を洗って新しい培養液にします。それから20時間、ペプチドなし (-)、同じ武漢株のペプチド (Wu)、患者のペプチド (Mut) で刺激してから分泌されたIFN-γ の濃度を測定した。
変異株ペプチドで、武漢株ペプチドよりもIFN-γ の誘導が低いものを探した。IFN-γ 誘導能が低下する 5つの変異を発見した。これらは実験室でT細胞細胞による ウイルス排除能を低下させる変異である。
S1145、ORF1ab2973、および ORF3a25 Wu ペプチドは、対応する変異ペプチドよりも大きな IFN-γ 発現を誘導した (図 3B)。
ORF1ab3061 mut ペプチドおよび ORF7a105 T115I mut ペプチドによって誘導される IFN-γ 発現は減少した。

5つのT細胞細胞による ウイルス排除能を低下させる変異に対応する武漢株のペプチドで刺激して増殖したT細胞には、CD4陽性T細胞と CD8陽性T細胞があった。
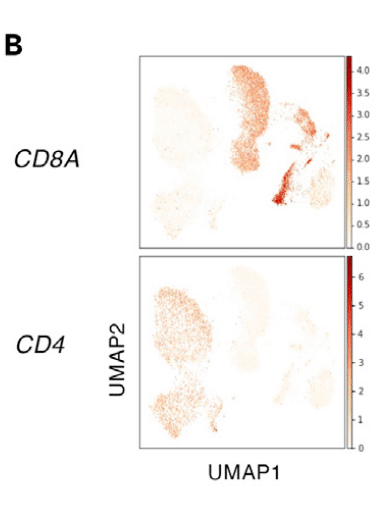
単一細胞解析で同定された上位 15 個の頻度の高い T 細胞クローンのうち、14 個のクローンが CD8+ CTL 様細胞を反映するクラスター内に位置していた (図 4C)。

残りのクローン-111 は CD4+ 細胞を含み (図 4C)、主に ORF3a25 刺激細胞由来でした (図 4D)。このことは、このクローンが ORF3a25 の刺激によって優先的に増殖したことを示唆する。

クローン 111 を除く上位 15 の頻度の高いクローンはすべて、in vitro 刺激前に患者の PBMC で検出されたので (図 4E)、クローン 111 だけが刺激前は低く、刺激後に優勢になった。

これと一致して、ORF3a25 Wu ペプチドは、再刺激時に in vitro で増殖した CD4+ T 細胞を活性化した (図 5A)。

クローン 111 のエピトープを確認するために、クローン 111 の TCR-α および TCR-β を TCR 欠損レポーター細胞株で再構成した。 レポーター細胞は、自己抗原提示細胞の存在下でORF3a25 Wuペプチドによって活性化されたが、T32I変異ペプチドは抗原性を失った(図5B)。

患者のヒト白血球抗原クラス II 遺伝子のうち、DRB1∗04:06 が ORF3a エピトープ認識の制限対立遺伝子として同定された (図 5C)。

これらの結果は、ORF3a の T32I 変異が T 細胞認識の回避をもたらしたことを示唆する。
CD4+ クラスター内の 28 の異なるバーコード付き細胞として検出されたクローン 111 (図 4C) は、高度に活性化された細胞の遺伝子サインを示した (図 5D)。 これらの細胞は、IFN-γ、IL-21、PRF1、IL-10 などの異種機能に関連する遺伝子も発現していた (図 5D)。
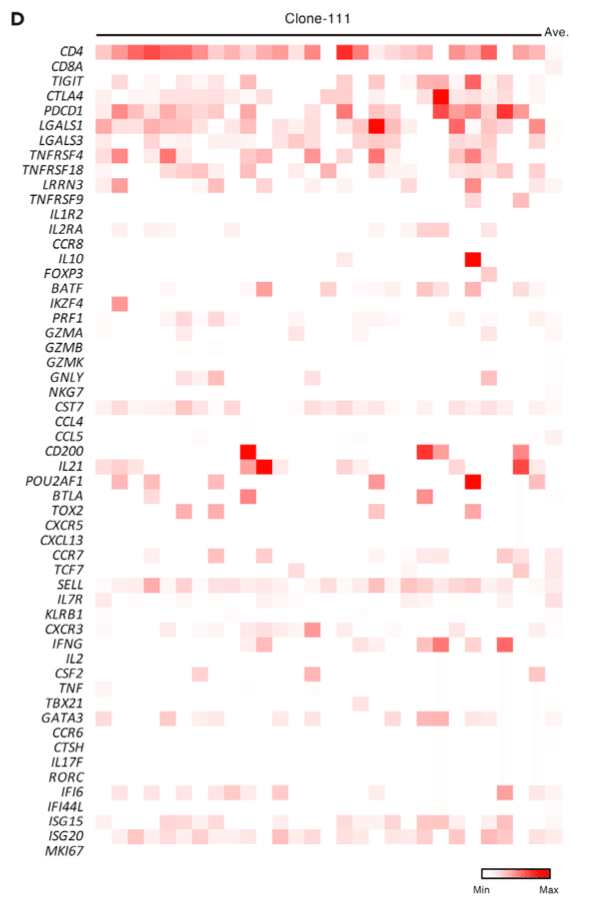
クローン-111 細胞のほとんどは FOXP3 を高度に発現していなかったにもかかわらず、クローン-111 は T 制御 (Treg) シグネチャ遺伝子の発現が高いクラスター内に位置する (図 5E)。

以上より、クローン-111 細胞が感染時にヘルパー機能、細胞障害活性、および調節活性を持つことが推測された。
2つ目の論文の日本語訳ブログ
この記事が気に入ったらサポートをしてみませんか?
