
異種移植の歴史、文献的まとめ
異種移植の歴史について検索してみたら、今年(2022年)のThe Annals of Thoracic SurgeryにEditorial(論説)として載っていました。 2005年の日本腎臓学会誌に異種移植の歴史についての日本語文献もあったので、2つをまとめた感じで歴史を振り返りたいと思います。
異種移植の黎明期(1900年代)
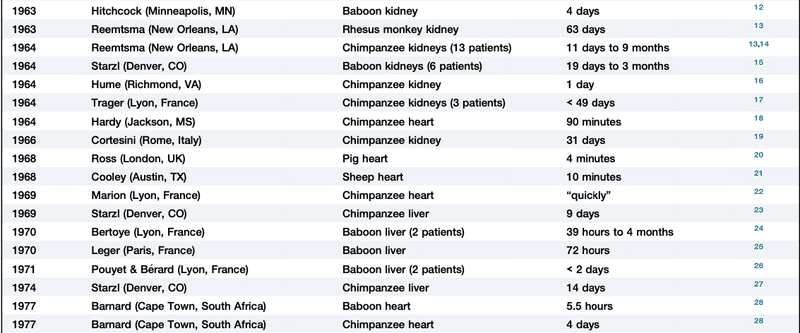
1900年初め、Mathieu JaboulayとAlexis Carrelが血管吻合技術を確立した(1912年にCarrelはこの業績を評価されノーベル賞を受賞)ことで、臓器移植が技術的に可能となり動物からの異種移植実験が行われるようになりました。文献として残っているものとして5件の異種移植があり、それはすべて動物(ブタ、ヤギ、ヒツジ、サルなど)の腎臓をヒトに移植したものでした。記載によると肘や太ももなどに移植されたとありました。しかし、生存期間はいずれも数時間から最長9日間という結果に終わっています。免疫抑制剤がないこの時代の異種移植の試みは失敗に終わり、1923年の報告を最後にこのあと40年は実験が行われることがありませんでした。

同種移植の成功と免疫抑制剤の登場(1950-1960年代)
1954年にMerill, Murrayらが一卵性双生児の間で腎移植を行い成功したことを皮切りに同種間(ヒトからヒト)の移植が活発に行われるようになってきた時代になります。1963年にはStarzlらが肝移植を、1967年にはBarnardらが心移植を行なったと言われています(心移植については肺炎により術後28日に亡くなっています)。またこの頃から移植後の治療として免疫抑制剤が使われるようになったようです。それをうけて異種移植も再び試みられるようになり、1963年11月にReemstsmaらによってサルの腎臓がヒトへ移植されました。この当時の術後の免疫抑制に使用されたレジメはアザチオプリン、アクチノマイシンC、プレドニゾン、そして全身への放射線照射だったようです。この患者さんは術後肺炎を発症し、移植後63日目に亡くなられたそうです。このグループはその後もチンパンジーの腎臓を合計13人の患者さんに移植し、結果は術後11日から9ヶ月の生存成績で、その当時の最長生存記録を更新したようです。
心移植については1964年、Hardy(世界で初めて肺の同種移植を成功させた外科医)らが虚血心筋症によりショック状態となっていた68歳の男性患者にチンパンジーの心臓を移植しています。このときは移植した心臓が小さく、患者さんの血圧維持ができなかったため術後2時間で亡くなったようです。解剖の結果、拒絶反応の所見を認めました。この結果をうけて、Hardy医師はマスコミからも医療界からもバッシングを受けてしまい、このあと彼が異種移植を行うことはなくなったそうです。ただ、他のグループにより霊長類の腎臓を用いた異種移植は引き続き行われていました。
この時期は多くの同種移植(ヒト-ヒト移植)の成功と、腎臓以外のさまざまな臓器を用いた異種移植が試みられた20年であり、また異種臓器に対する血液灌流が試されたりもしました。1968年にRossらがブタの心臓をヒトの血液で灌流したところ急性の拒絶反応を認めたようです。
シクロスポリンの登場と同種移植成功に伴う臓器不足(1980年代〜)
1976年に真菌からシクロスポリンが発見されたことにより免疫抑制療法が発展し、それに伴い移植治療の成績も随分と改善しました。移植件数が飛躍的に伸びていく中でドナー不足が問題となり、再び異種移植が注目されるようになりました。
この時代に世界的にもっとも注目を集めたのは1984年10月26日に行われた異種移植になると思います。カルフォルニアでBaileyらが生後12日なる左室低形成症候群の赤ちゃんにヒヒの心臓を移植しました。異種移植により救命できることが証明されたイベントでしたが、赤ちゃんは拒絶反応のため術後20日で亡くなりました。この当時は赤ちゃんの免疫システムが未熟であることが拒絶反応の原因と考えられ、1922年に新たな免疫抑制剤であるタクロリムスが市場にでるまで次の異種移植は行われませんでした。
この時代から1990年代にかけては免疫抑制剤のさらなる発展により、Starzlらによるヒヒの肝臓に移植、Religaらによるブタ心臓の移植、Makowkaらによるブタ肝臓の移植、そしてBaruahらによりブタ心臓の移植と多くの異種移植の挑戦が続いた。またこの時期に、基礎研究の結果、超急性拒絶反応を起こすメカニズムが解明されました。ブタに発現するαガラクトース糖鎖抗原(αGal抗原)とヒトに存在する抗αGal抗体による抗原抗体反応と補体の活性化が原因であることがつきとめられました。また時代の流れにより動物愛護を含めた倫理的問題や人畜共通感染症などの問題もあり霊長類からの移植は望まれないとして、ブタの臓器を用いた実験がさらに進んでいったのもこの時期です。

ゲノム編集技術と遺伝子組み換えブタの登場(1990年代〜)
これまでの研究結果から免疫抑制剤の改良だけでは異種移植で長期生存を期待することがとても難しいことが明確になってきました。さらにこの時代は免疫応答、補体の活性、凝固反応などがさらに研究され分子ネットワークの理解も進みました。世界で初めて遺伝子組み換えブタが登場したのは1992年12月のことです。ヒト崩壊促進因子(hDAF: human decay accelerating factor)という補体の活性を抑制するためのタンパクを導入したものです。このブタの心臓と腎臓をヒヒとカニクイザルに移植した結果、最長で3ヶ月以上生着することに成功しました。その他のヒト補体制御因子の遺伝子を導入した遺伝子組み換えブタの作成が世界中で試みられ、2004年にはヒヒの腹部に遺伝子組み換えブタの心臓を移植する実験が行われ、最長139日、中央値で76日移植した臓器が生着できたことが報告されました。補体制御因子遺伝子を導入することで、移植直後の超急性期拒絶反応は概ね克服できたものの、その後も起こる補体活性や血管内皮細胞活性、凝固系亢進などに伴う炎症生反応により拒絶反応を完全に制御するのはまだ困難で遺伝子操作により主要な異種抗原であったαGal抗原を除去したブタの作成が不可欠と考えられました。
また、それとは別に1994年にブタからヒトへのウイルス感染の危険性が報告されました。霊長類からヒトへ比べると、ブタからヒトへは人畜共通感染症のリスクは低いと考えられていましたが、ブタ内在性レトロウイルス(PERV)がヒト(移植者)に感染する可能性があることが明らかにされました。それによりFDAは1997年にPERVの感染がヒトに起こっているかどうかを検出できる技術が確立するまで全ての臨床治験を一時中断する指示を出しました。これは翌年にはすぐに解除されましたが、今もPERVをモニタリングする決まりになっていますし、感染症を起こすリスクが高いという理由で1999年にFDAは霊長類からの異種移植を禁止しました。こういった経緯より2000年12月国際委員会よりブタから霊長類への移植実験で、60%以上の成功率(健康な状態で3ヶ月以上生存)がないと、ヒトへの臨床試験をすべきでないと提唱し、最近では6ヶ月以上の生存が要求されるようになりました。
クローン X ノックアウト X 遺伝子組み換えの合わせ技(2000年代〜)
異種移植の拒絶反応に大きく関与しているものとして補体と凝固系の活性化であることが明らかになってくることでシンプルな遺伝子組み換えだけでは不十分であることが分かってきました。そこで拒絶反応をさらに抑制するためには、特定のブタの遺伝子をノックアウトし、尚且つヒトの補体の活性化を抑制するためにヒトの遺伝子を組み込むことも必要になってきました。こうやってブタ-ヒト間の相互反応が解明されていくについて、異種移植における障壁は徐々に少なくなっていき、特にゲノム編集技術、CRISPR-Cas9(クリスパー・キャスナイン)の登場により大きな変貌を遂げました。
2016年には新たな技術で遺伝子改変したブタ心臓をヒヒの腹部に移植し、最長で945日生存したことをMuhiuddinらが報告し、2018年には遺伝子改変したブタ心臓をヒヒに心移植した実験では5匹中2匹が6ヶ月以上生存し、最長で195日も生存できるようになりました。また、同時に移植のために摘出された臓器の保護法も温度調整や灌流液の発展により改良され、それにより移植臓器の機能不全を予防できるようになったことも成績の向上に貢献しています。
そして2022年1月7日。アメリカのメリーランド医療センターにて、重い心臓病をもちECMO(体外式膜型人工心肺)で1ヶ月以上治療を続けられていた57歳男性に、世界で初めて遺伝子改変をしたブタの心臓が移植される歴史的イベントに繋がったのでした。

参考文献
1.Chesney Siems et al. A Brief History of Xenotransplantation. Ann Thorac Surg 2022;113:706-10.
2.小 林 孝 彰. 異種移植の現状 と展望. 日腎 会 誌2005;47(2):83-93.
この記事が気に入ったらサポートをしてみませんか?
